指向核心素养的初中化学大单元教学实践研究
林世鑫

[摘 要]新课标要求提升义务教育阶段学生的核心素养,推行基于大概念的单元教学模式。文章以“空气中氧气含量的测定”复习课为例,以大单元课程设计为逻辑主线,以三种测定空气中氧气含量的经典方法(燃烧法、锈蚀法和加热法)引入课题,围绕“氧气”这一核心点将空气的组成、氧气的性质、金属的氧化等知识点有机地串联起来,帮助学生全面提升化学学科的知识结构和学科能力,形成对普遍事物的理性认识。
[关键词]核心素养;大单元教学;复习课;初中化学
[中图分类号] G633.8 [文献标识码] A [文章编号] 1674-6058(2023)02-0077-03
一、课程内容及目标
(一)课程内容的时代背景
为了培养担当民族复兴大任的时代新人,教育部于2022年4月颁布了《义务教育化学课程标准(2022年版)》(本文简称新课标)。新课标以化学课程的性质和教育价值为主线,结合我国高质量人才的培养蓝图,提炼了化学观念、科学思维、科学探究与实践、科学态度与责任四个方面的核心素养发展要求。对于“初中化学课应如何有效拼接碎片化的课程内容,引导学生形成整合型的知识结构?如何科学融合学生学情,实现学科逻辑顺序与学生认知规律的高效融合?”等问题,新课标给出了优化的教学建议,即基于大概念来组织单元教学内容。以大概念为统领进行大单元教学,有利于教师把握教学内容的本质和关系,这就要求教师要深度挖掘教学材料,使课程内容结构化;以主题为引领,使课程内容情境化;开发多元的教学方法,使课程内容精品化,最终促进学生核心素养的稳步落实。
(二)课程内容的实施依据
“空气中氧气含量的测定”在初中化学中有着举足轻重的作用。沪教版化学教材中设置了“空气中氧气含量的测定”探究性实验,让学生通过实验探究了解化学是研究物质的组成、结构、性质以及变化规律的学科,掌握纯净物和混合物的区分方法以及质量守恒定律。“用红磷测定空气中氧气的含量”是新授课中做过的实验,该实验误差大且污染环境。在复习课中若重复该实验则稳固有余而知新不足,很难让学生提起学习劲头。因此在复习课中,教师应避免采用简单记忆和机械训练的复习模式,而是要形成大单元课程结构,梳理学生原有的知识内容,提出具有驱动性的学习任务,引导学生根据实验现象和细节展开质疑、推理、归纳、总结等学习活动,促进学生形成整体性知识体系,提高学生发现问题、分析问题和解决问题的能力,提升学生的核心素养。
(三)核心素养下的学习内容
“空气中氧气含量的测定”复习课所涉及的核心素养及其对应的学习内容如下。一是化学观念:以氧气的性质为核心内容构建大单元教学,探索空气的组成,掌握测定空气中氧气含量的原理及方法,同时建立起平衡与守恒思想。二是科学思维:对运用到的测定方法进行优缺点比较、分析、归纳和总结,能够针对实验中产生的误差进行独立的思考和判断,进而对传统的测量方式提出疑问和进行改进,形成科学思维。三是科学探究与实践:本课的教学设计中包含方法和实验,学生通过对实验装置的设计与搭建,增强动手操作及逻辑思考的能力,同时借助所学化学知识发现实验中的不足,并通过自主探究改进实验装置,解决实际问题。四是科学态度与责任:在探索和改进实验的过程中,着重强调实事求是的原则,让学生明白今天“正确”的结论,今后有可能成为“不正确”或“不够正确”的结论,从而培养学生质疑和求实的科学态度。
(四)大单元课程目标
(1)通过“空气中氧气含量测定实验的改进”探究活动,分析实验所用试剂以及对应的测定原理;(2)在实验探究过程中,经历发现问题、提出问题、分析问题、解决问题、改进完善的过程,逐渐提升逻辑思维能力和实验设计能力;(3)通过对多种实验装置的分析、评价和改进,选择适合的实验装置和方法,同时体验合作学习与实验操作带来的愉悦感;(4)通过改进和优化实验,发现实验的实际结果要比标准答案复杂得多,在面对出现的错误和偏差时,能不断地纠错,进而培养耐挫精神。
二、大单元教学的实践过程
[教师] “八月秋高风怒号,卷我屋上三重茅。”我们从杜甫的诗中可以感受到空气的存在。那么空气是单质还是混合物?我们要感谢在科学探索过程中敢于打破常规的科学家,让我们站在知识之巅,以最简单的方式认识空气。通常可通过什么实验来探究空气中的氧气含量呢?该实验的优缺点是什么?
[学生]用红磷燃烧法来测定。该方法的优点是反应现象明显,缺点是:①当燃着的红磷伸入集气瓶中,瓶内空气会瞬间受热膨胀逃逸;②当空气中氧气的含量降低到一定浓度之后,红磷就不能再继续燃烧;③反应产物P2O5会污染环境。
[教师]木炭、硫燃烧也消耗氧气,能否用这些物质代替红磷呢?
[学生]不可以。这些物质虽然能够消耗氧气,但产物是CO2、SO2等氣体,无法使装置内形成气压差。
评析:虽然经过近一年的化学学习,学生的基本化学素养有了大幅度提升,但学生仍缺乏灵活运用所学知识的能力,复习课伊始教师创设情境提出问题,可引导学生思考解决问题的方法。
[教师]既然木炭燃烧会产生CO2,增补消耗掉的氧气,那么我们可以使用能够吸收CO2的试剂,以消除CO2的干扰,进而准确测定空气中氧气的含量。可以选择哪种试剂?如何设计实验?
[学生活动]讨论并设计实验方案:先准确测量集气瓶内的总体积[V1],随后在集气瓶中加入体积为[V2]的足量的NaOH浓溶液,让蜡烛在集气瓶中燃烧,待冷却后打开止水夹,记录瓶中溶液的体积[V3]。集气瓶中溶液前后的体积差就是倒吸入的水的体积[ΔV=V3-V2],用倒吸入的水的体积除以集气瓶体积与NaOH浓溶液体积的差即可计算出空气中氧气的体积分数[φ(O2)=(V3-V2)/(V1-V2)×100%]。经过实验发现,用NaOH浓溶液吸收CO2后,计算得出的氧气体积分数接近但小于20%。
[教师]为什么使用NaOH浓溶液来吸收CO2,仍然不能准确测定空气中氧气的含量呢?请同学们根据演示实验过程分析原因。
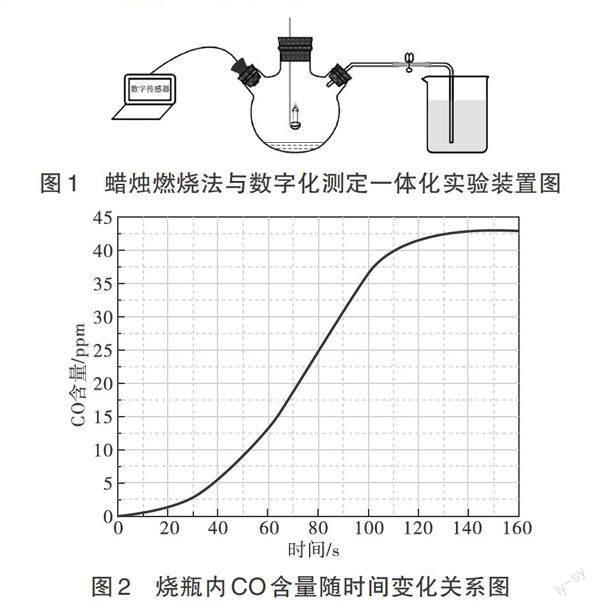
[演示实验]如图1所示,预先用水测量三颈烧瓶内部的体积(约250 mL),水倒出后在三颈烧瓶中加入15 mL的NaOH浓溶液,左侧瓶口连接CO数字化传感器,右侧瓶口连接导管,导管的另一端伸入烧杯中。随后,将点燃的蜡烛迅速伸入烧瓶中,蜡烛燃烧一段时间后熄灭。待烧瓶中温度恢复至室温后打开止水夹,水迅速倒吸入烧瓶中,用量筒量取烧瓶中的液体体积。此时CO数字化传感器的读数为42.7 ppm。
[学生]当氧气含量减少时,蜡烛不完全燃烧并产生CO气体,影响测定结果。
评析:由于实验结果和学生预判的结果大相径庭,促使学生带着强烈的好奇心,依据已有的知识和经验做出与问题相关的猜测,并设计解决问题的思路与方案,通过科学探究实验收集证据,修正猜想,得到合理的结论,充分揭示物质变化的普遍规律。
[教师]氧气是比较活泼的气体,能与大部分金属发生化学反应。请同学们使用金属材料设计实验方案,探究空气中氧气的含量。
[学生]选择铁丝锈蚀法,而非铁丝燃烧法,原因是铁丝无法在空气中燃烧。在含有酸或盐的环境中铁会加快生锈的速率,铁粉也可以加快反应速率,据此提出使用含有铁粉的“暖宝宝”作为反应物。
[实验步骤]①测量直筒玻璃杯的高度[H];②将“暖宝宝”粘在玻璃杯内壁;③将玻璃杯倒扣在水槽中;④记录玻璃杯内液体的高度[h];⑤根据玻璃杯内液面高度的变化,计算出氧气的体积分数[[φ(O2)=h/H×100%]]。(如图3)
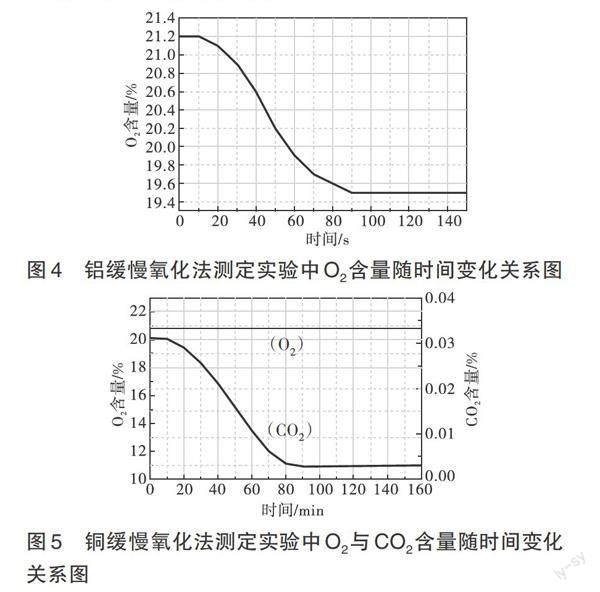
[资料提示]大部分金属在空气中都可以被氧化,如铝和铜,产物状态为固体。用铝和铜分别代替铁完成测定实验,并用数字化传感器测定实验装置内的氧气含量,得到的数据如图4和图5所示,请分析未能准确测定的原因。
[学生]铝表面氧化后会生成一层致密的氧化铝膜,阻止铝进一步氧化,导致实验失败;铜生锈的条件是铜、氧气、二氧化碳和水四种物质共同作用,而空气中二氧化碳的含量只有0.03%,当二氧化碳耗尽后铜不能再继续消耗氧气,导致实验失败。
[教师]改变反应条件,铜也可以用来测定空气中氧气的含量,那么需要什么样的反应条件呢?
[学生]灼烧铜时,铜可以和氧气反应,并且产物是固体,可以用来准确测定空气中氧气的含量。
[实验步骤]①检查装置气密性;②试管中装入足量的铜粉,旋紧橡胶塞,用止水夹夹紧橡胶管;③记录烧杯中水的初始体积[V1],将导管伸入烧杯中;④固定装置后加热试管底部;⑤停止加热,待试管冷却至室温后打开止水夹,取出导管,记录烧杯中水的体积[V2];⑥继续向试管中注水,记录试管的总体积[V3];⑦计算氧气的体积分数。
[教师]铜灼烧时,试管内部的气压会变大,活塞易被弹出,该如何控制试管内部气压?另外,试管内的气体不流通,会导致氧气不能充分反应,请同学们重新设计实验装置。
[实验改进]先提出在装置上方加一个气球,以达到缓冲气压的作用;再提出在玻璃管左右端各连接一个注射器,不但可以缓冲气压,还可以通过推拉针筒让气体流动,使金属与氧气充分反应,并可以直接从注射器上读取数据,准确便捷地获取消耗氧气的量。(如图6)
[教师]“择其善者而从之,其不善者而改之。”不同的测定方法各有优劣,遇到问题应像科学家一样辩证地去思考。
评析:测定空气中氧气含量的方法有很多种,归根结底取决于氧气的化学性质,而测量所用试剂的化学性质又决定了测定的方法。本环节旨在归纳总结测定空气中氧气含量的实验试剂以及对应测定方法的优缺点。
三、大单元教学反思
古人云:“学贵知疑,小疑则小进,大疑则大进。疑者,觉悟之机也。”化学是一门自然科学,也是一门变化的学科,它的发展存在着科学性与修正性。初中化学教师不仅要给学生教授知识,还要教会学生科学研究方法,使学生学会用化学思维方式认识世界,感知化学对人类社会文明所作出的贡献,培养终身学习的能力。
大单元教学可以使各个单元形成合力,例如以探究空气中的氧气含量为“大主题”,将物质的结构、氧气的化学性质、化学变化、金属的冶炼以及金属的防护和锈蚀等内容巧妙联系起来,将实验改进设置为“大过程”的指向性活动(包含教师活动和学生活动),把短小的、零散杂乱的学习活动串联在一起,形成贴近学生学情、整合学习内容、完善学习任务的过程链。总而言之,大单元课程设置可以重组化学知识模块,灵活把握教学方式,把化学学习与学生核心素养培养紧密联系起来。
[ 参 考 文 献 ]
[1] 中华人民共和国教育部.义务教育化学课程标准:2022年版[M].北京:北京师范大学出版社,2022.
[2] 王祖浩.义务教育教科书化学教师教学指导书:九年级上册[M].上海:上海教育出版社,2012.
(責任编辑 罗 艳)

