脑死亡器官捐献供体评估和供心选择临床分析
任琳玮,张熙伟,张辉,张歆杰,刘伟国,王东
1 山东第二医科大学临床医学院,山东潍坊 261053;2 山东大学齐鲁医学院;3 山东第一医科大学第一附属医院(山东省千佛山医院)心血管外科;4 山东第一医科大学第一附属医院(山东省千佛山医院)临床药学科
同种原位心脏移植手术是治疗终末期心力衰竭最有效的手段[1]。随着外科手术技术水平不断提高和新型抗排斥药物不断涌现,心脏移植手术日益成熟,该手术目前已在国内多家大型心脏中心常规开展。我国心脏移植供体来源主要为脑死亡器官捐献,但公民器官捐献意识匮乏,导致供心资源不足,而等待接受心脏移植手术患者众多,成为心脏移植的最大阻碍。据统计,我国每年等待接受心脏移植手术患者约3 000 例,而仅有500 例能够获得供心[2]。因此,积极宣传器官捐献、适当放宽供心选择标准、加强供体器官维护提高供心利用率等手段来解决供心缺乏,是当前心脏移植领域迫切需要解决的问题。传统的供心评估标准是由COPELAND 等于1995 年制定,即最佳供心应来源于脑死亡心不停跳供体,显然已不能满足临床需要,促使国内各大心脏移植中心制定自己的供心评估标准。2014年1月—2021年8月,山东第一医科大学第一附属医院(山东省千佛山医院)心脏外科共完成供心来源于脑死亡器官捐献的心脏移植手术73例,在供心选择上积累了一定的临床经验。本研究探讨了73 例脑死亡器官捐献供体评估和供心选择的临床经验。现报告如下。
1 资料与方法
1.1 临床资料 2014 年1 月—2021 年8 月山东第一医科大学第一附属医院(山东省千佛山医院)心脏外科共完成73 例脑死亡器官捐献的供心评估、维护、获取以及心脏移植手术。供心来源于器官获取组织主导的公民器官捐献,器官捐献者依据《中国脑死亡判定标准(成人)》[3]判定为脑死亡。脑死亡器官捐献者男52例、女21例,年龄16~51岁、中位年龄38岁,体质量60~110 kg、中位体质量78 kg,脑死亡原因:自发性脑出血17 例、脑外伤55 例、硫化氢中毒1例。心脏移植受者男55例、女18例,年龄16~68岁、中位年龄49岁,体质量38~90 kg、中位体质量65 kg,原发病:扩张型心肌病57 例、限制型心肌病2 例、缺血性心肌病11例、瓣膜性心肌病2例、甲亢性心肌病1例,NYHA心功能分级Ⅲ、Ⅳ级,经内科治疗无效或呈进行性加重。本研究经山东第一医科大学第一附属医院(山东省千佛山医院)伦理委员会批准。
1.2 供心管理 发现潜在供体,确定供者脑死亡后,评估并维护各器官功能,维持供者收缩压>100 mmHg、尿量>100 mL/h、动脉血氧分压>100 mmHg、血红蛋白>100 g/L。供心在体维护主要包括维持血流动力学、确保血容量充足、维持内环境稳定、预防性使用广谱抗生素、降低机体代谢、加强呼吸道管理;供心离体维护主要包括缩短热缺血时间、应用心肌保护液及缩短冷缺血时间。
1.2.1 供心在体维护 ①密切监测心率、血压,合理应用血管活性药物(如去甲肾上腺素、多巴胺、肾上腺素),尽可能应用单种血管活性药物,在血压、心率等生命体征平稳后减量或停用血管活性药物,联合或长期应用时务必多巴胺<10 µg/(kg·min)、肾上腺素<0.05µg/(kg·min)、去甲肾上腺素<0.1 µg/(kg·min),维持血流动力学稳定。②脑死亡供体因外伤出血、感染或其他并发症等出现血容量不足,需及时处理,确保血容量充足。如大量失血时及时输注同血型红细胞和血浆,合并尿崩症时予垂体后叶素。补足胶体溶液,维持正常胶体渗透压和出入量平衡,中心静脉压维持在8~12 mmHg 为宜。③纠正酸碱及离子平衡紊乱,维持内环境稳定。④预防性应用广谱抗生素,连续进行血培养、痰培养、尿培养等,积极寻找感染证据,根据培养结果调整使用敏感抗生素。⑤利用物理或药物降温的方法,控制心率,降低机体代谢消耗。⑥强化呼吸道管理,及时清除呼吸道分泌物,保持气道湿化,预防肺部感染等并发症,避免低氧血症发生。
1.2.2 供心离体维护 严格按照《中国心脏移植供心获取与保护技术规范》[4]获取供心,从主动脉根部灌注心肌停跳液并切开下腔静脉、左肺下静脉减压,尽量缩短供心热缺血时间;获取供心后立即使用冰生理盐水冲洗,置于装有冰屑的容器中检查有无损伤、结构异常及冠状动脉病变等,连续灌注UW 液2 000 mL,7 号丝线结扎标记左肺上静脉,置于UW液中保存,在0~4 ℃容器中转运并尽量减少转运时间[5]。
1.3 心脏移植手术方法 手术与麻醉由同一团队完成,在全麻低温体外循环下行双腔静脉法同种原位心脏移植术,上下腔静脉采用直角插管建立体外循环,用3-0 Prolene 线连续缝合吻合左心房,4-0 Prolene 线连续缝合依次吻合主动脉、下腔静脉、肺动脉和上腔静脉[5]。
2 结果
2.1 供体评估与供心选择 发现潜在供体,判定脑死亡状态,明确供体家属同意器官捐献后,评估供体,选择供心。供体评估项目及供心选择标准见表1。
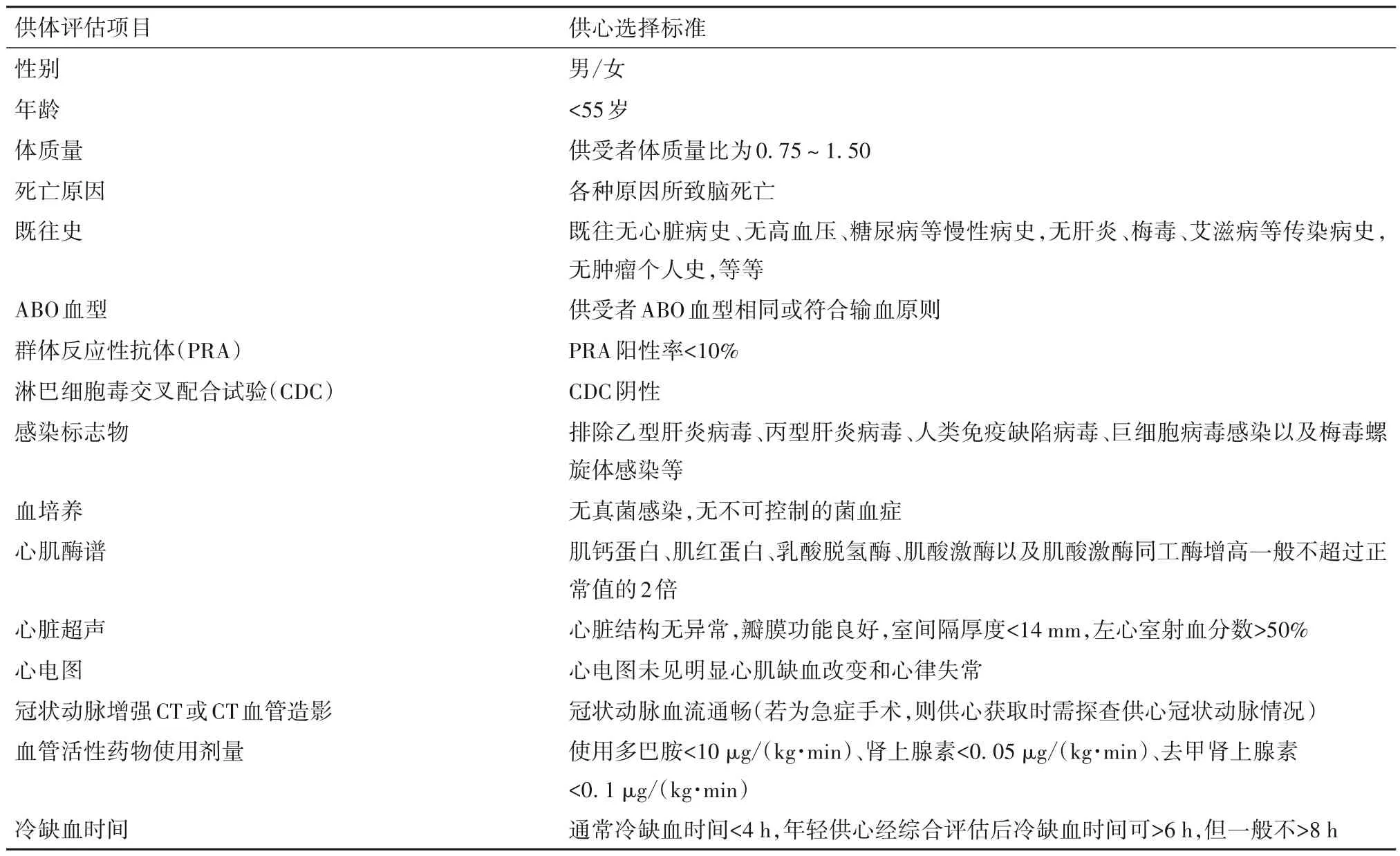
表1 供体评估项目及供心选择标准
2.2 心脏移植受者生存情况 73 例心脏移植受者手术成功率为94.5%(69/73),围手术期死亡4 例,其中2例因肺部重度感染导致呼吸衰竭死亡、1例因多脏器功能衰竭死亡、1 例因脑出血导致脑疝死亡。术后随访1 年,其间死亡4 例,1 例因口服减肥药导致抗排斥药物吸收障碍发生排斥反应死亡、1 例因自行减少抗排斥药物后发生排斥反应导致恶性心律失常死亡、2例因感染卡氏肺孢子虫病死亡。
2.3 边缘供体使用情况
2.3.1 高龄 使用年龄<45 岁的供心56 例,其中2例术中应用主动脉内球囊反搏(IABP)辅助,1 例术中联合应用IABP 及体外膜肺氧合(ECMO)辅助,其余病例术中复跳和停机顺利,术后心功能良好,未使用呼吸循环辅助装置。使用年龄45~50 岁的供心16例,供心冷缺血时间>4 h受者有11例出现不同程度心室收缩乏力,分别予以延长辅助时间、使用IABP和(或)ECMO辅助,顺利停机出院。使用年龄>51 岁的供心1 例,受者术前予以气管插管及ECMO辅助,由于紧急情况遂使用边缘供体,术后继续予以ECMO 辅助,逐渐降低血管活性药物剂量,撤除ECMO,最后顺利出院。
2.3.2 供受体体质量不匹配 供者体质量较受者偏低2 例,其中1 例受者术前检查提示肺动脉高压,心脏移植后出现低心排血量综合征,尝试停机失败,予ECMO 辅助后回到监护室;获取体质量匹配更为理想的供体进行二次心脏移植,手术顺利,术后呼吸机辅助呼吸51 h,ECMO 辅助98 h,心外监护室停留13 天,住院38 天顺利出院。另1 例术中出现心肌顿抑,予IABP 和ECMO 辅助,并在大剂量升压药物维持下勉强脱机;术后予去甲肾上腺素、肾上腺素及多巴胺等血管活性药物维持,ECMO辅助97 h、IABP辅助136 h 后顺利撤除,心外监护室停留8 天,住院35天顺利出院。
2.3.3 供体中毒 供体为硫化氢中毒1 例,受者手术顺利,术后呼吸机辅助13 h,心外监护室停留7天,住院30天顺利出院,随访1年心功能良好。
2.3.4 供心冷缺血时间长 冷缺血时间115~429 min。冷缺血时间<4 h 30 例。冷缺血时间≥4 h 43 例(包括冷缺血时间>6 h 9 例),其中9 例心脏移植受者心脏复跳后肺动脉阻力高,右心室收缩无力,予IABP 和(或)ECMO 辅助停机;1 例冷缺血时间长达429 min,予IABP 和ECMO 辅助,64 h撤除ECMO,179 h 撤除IABP,受者术后无法脱离呼吸机而行气管切开,术后80天转入当地医院继续治疗,术后1年患者死亡。其余病例术后4~6周顺利出院。
3 讨论
随着医学科技水平不断进步,心脏移植手术成为当前终末期心力衰竭最有效的治疗手段。但因心脏供体缺乏,再加上配型困难,严重制约了心脏移植手术开展。传统的供心评估标准是由COPELAND等于1995 年制定,即最佳供心应来源于脑死亡心不停跳供体,显然已不能满足临床需要,促使国内各大心脏移植中心制定自己的供心评估标准。供心的选择不但能够影响心脏移植手术成功率,还能影响受者预后和生活质量。近年来,由于对供心的需求不断增加,供心的选择标准在不断放宽,各心脏移植中心不断尝试突破原指南的供心选择标准,提出了边缘供体的概念。
山东第一医科大学第一附属医院(山东省千佛山医院)心脏外科完成的73例脑死亡器官捐献心脏移植手术,选择供心时一般要求供体年龄<50 岁、供受体体质量相差不大、供心结构正常、供心功能正常、热缺血时间<5 min、冷缺血时间<4 h、供体无感染或中毒,但也会根据实际情况而放宽供心选择标准。
3.1 供体年龄 由于供体缺乏问题日益突出,《中国心脏移植供心获取与保护技术规范》对心脏供体年龄逐渐放宽至50 岁,边缘供体甚至放宽至55岁[4]。但目前安全的供体年龄上限尚无标准。有研究表明,接受老龄供心与接受年轻供心的受者术后生存率比较差异无统计学意义,但接受老龄供心的受者罹患冠状动脉粥样硬化性心脏病的风险更高[6],这可能与其血管内皮功能减退有关。国际心肺移植协会(ISHLT)指出,心脏供体年龄越大,受者心脏移植术后病死风险越高[7]。另外,高龄心脏供体还可增加心脏移植术后其他器官衰竭的发生风险。我们认为,年龄<45 岁的供心一般能够耐受较长时间的冷缺血,而年龄45~50 岁的供心,若预计冷缺血时间<4 h亦可接受。但在接受高龄供心时要权衡利弊,对病情危重的受者,接受高龄供心可能比继续等待获益大。
3.2 供体体质量 ISHLT 推荐,供体与受体体质量相差不应超过30%[8]。对于大多数受者来说,体质量75 kg 左右的成年男性供心非常合适。供体体质量虽然不能决定受者术后生存率,但供心大小非常重要,心脏大小匹配的参数应当接近。如男性供者为女性受者供心,即使是供者体质量较小,若供心符合受体所需心脏的大小,亦可为受者提供充足的心排血量,继而克服受体的肺血管阻力。我们建议,尽可能选择体质量较大的供体,供受体体质量比值不应低于0.8。若受者术前超声心动图提示可能存在肺动脉高压时,较大的供心是有利的。此外,若紧急情况下选择与受体体质量相差较大的供心,术中出现低心排血量综合征和术后出现心功能不全时,应用IABP 辅助减轻心脏后负荷,改善心功能,或者联合应用ECMO保护性肺通气,降低心脏前后负荷,改善心肺功能。近年来,女性供体、男性受体这种性别错配问题成为心脏移植术后死亡率增加的重要危险因素[9]。2014 年REED 等[10]首次提出预测心脏质量(PHM)这一概念。有研究表明,基于PHM 的心脏移植供受者匹配标准能更有效地预测心脏移植患者预后[11],故进一步研究PHM是非常有必要的。
3.3 供心结构 理论上,供体既往要无心脏病史,心脏结构无异常,左心室射血分数≥50%,冠状动脉血流通畅。因等待心脏移植患者众多,对简单先天性心脏病或轻度二尖瓣、主动脉瓣畸形的供心也可用于心脏移植,通常不影响受者近期生存率。供心冠状动脉病变较轻时,心脏移植后血管病变不会加重。当供心左心室室壁厚度≥14 mm时,受者术后生存率显著降低,特别是当供体合并高血压以及冷缺血时间延长时,对受者长期生存率的影响较大[12]。KUPPAHALLY 等[13]研究认为,接受患有高血压供体的供心,心脏移植术后心室肥厚会加重,应积极控制血压抑制心室壁增厚。若将心室肥厚的供心用于危重受者,并且受者术前应用心室辅助装置,手术时体外循环时间会延长,这也是导致受者死亡率增加的危险因素。我们认为,若供体脑死亡的原发病为高血压脑出血时,术前需行心脏超声评估左心室室壁厚度,行冠状动脉增强CT 或CT 血管造影评估供心冠状动脉病变情况,弃用有左心室肥厚的供心,紧急情况时可使用轻度冠状动脉病变的边缘供心,但术后要长期监测冠状动脉血流情况。若受者出现冠状动脉严重狭窄,行冠状动脉搭桥治疗,其长期存活率可能不受影响。若供体血流动力学不稳定且血管活性药物无法维持或需要长期大剂量药物维持时,弃用此供心。
3.4 供体感染或中毒 供体感染是心脏移植术后受体早期死亡的主要原因之一。国内专家共识推荐,同时满足以下条件感染者可考虑为供体:供者为社区性感染且在96 h 内死亡;供体接受针对致病菌的特异性抗感染治疗;供体获取前多次血培养、痰培养等均为阴性;供心心功能正常且未发现感染性心内膜炎。此类供心移植后需连续血培养1 周,预防性使用广谱抗生素。有感染证据的,针对病原菌进行特异性治疗[4,14]。有研究报道,供体巨细胞病毒(CMV)血清抗体阳性与受体远期死亡风险增加密切相关[15]。受者移植后在远期各种微生物感染中以CMV 感染率最高,故弃用CMV 感染的供心。ALTSHULER 等[16]研究认为,丙型肝炎病毒(HCV)阳性供体不影响术后早期生存率。吴敏等[17]研究发现,乙型肝炎病毒(HBV)阳性供体移植于HBV 阴性受体,术后受体经乙肝免疫球蛋白治疗未感染HBV,该研究认为除肝脏移植外,其他实体器官移植时乙型肝炎的传染性不强。但HBV、HCV 阳性的供心安全性尚不明确。而目前对于使用硫化氢等中毒的供心数据较少,尚需进一步研究。
3.5 供心心肌保护 供心离体后的心肌保护主要有两个时期:热缺血时期和冷缺血时期。热缺血时间是指器官从供体供血停止到冷灌注开始的这段时间,此时间段心脏受损最为严重,心脏尽快停跳是此时期心肌保护的重点。本院心脏获取团队配合熟练,通常能将热缺血时间控制在5 min 左右,建议不应超过10 min。冷缺血时间是指供心获取后冷灌注开始至移植后心脏恢复供血的这段时间,此时间段心脏完全缺血缺氧,目前的心肌保护技术可安全保存供心3~4 h。ISHLT 推荐,供心冷缺血时间一般<4 h,年轻供心经综合评估后可>6 h,但一般不>8 h。JOHN 等[18]研究报道,年龄≤18 岁的供者供心衰竭与冷缺血时间无明显相关性,但对于18岁以上的供者来说,冷缺血时间>4 h 会显著降低受者的存活率。我们认为,虽然供心管理技术的进步在一定程度上减轻了较长冷缺血时间对供心带来的负面影响,但尽量缩短冷缺血时间仍然是必要的,建议冷缺血时间<6 h,仅有少部分心功能极佳且应用极少量正性肌力药物的年轻供心可忍受较长时间的冷缺血。
综上所述,供受体最大限度匹配可使心脏移植患者获益最大;同时,适当放宽供心选择标准,增加供心数量,将为众多等待心脏移植患者带来希望。但应避免盲目扩大使用边缘供心,从而影响受者的远期生存率和生活质量。

