胰腺罕见碰撞肿瘤:胰腺导管腺癌合并神经内分泌肿瘤1例
蓝传强 周永进 胡玉敏 胡伟铭 沈菲菲 纪建松
患者男,74岁。因健康体检B超检查发现胰腺囊性肿物于2018年12月7日在丽水市中心医院就诊。入院后查体:体温37℃,呼吸20次/min,心率60次/min,血压151/85 mmHg(1 mmHg=0.133 kPa),全身皮肤、巩膜无黄染,腹平软、全腹无压痛及反跳痛,无明显包块,肝区叩击痛阴性,移动性浊音阴性,Murphy征阴性。患者有糖尿病10年,高血压1级5年,既往有肠穿孔手术史。实验室检查:CA19-9为180.8 U/ml,CA50为 65.42 U/ml,癌胚抗原(CEA)、CA125等其他肿瘤指标正常,大便隐血试验+,肝肾功能、血常规、小便常规基本正常。影像学检查:B超检查示胰腺颈体部65 mm×62 mm液性暗区,内透声差,囊壁可见数个强回声结节,彩色多普勒未见明显血流信号;远端胰腺萎缩,胰管明显扩张(图1)。腹部增强CT检查示胰颈体部囊实性肿块,肿块最大径约为69 mm×68 mm,囊壁可见结节,囊性部分似与胰管相通;平扫示实性部分密度不均,增强扫描示部分实性成分呈轻度延迟强化,部分实性成分中度强化、强化峰值为门脉期;囊性部分不强化;胰腺尾部萎缩,体尾部胰管明显扩张,直径约13 mm,诊断为恶性导管内乳头状黏液性肿瘤(intraductal papillary mucinous neoplasm,IPMN),囊腺瘤待排(图2)。患者于12月13日行经腹腔镜下全胰切除+脾脏切除术,术中所见:胰颈体部可见一约8 cm×7 cm×6 cm大小囊实性肿块,边界欠清。肿块与结肠系膜致密黏连。远端胰腺萎缩,胰管明显扩张,内见灰白色瘤栓。近端胰腺质地偏硬,剖面呈黄白色。快速病理检查:胰颈体尾低级别浆液性肿瘤伴退变坏死、累及神经及手术切缘,脾脏无殊。最终病理检查结果诊断为低分化胰腺导管腺癌(pancreatic ductal adenocarcinoma,PDAC)伴潴留囊肿形成,其中可见导管原位癌成分,合并弥漫性胰腺神经内分泌肿瘤(pancreatic neuroendocrine neoplasm,pNEN)G1期,侵犯神经。免疫组化:导管腺癌成分ER(-)、PR(-)、Ki-67(+)(80%)、CK19(+)、CK7(+)、CerbB-2(-);神经内分泌肿瘤CgA(+)、CD56(+)、Syn(-)、Ki-67(+)(<2%)。最终诊断为PDAC合并pNEN的碰撞肿瘤(图3,插页)。
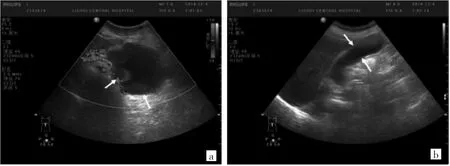
图1 B超检查结果图[a:超声检查示胰腺颈体部囊实性肿块,囊壁可见多个结节状强回声(箭头所示),彩色多普勒血流显像未见明显血流信号;b:胰管明显扩张(箭头所示)]
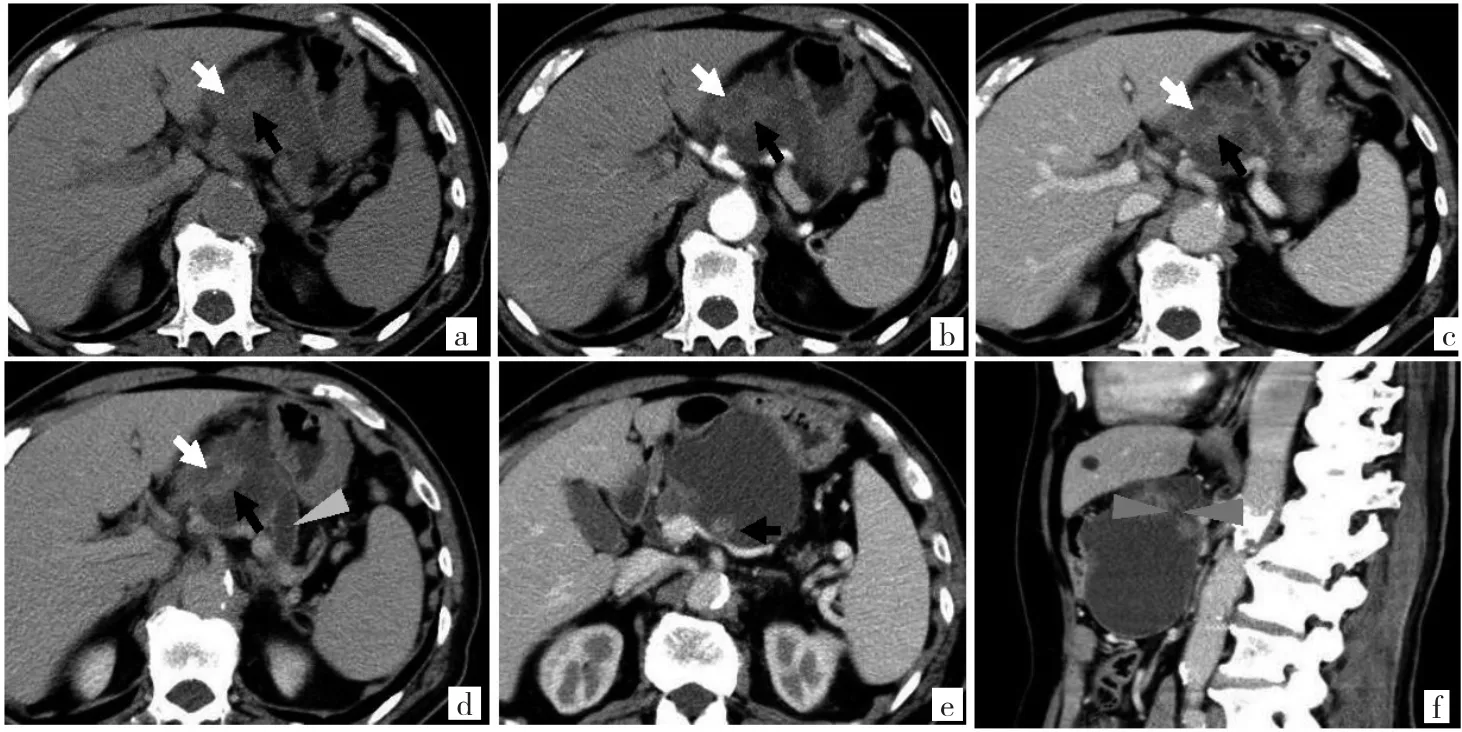
图2 腹部增强CT检查图[a-d:部分实性成分(白箭所示)呈轻度延迟强化,平扫CT值32 Hu,动脉期34 Hu,门脉期44 Hu,延迟期52 Hu,另一部分实性成分中度强化(黑箭所示),平扫CT值34 Hu,动脉期47 Hu,门脉期70 Hu,延迟期63 Hu;胰腺远端萎缩,胰腺体尾部胰管明显扩张(三角所示);e:囊壁可见中度强化实性结节(黑箭所示),强化峰值为门脉期;f:囊性部分向下生长,局部似与胰管相通(三角所示),囊壁菲薄,内未见分隔,囊壁轻度强化]

图3 病理检查结果图[a:胰腺导管腺癌(白箭)与神经内分泌肿瘤(黑箭)并存,两种肿瘤成分有一定的分界;b:胰腺的碰撞肿瘤滑动视图,下方见低分化胰腺导管腺癌肿瘤细胞(红五角),上方见散在神经内分泌肿瘤细胞(红三角),两者之间存在明确分界(HE染色,×10);c:低分化导管腺癌(HE染色,×10);d:神经内分泌肿瘤(G1)(HE染色,×10);e:神经内分泌区CD56+(HE染色,×10);f:神经内分泌区CgA+(HE染色,×10)]
讨论碰撞肿瘤是指在原发于同一宿主、同一器官的或部位两种或多种共存的肿瘤,且各肿瘤成分间无混合及移行状态,消化系统常见,而发生在胰腺的碰撞肿瘤较为少见[1]。IPMN合并pNEN、胆管癌合并胰腺癌、实性假乳头状肿瘤合并pNEN等碰撞肿瘤此前已有报道[2]。本文报道1例罕见PDAC合并pNEN(G1期),并对其影像学特征进行回顾分析,以期为该罕见碰撞肿瘤的诊断提供一些思路。
碰撞肿瘤的发生机制尚不明确,目前提出3条推论来解释其发生机制[3]:(1)一种肿瘤周围微环境发生改变,导致另一种原发肿瘤或转移瘤周边生长的可能性增加;(2)来源不同的两种或多种肿瘤偶然并发在同一部位;(3)两种肿瘤来源于同一胚胎多能干细胞。但有其他学者提出不同的理论,其发生机制仍有待进一步分析。
通过回顾性对照分析此患者CT及病理检查结果,笔者观察到增强CT图像上两种不同强化模式的成分,在对应的病理检查图上有明确界限,其意义在于当影像学检查图上观察到符合发生于该脏器的不同两种肿瘤的特性时,应该拓展思路,考虑是否发生碰撞肿瘤,当然作出此类诊断应十分慎重,如该病灶中的低强化区为明确的延迟强化而不是坏死区域,此强化特点符合PDAC,而病灶内的壁结节强化为明显高于且不同于低强化区较明显的强化特征,符合pNEN G1期强化特点。根据既往报道,胰腺碰撞肿瘤影像学表现复杂,误诊、漏诊率高,主要原因包括[4]:(1)主瘤灶较明显,副瘤灶位于边缘且小而平坦,易造成副瘤灶的漏诊;(2)两种或两种以上瘤灶并存,各肿瘤的影像学特征易相互掩盖、混淆;(3)同一器官的多个瘤灶影像学表现类似良性病变。因此,虽然有相关文献对胰腺碰撞肿瘤进行影像学特征分析,其诊断仍十分困难。
胰腺PDAC合并pNEN碰撞肿瘤的诊断主要依靠病理学明确,靠影像学诊断十分困难。胰腺碰撞肿瘤在治疗上目前仍以手术为主,术后辅以放化疗。Ryan等[5]认为碰撞肿瘤应根据肿瘤相关的组织学类型及患者的身体状态应来选择是否手术和合适的辅助治疗。碰撞恶性肿瘤的预后与其发生的肿瘤类型密切相关,Kim等[6]认为碰撞肿瘤中通常有恶性肿瘤共存,预后较差,且比单发恶性肿瘤的预后更差。本例患者术后接受辅助放化疗,术后8个月出现胰腺导管腺癌肝脏多发转移瘤,随访1年后死亡。
本文报道罕见PDAC合并pNEN碰撞肿瘤,通过回顾分析其临床、影像学及病理特征,有助于临床医师更深入认识该类肿瘤,在临床工作中可以拓展思路,警惕此类恶性碰撞肿瘤发生的可能性,及时诊断以及有效的术前评估对患者生存期的提升具有重要意义。

