食管鳞癌免疫治疗序贯放疗后放射性肺炎的危险因素分析
杨静 庄蕾 曾剑 张丹红 陈影 孙晶晶 杜向慧 盛李明
同步放化疗是局部晚期食管癌的标准治疗方法,然而随着以免疫检查点抑制剂为代表的免疫治疗在晚期食管鳞癌上的广泛应用,免疫治疗也逐渐应用于局部晚期食管癌[1-2]。目前有两种应用方法,第一种是类似局部晚期不可切除非小细胞肺癌的同步放化疗序贯免疫治疗的PACIFIC研究模式,第二种是同步放化疗前进行免疫诱导治疗。免疫治疗联合放疗是否会增加放射性肺炎的发生率和严重程度,以及如何在局部晚期食管癌患者免疫诱导治疗后对正常肺放疗照射剂量进行限制,以降低放射性肺炎的发生率,成为当前需要关注的问题。笔者对接受免疫检查点抑制剂联合化疗后进行根治性放疗的局部晚期食管鳞癌患者进行回顾性分析,计算治疗后放射性肺炎的发生率,以临床病理因素以及剂量学参数角度探讨放射性肺炎的危险因素。
1 对象和方法
1.1 对象 选择2020年1月至2021年8月浙江省肿瘤医院收治局部晚期食管癌患者107例,其中男101例,女6例;年龄≤65岁62例,>65岁45例。纳入标准:(1)治疗前病理学检查证实为局部晚期食管鳞癌;(2)放疗前接受了2个周期以上免疫治疗联合化疗的诱导治疗;(3)诱导治疗后仍无法进行手术治疗或拒绝手术治疗;(4)已接受50 Gy以上的根治性放疗;(5)免疫抑制剂诱导治疗期间未出现免疫相关肺炎;(6)有详细的放疗后半年内随访资料和胸部CT检查结果。本研究经浙江省肿瘤医院医学伦理委员会批准。
1.2 免疫联合化疗的诱导治疗 采用紫杉醇+铂类的双药联合化疗,紫杉醇主要选择白蛋白紫杉醇(260 mg/m2,第1天)或者紫杉醇(175 mg/m2,第1天),铂类主要选择卡铂(具体剂量根据性别、年龄、肌酐清除率及AUC=5计算得出);免疫治疗药物主要有卡瑞利珠单抗(中国恒瑞有限公司,规格:200 mg/支,200 mg/周期)、帕博丽珠单抗(美国默沙东公司,规格:100 mg/支,200 mg/周期)、信迪利单抗(中国信达公司,规格:100 mg/支,200 mg/周期)以及替雷丽珠单抗(中国百济神州公司,规格:100 mg/支,200 mg/周期)等,与化疗药物同1天静脉滴注治疗,先输注免疫药物,再输注化疗药物;间隔3周进行下一个治疗周期,诱导治疗结束后进行食管增强CT和胃镜检查,然后进行食管癌根治性放疗。
1.3 放射治疗 患者取仰卧位,双上肢下垂置于体侧,热塑体膜固定,进行增强CT定位扫描,扫描范围颈部锁骨上、胸部加上腹部,层厚5 mm;结合患者的食管造影、胃镜、超声胃镜、胸部CT以及PET-CT等检查结果进行食管癌根治性放疗靶区勾画,GTVeso为食管原发病灶,GTVnd为肿大转移淋巴结,临床靶区(CTV)包含GTVeso、GTVnd和周围淋巴引流区,并在GTVeso上下外放3~5 cm,水平外放0.5~1.0 cm;计划靶体积(PTV)为CTV均匀外放0.5 cm,处方剂量为50.4~66.0 Gy、1.8~2.0 Gy/d、5次/周,主要危及器官勾画双肺、心脏和脊髓,危及器官限量如下:脊髓最高剂量≤45 Gy,双肺V5Gy<55%,V20Gy<28%,V30Gy<20%,平均肺剂量(mean lung dose,MLD)<15 Gy,心脏V40Gy<40%,应用剂量体积直方图(dose volume histogram,DVH)计算危及器官受累剂量。
1.4 放射性肺炎分级 放疗开始后观察患者咳嗽、咳痰以及呼吸情况,必要时进行胸部CT平扫检查,使用美国国立癌症研究所常见不良反应术语评定标准5.0版(CTCAE 5.0)进行放射性肺炎分级评价,1级:无症状,仅放射学表现;2级:有症状,但不影响日常生活能力;3级:有症状,影响日常生活能力,需要吸氧;4级:危及生命,需要机械通气治疗;5级:死亡。
1.5 治疗疗效判断标准 采用实体瘤疗效评价标准(response evaluation criteria in solid tumors,RECIST 1.1)进行诱导治疗疗效评价,完全缓解(complete response,CR):所有病灶消失;部分缓解(partial response,PR):病灶最长径与基线状态相比,至少减少30%;病变进展(progression disease,PD):病灶最长径与基线状态相比,增加了20%,或出现了新发病灶;疾病稳定(stable disease,SD):疗效介于PR和PD之间。
1.6 统计学处理 采用SPSS 25.0统计软件。计数资料的比较采用χ2检验;绘制ROC曲线,通过AUC计算双肺剂量学参数V5Gy、V20Gy、V30Gy和MLD的最佳截断值;使用Kaplan-Meier法绘制生存曲线,logistic回归模型计算2级以上放射性肺炎的危险因素,将单因素分析中P<0.05者纳入多因素logistic回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 一般临床资料 107例患者中有吸烟史82例(76.6%);肿瘤位于颈段4例,胸上段13例,胸中段52例,胸下段38例;肿瘤最大径2~14 cm;诱导化疗时使用白蛋白紫杉醇91例,紫杉醇16例;接受免疫药物卡瑞利珠单抗患者67例,帕博利珠单抗23例,信迪利单抗11例,替雷利珠单抗6例;免疫治疗联合化疗后达到CR 3例,PR 35例,SD 63例,PD 6例,治疗后拒绝手术治疗35例,无法手术切除72例;免疫治疗至开始放疗时间范围1~98 d,中位时间36 d;根治性放疗后接受免疫维持治疗27例。
2.2 临床特征与放射性肺炎的关系 放疗后出现2级及以上放射性肺炎23例(21.5%),其中2级16例,3级6例,5级1例;诱导治疗周期数≥3个周期和<3个周期的患者分别有18例(31.6%)和5例(10.0%)出现了2级以上放射性肺炎,组间比较差异有统计学意义(P<0.05);放射性肺炎<2级患者的双肺V5Gy、V20Gy、V30Gy和MLD剂量占比均高于≥2级患者,差异均有统计学意义(均P<0.05),而性别、年龄、是否吸烟、诱导化疗药物、免疫检查点抑制剂、免疫放疗间隔时间、放疗剂量、免疫维持等方面在放射性肺炎<2级和≥2级患者间比较差异均无统计学意义(均P>0.05),见表1。

表1 107例食管鳞癌患者临床特征与放射性肺炎的关系[例(%)]
2.3 放射剂量学参数与放射性肺炎的关系 双肺剂量学参数的最佳截断值分别为V5Gy=45%(AUC=0.756,P<0.01)、V20Gy=17%(AUC=0.731,P<0.01)、V30Gy=8%(AUC=0.728,P<0.01)和 MLD=9.5 Gy(AUC=0.734,P<0.01),见图 1;单因素分析显示 V5Gy≥45%、V20Gy≥17%、V30Gy≥8%和MLD≥9.5 Gy均为放射性肺炎的危险因素(均P<0.05),多因素logistic分析显示诱导治疗周期数和双肺V5Gy是发生放射性肺炎的独立危险因素,诱导治疗周期数在3个周期以上患者的放射性肺炎发生风险是2个周期内患者的3.93倍,双肺V5Gy≥45%患者的放射性肺炎发生风险是V5Gy<45%的3.87倍,见表2。

表2 107例食管鳞癌患者临床病理资料与放射性肺炎的单、多因素logistic回归分析
3 讨论
以抗程序性死亡蛋白1/程序性死亡受体-配体1(programmed cell death 1/programmed cell death 1 ligand 1,PD-1/PD-L1)为代表的免疫检查点抑制剂成为当前实体瘤治疗主要进展,在食管癌领域也取得了一定进展。有研究显示,可手术食管癌及食管胃结合部癌进行术后辅助免疫治疗能够明显延长无疾病进展生存时间[3];晚期食管癌二线治疗中应用纳武单抗[4]、帕博利珠单抗[5]或卡瑞利珠单抗[6]均能够有效改善患者生存情况;一线治疗中化疗联合免疫治疗患者与单纯化疗患者相比,总生存时间明显延长[7-8];目前在局部晚期不可手术的食管癌中,免疫治疗联合同步放化疗的随机多中心临床试验也正在开展之中[9]。
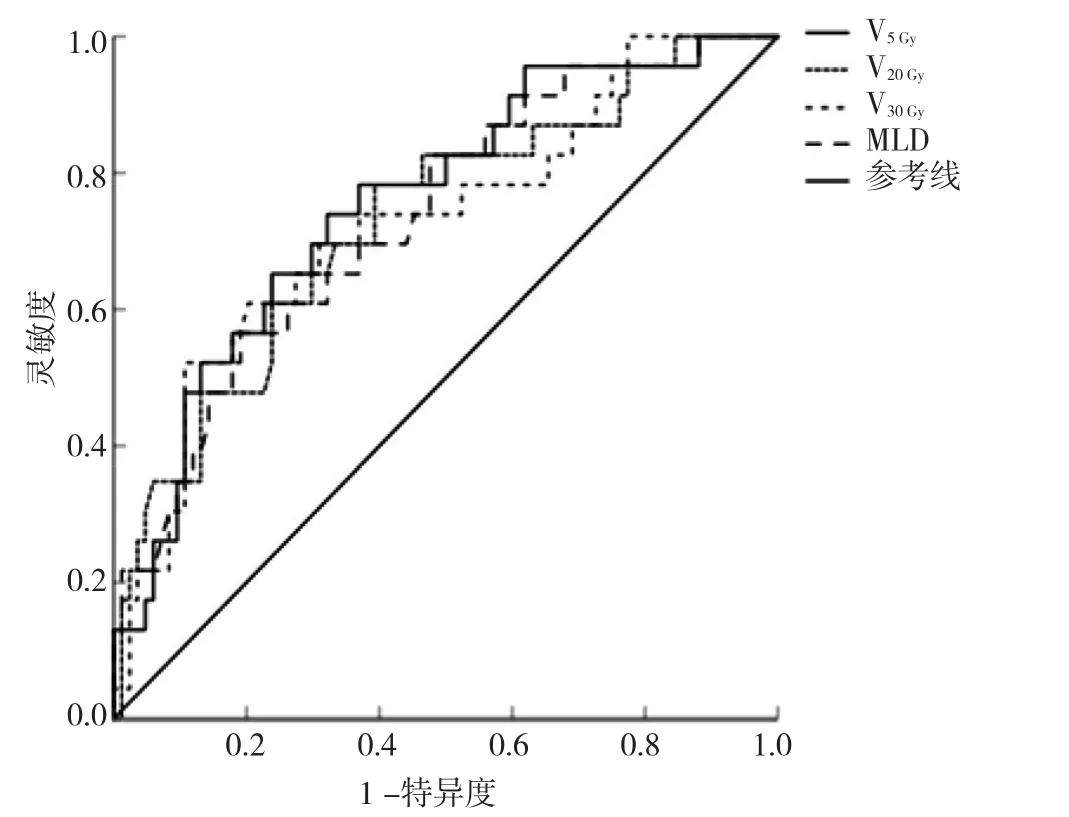
图1 双肺剂量学参数V5 Gy、V20 Gy、V30 Gy和MLD预测放射性肺炎的ROC曲线
免疫治疗和放疗有着天然的协同作用[10-11],然而两者都对正常肺组织有着不可避免的毒性损伤,两者联合使用是否会增加放射性肺炎的发生风险?这个问题目前仍没有答案,在既往的研究中,同步放化疗前应用肺毒性同样明显的吉西他滨会增加放射性肺炎的发生概率[12]。因此本研究对接受免疫联合化疗诱导治疗后进行根治性放疗的局部晚期食管癌患者进行回顾性分析,结果发现2级及以上放射性肺炎发生率为21.5%,这与食管癌根治性放化疗的历史数据类似[13];免疫治疗的诱导周期数与放射性肺炎的发生有着直接关系,而免疫治疗与放疗的间隔时间、不同的免疫药物之间以及是否进行免疫维持治疗与放射性肺炎无关。
许多临床研究结果表明非小细胞肺癌患者免疫治疗联合放疗的治疗模式下肺炎的发生率会有所上升。有研究显示,既往接受放疗的患者免疫治疗后出现任意级别肺炎的发生率高达63%,而未接受过放疗患者为40%[14];帕博利珠单抗联合立体定向放射治疗(8 Gy×3 F)治疗后出现放射性肺炎的风险较单纯免疫治疗的患者高(26%比8%)[15];PACIFIC模式的真实世界研究中同步放化疗后德瓦鲁单抗维持治疗组有症状的肺炎发生率为18%[16]。然而关于食管鳞癌免疫检查点抑制剂诱导治疗序贯根治性放疗后放射性肺炎的情况仍罕见报道,Bi等[17]回顾性分析了40例免疫诱导治疗后进行胸部放疗患者的放射性肺炎发生情况,结果发现2级以上放射性肺炎发生率为17.5%,V20Gy和MLD与放射性肺炎的关系密切,但是这个研究的异质性非常明显,食管癌只占了20%,而且疾病分期跨度较大,根治性放疗患者只有19例。而本研究均为局部晚期食管鳞癌患者,病例数也相对较大,因此更加具有临床应用价值。本研究团队正在启动免疫检查点抑制剂诱导治疗后胸部根治性放疗的剂量学的前瞻性研究,希望能为接受免疫治疗联合放射治疗的食管癌、肺癌患者如何减少放射性肺炎提供新的依据。
综上所述,局部晚期食管鳞癌免疫检查点抑制剂诱导治疗序贯根治性放疗后放射性肺炎的发生率与既往同步放化疗的数据是类似的,诱导治疗周期数和双肺剂量学参数V5Gy是发生放射性肺炎的独立危险因素。

