CT灌注成像预测贝伐珠单抗治疗晚期非鳞非小细胞肺癌的疗效研究
丁玲玉 吴昂 杨京京 张艳 杨秋霞 孟铁豹 钱新宇
肺癌是世界范围内最常见导致死亡的癌症[1]。大部分患者确诊时已处于晚期,靶向治疗和免疫治疗能使晚期肺癌患者5年生存率提高到15%~50%[2-4]。目前化疗仍然占据了重要地位,但疗效却有待提高。血管内皮生长因子A(vascular endothelial growth factor A,VEGF-A)单克隆抗体(贝伐珠单抗)联合含铂双药标准化疗在晚期非鳞非小细胞肺癌(non-squamous nonsmall-cell lung cancer,ns-NSCLC)中疗效较好[5-7]。肿瘤具有明显的组织类型及分子分型异质性,筛选出贝伐珠单抗治疗有效的患者非常重要。贝伐珠单抗通过阻断肿瘤血管新生,影响肿瘤的微环境而发挥抗肿瘤作用[8-9]。传统的实体瘤疗效评价标准(response evaluation criteria in solid tumors,RECIST)主要考虑肿瘤病灶的大小,无法评估肿瘤的血供及活性,不能较好地反映贝伐珠单抗的疗效。CT灌注成像对肿瘤感兴趣区(region of interest,ROI)的层面进行连续扫描,计算各种灌注参数值,反映肿瘤内部血流灌注情况以及肿瘤组织的血流微循环规律[10]。随着对CT灌注成像研究的深入,开展了一些CT灌注成像与肺癌化疗、放疗疗效相关性的研究[11-12]。本研究旨在探索在晚期ns-NSCLC患者中,目标肿瘤的CT灌注成像是否能评估培美曲塞/顺铂联合贝伐珠单抗治疗的疗效,以及CT灌注成像参数的动态变化与RECIST标准评价的疗效之间的相关性,为临床治疗提供参考。
1 对象和方法
1.1 对象 收集2017年12月至2020年1月杭州市肿瘤医院18例和中山大学附属肿瘤医院6例晚期ns-NSCLC患者共24例,男15例,女9例,年龄32~74岁,中位年龄57(41,65)岁;均为Ⅳ期肺癌。24例患者中19例(79.2%)美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体能状态(performance status,PS)为1分,有吸烟史9例(37.5%)。组织类型:腺癌23例(95.8%),大细胞癌1例(4.2%)。表皮生长因子受体(epidermal growth factor receptor,EGFR)基因敏感突变5例,淋巴瘤激酶(anaplastic lymphoma kinase,ALK)基因融合阳性1例,经口服靶向药物治疗进展后,二线予培美曲塞/顺铂/贝伐珠单抗方案。纳入标准:(1)年龄18岁以上;(2)经组织学或细胞学检查证实为局部晚期、复发或转移的ns-NSCLC患者;(3)既往未经治疗,除驱动基因阳性经口服靶向药治疗外;(4)ECOG PS为0~2分;(5)有RECIST 1.1版所定义的可测量或可评价的病灶;(6)血常规、肝肾功能检查结果基本正常。排除标准:(1)主要组织学类型为鳞状细胞癌;(2)有2度及以上咯血病史(每次出血量≥60 ml);(3)难以控制的高血压(血压≥150/100 mmHg,1 mmHg=0.133 kPa);(4)有症状的中枢神经系统(central nervous system,CNS)转移或不能中断使用阿司匹林、抗凝药或其他非甾体类抗炎药。本研究经杭州市肿瘤医院医学伦理委员会批准,所有患者均签署知情同意书。
1.2 方法 患者在入院后静脉注射培美曲塞(江苏豪森药业集团有限公司,0.2 g/瓶)500 mg/m2(第1天),顺铂(江苏豪森药业集团有限公司,30 mg/瓶)75 mg/m2(第1天),贝伐珠单抗(上海罗氏制药有限公司,规格:0.1 g/瓶)7.5 mg/kg(第1天),21 d为1个周期。最佳疗效为完全缓解(complete response,CR)、部分缓解(partial response,PR)或疾病稳定(stable disease,SD)的患者,完成4~6个周期后继续予相同剂量培美曲塞联合贝伐珠单抗治疗直到疾病进展(progression disease,PD)、不可耐受的不良反应或患者要求终止治疗。患者预给予地塞米松(3.75 mg,口服,2次/d,每个周期培美曲塞给药前1天、当天和给药后1天,连续3 d)、维生素B12(1 000 μg,肌肉注射,第1次于培美曲塞之前,每9周重复1次)和叶酸(350~1 000 μg,口服,1次/d)。
1.3 CT灌注成像扫描 分别于治疗前及2个周期治疗后进行CT灌注成像扫描,采用Toshiba Aquilion 64排CT扫描系统(Toshiba Medical Systems,东芝医疗系统公司)。利用随机配置的体部CT灌注成像技术进行肺部扫描,所有患者在扫描前均进行严格的呼吸训练,部分呼吸控制不佳的患者以腹带辅助尽量减少呼吸运动幅度,以确保CT灌注成像扫描层面在整个过程中无移动。选取体部肿瘤灌注系列进行扫描,患者扫描过程中在平静吸气末屏气至扫描结束。患者取仰卧位,屏气扫描定位像,确定扫描范围。扫描范围以病灶最大层面为中心,上下各2层,层厚4 mm或8 mm(根据病灶大小)。先平扫,确认病灶的扫描层面,再行增强扫描(灌注扫描)。具体参数:管电压/电流为100 kV/80 mA,球管转速0.5 s/r,旋转角度360°,矩阵512×512,视野320 mm×320 mm;高压注射器于扫描第1秒起以5 mm/s注射流率经肘静脉注入80~100 ml碘海醇(规格:50 ml/瓶,通用电气有限公司),延迟扫描5 s,共得到40×4幅连续图像。采集的灌注数据传输至GE Advantage Window 4.3工作站,应用Perfusion 3.0软件包中Body Perfusion系列软件进行数据处理。选定扫描病灶及参照动脉,手动描绘确定ROI,软件自动分析得到ROI的时间-密度曲线(time density curve,TDC)。
1.4 数据后处理和分析 肿瘤的灌注规律成像后获得ROI的TDC,进而得出相关参数:血流速度、血流量、平均通过时间及表面通透性。探索不同扫描参数是否能预测疗效,以及与RECIST 1.1版标准的相关性。采用RECIST 1.1版评价肿瘤长径及疗效,包括CR、PR、SD和PD,计算客观缓解率(objective response rate,ORR)和疾病控制率(disease control rate,DCR),ORR=CR+PR,DCR=CR+PR+SD。无进展生存时间(progression free survival,PFS)定义为从入组到疾病出现进展或任何原因导致死亡的时间;总体生存期(overall survival,OS)定义为从入组到任何原因导致死亡的时间;采用美国国立癌症研究所常见毒性反应标准(National Cancer Institute Common Toxicity Criteria,NCICTC)第3版在每个治疗周期进行毒副反应评价,观察方案的血液学、非血液学及贝伐珠单抗相关的特殊不良反应(高血压、出血及蛋白尿等)。不良反应按严重程度分为1级(轻度)、2级(中度)、3级(重度)、4级(危及生命)和5级(死亡)。
1.5 统计学处理 采用SPSS 19.0统计软件。正态分布的计量资料以表示,基线和2个周期治疗后灌注参数的比较采用配对t检验,不同疗效亚组基线灌注参数的比较采用单因素方差分析;非正态分布的计量资料以M(P25,P75)表示。采用Pearson相关系数评价上述灌注参数的相关性。采用Kaplan-Meier法以95%CI分析各事件终点的时间。P<0.05为差异有统计学意义。
2 结果
2.1 基线和2个周期治疗后检查结果 24例患者均在贝伐珠单抗联合化疗前进行了基线CT灌注成像检查,中位时间为7(5,10)d。在2个周期治疗后,第2次检查中位时间为41(39,44)d。基线选取目标肿瘤长径为(4.71±1.29)cm。
2.2 治疗前后肿瘤长径和CT灌注成像参数的比较2个周期治疗后,RECIST 1.1版肿瘤长径、血流速度及表面通透性较基线降低,差异均有统计学意义(均P<0.05),而血流量、平均通过时间的差异均无统计学意义(均P>0.05),见表1。相关性分析结果提示,血流速度与血流量呈正相关(r=0.428,P<0.05),但与平均通过时间呈负相关(r=-0.609,P<0.05),血流速度与表面通透性,血流量与平均通过时间以及表面通透性,平均通过时间与表面通透性之间均无相关性(均P>0.05)。疗效达到PR 9例(37.5%),SD 10例(41.7),PD 5例(20.8%)。PR患者基线血流速度较SD、PD患者更高,差异有统计学意义(P<0.05),而基线血流量、平均通过时间和表面通透性在疗效为PR、SD或PD的患者间差异均无统计学意义(均P>0.05)。不同疗效患者分析发现,PR患者血流速度和血流量较基线明显下降,差异均有统计学意义(均P<0.05),而平均通过时间和表面通透性比较差异均无统计学意义(均P>0.05);SD患者血流速度和表面通透性较基线明显下降,差异均有统计学意义(均P<0.05),而血流量和平均通过时间比较差异均无统计学意义(均P>0.05);PD患者血流速度、血流量、平均通过时间和表面通透性与基线比较差异均无统计学意义(均P>0.05),见表2。

表1 治疗前后肿瘤长径和CT灌注成像参数的比较

表2 不同疗效患者治疗前后肿瘤长径和CT灌注成像参数的比较
2.3 疗效 24例患者的ORR为37.5%,DCR为79.2%。PFS为5.5个月(95%CI:3.1~8.3),中位OS为13.5个月(95%CI:8.6~17.0)。
2.4 24例患者不良反应发生情况 21例患者(87.5%)出现1级以上的不良反应,最常见的不良反应为1/2级。最常见的血液学不良反应是白细胞下降(66.7%,其中3/4级为20.8%)。最常见的非血液学不良反应是恶心、呕吐(50%,其中3级为12.5%)。CT灌注成像检查相关的不良反应:恶心5例(20.8%),皮疹2例(8.3%)。贝伐珠单抗相关的不良反应:蛋白尿6例(25.0%),高血压4例(16.7%),鼻出血4例(16.7%)。所有患者未出现新的毒副反应,未出现药物相关的死亡,见表3。
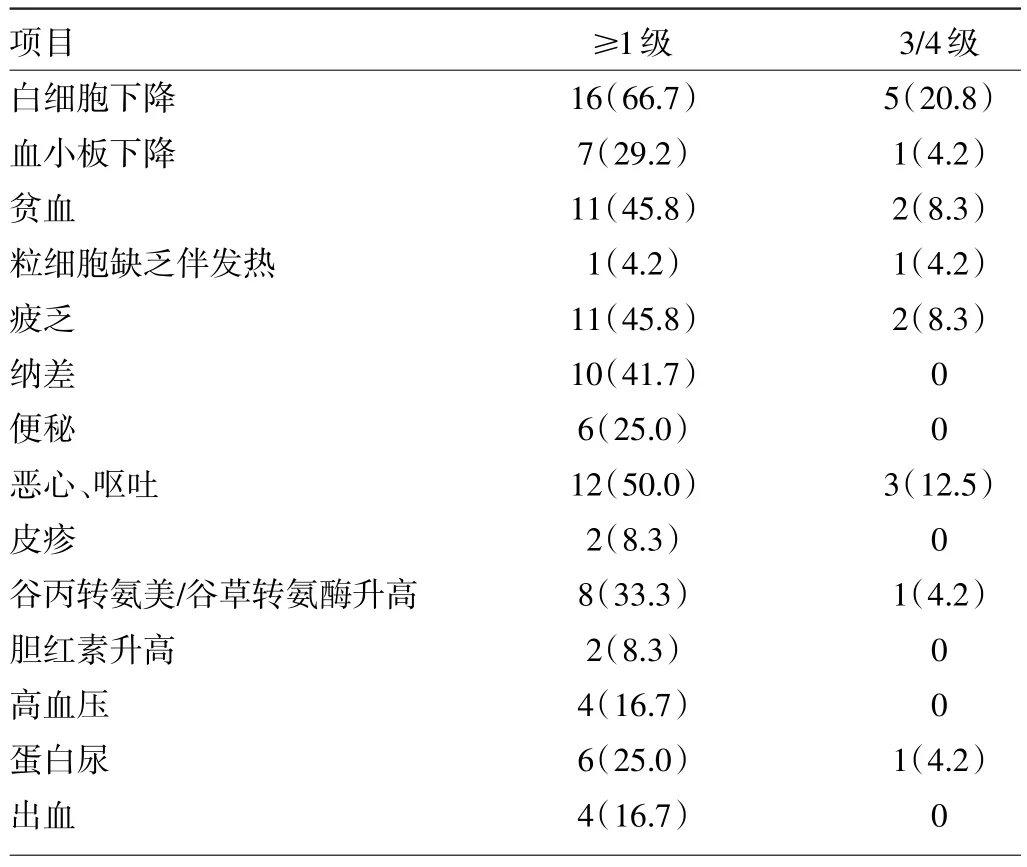
表3 24例患者不良反应发生情况[例(%)]
3 讨论
贝伐珠单抗作为VEGF-A单克隆抗体,联合化疗治疗肺癌显示了不错的疗效[5-7]。近期还有研究表明,分子靶向治疗或免疫治疗联合贝伐珠单抗也能提高疗效[13-14]。寻找一种较好的方法评价贝伐珠单抗疗效显得至关重要。在非小细胞肺癌中曾经开展过一些预测贝伐珠单抗疗效的研究,主要是一些血浆标志物,如VEGF配体和受体(VEGF receptors,VEGFRs)、成纤维细胞生长因子(fibroblast growth factor,FGF)等[15-16]。血浆标志物的预测作用至今没有得到证实,且常规CT扫描通过测量病灶最大径来评价治疗的效果,很多时候肿瘤活性下降而最大径无明显变化,造成评价的误差较大[17]。因此,找寻有效的预测疗效及评估疗效的辅助检查方法成为临床关注的热点。
CT灌注成像可以探索肿瘤新生血管形成及毛细血管通透性增加所引起的灌注值变化,而贝伐珠单抗的作用机制正是通过抑制新生血管形成、降低毛细血管通透性以及使肿瘤血管正常化[18-19]。目前有关CT灌注成像在肺癌应用的研究较少。本研究探索CT灌注成像在晚期ns-NSCLC患者采用贝伐珠单抗联合培美曲塞加顺铂治疗的价值,是否能预测疗效及评估疗效。本研究发现血流速度、血流量和表面通透性在治疗后均有下降,和RECIST标准评价的肿瘤长径缩小是一致的,而平均通过时间延长,但只有血流速度和表面通透性与基线比较差异有统计学意义(P<0.05)。不同疗效亚组分析则发现,对治疗有获益的患者(包括PR和SD),血流速度下降明显,而对治疗无获益的患者,血流速度反而有所升高。Aya等[12]发现基线血流量明显下降可能识别出肿瘤对抗血管生成药物不太可能产生反应。但也有既往研究表明,治疗前表面通透性较高或血流量较高的患者肿瘤组织处于高灌注状态,血管通路比较发达(最主要是VEGF通路),对贝伐珠单抗治疗的反应更好[20-21]。而本研究发现对治疗评估为PR的患者比SD或PD的患者,基线血流速度明显升高(P<0.05),说明血流速度能在一定程度上预测贝伐珠单抗疗效。血流速度、血流量和表面通透性越高,反映肿瘤组织血流灌注更好,而平均通过时间则相反,这些参数之间存在着相关性[22-24]。而本研究发现只有血流速度和血流量、血流速度和平均通过时间的相关性有统计学差异,认为可能是样本量较小的原因。
综上所述,CT灌注成像可在一定程度上预测化疗联合贝伐珠单抗在晚期ns-NSCLC患者中的疗效,说明CT灌注成像作为一个潜在预测指标的价值,尤其血流速度较高的肿瘤更有可能对贝伐珠单抗抗血管治疗有应答。患者行灌注扫描时只取一个目标病灶,不能很好地代表全身肿瘤,有待更好的方法学对多个病灶同时行灌注扫描。但本研究入组患者较少,有待进一步大样本临床研究证实CT灌注成像的潜在预测作用。

