新药时代多发性骨髓瘤患者早期死亡原因及其危险因素分析
高 珊,王宇彤,陆敏秋,石 磊,褚 彬,丁月华,王梦真,鲍 立
(北京积水潭医院血液科,北京 100096)
多发性骨髓瘤(multiple myeloma,MM)是血液系统第二大恶性肿瘤,目前尚无法治愈。随着蛋白酶体抑制剂和免疫调节剂在临床上的广泛应用,新药时代MM患者总生存期(overall survival,OS)从3年延长至7~10年[1-2],但早期死亡仍不可避免。在新药时代之前,约10%的新诊断MM(newly diagnosed MM,NDMM)患者在诊断后60 d内死亡,死因主要是感染[3]。新药时代下KUMAR等[4]曾报道NDMM患者的1年死亡率高达13%,主要的死亡原因为疾病进展。不同研究[5-7]对早期死亡的时间界定标准尚未统一(包括2、6、12和24个月),因此不同中心报告的早期死亡时间不尽相同,早期死亡时间也与纳入人群和治疗方案等密切相关。目前临床常用的预后分期系统包括国际分期系统(International Staging System,ISS)、修订国际分期系统(Revised International Staging System,R-ISS)、国际骨髓瘤工作组(International Myeloma Working Group,IMWG)危险分层和美国梅奥诊所的梅奥骨髓瘤分层和适应风险治疗 (Mayo Myeloma Stratification and Adaptive Risk Treatment,mSMART)[8-10],均不能准确预测早期死亡。在此基础上建立的双打击概念[11]和纳入测序结果的人工智能模型[12]等尚待进一步临床验证。同时,上述研究均基于临床试验结果,无法反映新药时代NDMM患者的情况。因此,仍需更多的来源于新药时代的临床研究探讨EM的高危因素,以期早期识别高风险NDMM患者并通过强化治疗改善预后。本研究纳入本科室收治的采用蛋白酶体抑制剂或免疫调节剂为基础化疗方案治疗的NDMM患者,探讨新药时代NDMM患者早期死亡的主要原因及其高危因素,为早期识别并为患者临床选择治疗方案提供依据。
1 资料与方法
1.1 研究对象选择2015年1月1日—2020年3月于本科室就诊并明确诊断为NDMM的患者共369例。诊断标准:依据2014年版IMWG多发性骨髓瘤的诊断标准明确诊断MM[4]。纳入标准:①NDMM患者;②一线治疗方案含蛋白酶体抑制剂或免疫调节剂;③除死亡患者外,随访时间均超过2年。排除标准:①一线未接受蛋白酶体抑制剂或免疫调节剂治疗的患者;②失访患者。本研究最终纳入237例MM患者。本方案通过北京积水潭医院伦理委员会的审批(伦理审批号:202104-46)。定义总生存期(overall survival,OS)<24个月为早期死亡,并依据是否早期死亡将237例NDMM患者分为早期死亡组(OS<24个月)和对照组(OS≥24个月)。
1.2 临床资料一般人口学资料:患者性别和年龄)和临床资料(疾病诊断、临床分期、血红蛋白(hemoglobin,Hb)、血钙(Ca)、血肌酐、乳酸脱氢酶(lactate dehydrogenase,LDH)、血清β2微球蛋白(β2 microglobulin,β2-MG)、骨髓浆细胞百分率、荧光原位杂交 (fluorescencein situhybridization,FISH)检测、化疗方案及疗效评估等信息。贫血定义为Hb<100 g·L-1,高钙血症定义为血Ca≥2.75 mmol·L-1,肾功能不全定义为血肌酐>177μmol·L-1,LDH升高定义为LDH>250 U·L-1,FISH检测1q21四倍扩增和17p缺失>5%为阳性,FGFR3和MAF融合基因异常信号>8%定义为阳性。
1.3 随访MM患者每月门诊或入院进行随诊,对未能就诊患者进行电话随访。随访内容:患者治疗情况和预后(复发和死亡)情况,若患者死亡需记录死因及死亡日期。随访时间自患者接受治疗之日起,截至2022年4月,除死亡患者外,随访时间均超过2年。中位随访时间为45.3个月,随访时间最短为1.5个月,最长为87.4个月。随访期间患者共死亡97例,健在140例。OS定义为患者自确诊日起直至患者死亡的时间(若死亡)或到末次随访时间(若存活)。
1.4 治疗方案与疗效评估以蛋白酶体抑制剂为基础的方案包括BAD方案(硼替佐米+阿霉素+地塞米松)、BCD方案(硼替佐米+环磷酰胺+地塞米松)、BDPACE方案(硼替佐米+顺铂+地塞米松+阿霉素+环磷酰胺+依托泊苷)和IAD方案(伊沙佐米+阿霉素+地塞米松)。以免疫调节剂为基础的方案包括RAD方案(来那度胺+阿霉素+地塞米松)、TAD方案(沙利度胺+阿霉素+地塞米松)和TCD方案(沙利度胺+环磷酰胺+地塞米松)。依据2016年IMWG疗效评估标准[13]定义患者治疗疗效分为完全缓解(complete response,CR)、非常好的部分缓解(very good partial response,VGPR)、部 分 缓 解(partial response,PR)、微小缓解(minor response,MR)、病情稳定(stable disease,SD)和疾病进展(progression disease,PD)。记录疗效为最佳疗效,观察终点为死亡。
1.5 统计学分析采用SPSS 25.0统计软件进行统计学分析。采用Prism8.0统计软件绘制图。患者年龄呈偏态分布,以中位数和四分位数表示;患者性别、疾病分期、贫血、高钙血症百分率、肾功能不全百分率、LDH水平升高百分率、低白蛋白血症百分率、血β2-MG水平升高百分率、浆细胞白血病百分率、骨髓浆细胞比例>60%百分率、髓外浆细胞瘤百分率、FISH检测结果及疗效以频数或构成比表示,组间比较采用χ2检验或Fisher’s精确概率法。生存分析采用Kaplan-Meier法绘制生存曲线,Log-rank检验比较生存曲线的差异。危险因素分析采用Logistic回归模型逐步法进行筛选。以P<0.05为差异有统计学意义。
2 结 果
2.1 NDMM患者基线资料237例NDMM患者中早期死亡组患者53例(22.36%),对照组患者184例(77.64%)。早期死亡组年龄>65岁患者24例(45.28%),对照组49例(26.63%)。2组患者初诊时基线资料见表1。早期死亡组患者的指标如高龄(年龄>65岁)、ISS分期Ⅲ期、R-ISS分期Ⅲ期、贫血、LDH水平升高、血β2-MG水平升高、骨髓浆细胞比例>60%、髓外浆细胞瘤和FISH检测17P缺失的百分率均高于对照组(P<0.05)。而高钙血症、肾功能不全、白蛋白降低、高危遗传学异常1q21四倍扩增、FGFR3和MAF融合基因异常的百分率组间比较差异无统计学意义(P>0.05)。早期死亡组和对照组分别有46例(86.79%)和156例(84.78%)患者接受过含蛋白酶体抑制剂的方案;早期死亡组和对照组分别有7例(13.21%)和28例(15.22%)患者接受过含免疫调节剂方案。评估2组患者诱导缓解治疗后的最佳疗效,早期死亡组和对照组患者总反应率(overall reaction rate,ORR)分别为49.06%和80.43%,组间比较差异有统计学意义(P<0.01)。
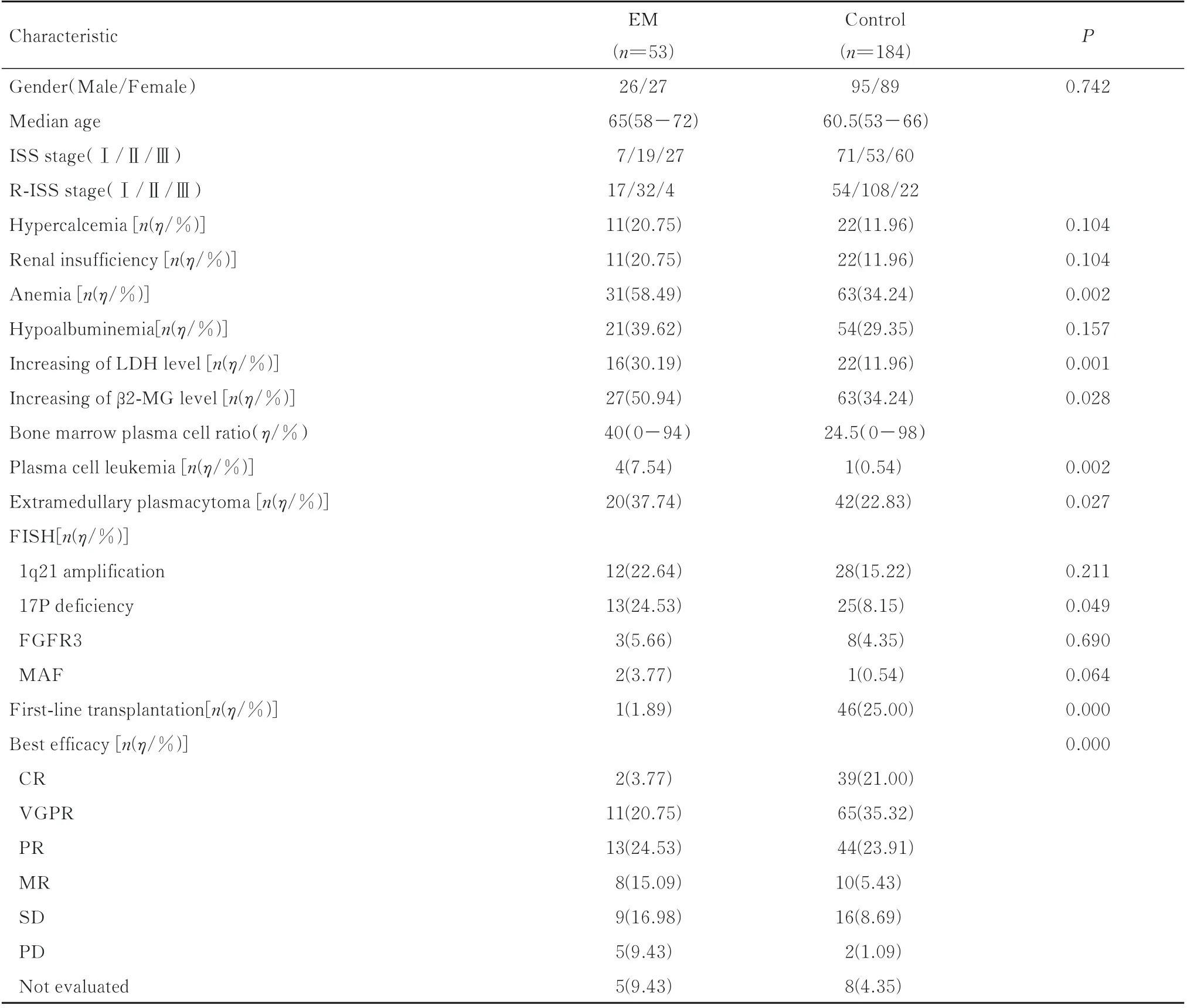
表1 早期死亡组和对照组患者基线资料Tab.1 Baseline data of patients in early death group and control group
2.2 2组患者死亡原因和生存分析至随访截止,早期死亡组53例患者全部死亡,对照组有44例患者死亡(23.9%)。早期死亡组中有41例(77.36%)患者因病情复发死亡,其中12例患者为非疾病复发导致死亡,具体死亡原因包括急性心肌梗死3例(5.66%)、肺炎4例(7.55%)、脑梗死1例(1.89%),有4例(7.55%)患者自动放弃治疗,死因不祥。早期死亡组中有15例(19.39%)患者病情复发过程中因严重并发症导致直接死亡,其中肺炎7例(13.21%),肾功能衰竭2例(3.77%),心脏衰竭2例(3.77%),急性心肌梗死1例(1.89%),肺栓塞2例(3.77%),败血症2例(3.77%),脑出血1例(1.89%)。中位随访时间为45.3个月(1.5~87.4个月),早期死亡组中位OS为16个月,对照组至随访截止时中位OS仍未达到(图1)。60 d内死亡患者1例,OS为24 d,患者死于肺部感染。
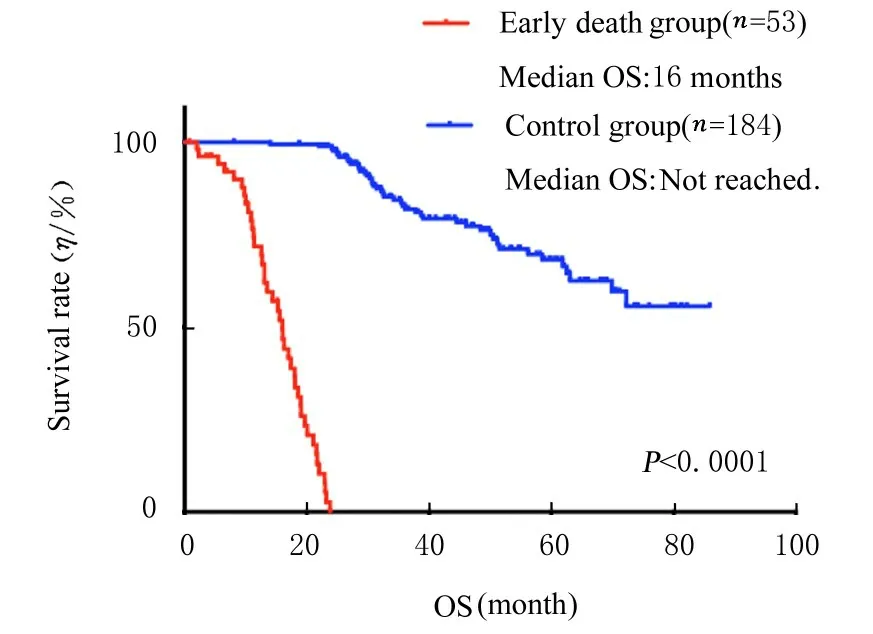
图1 2组患者生存曲线Fig.1 Survival curves of patients in two groups
2.3 早期死亡危险因素的分析单因素结果显示:年龄>65岁(P=0.005)、ISS分期Ⅲ期(P=0.029)、R-ISS分期Ⅲ期(P=0.001)、贫血(P=0.002)、LDH水平升高(P=0.002)、骨髓浆细胞比例>60%(P=0.011)、17p缺失(P=0.049)、髓外病灶(P=0.028)及疗效小于PR(P<0.01)是早期死亡患者预后不良的危险因素。多因素分析结果显示:年龄>65岁、R-ISS分期Ⅲ期、髓外浆细胞瘤和最佳疗效未达PR是新药时代NDMM患者早期死亡的独立危险因素(P=0.007,P=0.003,P=0.008,P<0.01)。见表2。

表2 MM患者早期死亡的多因素分析T ab.2 Multivariate analysis on causes for early death in MM patients
3 讨 论
MM的治疗已进入新药时代,并不断涌现单克隆抗体药物、抗体偶联药物和CAR-T细胞治疗等手段,MM患者的生存期有明显延长[1-2]。但MM具有极强的异质性,仍有患者在新药时代无法获得长期生存。发现导致早期死亡的危险因素有助于更精准地识别高危患者,针对NDMM的患者进行分层治疗,能进一步延长MM患者的生存期。
本研究结果显示:以硼替佐米为基础化疗方案的NDMM患者2年内早期死亡患者百分率为22.36%。IFM 2005-01研究[14]纳入移植候选者且采用硼替佐米联合地塞米松或长春新碱为基础的化疗方案诱导化疗的患者24个月死亡率为9.1%。另一项研究[6]分析一线自体造血干细胞移植NDMM患者24个月内死亡率为9.6%。研究者[15]纳入GEM 2005和GEM 2020研究中490例年龄≥65岁NDMM患者,所有患者均接受以硼替佐米为基础的化疗方案,24个月内早期死亡率为13.9%。本研究结果中患者死亡率高于一线移植患者及临床试验[16]患者,考虑与一线移植患者年龄多<65岁且移植可明显改善无进展生存期(progression free survival,PFS)及OS有关,而临床试验患者入组要求较高,包括ECOG评分和并发症等。庄俊玲等[17]发现:以硼替佐米或沙利度胺等药物为基础方案的177例NDMM患者24个月的早期死亡率为41.2%,疾病进展为主要的死亡原因(67.12%);同时期田梦茹等[7]发现:患者24个月早期死亡率为30.2%,其中84.3%死于PD。本研究中患者早期死亡率(22.36%)明显低于上述两项国内报道,考虑与所有患者均为硼替佐米为基础化疗方案有关,最常见的死亡原因为疾病复发(77.36%),与国内报道(67.12%~84.30%)[7,17]相似。此外,MM复发时并发肺炎、肾功能衰竭和心功能衰竭等疾病也成为加速复发患者死亡的重要原因之一。
本研究多因素分析结果显示:年龄>65岁、R-ISS分期Ⅲ期、髓外浆细胞瘤和最佳疗效未达PR是新药时代NDMM患者早期死亡的独立危险因素。MM多见于老年人,IMWG定义年龄>75岁是MM患者中的高龄人群[18],但≥65岁患者不适合自体造血干细胞移植,且与65岁以下患者比较,其PFS及OS均明显缩短[16]。因此本研究定义年龄≥65岁患者为高龄人群,多因素分析结果显示:年龄≥65岁是NDMM患者发生早期死亡的独立危险因素,与文献[18-19]报道一致。对于老年患者,心、肝、肾和骨髓等多器官功能减退均会影响其药物的药代动力学,从而增加治疗毒性、降低疗效和治疗耐受性,这是导致老年患者预后差的主要原因。
ISS系统和R-ISS系统目前广泛用于MM患者的分期和评价预后,本研究结果显示:早期死亡组ISS分期Ⅱ/Ⅲ期患者的百分率明显高于对照组;但多因素分析结果显示:ISS分期Ⅱ/Ⅲ期并非独立预后不良的因素。庄俊玲等[17]研究显示:高危组患者早期死亡率达到100%,本研究多因素分析中R-ISS分期Ⅲ期是MM患者早期死亡的独立危险因素,提示结合细胞遗传学结果的R-ISS分期更能分辨出高危患者,更有预后意义。
MOREAU等在ISS分期基础上联合LDH水平升高、t(4;14)易位和(或)17p缺失构建了预测一线移植MM患者24个月早期死亡风险模型,并通过GEMMENOS65和HOVON-GMMG-HD4队列研究[5]进行了验证。研究[15]显示:LDH水平升高、ISS分期Ⅲ期和高危遗传学异常[包括(t(4;14)、t(14;16)和17缺失]是新药时代老年MM患者24个月早期死亡的危险因素,且非持续治疗反应(疗效持续时间<6个月)亦成为早期死亡的一个重要预测因子,且与MM进展相关的死亡风险增加相关[15]。本研究中的危险因素分析结果与上述结果相似,R-ISS分期纳入了高危遗传学异常及LDH水平升高,并且诱导治疗疗效欠佳患者的早期死亡风险更高。
本研究纳入了髓外浆细胞瘤这一高危因素,在PET-CT广泛临床应用后多项研究[20-23]显示:髓外浆细胞瘤是MM患者预后不良的因素;考虑与肿瘤负荷高、髓外肿块对治疗反应差、易复发和更多高危遗传学表达有关。多因素分析结果显示:髓外浆细胞瘤也是MM患者早期死亡的高危因素,治疗方面需调整方案或联合大剂量化疗。
本研究回顾性分析新药时代NDMM患者早期死亡的原因及其危险因素,识别早期死亡风险高的患者并给予高危患者四药联合或更有效的治疗方案,可进一步改善MM患者生存质量,但本研究结果有待更大样本量及前瞻性研究进一步验证。

