继发性气道-消化道瘘介入诊治专家共识
北京健康促进会呼吸及肿瘤介入诊疗联盟专家委员会
由于各种原因造成气道管壁的完整性受到破坏,管壁上出现瘘口时称为气道壁瘘。可分为先天性和继发性两种。本共识只讨论继发性瘘。根据瘘口相通的部位,继发性气道壁瘘可以分为气道-消化道瘘及气道纵隔瘘等。继发性气道-消化道瘘是指继发于某些疾病的病理损害,在气道与消化道间存在异常通道,导致消化道腔内和气道内的气、液体相互流通,患者不能正常进食、咳嗽剧烈、常常存在难以控制的肺部感染,生活质量差,一般情况迅速恶化。患者若不积极治疗,多在数天至数月内死亡,其中90%以上患者死于肺部感染,是呼吸科、消化科、胸外科、介入科、放射科和肿瘤科等多个学科共同关注的一种危重疾病。
近年来各种支气管镜、胃镜下封闭瘘口技术的成功开展,在改善此类患者生存质量、延长生存期的姑息治疗中具有重要、积极的作用。但目前继发性气道-消化道瘘的临床循证医学数据非常有限,主要来自个案报道或系列病例研究,所以缺乏临床诊疗指南。为规范我国继发性气道-消化道瘘的诊治,北京健康促进会呼吸及肿瘤介入诊疗联盟特邀请相关领域的专家,组成专家委员会,通过检索PubMed、Embase、Cochrane Library、中国期刊全文数据库、中文科技期刊数据库和万方全文数据库等,根据国际研究进展、中国实际经验和研究积累等制定专家共识草案,经专家委员会多轮讨论修改与投票后达成共识意见。
一、修订原则
在循证医学原则指导下,参考国际规范,结合国情、可操作性和新研究数据进行修订。专家投票意见分为①~⑤级:①完全同意;②同意, 有保留意见;③意见未定;④反对;⑤完全反对。投表决意见②-⑤者需说明理由,以及如何改进声明;表决意见①+②>80% 属于达成共识
二、继发性气道-消化道瘘病因
1. 良性疾病: 严重胸廓挤压伤或外伤、食管异物;严重的食管化学性灼伤;肺、气管、食管和纵隔淋巴结等部位结核;自发食管破裂;医源性:带气囊气管导管长期压迫;手术后,食管支架后,术后放疗;食管、气管/支气管梅毒;其它非特异性感染等[1-2]。
2. 恶性疾病: 恶性病变更为常见,多继发于食管、纵隔或肺部恶性肿瘤。其中大部分继发于晚期食管癌,比例70%以上[3-4];约0.2%~5%食管癌患者发生气管食管瘘(esophagorespiratory fistulae, ERF),约1%肺癌患者发生ERF[5- 6]。包括晚期食管癌;晚期肺癌;纵隔恶性肿瘤;甲状腺癌;其它部位的肿瘤转移至气道;胸部肿瘤放疗后。
三、继发性气道-消化道瘘分类及发病机制
1. ERF: ERF是由于各种良恶性因素导致气道与邻近食管破溃形成病理性交通,是一种威胁生命的严重并发症[1,7-8],病死率高,生存率低,生活质量差。ERF瘘口可发生于喉以下气管和双侧主支气管的任何部位,但最常见的部位为食管中段与左主支气管之间。ERF根据原发病因分为良恶性两大类。
良性ERF多源于外科术后、食管支架置入术后、气管插管后等气道损伤、感染性疾病(如结核、克罗恩病等食管肉芽肿性疾病、梅毒、真菌感染等)、创伤等。
恶性食管癌ERF形成的机制包括:(1)晚期食管癌因癌组织侵犯食管壁全层,而食管上中段前壁毗邻气管、左主支气管后壁,当肿瘤累及气道壁且生长过快而出现缺血坏死时易形成瘘;(2)放射治疗在杀伤肿瘤组织的同时也损伤正常食管组织的再生能力,致使肿瘤坏死而正常组织修复能力低下形成瘘,同时导致食管壁发生纤维化、管壁僵硬、舒缩功能减退,容易导致瘘的形成;(3)全身化疗后肿瘤组织坏死吸收也易导致瘘的形成;局部动脉灌注化疗,肿瘤组织坏死过快,正常组织再生较慢也可形成瘘;(4)食管癌晚期因食管狭窄行食管内支架治疗时,为防止食管支架移位,常采用哑铃状或喇叭口状支架,使支架两端对食管壁产生较大压力或剪切力,影响食管壁尤其前壁的血液供应,食管癌手术后吻合口(弓上、颈部)复发,残留食管和吻合口置入内支架,直行的管状内支架上口刺激弧形弯曲的正常食管壁和气管壁,摩擦易引起组织坏死形成瘘[8-9]。
2. 气道-胸腔胃瘘: 是食管癌行食管-胃弓上吻合术或颈部吻合术后胃上提到胸腔或走行于后纵隔食管床,胃与气道形成新的毗邻关系,肿瘤残留,胃与气管或支气管之间相通而形成的瘘,是食管癌切除术后严重且威胁生命的并发症之一[10-11]。
形成气道-胸腔胃瘘的相关因素有:①放疗:手术后若肿瘤残留,将对食管床区进行放疗,食管放疗剂量和耐受量为60~70 Gy,而胃的耐受剂量仅为食管的一半,约为30~40 Gy,位居食管床区的胸腔胃部位接受过量的射线容易导致放射性胃溃疡、胃壁坏死、穿孔和气道损伤;②胃酸化学性刺激及胃液消化酶局部腐蚀胃穿孔,进而损伤气道壁;③肺部感染及纵隔局部炎症;④肿瘤复发及侵袭;⑤手术缝合不良及局部缺血;⑥化疗;⑦全身营养不良等。
3. 食管吻合口-气道瘘: 食管癌术后食管与胃的吻合口与气道相通即为气道吻合口瘘,瘘口位于吻合口这个特殊位置,其上方为食管、下方为宽大的胃腔,解剖结构特殊。食管癌手术切除弓上吻合后,吻合口区域的大剂量放射线治疗或吻合口肿瘤复发、直接蔓延浸润气道易造成吻合口瘘;另外,吻合口狭窄扩张治疗后、吻合口出现感染等情况也容易导致吻合口瘘的形成。
4. 食管-肺泡瘘: 目前习惯用ERF描述所有存在于食管和气道之间的瘘口,但是50%~60%的患者瘘口位于食管和气管之间,37%~40%的患者瘘口位于食管和支气管之间;另外,仍有少部分患者会形成食管-肺泡瘘[5, 12]。研究显示食管-肺瘘主要源于食管癌和支气管癌,放化疗导致食管瘘、瘘破坏纵隔、胸膜和肺组织,促进了食管-胸膜腔-肺泡瘘口形成;所有患者存在误吸性肺炎,79%的患者存在肺部炎症或脓肿[13]。对于食管-肺泡瘘患者,食管支架置入是主要的治疗方式,支架置入后,肺脓肿范围会缩小,但会持续存在,因支架置入封闭了脓腔,支架置入后的脓肿引流是需要考虑的治疗措施[13]。
四、诊断
通过结合临床症状、影像学检查、支气管镜及胃镜所见,继发性气道-消化道瘘的诊断一般不难,但较为复杂。
1. 临床症状: 继发性气道-消化道瘘特征性的症状为吞咽后出现阵发性呛咳,咳出食物残渣并伴随着持续加重的吞咽困难和呼吸困难。部分患者表现为“卧位烧灼样呛咳综合征”,患者出现烧灼样剧烈刺激性呛咳,平卧位呛咳或呛咳加重,坐立位呛咳减轻或消失;患者可以有大量白粘痰或血性痰、脓性痰。
气道-胸腔胃瘘临床症状较一般ERF更为严重和凶险,禁食仅能减少食物进入气道,但胃液、胆汁等消化液仍通过瘘口大量流入气道,胃液的消化作用瘘口往往在短期内迅速扩大。患者即使不进食也会咳嗽剧烈,肺部炎症一般较严重,早期为化学性炎症,后期常合并有细菌、真菌等感染性炎症。瘘口较大时,由于大量的吸入气体流入胃腔,患者出现呼吸功能下降、呼吸衰竭等,如果不及时处理,患者会很快死亡。
食管吻合口-气道瘘临床症状与胸腔胃瘘相似,但严重程度一般较轻。
2. 影像学检查: 食管X线造影有重要价值,应选用40%泛影葡胺为造影剂(碘水对比),造影时用手压迫上腹部进行摄片,可提高诊断率,但对食管气道瘘者不作为首选检查,特别是瘘口较大时造影需谨慎,在吞咽造影剂时存在严重误吸可能。由于对比剂误入气道易引起剧烈呛咳,造影时难以对瘘管位置、形状、长短、直径等进行准确评估。造影有时也难以显示细小瘘管。禁用硫酸钡造影,以防钡剂通过瘘口进入肺部形成顽固性异物沉积性肺炎。
为避免吞咽带进大量细菌和剧烈呛咳所致图像模糊,推荐经口腔食管或胃管造影,影像学监测下见导管插至预定瘘口部位,在可疑食管瘘口经导管注射40%的碘水对比剂3 ml左右,可疑胃瘘口经导管注射5 ml左右对比剂造影,能够避免大量吞咽的误咽呛咳,能够获得较为清晰的图像。
CT或MRI亦是对气道-消化道瘘诊断的敏感方法,能较好细致的观察气道、食管、胸腔、纵隔和胃部病变,对于评估疾病程度和肺炎等非常有帮助,并且有助于明确瘘口与周围组织的关系,有助于后续支架置入类型和方式的选择。另外,对于需要放置气管支架的患者来说,利用CT重建图像有助准确测量气道径线、瘘口与隆突或声门间的距离,便于确定最佳的支架规格。
3. 内镜检查
(1)支气管镜检查:一般可以直接见到瘘口,确认瘘口在气管或支气管内的位置;当气道内存在分泌物时,应先吸净分泌物后再仔细观察,这样比较容易见到瘘口。如果瘘口很小有时不易发现,口服美兰后再行支气管镜检查有助于发现瘘口,通过动态观察气道壁是否有气泡溢出也有助于判断小瘘口的存在。
(2)胃镜:也是重要确诊手段之一,可以直视瘘口,或观察到瘘口冒气泡,需要结合食管造影等来证实瘘口的存在。胃镜检查可帮助观察瘘口周围黏膜和胃壁的情况,必要时可进行活检确诊疾病病因,并可帮助制定治疗措施。胃镜还可以在气道内支架封堵瘘口后观察瘘口的愈合变化。
五、手术治疗
对良性继发性气道-消化道瘘患者,如有手术机会应尽量争取手术切除瘘管和病变的组织,对于病变不可逆的肺组织可行肺叶或全肺切除术,与瘘有关的食管憩室亦应切除,气管、支气管、食管缺损处应分别双层缝合[14]。可于食管和气管之间置入如胸膜、肌肉、心包膜或膈肌瓣等组织包裹瘘口以减少复发。如气道缺损较多,可行气道替代物移植。但对恶性继发性气道-消化道瘘患者一般为肿瘤晚期,身体状况差,基本不适合手术治疗[15-16]。
六、支架介入治疗
经支气管镜、胃镜及影像引导下的介入治疗是对不适合手术的继发性气道-消化道瘘的主要治疗手段,可很大程度的减轻患者的症状,改善生活质量。介入治疗目前最常用的为气道和/或消化道支架的置入[8,11,17-22],以及镜下药物注射、烧灼、金属夹等。
理想的堵瘘支架应满足: 完全覆盖瘘口及瘘管并与周围管壁贴合良好; 置入支架稳定性良好,特别是支架覆膜牢靠不易破损; 支架置入后不易移位; 支架能长时间维持一定张力;良性瘘口应放置可回收支架,而恶性病变则需长久置入支架。
1. 气道支架
(1)材料选择:封堵瘘口既可选择气道覆膜金属支架也可选择硅酮支架,均能有效减少消化道分泌物流入气道,减少气道内气体流入消化道,改善患者的生活质量。目前临床常用的覆膜金属支架包括镍钛合金支架、Z形不锈钢覆膜金属支架和Ultraflex支架等。
(2)支架的个体化设计
A 根据瘘口位置选择支架形态:瘘口及病变管腔上下至少超过10 mm正常管腔者可选用普通直管型支架,瘘口距离隆突较近时(如Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅶ区)可设计成分叉形支架(Y或L形)[23];瘘口病变管腔上下无足够的固位点时,应选用分叉形支架[21]。
中央型气道的8分区方法[21]:主气管自上而下分为三等分,命名为Ⅰ、Ⅱ、Ⅲ区,隆突为Ⅳ区,右主支气管为Ⅴ区,右中间段支气管为Ⅵ区,左主支气管一分为二,近1/2为Ⅶ区,远1/2为Ⅷ区。
B 根据病变长度确定支架长度:支架两端长度以超过病变范围20 mm为宜;对于镍钛记忆合金支架,应把支架受压的伸展长度计算在内;瘘口较大时支架最好覆盖瘘口两端各20 mm以上。
C 根据瘘口上下气道管径及狭窄程度确定支架直径:一般选择直径大于正常气道内径10%~20%或等于气道前后径,但对于瘘口附近管腔明显狭窄者应设计成哑铃型、手电筒型或管形。
D 气道长度的测量:一般在支气管镜直视下测量,用定位尺或活检钳能使测量值更加准确;亦可从CT扫描层面计算而得。
E 气道直径的测量:一般在深吸气时病灶处薄层CT的脂肪窗上测量较为准确,CT扫描为气道的斜切面时直接测量不准确,需根据勾股定律公式换算。
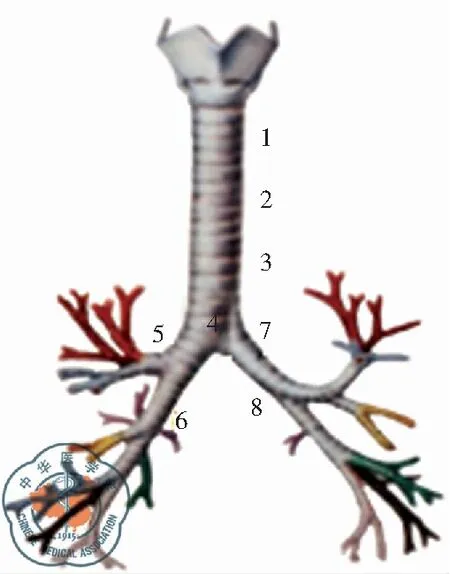
图1 中央型气道八分区示意图
(3)支架置入方法:气道金属直筒形(Ⅰ形)支架一般在软式镜引导下置入,L形和Y形支架最好经硬质镜下置入,亦可在X线透视下释放所有支架。金属支架输送器由带有导引头(输送鞘内芯)的支架输送鞘、装有支架的内管、和支架后方的顶推杆组成,故又称为三套管放置法。在定位尺下释放支架,位置更为准确。硅酮支架则需在硬质镜下放置。全身静脉麻醉后,根据置入支架的型号,经口插入不同口径的硬质镜,再放置硅酮支架。术后复查胸片观察支架位置、有无气胸、纵隔气肿等,并于术后定期行气管镜检查,动态监测支架变化情况,若发生并发症及时处理。
2. 食管支架
(1) 材料选择:临床上常用的食管金属支架多来自美国Boston Scientific和Cook Endoscopy[18],韩国S & G Biotech和Taewoong Medical公司,以及国产的镍钛记忆合金支架和Z型不锈钢支架等[17]。食管金属支架可为全覆膜或部分覆膜。目前普遍采用两端带蘑菇头的食管自膨式全覆膜或部分覆膜金属支架,其特点是可有效封闭瘘口,防止食物、胃液等接触瘘口,并阻止其通过瘘口进入气道,避免引起胸腔及肺部感染;减少反流对瘘口的刺激,防止瘘口进一步扩大;防止肿瘤及肉芽组织堵塞支架腔,降低支架置入后狭窄的发生率。
(2)支架的个体化设计
A ERF食管覆膜金属支架的设计:支架长度要求至少超过瘘口的长度5 cm以上,置入后要确保支架(两端各长于瘘口)上缘高于瘘口上缘2 cm以上,支架直径一般选择直径17~20 mm,对于有食管放疗病史者一般选择直径14~16 mm,对于支架上缘拟放置到食管入口附近者应选择小直径(15~17 mm)且上缘无喇叭口的支架。
B食管吻合口-气道瘘的消化道支架设计:包括分节型全覆膜食管内支架、分节型蘑菇状全覆膜内支架,置入消化道的支架直径不宜太大;支架一部分位于食管,该部分参照食管支架设计;一部分位于胸腔胃内,其下端可设计成大喇叭口形状,以减少胃内容物沿支架外表面和胃壁之间进入瘘口而形成侧漏的现象。另外,支架下段最好加上防反流瓣膜,减少胸腔胃内容物的反流。如有可能,最好放置气道支架。
(3)置入方法
A X线引导置入法:优点是可准确判断导丝位置、是否通过病变段,减少医源性穿孔;可动态监测支架释放过程,特别是支架下缘释放的状态[24]。支架安置完毕后,可造影观察瘘口封闭的效果。单纯X线引导的缺点是无法有效(直接)观察食管病变和瘘口,无法实时、有效的判断支架置入过程中出血、穿孔等并发症情况,且一旦发生并发症也无法及时处理。
B胃镜直视置入法:主要优点是胃镜直视下置入操作简便、成功率高,可避免X线(辐射)损伤;可及时处理术中出血,使置入过程更为安全,且可在直视下及时调整支架位置。 但单纯胃镜直视下置入支架时易出现定位准确性欠佳等问题。
支架置入后分别于术后1周,以及后续每隔1~2个月根据患者情况可行食管造影、CT或内镜检查,评估瘘口闭合、支架开放和移位情况[17]。
3. 不同气道-消化道瘘置入支架的选择
(1)ERF
A单用食管支架:对于无手术指征的恶性和部分良性ERF患者,可采用食管金属支架置入封闭瘘口[25]。当患者存在食管狭窄,无或并存轻微气道狭窄,选择单用食管支架即可。对于食管并无明显狭窄ERF患者(如晚期肺癌导致ERF),单独放置食管覆膜支架移位率较高,可考虑食管无覆膜联合覆膜双金属支架置入的方式,前者起到固定作用,后者起到封堵瘘口的作用[26]。早期观点认为食管支架只适用于距门齿21 cm以下的ERF,因食管上段为横纹肌且位置高,支架置入后易引起患者疼痛和异物感较为突出。但随着覆膜金属支架工艺改进,以及消化内镜技术的提高,食管上段ERF也可通过支架置入进行治疗。研究认为支架上缘不超过食管颈段第一个生理性狭窄上缘的高位瘘仍为适应证,远期疗效满意,且并发症并未增多[27]。食管金属支架一般不适用于胸腔胃瘘和大部分吻合口瘘(蘑菇状覆膜内支架)。
B单用气道支架:位于颈部上段食管的ERF,经胃镜和影像学等评估后确实无法放置食管支架的,可考虑气管支架置入。瘘口远端食管管腔完全阻塞者,如不能顺利插入导丝至胃腔,则无法置入食管支架。对食管支架置入容易导致食管破裂,存在中-重度气道狭窄,且不存在或存在轻度食管狭窄的患者,置入气道内支架既可解除狭窄,又可封堵瘘口。
C联合置入气道支架: 在食管多枚支架置入后仍未完全封闭瘘口时,此时可考虑置入气管支架,如有必要可取出食管支架[28]。涉及食管和中央型气道的中-重度狭窄时,由于插入单个支架可能不足以缓解症状,可考虑采用食管和气管支架联合置入的方式解除食管和气道的狭窄[29]。这种情况应首先置入气道支架,再置入食管支架。如先放置食管支架,可因支架对气道的压迫作用而致气道狭窄加重,加剧患者呼吸困难甚至威胁生命。食管和气道双支架置入后支架间摩擦可能会导致组织压力性坏死,进而导致致命性的出血等;因此,食管和气道覆膜金属支架联合置入前需要对ERF患者进行系统全面的评估后实施。注意瘘口大小及与血管的关系。如果瘘口离大血管太近,慎用支架。对食管支架容易移位者,通过置入气道支架,气道支架与食管支架相互作用可使食管支架不易移动。
(2)气道-胸腔胃瘘
如果瘘口位于宽大的胃体,从食管-胃途径置入支架不能封堵瘘口,只能单用气道支架封堵瘘口,多数情况下需要用分叉形气道支架。但若发生于管状胃,还可用食管支架封堵。
(3)食管吻合口-气道瘘
应首先置入气道支架,必要时可特制食管覆膜支架。由于食管吻合口位置特殊,置入的消化道支架难以完全封堵瘘口,只能减少消化道内的食物及分泌物流入气道。
4. 疗效评价: 绝大多数继发性气道-消化道瘘不适合手术根治,也不能通过药物治愈,目前仍是医学界存在的难题。置入气道支架及置入消化道支架是继发性气道-消化道瘘最主要也是最好的治疗方法,通过物理学方法可以遮盖瘘口,从而防止食物及分泌物通过瘘口进入呼吸道,控制吸入性肺炎,同时防止呼吸道的气体进入消化道。支架置入后也能解除并存的气道或食管狭窄。
临床实践已证实气道及食管支架置入具有操作创伤小、并发症少、疗效确切等优点。操作不受患者身体状况及年龄的限制,且支架可随时取放,已成为继发性气道-消化道瘘姑息治疗最可行和常用的方法。
目前国内外尚无统一的气道瘘疗效判断标准,王洪武教授根据自己的经验制定了支架瘘口封堵疗效的判断标准[22]: 完全缓解(complete remission, CR),瘘口愈合, 临床症状(如饮水呛咳、发热等)完全缓解持续一个月; 临床完全缓解(clinical complete remission, CCR),瘘口未愈合,但被支架完全封堵, 临床症状完全缓解持续一个月; 部分缓解(partial remission, PR),瘘口未闭合, 部分被支架封堵, 临床症状部分缓解; 无效(NR),瘘口未闭合,未被支架封堵,临床症状无缓解。
支架置入能否成功封堵瘘口,与支架的个体化设计关系紧密。只有根据瘘口的位置、性质及病变区域气道、食管的特点设计出个体化支架,才能最大限度的封堵瘘口,控制感染,恢复患者进食。根据中央型气道八分区方法,位于Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅶ区的瘘口宜放置气道分叉支架,而位于Ⅰ、Ⅵ、Ⅷ区的瘘口则宜放直筒形气道支架或食管支架,Ⅷ区的瘘口亦可设计小Y支架。有研究报道了48例ERF患者共有52个瘘口,瘘口直径0.3~7.0 cm,并且瘘口多亦位于主气管中下端(Ⅱ和Ⅲ区)和双侧支气管开口(Ⅴ和Ⅶ区)[22]。放置Z型覆膜金属支架52个(其中Y形36个,L和I各8个)。食管放置覆膜金属支架28个,其中CR 4.0%,CCR 68.0%,PR 18.0%,NR 10.0%,中位生存期为6个月,选择合适形状和类型的气管和/或食管覆膜金属支架能有效封堵ERF[22]。
目前,关于良性ERF的临床疗效尚无较多循证医学数据支持,基于现有多项回顾性研究显示,各类干预方法治疗良性ERF的成功率近95%,获得持续性临床缓解的成功率也在90%以上。近期,ESGE建议对于良性ERF可考虑支架置入,但不推荐特定类型的支架,支架的放置的时间应根据个体间差异制定。自膨式覆膜金属支架可用于治疗良性ERF,也可选择其它内镜治疗方法,如OTSC等封闭瘘口。另外,关于生物可降解支架治疗良性ERF的临床数据有限,仅有小样本研究显示生物可降解支架置入可获得较好的临床疗效。
对于恶性ERF支架置入的患者,自上世纪90年代以来,主要采用自膨式金属支架来封闭瘘口。多项回顾性的研究显示自膨式覆膜金属支架治疗ERF的瘘口闭合成功率在70%~100%[9,17, 30-34]。近期,欧洲胃肠内镜学会(ESGE)制定的食管支架治疗良恶性疾病的临床指南建议,封闭恶性ERF瘘口,应首选自膨式覆膜金属支架置入治疗,但是关于支架留置的最佳时间尚不明确,应视个体化而定[18]。由食管癌引起的ERF伴有食管狭窄而无或轻度气管狭窄时,自膨式覆膜金属食管支架置入封堵瘘口后效果立竿见影,但存在支架移位等问题,且术后存在复发可能。食管支架置入1周内存在瘘口不完全闭合的问题,发生率约12%[8],其原因多因支架近端边缘和食管壁之间存在间隙,后续可再次置入支架及其他封堵技术[8, 34-36],但因“漏斗现象”存在而疗效欠佳。另外,当存在气管狭窄时应考虑单纯置入气管支架;当食管和气管均有中至重度狭窄或瘘口较大时,则需在两侧同时放置支架[8, 32, 37]。ESGE也推荐在单独使用食管或气管支架封闭瘘口不能实现时,可考虑双支架置入[18]。
硅酮支架具有不易损坏、治疗维持时间较长、封堵效果可靠且堵漏效果受咳嗽影响小等优点[19]。在支架与瘘口周围管壁良好贴合的前提下,硅酮支架甚至可以获得较金属支架更满意的封堵效果、较长的封堵时间。硅酮支架需根据瘘口的位置可作适当处理。对气道膜部的气道瘘可直接放置硅酮支架,但对发生于气道侧壁的瘘口,放置支架前需去除支架侧壁的钉突,以免影响封堵效果。
硅酮支架的使用目前还受到适形性较差且有防滑钉、部分病例支架无法贴紧瘘口周围管壁、置入困难且放置中存在使瘘口扩大的危险、对操作者技术要求较高等因素的限制。在以下情况不宜采用硅酮支架治疗气道-胸腔胃瘘,包括因适形性较差或直径限制,支架壁与瘘口周围管壁贴合不好者;相应型号的硬质镜插入困难或未能插到瘘口远端者。
一项研究报道了硅酮支架治疗继发性气道-消化道瘘31例的近期疗效,所有患者均成功置入硅酮支架,放置成功率达100%,48.4%的患者获得完全缓解,41.9%获得部分缓解,症状总体缓解率90.3%[19]。另外,国内有研究采用硅酮支架治疗16例气道-胸腔胃瘘患者,其中CR 25%,PR 56.3%,NR 18.7%,疗效与金属支架相似[38]。
关于支架置入治疗继发性气道-消化道瘘的长期生存期尚无定论。恶性ERF患者接受食管和/或气道支架置入后,生存期取决于瘘口封闭的情况,如能有效闭合瘘口,控制肺部感染,可显著提高患者生活质量和生存期。一项对照研究显示支架置入组的恶性ERF患者较对照组和胃造瘘组生活质量显著改善[18, 39],尤其在改善呼吸困难、吞咽困难、饮食问题、口干、咳嗽及唾液过多分泌等方面更为明显。一项系列病例研究报道支架置入组生存期平均3.4个月,显著高于肠造瘘组和单纯营养支持组[33];支架置入与患者生存期提高显著相关[18]。
5. 并发症
继发性气道-消化道瘘各类支架置入的早期和远期并发症情况,目前循证医学数据多来自于个案或回顾性病例报道。
(1)气管支架:金属支架置入的主要并发症有咳嗽,痰液潴留,瘘口堵塞不严,支架移位或脱出,支架两端肉芽组织增生,口臭,金属疲劳,支架断裂,呼吸道感染,气管-支气管壁穿孔,大出血等。硅酮支架置入的主要并发症有咳嗽、分泌物潴留、瘘口堵塞不严,肉芽组织增生、肺部感染等,这些并发症总的说来是非致死性,且可处理[19,38]。
(2)食管支架:与操作相关的并发症发生率大约为0~27%,病死率0~12%;并发症包括瘘口再开放,肿瘤组织生长或食物导致支架堵塞,支架移位、支架覆膜破坏,以及疼痛、吞咽困难、异物感、出血和肺炎等[17, 32, 37, 40]。其中瘘口闭合后再开放较为棘手,预示着误吸等症状再次出现。基于部分回顾性研究报道支架置入术后1个月以后,10%~30%的初始治疗成功的ERF患者可出现瘘口再开放的问题[8]。内镜下调整支架或再次支架置入可解决瘘口封闭不完整,支架堵塞和移位等问题。
6. 术后管理及随访: 无论置入气道或食道支架,术后均应严格管理及定期随访。一般术后1周内至少复查一次内镜,如有并发症,随时处理。气道支架术后2周内易有分泌物潴留,每天应至少4~6次超声雾化吸入碱性液体,结合静脉补液,湿化痰液,使痰液易于咳出,并每周复查一次支气管镜。一月后易出现肉芽肿,3个月内应每月复查一次支气管镜。半年后有些金属覆膜支架会出现膜破裂,相应会再次出现呛咳症状,需及时更换支架。食管支架早期易移位,需严密观察,及时调整支架的位置。3个月后支架两端易出现肉芽,需及时处理。
七、其他介入治疗方法
1. 内镜下药物注射:瘘口周围可注射硬化剂、干细胞等,亦可达到一定疗效。 Petrella等[41]通过动物实验证实骨髓间充质干细胞具有修复支气管胸膜瘘的作用。也有临床报道使用注射骨髓间充质干细胞的方法,治疗1例右全肺切除术后并发右主支气管胸膜瘘的患者(瘘口大小约3 mm),其将分离并培养骨髓间充质干细胞后,在支气管镜下将1千万个干细胞注射于瘘口周围,术后60 d复查CT和支气管镜检查提示瘘口已完全闭合。瘘口处的活检组织病理提示在纤维固有层的上层存在呼吸道上皮细胞增生,同时平滑肌细胞减少并被成纤维细胞所取代,免疫组化显示为p40和DNp63 表型,提示基底细胞分化为鳞状上皮,展现了良好的修复效果[42]。
除了骨髓间充质干细胞治疗外,有研究显示支气管镜下局部注射脂肪干细胞治疗2例支气管胸膜瘘的患者,通过3年的随访观察显示瘘口均取得了愈合,且无治疗相关风险或者恶性肿瘤复发的表现[43]。另外该研究还应用脂肪干细胞成功治疗了1例支气管纵隔瘘的患者[44]。
2. 消化内镜干预措施: 包括内镜吻合夹(over-the-scopeclips, OTSC)闭合瘘口,国内有采用内镜下OTSC吻合系统成功夹闭良性外伤性ERF的报道[45-46]。对于良性ERF,如瘘口较小的外伤性ERF(创伤或异物)多选用尖齿型OTSC来封闭瘘口。
2008年,德国Ovesco公司研发推出OTSC吻合系统,其是一种新兴的镍钛锘合金夹,较传统内镜金属夹具有可闭合更大范围组织、闭合全层消化道和对周围组织张力小的特点。OTSC闭合消化道瘘口的作用优于一般内镜金属夹,但价格较昂贵,目前没有完全在临床普及。OTSC实施前需根据瘘口大小选择合适尺寸的吻合夹。食管管腔较小,OTSC在食管应用相对困难,如瘘口边缘组织有纤维化或坏死,易造成吻合夹不稳而发生脱落;操作时可使用辅助设备并充分吸引,将边缘组织完全拉入施夹帽后才能释放吻合夹。现阶段,OTSC在ERF临床应用经验有限,针对不同类型ERF的瘘口封闭如何选择OTSC尺寸和类型仍缺乏高质量的数据支持。亦可采用金属夹夹闭,并联合氩离子凝固术(argon plasma coagulation, APC)等。
3. 气管内镜技术: 如气管支架置入联合气管镜下烧灼术,还有生物蛋白胶瘘口局部灌注封堵术,均适合治疗小瘘口或与支架联合应用,但封堵1~2周后因生物胶的溶解瘘口会发生再通,因而临床应用较少[47]。
八、内科保守治疗
一般情况较差不能耐受手术的继发性气道-消化道瘘,内科保守治疗是基本的治疗措施,包括使用抗生素控制肺部感染,静脉高营养、空肠造瘘等支持治疗,化痰、适当止咳等对症治疗。此外,对于气道-胸腔胃瘘、食管吻合口-气道瘘患者,除禁食外,还需留置胃管,进行胃肠减压,以减少酸性胃液流入气道。主要的治疗方案如下。
1. 抗感染:一旦发生继发性气道-消化道瘘后往往预后不良,大多数患者于1个月内会死于呼吸道感染和营养不良。国内有研究报道ERF患者下呼吸道病原学培养以革兰阴性菌和真菌为主,分别占64.7%和25.5%,其中以铜绿假单胞菌最为常见,这可能与反复使用抗生素及肠道菌群移位有关[48]。
2. 营养支持: ERF患者由于无法经口进食,以及感染所导致的应激及炎症反应,患者常出现严重的营养不良。营养不良一方面导致瘘口延迟愈合或无法愈合,同时也导致临床并发症显著增加。因此积极有效的营养支持对于ERF的整体治疗效果至关重要[49-52]。
(1)营养支持治疗方案:全面评价营养状况,包括营养筛查、人体测量、血液指标、体成分分析、代谢测定等;制定营养治疗计划,包括营养支持通路及营养素的选择。
(2)营养支持通路: 瘘发生的早期,还没有建立空肠营养阶段,宜采用肠外营养支持; 尽早建立肠内营养通路,实施肠内营养支持,在肠外向肠内营养过渡阶段,保证每日营养素总体目标需要量的满足;由于胃液向食管返流会加重患者病情,推荐建立空肠营养通路,根据患者病情决定经鼻或经皮空肠营养管通路的建立; 推荐使用持续微量泵控速泵入肠内营养液,由低速起,逐步加速。
(3)营养素:能量按25~35 kcal/(kg·d)给予。根据患者应激程度,可适当提高脂肪供能比,占非蛋白能量的40%~50%; 蛋白质按1 g/(kg·d)起步,目标供应量为1.2~2 g/(kg·d)。选择的营养制剂如果蛋白质不足,推荐额外补充乳清蛋白;肠道功能正常时,推荐使用整蛋白型肠内营养制剂,肠功能差时,可以选择要素型肠内营养制剂。可考虑选择富含免疫营养素的营养制剂; 根据推荐营养素摄入量补充微量元素,并根据监测结果调整;重度营养不良病人在营养支持早期,应注意避免再喂养综合征的发生。注意监测和补充磷、钾、钙、镁、维生素B1等。
(4)定期评价营养治疗效果:根据病情,每周至每月监测体重、握力、血液电解质、肝肾功能、体成分分析等指标。
专家组成员(按姓氏汉语拼音排序)
陈良安(解放军总医院)
李辉(北京红十字朝阳医院)
金发光(第四军医大学唐都医院)
丛明华(中国医学科学院肿瘤医院)
韩新巍(郑州医科大学第一附属医院)
赖国祥(解放军福州总医院)
李冬妹(煤炭总医院)
李王平 (第四军医大学唐都医院)
李闻(解放军总医院)
林殿杰(山东省立医院)
罗凌飞(煤炭总医院)
马洪明(煤炭总医院)
曲保林(解放军总医院)
沙正步(徐州医科大学附属医院),
石殿鹏(煤炭总医院)
宋小莲(上海第十人民医院)
谭培昭(中国医学科学院肿瘤医院)
谭强(上海肺科医院)
陶梅梅(煤炭总医院)
王洪武(煤炭总医院)
王娟 (北京天坛医院)
王晓平(山东胸科医院)
王志强(解放军总医院)
王子恺(解放军总医院)
吴世满(山西医科大学第一附属医院)
杨俊勇(新疆胸科医院)
曾奕明(福建医科大学第二附属医院)
张华平(福建医科大学第二附属医院)
张杰(北京天坛医院)
张雷(解放军福州总医院)
张楠(煤炭总医院)
周红梅(广东医科大学附属中山医院)
周云芝(煤炭总医院)
执笔人(按姓氏汉语拼音排序)
丛明华 金发光 柯明耀 李辉 李闻
王洪武 王子恺 曾奕明
参 考 文 献
1 Lenz CJ, Bick BL, Katzka D, et al. Esophagorespiratory Fistulas: Survival and Outcomes of Treatment[J]. J Clin Gastroenterol, 2018, 52(2): 131-136.
2 van Halsema EE, van Hooft JE. Clinical outcomes of self-expandable stent placement for benign esophageal diseases: A pooled analysis of the literature[J]. World J Gastrointest Endosc, 2015, 7(2): 135-153.
3 Marczyński W, Pająk M, Komandowska T, et al. Self-expandable metallic stents in oesophago-respiratory fistulas treatment in neoplasms-case reports and literature review[J]. Pneumonol Alergol Pol, 2015, 83(4): 303-306.
4 Shin JH, Kim JH, Song HY. Interventional management of esophagorespiratory fistula[J]. Korean J Radiol, 2010, 11(2): 133-140.
5 Martini N, Goodner JT, D′Angio GJ, et al. Tracheoesophageal fistula due to cancer[J]. J Thorac Cardiovasc Surg, 1970, 59(3): 319-324.
6 Balazs A, Galambos Z, Kupcsulik PK. Characteristics of esophagorespiratory fistulas resulting from esophageal cancers: a single-center study on 243 cases in a 20-year period[J]. World J Surg, 2009, 33(5): 994-1001.
7 Lutz FA, Herth FJ. Treatment of airway-esophageal fistulas[M]/Principles and practice of interventional pulmonology. New York, Springer, 2013: 421-434.
8 Shin JH, Song HY, Ko GY, et al. Esophagorespiratory fistula: long-term results of palliative treatment with covered expandable metallic stents in 61 patients[J]. Radiology,2004, 232(1): 252-259.
9 Murthy S, Gonzalez-Stawinski GV, Rozas MS, et al. Palliation of malignant aerodigestive fistulae with self-expanding metallic stents[J]. Dis Esophagus, 2007, 20(5): 386-389.
10 韩新巍, 吴刚, 马南, 等. 胸腔胃—气管(主支气管)瘘临床与影像学诊断体会[J]. 郑州大学学报(医学版), 2003, 38(3): 395-397.
11 吴雪梅, 柯明耀, 罗炳清, 等. 气道覆膜支架治疗胸腔胃-气道瘘48例临床分析[J]. 国际呼吸杂志, 2014, 34(20): 1554-1557.
12 Duranceau A, Jamieson GG. Malignant tracheoesophageal fistula[J].Ann Thorac Surg, 1984, 37(4): 346-354.
13 Kim KR, Shin JH, Song HY, et al. Palliative treatment of malignant esophagopulmonary fistulas with covered expandable metallic stents[J]. AJR Am J Roentgenol, 2009, 193(4): W278-W282.
14 Seto Y, Yamada K, Fukuda T, et al. Esophageal bypass using a gastric tube and a cardiostomy for malignant esophagorespiratory fistula[J]. Am J Surg, 2007, 193(6): 792-793.
15 王洪涛, 王国磊, 王文光, 等. 外科治疗食管呼吸道瘘——附7例报道[J]. 中国癌症杂志, 2015, 25(7): 549-554.
16 Shen KR, Allen MS, Cassivi SD, et al. Surgical management of acquired nonmalignant tracheoesophageal and bronchoesophageal fistulae[J]. Ann Thorac Surg, 2010, 90(3): 914-918.
17 Shin JH, Kim JH, Song HY. Interventional management of esophagorespiratory fistula[J]. Korean J Radiol, 2010, 11(2): 133-140.
18 Spaander MC, Baron TH, Siersema PD, et al. Esophageal stenting for benign and malignant disease: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline[J]. Endoscopy, 2016, 48(10): 939-948.
19 吴雪梅, 柯明耀, 罗炳清, 等. dumon支架治疗气道消化道瘘31例近期疗效观察[J]. 国际呼吸杂志, 2016, 36(4): 292-296.
20 Melendez J, Chu D, Bakaeen FG, et al. Tracheoesophageal fistula due to migration of a self-expanding esophageal stent successfully treated with a silicone “Y” tracheobronchial stent[J]. J Thorac Cardiovasc Surg, 2011, 141(6): e43-e44.
21 Wang H, Tao M, Zhang N, et al. Airway Covered Metallic Stent Based on Different Fistula Location and Size in Malignant Tracheoesophageal Fistula[J]. Am J Med Sci, 2015, 350(5): 364-368.
22 王洪武, 李冬妹, 张楠, 等. 气管内覆膜金属支架置入治疗食管气管瘘[J]. 中华结核和呼吸杂志, 2013, 36(5): 390-392.
23 殷世武, 项延淼, 叶录安. 全覆膜分叉形气管支架治疗食管气管瘘一例[J]. 介入放射学杂志, 2004, 13(5): 471-471.
24 谢亚敏, 章俊, 谌琴. dsa定位下不同原因食管气管瘘内支架置入的临床应用[J]. 安徽医学, 2014, 35(3): 315-317.
25 杨迪, 马洪升, 张雪梅, 等. 食管瘘治疗新进展[J]. 华西医学, 2015, 30(10): 24-25.
26 马洪明, 邹珩, 张洁莉, 等. 食道双支架置入治疗食管气管瘘临床初探[J]. 基础医学与临床, 2015, 35(7): 968-971.
27 杨营军, 庞志锋, 刘新光. 内镜下置入带膜支架治疗食管上段癌性食管气管瘘31例疗效评价[J]. 胃肠病学, 2004, 9(6): 377-378.
28 武贝, 茅爱武, 吴绍秋. 内镜直视联合x线导向介入治疗食管气管瘘一例[J]. 介入放射学杂志, 2013, 22(7): 615-616.
29 李远鹏, 柯明耀, 吴雪梅, 等. 气管食管双支架治疗合并气管狭窄的恶性食管气管瘘55例[J]. 实用医学杂志, 2016, 32(11): 1847-1849.
30 Abadal JM, Echenagusia A, Simo G, et al. Treatment of malignant esophagorespiratory fistulas with covered stents[J]. Abdom Imaging, 2001, 26(6): 565-569.
31 Saxon RR, Barton RE, Katon RM, et al. Treatment of malignant esophageal obstructions with covered metallic Z stents: long-term results in 52 patients[J]. J Vasc Interv Radiol, 1995, 6(5): 747-754.
32 Kishi K, Nakao T, Goto H, et al. A fast placement technique for covered tracheobronchial stents in patients with complicated esophagorespiratory fistulas[J]. Cardiovasc Intervent Radiol, 2005, 28(4): 485-489.
33 Balazs A, Kupcsulik PK, Galambos Z. Esophagorespiratory fistulas of tumorous origin. Non-operative management of 264 cases in a 20-year period[J]. Eur J Cardiothorac Surg, 2008, 34(5): 1103-1107.
34 Saxon RR, Barton RE, Katon RM, et al. Treatment of malignant esophagorespiratory fistulas with silicone-covered metallic Z stents[J]. J Vasc Interv Radiol, 1995, 6(2): 237-242.
35 Wang MQ, Sze DY, Wang ZP, et al. Delayed complications after esophageal stent placement for treatment of malignant esophageal obstructions and esophagorespiratory fistulas[J]. J Vasc Interv Radiol, 2001, 12(4): 465-474.
36 Devière J, Quarre JP, Love J, et al. Self-expandable stent and injection of tissue adhesive for malignant bronchoesophageal fistula[J]. Gastrointest Endosc, 1994, 40(4): 508-510.
37 Nam DH, Shin JH, Song HY, et al. Malignant esophageal-tracheobronchial strictures: parallel placement of covered retrievable expandable nitinol stents[J]. Acta Radiol, 2006, 47(1): 3-9.
38 Ke MY, Huang R, Lin LC, et al. Efficacy of the DumonTMStent in the Treatment of Airway Gastric Fistula: A Case Series Involving 16 Patients[J]. Chin Med J (Engl), 2017, 130(17): 2119-2120.
39 Hu Y, Zhao YF, Chen LQ, et al. Comparative study of different treatments for malignant tracheoesophageal/bronchoesophageal fistulae[J]. Dis Esophagus, 2009, 22(6): 526-531.
40 Binkert CA, Petersen BD. Two fatal complications after parallel tracheal-esophageal stenting[J]. Cardiovasc Intervent Radiol, 2002, 25(2): 144-147.
41 Petrella F, Toffalorio F, Brizzola S, et al. Stem Cell Transplantation Effectively Occludes Bronchopleural Fistula in an Animal Model[J]. Ann Thorac Surg, 2014, 97(2): 480-483.
42 Petrella F, Acocella F, Barberis M, et al. Airway fistula closure after stem-cell infusion[J]. N Engl J Med, 2015, 372(1): 96-97.
44 Alvarez PD, Garcíaarranz M, Georgievhristov T, et al. A new bronchoscopic treatment of tracheomediastinal fistula using autologous adipose-derived stem cells[J]. Thorax, 2008, 63(4): 374-376.
45 杨蔚峰, 饶官华, 班洁虹, 等. 内镜下otsc系统闭合术治疗食管瘘3例报告[J]. 微创医学, 2017, 12(2): 272-273.
46 叶梦思, 周羽翙, 何云, 等. 内镜下otsc吻合系统夹闭外伤性食管气管瘘1例[J]. 中国内镜杂志, 2016, 22(3): 108-110.
47 刘石萍, 王军民, 刘振祥, 等. 胃镜下医用生物蛋白胶治疗食管气管瘘32例[J]. 中华消化内镜杂志, 2010, 27(4): 215-216.
48 高永平, 王洪武, 周云芝, 等. 食管气管瘘合并下呼吸道感染的病原学特点[J]. 国际呼吸杂志, 2017, 37(3): 171-172.
49 Arends J, Bachmann P, Baracos V, et al. ESPEN guidelines on nutrition in cancer patients[J]. Clin Nutr, 2017, 36(1): 11-48.
50 黄河, 郭婷, 程国昌. 食管癌并发气管食管瘘63例临床分析[J]. 海南医学, 2013, 24(24): 3624-3626.
51 Persson S, Rouvelas I, Irino T, et al. Outcomes following the main treatment options in patients with a leaking esophagus: a systematic literature review[J]. Dis Esophagus, 2017, 30(12): 1-10.
52 Silon B, Siddiqui AA, Taylor LJ, et al. Endoscopic Management of Esophagorespiratory Fistulas: A Multicenter Retrospective Study of Techniques and Outcomes[J]. Dig Dis Sci, 2017, 62(2): 424-431.

