对必修模块“化学能与热能”有效教学的思考
摘 要:以必修模块高中化学教材《必修二》中《化学能与热能》的内容,根据学生的认知规律进行有效教学的思考。
关键词:化学能;化学反应的热效应;化学键;教学设计
本文所讨论的内容为人教版《化学2》第二章“化学反应与能量”第一节“化学能与热能”的教学内容。从化学反应化学键的变化与能量的转化认识化学反应的热效应,此部分的内容是高中学习的一个重点内容,又对《选修四》的学习起着承前的作用。
一、对教材知识要求的认识
新课标的教学要求:理解化学键的断裂与形成是化学反应是能量变化的主要原因,能够从微观结构的变化看化学反应与能量变化过程,建立科学的能量观。
从课标的要求与本节的内容来看,涉及的知识点有:认识化学反应的热效应;了解常见的化学反应的热效应;认识化学能的存在与物质性质之间的关系以及同一物质不同状态下的化学能高低和化学反应中能量的转换关系;理解化学键的变化过程中的能量变化以及在这种变化过程中分子、原子的能量大小关系及转化;了解人类文明的发展与对化学能的利用的联系等。其中从能量变化的角度认识化学反应的热效应与从微观化学键的角度来解释化学反应的热效应是本节的难点。
二、教材的编排与笔者的设计思考
教材从化学键引起热量的变化从而引起化学能与热能之间的转化,通过三个典型的实验体验化学反应中的热效应并掌握常见的化学反应的热效应。其优点是与上一节所学化学键内容相扣,先从理论找依据,再从实验验证与理解,环环相扣,紧密相连。但在教学的过程中笔者发现,以此编排进行的教学中一开始给出化学键的变化与能量的关系对初学化学键的学生来说难度过大,引入化学反应中能量的转化过于生硬,学生容易把微观的化学键变化的相关能量与化学能的变化弄混,在分析中只能机械地记住结论,经常得出自相矛盾的结论,教材中化学能的概念不明确且与其他概念相互关系复杂。因而只有明晰概念,理清关系,才能解决教学中的难点。
只有从尊重学生的认知的角度去设计教学,理顺教学关系,才能让学生成为学习的主人。因而可设计先从分组实验让学生从感性上认识化学反应的热效应,再以能量守恒进入化学能与热能之间的转化,最后再用化学键在化学反应中的变化解释能量转化的设计。这种先让学生认知现象,再探究本质,理论与实际相结合,或许会更加符合新课标对探究式教学的要求和学生的认知规律。
三、对教材设计实验的运用
在教学中可先从教材设计了三个典型的实验,设计探究式学生分组,依据实验展开问题讨论,如下:
实验2-1放热反应的概念可用于探究化学反应速率的影响因素金属与酸反应的热效应小结
实验2-2吸热反应的概念常见的吸热反应吸热反应与反应条件的关系
实验2-3中和反应的热效应化学反应的热效应分类与四种基本反应的交叉小结能量的变化是化学反应的另一基本特征
通过三组简单的实验与问题探究,充分地利用学生分组讨论,教师进行合理的引导,从而使学生对“能量变化是化学反应的另一基本特征”有了深刻的感性认识,激发了学生的学习兴趣与培养了探究意识,进一步发问:“化学反应的热效应究竟由什么决定?”更加能激发学生的思考与预习,为对化学反应热效应的理论学习打好基础和做好准备。
四、对化学反應热效应的理论探究
从探究中认识到有能量变化是化学反应的另一特征,思考能量既不能凭空产生,又不能凭空消失,那么放热反应放出的能量来自何方,吸热反应吸收的热量又去何处了呢?如此从现象到本质的学习提上研究议程,引出物质本身具有化学能可在化学反应中体现出来。
1.什么是化学能
任何物质都有化学能,教学中可认为化学能是物质本身具有的且能在化学变化中体现出来的内能。
问题探究:
(1)同一物质不同状态的化学能的变化,如,水、水蒸气、冰。
(2)金刚石与石墨化学能和稳定性比较。
教学结论:
①同一种物质所具有的化学能:气态 >液态>固态。
②一般来说具有的化学能越高的物质越不稳定,化学性质越活泼。
2.化学能中化学反应中的变化
化学反应中物质变化的同时所对应的化学能也发生了变化。
对比讨论:
化学反应中能量的转化关系:
化学反应A+B=C+D
若物质的化学能的关系:
A与B的化学能>C与D的化学能,则该反应放热,能量的转化关系为化学能转化为热能。
若物质的化学能的关系:
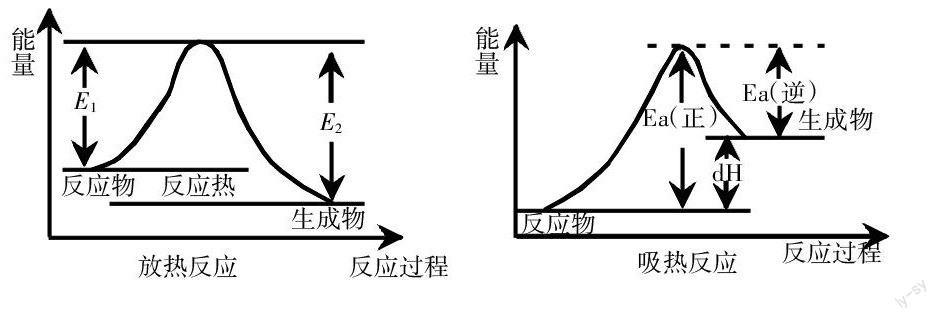
A与B的化学能 结论: 化学反应的热效应与反应物的总能量与生成物的总能量的相对大小有关,作图分析: ■ ■ 3.化学能为什么能转化 化学能的转化与化学反应的进行过程有关,因而与化学反应中化学键的变化有关。 《分析》从化学键去分析化学反应的过程: ■ 举例:H2+Cl2=2HCl (1)从分子拆分为原子需要断裂化学键,把结合紧密的原子分开,需要提供能量,此时外部的能量转化为原子的化学能。 H—H→H + H 吸收能量436 kJ /mol E(H2)< 2E(H) Cl—Cl→Cl+Cl 吸收能量243 kJ /mol E(Cl2)<2E(Cl) 断键一共需吸收热量为=436kJ+243kJ=679kJ (2)原子重新组合为新分子,把高能量的原子结合形成作用,此时多余化学能便会释放出来转化为了热能。 H+Cl→H—Cl放出能量432kJ/mol E(H)+E(Cl)>E(HCl) 成键一共需放出能量为=2×432kJ=864kJ所以:此1mol反应对外放出能量=864kJ-679kJ=185kJ 因而,结合两个过程的能量的不同变化,由于断裂的化学键与形成的新化学键不一样,因而两个过程中的化学能的转化大小一定不相等,因而总体上便会有能量的变化: 当断键所需的总能量小于成键所放的总能量时,此反应对外放热。 当断键所需的总能量大于成键所放出的总能量时,此反应对外吸热。 四、教学实践过程中的小结 从实验发现问题到理论解释再到寻找原因,学生已经完成一轮科学探究式的学习过程。从宏观的化学反应的能量特征、能量变化再到微观的化学键变化,配合了学生的认知规律与学习能力,同时教学切入点简单,知识深度层层相扣,各知识点完全成线连结。学生对常见的化学反应的热效应、化学能的概念、物质的性质与能量的关系,化学反应中能量的相互转化、化学键与能量的关系等知识有了较为深刻的了解,再结合相关的练习,相信一定可以达到新课标的教学要求。 参考文献: [1]杨圣群.谈基于学生认知能力的“化学能与热能”的教学[J].化学教与学,2011(03):21-22. [2]保志明.从尊重与丰富学生认知的角度设计教学:必修模块“化学能与热能”的教学思考[J].中学化学教学参考,2012(08):14-15. 作者简介:彭爱华,男,广东省珠海市,1977年出生,学历:本科,职称:中学一级教师,研究方向:中学化学教育。 编辑 王团兰