钠-葡萄糖协同转运蛋白-2抑制剂治疗2型糖尿安全性的荟萃分析
李志红,张海桥,刘玉婷,江芳芳,朱艳,秦淑兰
(1.江西省南昌市第一医院;2.江西省南昌市第三医院,南昌 330008;3.南方医科大学第五附属医院,广州 510900)
2型糖尿病是一种进行性发展的复杂的慢性代谢性疾病,已成为当今重大健康问题[1]。据估计,2017年全球有4.51亿(18~99岁)糖尿病患者,到2045年,这些数字预计将增加到6.93亿。据估计,几乎一半的糖尿病患者(49.7%)没有得到诊断,此外,估计有3.74亿人患有葡萄糖耐量异常(IGT)。2017年,全球糖尿病患者的医疗支出约为8500亿美元[2],治疗糖尿病已成为我们现在热点话题。目前,临床上降糖药物包括磺脲类、非磺脲类促胰岛素分泌剂、双胍类、α-糖苷酶抑制剂、噻唑烷二酮类、DPP-IV抑制剂、胰岛素及GLP-1受体激动剂[3]。现有的口服抗糖尿病药物有局限性,如使用噻唑烷二酮类和磺脲类药物会导致体重增加,使用磺脲类药物会导致低血糖,使用双胍类药物和a-糖苷酶抑制剂会导致胃肠道副作用等[4-5]。因此,需要一种新型的抗糖尿病药物,对T2DM患者长期有效且耐受性良好。钠—葡萄糖协同转运蛋白-2抑制剂(SGLT-2I)是一种新型的口服降糖药,可通过抑制肾脏近曲小管对葡萄糖重吸收,并不依赖胰岛素分泌,不受胰腺β细胞功能的影响,促进尿糖排泄进而降低血糖[6]。多项研究结果表明SGLT-2I具有降低血糖、减轻体重及降低血压的作用[7-9]。然而,研究[7-9]表明SGLT-2I由于抑制肾脏葡萄糖重吸收,引起血糖降低、尿糖升高,故易发生生殖系统和泌尿系统感染,因此存在一些安全性问题。目前国内仍缺乏针对SGLT-2I治疗2型糖尿病患者安全性的资料。因此,我们应用Meta分析(Meta-analysis)对SGLT-2I治疗2型糖尿病的相关文献进行综合分析,目的是为临床应用SGLT-2I提供一定的参考依据。
1 资料与方法
1.1 检索策略 2名研究者通过对pubmed、MEDLINE、EMBASE、Cochrane和Web of science数据库的文献进行检索。检索时间为从建库到2019年4月。英文检索词为“SGLT-2I”or“Sodiumglucose cotransporter 2 inhibitors”or“dapagliflozin”or“canagliflozin”or“empagliflozin”or“ipragliflozin”or“luseogliflozin”or “tofogliflozin”and “T2DM”or“type 2 of diabetes”and “randomized controlled trial”or“controlled clinical trial”or“randomized or randomly trial”。将检索到的文章进行标题、关键字、摘要及下载到的全文进行评估。
1.2 文献纳入与排除标准 入选标准:随机、双盲对照研究;所有受试者均为明确诊断2型糖尿病患者,且试验前未使用过降糖药;随机对照临床试验的治疗组及对照组分别给予SGLT-2I或安慰剂治疗。排除标准:入选研究为非随机对照研究;研究对象治疗前后接受过其他降糖药的治疗,且这种治疗方式应用时间长,可能影响本次研究的结果;研究语种非英文;研究对象是动物或健康人或1型糖尿病;对照组为其他降糖药、胰岛素等;肾功能不全(血清肌酐水平为参考范围上限)、肝功能损害(AST或ALT水平为参考范围上限的3倍)和其它内分泌疾病。
1.3 数据提取与质量评价 由2位研究人员分别独立检索并阅读相关文献,根据入选标准及排除标准提取出入选文献,当意见不同时再一起进行讨论。提取的资料包括文献名称、发表年份、患者年龄、性别、病例数、用药类型、用药剂量、用药前后谷草转氨酶、谷丙转氨酶、肌酐、低血糖发生例数、生殖系统感染发生例数、泌尿系统感染发生例数。采用jadad评分法对文献进行质量评价,1~3分为低质量文献,4~7分为高质量文献。
1.4 统计学分析 本Meta-分析应用RevMan 5.3软件,该软件由Cochrane协作网提供。连续变量(如AST及ALT)用WMD(Weighted Mean Difference,加权均数差)及其95%置信区间(95%CI)作为疗效分析统计量;计数资料(如低血糖发生例数、生殖系统感染发生例数、泌尿系统感染发生例数)用RR(Related Risk,风险比)及95%可信区间(95%CI)作为疗效分析统计量。采用I2值检验各研究间的异质性,如果I2值大于50%,说明文献的统计异质性明显。否则,我们认为不存在显著的统计学异质性。Meta分析采用随机效应模型,Meta分析以0.05为检验标准,P≤0.05为差异有统计学意义。
2 结果
2.1 纳入文献特点 在各个数据库输入关键词后,初检出相关文献共1227篇。依据文献纳入及排除标准,最终本研究共纳入11篇文献,具体筛选流程见图l。各篇文献的基本资料及数据,见表1-3。
2.2 治疗前后肝功能的变化值 4篇文献评价了SGLT-2I对谷草转氨酶和谷丙转氨酶的影响,其中SGLT-2I组870例,安慰剂组661例。I2值检验提示各研究间有显著的异质性(谷草转氨酶I2=90%;谷丙转氨酶I2=90%)。SGLT-2I组与安慰剂组相比可降低糖尿病患者谷草转氨酶(WMD=-1.23 U/L,95%的置信区间为-1.98~-0.47;P=0.001)。SGLT-2I组与安慰剂组相比可显著降低糖尿病患者谷丙转氨酶(WMD=-3.09 U/L,95%的置信区间为-4.14~-2.04;P<0.001)。
2.3 治疗前后肌酐的变化值 5篇文献评价了SGLT-2I对肌酐的影响,其中SGLT-2I组378例,安慰剂组441例。I2值检验提示各研究间具有显著的异质性(I2=97%)。SGLT-2I组与安慰剂组相比血清肌酐的变化无显著差异(WMD=-3.09 U/L,95%的置信区间为-4.14~-2.04;P<0.001)。
2.4 低血糖 7篇文献报道了低血糖的发生事件,其中SGLT-2I组3073例,安慰剂组3005例。I2值检验提示各研究间无异质性(I2=0%)。SGLT-2I组低血糖的发生率与安慰剂组相比无统计学差异(RR=1.12,95%的置信区间为0.97~1.30;P=0.11)。
2.5 生殖系统的感染 8篇文献报道了生殖系统的感染发生事件,其中SGLT-2I组3108例,安慰剂组3041例。I2值检验提示各研究间无异质性(I2=0%)。SGLT-2I组生殖系统感染的发生率明显高于安慰剂组(RR=7.19,95%的置信区间为4.50~11.47;P<0.001)。

图1 文献筛选流程图
2.6 泌尿系统的感染 7篇文献报道了泌尿系统的感染的发生事件,其中SGLT-2I组2990例,安慰剂组2932例。I2值检验提示各研究间无异质性(I2=0%)。SGLT-2I组生殖系统感染的发生率稍高于安慰剂组(RR=1.36,95%的置信区间为1.06~1.75;P=0.02)。
2.7 异质性分析 Meta分析的异质性一部分来源于原始文献质量的异质性。本文所纳入的研究均为随机双盲研究,由表1可看出,存在6篇低质量研究。本研究纳入的原始文献实验组所用SGLT-2I的种类及剂量各有不同,研究对象来自不同的国家。我们所纳入的各个研究血清肌酐的单位不同(Linong N 2014、Yutaka M 2014、Sano M 2018使用mg/dL,而C.J.Bailey 2012和Ferrannini J 2010使用μmol/L,虽然我们统一转换为μmol/L),所使用测量试剂有所差异。另一个来源是纳入分析的各研究结果的一致性或趋向性。本研究纳入的原始文献数量少,限制了我们使用漏斗图分析发表偏倚。因此我们认为本文异质性可能来自发表偏倚及文献质量、研究的干预措施及研究对象、结局测量上等的差异。
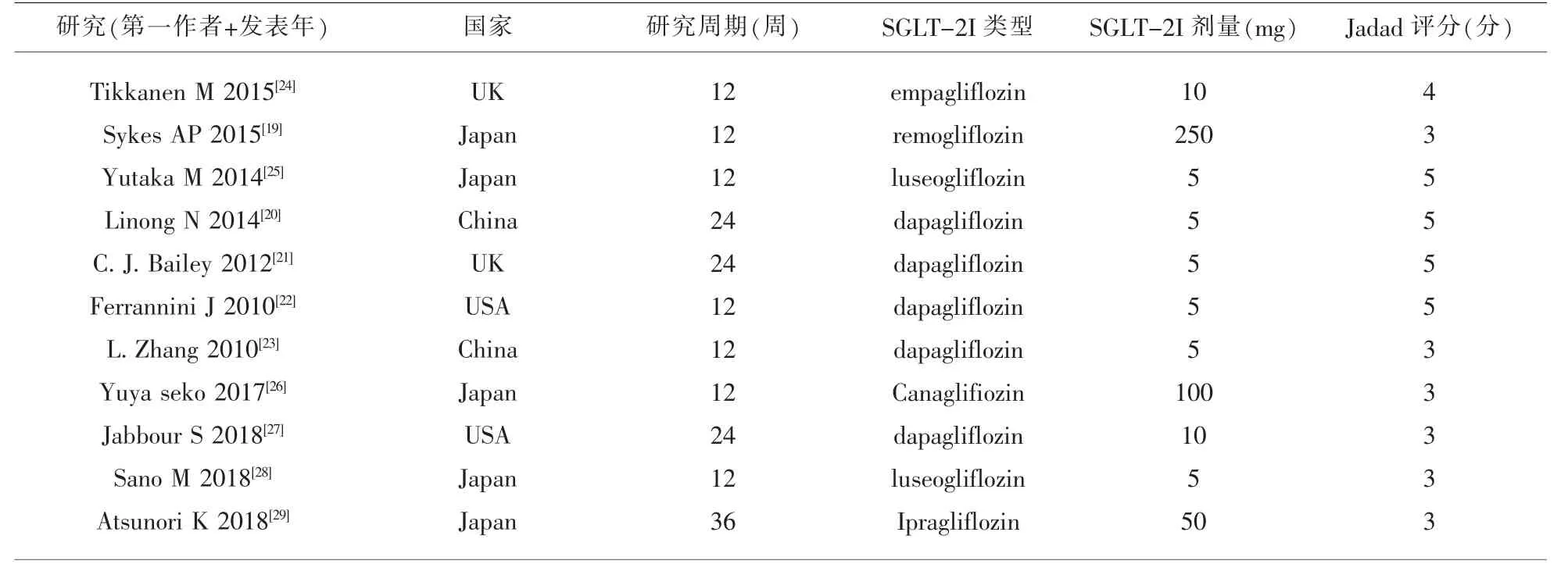
表1 入选研究的基本资料

表2 纳入研究的数据总结表

表3 纳入研究的数据总结表
3 讨论
2型糖尿病是由胰岛素分泌不足或胰岛素抵抗引起血糖水平升高的一种代谢性疾病,若长期高血糖无法得到良好控制,会引发微血管(糖尿病肾病及糖尿病视网膜病变)和大血管(冠心病、脑中风及周围血管疾病)多种并发症,严重影响患者的生活质量及生命安全[10]。因此,2型糖尿病患者血糖控制是非常重要的。SGLT-2I是一类新型口服治疗2型糖尿病的药物。它是通过钠-葡萄糖协同转运蛋白-2受体抑制肾脏对葡萄糖的再吸收,从而促进肾脏葡萄糖在尿液中的排泄来降低血糖[11]。然而,SGLT-2I的具体作用机制及其他药效学影响结果有些是有益的(如降低血糖、减轻体重及降低血压等),但另一些是潜在的有害不良反应。因此,在这篇Meta分析中综合评价SGLT-2I的安全性。本研究发现,SGLT-2I组与安慰剂组相比并不会损害肝功能。根据最近的研究,肝功能的变化可能与体重减轻、血糖控制和胰岛素抵抗改善有关[12]。一些研究发现,糖尿病会增加肝功能异常的风险[13],这对于SGLT-2I不会导致肝功能异常具有重要意义。
本研究显示SGLT-2I组与安慰剂组相比血清肌酐无明显差异,提示SGLT-2I不引起肾功能障碍。在2型糖尿病肾病患者的初始阶段常引起肾小球滤过率(GFR)升高[11]。SGLT-2I通过降低近端小管对钠的重吸收,使得远曲小管中钠离子浓度升高,小管液通过致密斑的钠负荷量增加,进而通过管球反馈机制使得肾小球血液动力学发生改变,导致肾小球内压下降,降低了GFR[14],故在2型糖尿病初期SGLT-2I不会引起肾功能异常。然而,对于肾功能异常的2型糖尿病患者是否合适用SGLT-2I及长期使用仍有待确定。
Meta分析发现,SGLT-2I与安慰剂相比生殖系统感染风险增加约七倍,泌尿系统感染风险轻微升高。这种作用可能部分归因于糖尿的增加[15],但免疫功能障碍和尿上皮细胞糖基化改变也会影响[16]。尽管如此,大多数泌尿生殖系统感染为轻度至中度,几乎没有患者因此而停药,且经常规抗菌治疗后即可有效缓解[15]。结果还表明,SGLT-2I发生低血糖的概率与安慰剂相比无无显著差异。因为SGLT-2I独特的作用机制,并不依赖于促进β细胞功能和改善胰岛素抵抗,所以低血糖的发生率非常低[17]。其次,在血糖水平较低的情况下,SGLT2抑制剂会降低尿糖排泄,从而降低了低血糖的风险[18]。
本研究也有不足之处。首先,为了直接观察SGLT-2I对2型糖尿病的疗效,我们排除了其他药物的影响,正因如此,本研究纳入的原始文献数量少,研究结果仍需进一步证实。其次,我们没有发现肝功能和血清肌酐的异质性来源。我们认为异质性可能来自于发表偏倚、研究质量、干预措施、研究对象和结果测量的差异。最后,虽然我们的研究仅限于随机对照试验,但一些研究的质量较低。
综上所述,SGLT-2抑制剂不会损害肝肾功能,同时发生低血糖风险低,虽然有泌尿生殖系统的感染,但抗感染药物疗效较好,易于为病人所接受,故SGLT2抑制剂有很好的应用前景。

