轻型卒中及TIA患者静脉溶栓后短期不良结局的危险因素研究
陆叶婷,袁霞
近年卒中已跃居中国致死率最高的疾病[1]。其中,轻型缺血性卒中由于其症状轻、自发好转倾向[2]常为大众轻视,实际约29%的轻型卒中患者预后不良,可能进展或存在极高的进展、复发风险[3]。因此,尽早干预极为重要。
国内外指南[4-6]认为,轻型致残性卒中推荐时间窗内应尽早溶栓,而非致残性则需要根据获益情况而定,仍需要其他相对客观的临床指标来指导轻型卒中的静脉溶栓。近年来,多模式影像学技术发展迅猛,许多大型前瞻性研究如影像评估筛选缺血性卒中患者血管内治疗研究(DEFUSE-3)等得益于此,已指导临床筛选出较多适合血管内治疗的患者,其利用血管狭窄以及缺血/梗死体积不匹配(mismatch)相结合的研究思路对于轻型卒中的治疗决策亦有提示作用。目前已有一些研究[7-8]通过单一比较血管狭窄或缺血灌注的体积来评估轻型卒中的预后,但将二者结合的研究仍较少,故本研究结合血管、灌注情况探索基线NIHSS评分0~5分的轻型卒中或TIA患者静脉溶栓治疗后结局不良的危险因素。
1 对象与方法
1.1 对象 连续纳入自2019年10月至2020年7月就诊于苏州大学附属第一医院神经内科门急诊NIHSS评分0~5分的轻型卒中或TIA患者,并根据起病14 d mRS评分将其分为两组:mRS>1分为不良结局组,≤1分则为良好结局组。纳入标准:(1)均予标准剂量阿替普酶静脉溶栓(0.9 mg/kg,10%静脉推注,1 h内滴注其余90%);(2)存在持续性或发作性神经功能缺损症状,溶栓时基线NIHSS评分为0~5分;(3)发病前mRS为0分;(4)溶栓前均完善一站式CT(CTA以及CT灌注成像)。排除标准:(1)无法行头颅MRI者;(2)失访或资料不完整;(3)不良临床结局与血管事件不相关(如恶性肿瘤,意外等);(4)判定为假性卒中者;(5)进行桥接取栓治疗。
1.2 方法
1.2.1 溶栓治疗 所有静脉溶栓患者均记录溶栓基线指标,溶栓后24 h内复查头颅CT,无出血转化者遵指南[7-8]个体化抗栓治疗,存在出血转化者待血肿吸收后抗栓治疗。所有患者均收治于卒中中心,溶栓后行3.0 T或1.5 T头颅MR并完善危险因素筛查。
1.2.2 溶栓前一站式CT检查 使用64排螺旋Revolution CT(通用电气医疗系统,美国),造影剂为碘普罗胺注射液(优维显;拜耳公司,德国),CT扫描自主动脉弓下缘至颅顶,扫描参数如下:往复动态扫描模式,管电压100 kV,管电流200 mA,螺距1.0,采集层厚5 mm,层距5 mm;原始CTA由影像科专业医师重建。
1.2.3 评价标准 (1)基于CTP利用MIStar软件(阿波罗医疗成像科技公司,澳大利亚)计算低灌注区及核心梗死区域体积,低灌注区定义为相对延迟时间(DT)>3 s的区域,梗死核心区定义为CT上相对脑血流量(CBF)<30%的区域,错配区定义为低灌注区域与核心梗死区的差值,存在错配区即差值>0(以下简称为Mismatch+),无错配区即差值为0(简称为Mismatch-),见图1。(2)责任血管狭窄(以下简称为CTA+)定义为基于CTA上狭窄率≥50%,狭窄率计算公式为病变血管最狭窄处直径/病变血管近端正常血管直径×100%(包括颈内动脉,大脑前动脉A1段,大脑中动脉M1或M2段,大脑后动脉P1段,椎动脉以及基底动脉颅内段);且与本次新发梗死灶相符或能解释起病时的神经功能缺损症状,相反,<50%定义为无责任血管狭窄(简称为CTA-)。见图2。(3)将标准(1)和(2)进一步结合可将患者分为4类,即CTA+Mismatch+、CTA+Mismatch-、CTA-Mismatch+、CTA-Mismatch-。举例见图1、图2。(4)发作性起病定义为1周内至少两次类似神经缺损症状并且除外最后一次的发作均应完全缓解。(5)复发:溶栓后14 d内新出现的神经缺损症状(包括发作性起病完全缓解溶栓后再发)。(6)基线运动功能缺损:基线NIHSS评分中涉及肌力评分条目的神经功能缺损症状,无论评分高低。
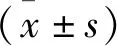
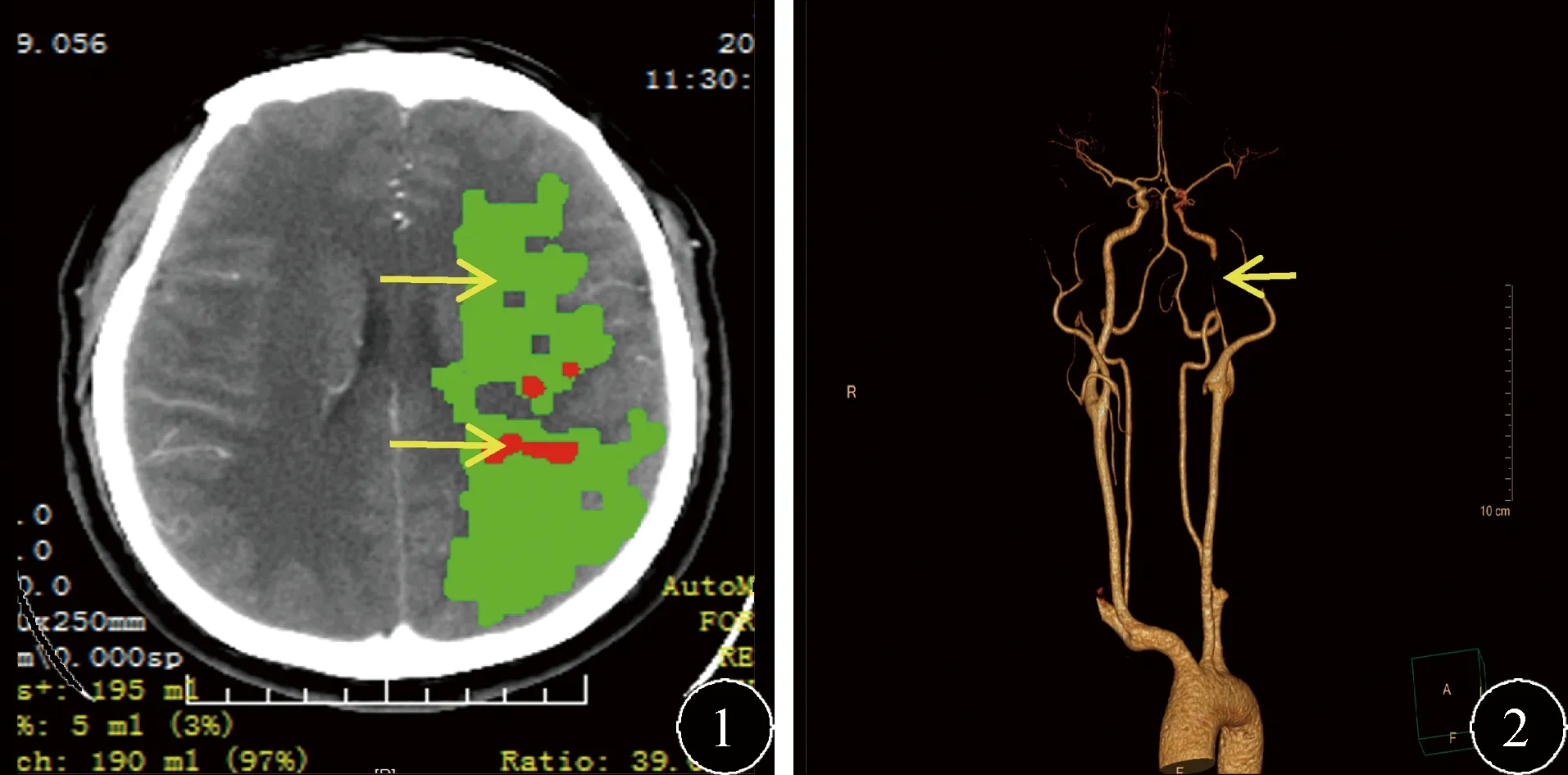
图1 CTP经MIStar软件处理后所得图像 图中箭头所指绿色部分为低灌注区(DT>3 s),红色部分为核心梗死区(CBF<30%),错配区即为绿色部分195 ml与红色部分体积5 ml之差,即190 ml,根据评价标准(4)为Mismatch+ 图2 主动脉弓上CTA CTA 箭头所示为责任动脉,提示左侧颈内动脉C1段重度狭窄局部闭塞,根据评价标准(5)为CTA+。根据评价标准(6)该病例既存在责任血管狭窄又存在错配区,分类为CTA+Mismatch+,其他病例可依此类推。图1与图2来自同一患者
2 结 果
符合纳入标准的患者共101例,其中6例基线资料不完整,假性卒中1例,最终94例患者纳入本研究。其中结局不良组28例(29.8%),结局良好组66例(70.2%)。所有患者发病至MR检查时间为(2.3±1.1)d。76例患者在MR弥散加权像上存在责任高信号病灶,即急性梗死灶;18例无病灶,最终诊断为TIA。
2.1 两组基线资料的比较 见表1。男62例(66%),女32例(34%),不同结局组间性别差异无统计学意义(P<0.05)。平均年龄为(63.4±13.2)岁,结局良好组年龄[(60.7±12.5)岁]较结局不良组[(67.1±11.3)岁]明显降低(P<0.05)。2例(2.1%)出血转化,欧洲急性卒中协作研究(ECASS)分级为出血性脑梗死-1(HI-1)型及脑实质出血-1(PH-1)型。NIHSS评分在两组间差异有统计学意义(P<0.05),其余基础抗栓治疗、溶栓基线指标、危险因素、溶栓后抗栓方案、有无复发、有无出血转化在不同结局组间差异均无统计学意义(均P>0.05)。
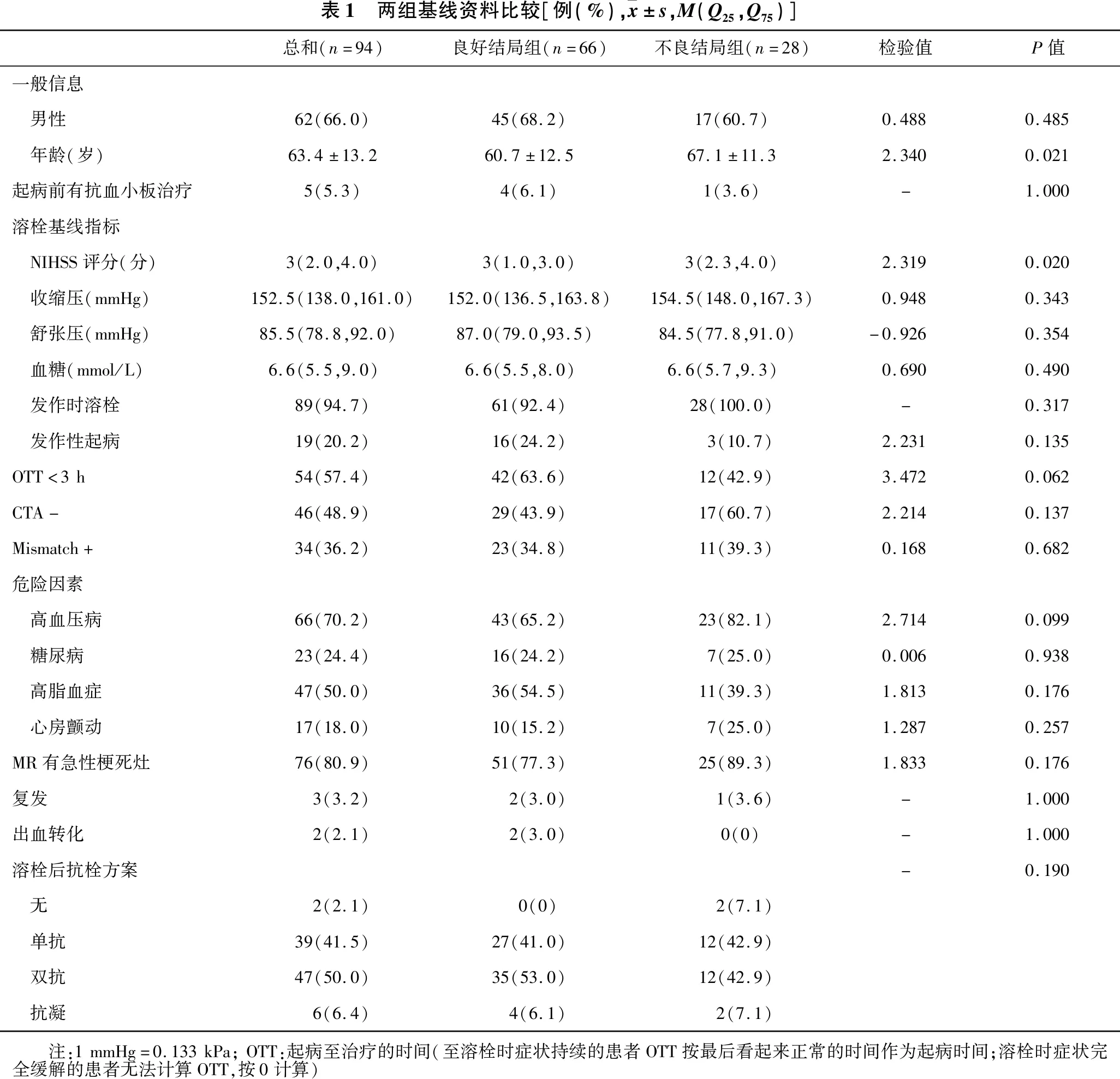
表1 两组基线资料比较[例(%), x±s,M(Q25,Q75)]总和(n=94)良好结局组(n=66)不良结局组(n=28)检验值P值一般信息 男性62(66.0)45(68.2)17(60.7)0.4880.485 年龄(岁)63.4±13.260.7±12.567.1±11.32.3400.021起病前有抗血小板治疗5(5.3)4(6.1)1(3.6)-1.000溶栓基线指标 NIHSS评分(分)3(2.0,4.0)3(1.0,3.0)3(2.3,4.0)2.3190.020 收缩压(mmHg)152.5(138.0,161.0)152.0(136.5,163.8)154.5(148.0,167.3)0.9480.343 舒张压(mmHg)85.5(78.8,92.0)87.0(79.0,93.5)84.5(77.8,91.0)-0.9260.354 血糖(mmol/L)6.6(5.5,9.0)6.6(5.5,8.0)6.6(5.7,9.3)0.6900.490 发作时溶栓89(94.7)61(92.4)28(100.0)-0.317 发作性起病19(20.2)16(24.2)3(10.7)2.2310.135OTT<3h54(57.4)42(63.6)12(42.9)3.4720.062CTA-46(48.9)29(43.9)17(60.7)2.2140.137Mismatch+34(36.2)23(34.8)11(39.3)0.1680.682危险因素 高血压病66(70.2)43(65.2)23(82.1)2.7140.099 糖尿病23(24.4)16(24.2)7(25.0)0.0060.938 高脂血症47(50.0)36(54.5)11(39.3)1.8130.176 心房颤动17(18.0)10(15.2)7(25.0)1.2870.257MR有急性梗死灶76(80.9)51(77.3)25(89.3)1.8330.176复发3(3.2)2(3.0)1(3.6)-1.000出血转化2(2.1)2(3.0)0(0)-1.000溶栓后抗栓方案-0.190 无2(2.1)0(0)2(7.1) 单抗39(41.5)27(41.0)12(42.9) 双抗47(50.0)35(53.0)12(42.9) 抗凝6(6.4)4(6.1)2(7.1) 注:1mmHg=0.133kPa;OTT:起病至治疗的时间(至溶栓时症状持续的患者OTT按最后看起来正常的时间作为起病时间;溶栓时症状完全缓解的患者无法计算OTT,按0计算)
2.2 责任血管狭窄联合错配区对预后的影响分析 见表2、表3。通过对基线指标分析,单独CTA及Mismatch对预后的影响较小,故将二者联合后进一步比较。在CTA+条件下,是否存在错配区在不同结局组间差异无统计学意义;CTA-条件下类似,差异亦无统计学意义。Mismatch+条件下,是否存在血管狭窄在不同结局组间差异无统计学意义;Mismatch-条件下,无血管狭窄在预后不良组占比更高,差异具有统计学意义(P=0.035),CTA仅与Mismatch-此因素联合对预后的判断有意义。进一步分析CTA-Mismatch-亚组(共38例),56.5%存在责任病灶,其中病灶主要分布基底节、脑干以及皮质(表3),不同病灶位置的短期预后在组间学差异有统计学意义(P=0.027);基线运动功能缺损患者在预后不良组比率更高,具有统计学意义(P=0.004)。
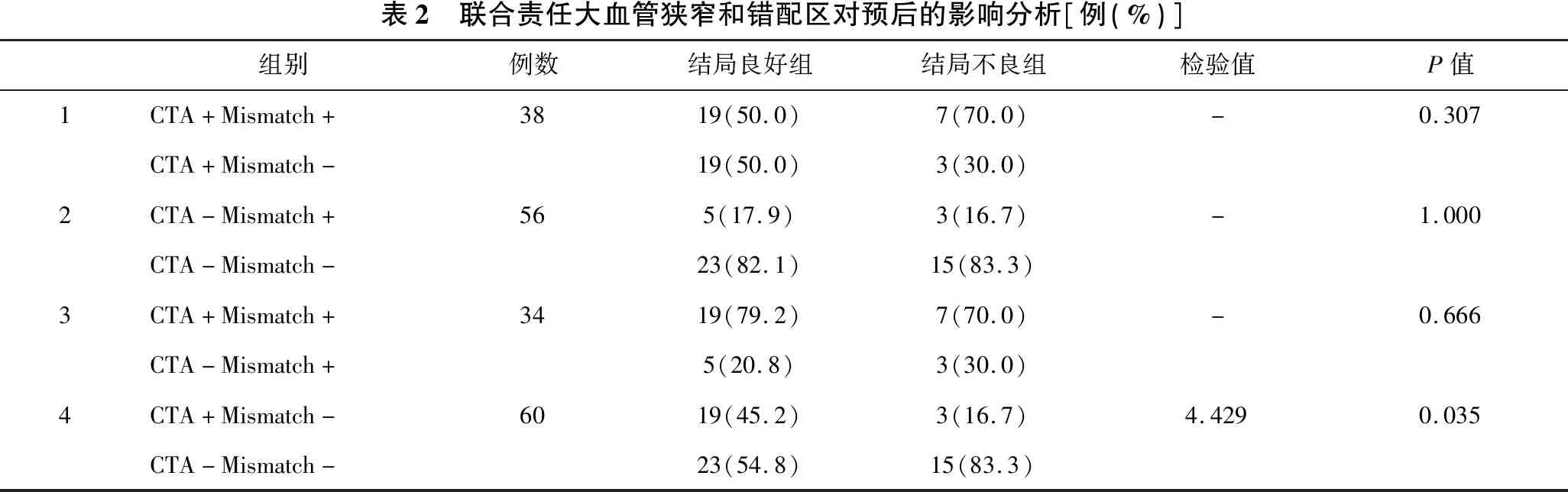
表2 联合责任大血管狭窄和错配区对预后的影响分析[例(%)]组别例数结局良好组结局不良组检验值P值1CTA+Mismatch+3819(50.0)7(70.0)-0.307CTA+Mismatch-19(50.0)3(30.0)2CTA-Mismatch+565(17.9)3(16.7)-1.000CTA-Mismatch-23(82.1)15(83.3)3CTA+Mismatch+3419(79.2)7(70.0)-0.666CTA-Mismatch+5(20.8)3(30.0)4CTA+Mismatch-6019(45.2)3(16.7)4.4290.035CTA-Mismatch-23(54.8)15(83.3)
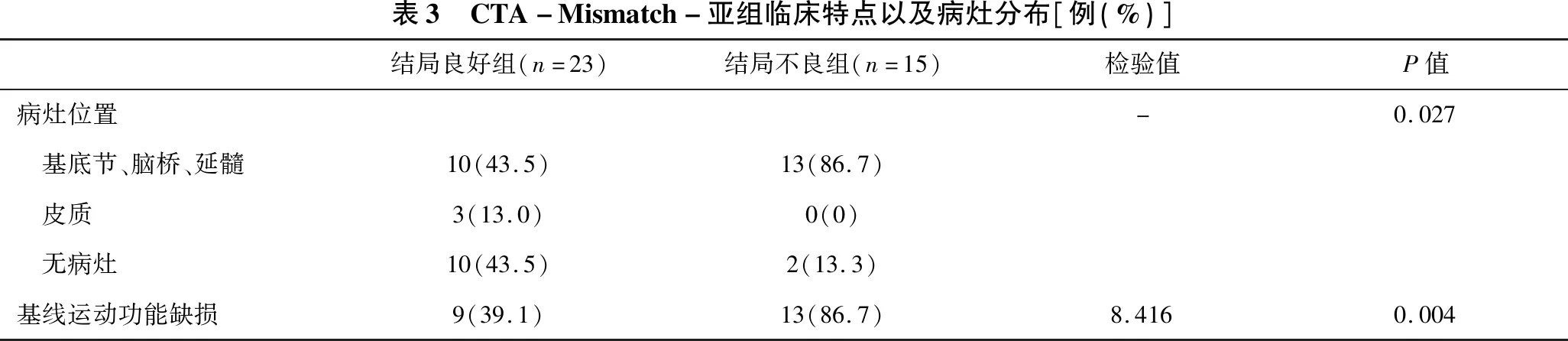
表3 CTA-Mismatch-亚组临床特点以及病灶分布[例(%)]结局良好组(n=23)结局不良组(n=15)检验值P值病灶位置-0.027 基底节、脑桥、延髓10(43.5)13(86.7) 皮质3(13.0)0(0) 无病灶10(43.5)2(13.3)基线运动功能缺损9(39.1)13(86.7)8.4160.004
2.3 溶栓后不良结局危险因素分析 见表4。不良结局危险因素分析共纳入3个因素,最终得出年龄、CTA-Mismatch-为溶栓后不良结局的独立危险因素,模型准确性为73.4%。年龄每增长1岁,溶栓后结局不良的风险是结局良好的1.049倍(P=0.035,95%CI:1.003~1.096);CTA-Mismatch-组患者结局不良可能性为良好的2.808倍(P=0.040,95%CI:1.051~7.504)。
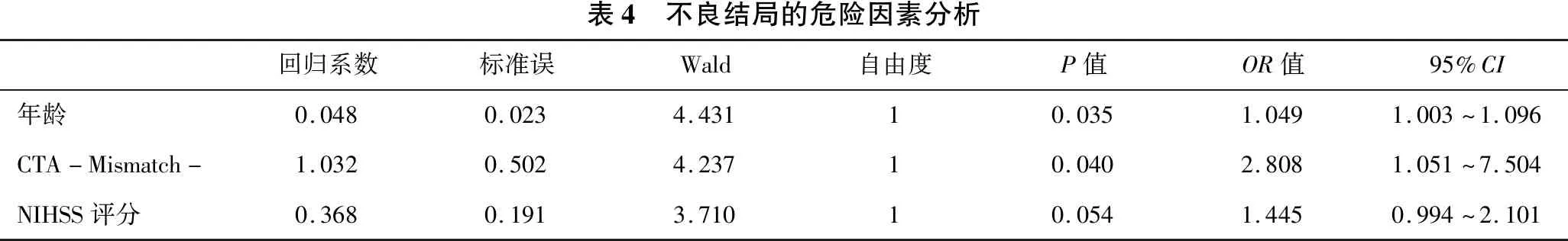
表4 不良结局的危险因素分析回归系数标准误Wald自由度P值OR值95%CI年龄0.0480.0234.43110.0351.0491.003~1.096CTA-Mismatch-1.0320.5024.23710.0402.8081.051~7.504NIHSS评分0.3680.1913.71010.0541.4450.994~2.101
3 讨 论
轻型卒中的静脉溶栓治疗相对安全,有效性仍未确定,且证据多来自大型研究的事后分析或回顾性队列研究[9],缺乏设计良好的针对性随机对照试验支持。备受瞩目的轻型卒中溶栓疗效研究(PRISMS)主要考察阿替普酶与阿司匹林对轻型卒中的治疗效果差异,得出溶栓并不能改善此类患者预后的结论[10]。仅根据症状学入组患者使纳入人群范围过大可能是其得出阴性结果的原因之一。若能识别出具有预后不良风险的患者,再给予其溶栓治疗,可能会有比较理想的获益。目前,基于多模影像筛选适合的溶栓患者已逐渐成为临床治疗趋势。相比于MR,多模式CT耗时短,利于广泛开展,能提供更多血管与灌注的信息,在轻型卒中亦有应用价值。另一方面,TIA与卒中被认为是一个连续的发病过程,初诊时不能完全将其区分。临床实践中,初诊怀疑TIA发作而后期证实为卒中、缺损症状持续且CTP存在低灌注但溶栓后行MR未见新发梗死灶的情况并不少见,这些患者虽然在诊断上可以区分为卒中和TIA,但在超急性期应视为一体尽早治疗。据多个国家卒中登记数据[3,11]显示,症状轻微或迅速缓解仍然是卒中患者未溶栓的首要原因。故本研究将这类患者一并纳入研究,通过对其CT多模式影像学特征以及溶栓基线的相关指标进行回顾性分析,弥补了既往研究的空缺。
年龄是轻型卒中预后不良的危险因素,这在不少研究[12-14]中已得到证实。而在本文中,即使在静脉溶栓后年龄依然影响预后,这也提示高龄患者无论静脉溶栓与否,预后均欠佳。
CTA-Mismatch-作为另一危险因素,同时涉及血管狭窄和灌注情况,能够更全面筛选适合的溶栓人群。首先,无责任血管狭窄提示闭塞的很可能是穿支动脉。这类动脉多为短旋动脉、旁中央动脉,从功能上被定义为终动脉,一旦闭塞造成的神经功能缺失可能比其他血管更快[15],并且缺乏吻合支[16]。阿替普酶通过吻合支作用于血栓的途径减少,血管再通率降低,有效灌注率可能因此降低。很多文献[17-18]已证明穿支动脉区梗死是预后不良的危险因素,尤其是涉及豆纹动脉、脑桥旁正中动脉时,即使溶栓后也存在症状进展,这可能是预后欠佳的原因。进一步综合灌注情况来看,CTP以及后处理软件在体积较小的基底节、丘脑、后循环区域敏感度很差[19],因而在这些部位即使有梗死核心也呈现出无缺血灌注的情况。本研究对这组患者进一步分析发现,合并基线运动功能缺损的患者溶栓后预后更差,且不良结局患者最终梗死病灶主要在基底节、脑桥、延髓腹侧,推测皮质脊髓束在以上部位较为聚集,缺血损伤后影响运动功能,而mRS评分又相当依赖运动功能,故即使小范围梗死也造成不良预后[20-21]。
对于轻型卒中以及TIA患者,最理想的状态是从中识别出一部分患者进行早期静脉溶栓治疗,而另一部分予以内科常规治疗。通过本研究发现,进行溶栓决策时时间窗内应充分关注多模式CT,对于无责任血管狭窄也无错配的患者溶栓应谨慎,同时观察有无肢体运动功能症状,如有,溶栓可能并不能改善预后,早期康复训练比血管再通治疗也许更为重要。当然这需要结合更大型的前瞻性研究以及与未溶栓患者进一步对比验证。本研究也存在一些不足之处,如众多研究衡量发病90 d的预后情况,而本研究选择了14 d作为评估标准,支持文献较少。这一点主要是考虑到溶栓为急性期治疗,且中国人群康复训练存在差异、二级预防依从性欠佳,14 d可能更合适。

