枸橼酸咖啡因联合加温湿化高流量鼻导管通气治疗早产儿呼吸窘迫综合征的效果
黄玉焕
(南阳市第一人民医院 新生儿科,河南 南阳 473000)
新生儿呼吸窘迫综合征(respiratory distress syndrome,RDS)多发于早产儿,患儿出生后可出现进行性加重的呼吸困难,且胎龄越小,发病率越高,若不及时治疗,可诱发呼吸衰竭,威胁患儿生命[1]。目前,临床治疗本病多采用药物联合无创通气治疗,以迅速纠正患儿呼吸状况,挽救患儿生命,枸橼酸咖啡因是常用治疗药物,其可兴奋呼吸中枢,增加每分通气量,以减轻呼吸困难症状[2]。鼻持续气道正压通气(nasal continuous positive airway pressure,NCPAP)属于常用的无创通气方式,可持续开放患儿肺泡,阻止肺泡萎缩,以提高肺通气换气能力,配合药物可增强治疗效果,加快病情好转[3]。但NCPAP耐受性欠佳,易引起鼻损伤、腹胀等并发症。加温湿化高流量鼻导管通气(heated humidified high flow nasal cannula,HHFNC)属于新型无创通气方式,其装置简便,经无需密封的鼻导管直接将一定氧浓度的空氧混合高流量气体输送给患者,且该装置具有加温湿化功能,吸入气体更加符合人体自然吸气状态,舒适性高,不会引起鼻腔干燥等现象,利于增强氧疗依从性,纠正机体低氧状态。本研究选取82例早产儿RDS患儿作为研究对象,分析咖啡因联合HHFNC治疗早产儿RDS的临床效果。
1 资料与方法
1.1 一般资料选取2018年9月至2020年9月南阳市第一人民医院收治的82例早产儿RDS患儿作为研究对象,按随机数表法分为对照组与观察组,各41例。对照组男24例,女17例;胎龄28~35周,平均(31.42±2.19)周;出生体质量1 256~1 785 g,平均(1 412.41±158.69)g;分娩方式:36剖宫产,5例自然分娩。观察组男23例,女18例;胎龄28~36周,平均(31.45±2.21)周;出生体质量1 243~1 789 g,平均(1 415.43±159.72)g;分娩方式:35剖宫产,6例自然分娩。两组性别、胎龄、出生体质量、分娩方式比较,差异无统计学意义(P>0.05),具有可比性。本研究经南阳市第一人民医院医学伦理委员会批准。
1.2 选取标准(1)纳入标准:①符合《实用新生儿学》[4]中RDS相关诊断;②胎龄均不足37周;③出生24 h内出现呼吸窘迫,且呈进行性加重;④经皮血氧饱和度低于85%;⑤患儿家属知情同意。(2)排除标准:①胎龄小于28周;②重度窒息;③对本研究用药过敏;④中途放弃治疗。
1.3 方法两组均监测生命体征变化,保持呼吸道通畅,进行肠内营养支持,并给予枸橼酸咖啡因注射液(成都苑东生物制药股份有限公司,国药准字:H20163401)治疗,初次负荷量20 mg·kg-1,24 h后维持量5 mg·kg-1,均每日1次。对照组常规治疗基础上加用NCPAP治疗,选取适宜鼻塞,连接新生儿呼吸机,调节为无创CPAP模式。参数设置:吸入氧浓度0.3~0.4,呼气末正压6 cmH2O(1 cmH2O=98.06 Pa),最大吸入氧浓度不超过0.6,呼气末正压不超过10 cmH2O。观察组常规治疗基础上加用HHFNC治疗,仪器选择新西兰Fisher Paykel公司提供的RT810专用呼吸机辅助治疗,选取适宜鼻导管,参数设置:吸入氧体积分数为0.3~0.4,氧流量3~6 L·min-1,加温湿化气体温度为37 ℃。两组均依据病情调整参数,维持血氧饱和度为90%~94%。若血气分析正常,并持续24 h以上,可考虑撤机。
1.4 观察指标(1)血气分析指标:治疗前及治疗24 h后,经血气分析仪检测两组血氧分压(PaO2)、二氧化碳分压(PaCO2)、血氧饱和度(SaO2)和pH值变化。(2)呼吸支持状况:比较两组患儿无创通气时间、总用氧时间。(3)并发症:鼻损伤、腹胀、气胸。

2 结果
2.1 血气分析指标治疗前,两组血气分析指标比较,差异无统计学意义(P>0.05);治疗后,观察组PaO2、SaO2、pH值高于对照组,PaCO2低于对照组,差异有统计学意义(P<0.05)。见表1。

表1 两组血气分析指标比较
2.2 呼吸支持状况观察组无创通气时间、总用氧时间短于对照组,差异有统计学意义(P<0.05)。见表2。
2.3 并发症对照组出现3例鼻损伤,4例腹胀,1例气胸,并发症发生率为19.51%(8/41);观察组出现1例鼻损伤,1例腹胀,并发症发生率为4.88%(2/41)。观察组并发症发生率低于对照组,差异有统计学意义(χ2=4.100,P=0.043)。
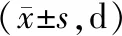
表2 两组呼吸支持状况比较
3 讨论
早产儿是RDS多发群体,正常情况下随着胎龄的增长,胎儿肺组织逐渐发育成熟,18~20周会产生肺表面活性物质(PS),35~36周时肺部可达到成熟状态。而早产儿肺部Ⅱ型细胞发育尚未完善,促使PS分泌不足,难以降低肺泡表面张力,肺泡可逐渐萎缩,出现进行性肺不张,进而诱发低氧、酸中毒等现象[5-6]。加之肺毛细血管会渗出纤维蛋白,形成肺透明膜,可进一步加重低氧中毒,造成恶性循环。目前,临床对于本病提倡综合治疗,枸橼酸咖啡因是早期常用治疗药物,其属于甲基黄嘌呤类药物,可阻断腺苷与受体结合,提高感受器对二氧化碳敏感性,并能改善患儿膈肌收缩力,兴奋中枢呼吸系统,促进肺氧合功能恢复,以减少呼吸暂停发生,纠正机体低氧状态。另外,该药安全性高,血药浓度波动小,可24 h间隔给药,故广泛应用于早产儿RDS治疗中。但单纯药物治疗无法快速改善通气效果,仍需联合呼吸机治疗以迅速纠正动脉血气状况。
NCPAP是治疗本病的重要通气方式,其给氧时可产生持续气道正压,以维持患儿肺泡长期处于开放状态,避免肺不张发生,以提高肺顺应性,增加残气量,改善肺通气换气能力,减轻呼吸困难等症状[7-8]。NCPAP还可刺激肺牵张感受器,促进胸廓支架稳定体系形成,预防胸廓塌陷,并提高膈肌呼吸强度,降低呼吸道阻力,帮助患儿尽早恢复自主呼吸。但实际应用中发现,NCPAP易引起鼻损伤、腹胀等并发症,降低患儿通气舒适性。本研究结果显示,观察组治疗后PaO2、SaO2、pH值高于对照组,PaCO2低于对照组,无创通气时间、总用氧时间短于对照组,并发症少于对照组,表明枸橼酸咖啡因联合HHFNC治疗早产儿RDS效果显著,可快速纠正患儿动脉血气分析状况,缩短无创通气时间,且并发症少,利于尽早康复。HHFNC是自鼻导管氧疗基础上发展而来的一种无创通气方式,其操作简单、舒适性高,通过鼻导管持续输入高流量气体,可帮助患儿恢复肺容量,增加肺泡通气量占比,从而提高肺换气能力,加快CO2呼出,以减少解剖无效腔及CO2重吸收,纠正低氧引起的低氧血症[9]。同时,高流量气体冲刷下,患儿鼻咽部吸气时无需扩张,利于降低吸气阻力,减轻呼吸作功,缓解呼吸肌疲劳,并能产生类似于NCPAP的气道正压,阻止肺不张发生,维持呼气末肺泡稳定性。相较于NCPAP,HHFNC吸入气体均经加温加湿化处理,有助于提高肺顺应性,增强气道传导性和防御功能,减缓机体热量的耗散,且因其更符合生理呼吸状态,不会引起鼻腔干燥等情况发生,利于保护鼻黏膜组织[10]。此外,HHFNC固定较为简单,患儿舒适性高,氧疗时不影响正常喂养,能为母子接触创造良好条件。与枸橼酸咖啡因联用后可协同增效,快速提高肺氧合功能,纠正机体低氧状态,促进自主呼吸恢复,并可缩短无创辅助通气时间,加快患儿早日撤机。
综上所述,枸橼酸咖啡因联合HHFNC可增强早产儿RDS治疗效果,快速改善机体动脉血气,促进呼吸困难等症状消失,且安全性高,利于患儿尽早恢复。

