乳鼠及成年大鼠脑皮质膜蛋白差异的分析
田晓琳,张赛航,孔德志,任雷鸣
(河北医科大学中西医结合学院,河北 石家庄 050017)
生物膜上所包含的蛋白质统称膜蛋白,膜蛋白是细胞与周围环境之间进行物质交换和维系细胞生理功能的关键成分,执行许多重要的生物功能,如信号的识别与转导、离子交换、物质运输、细胞和组织结构的维护等。大多数膜蛋白不同程度地嵌入脂质双分子层中,其膜内部分由一些非极性氨基酸组成,与膜紧密结合;膜外部分则由极性较高的亲水性氨基酸组成。与基因组学不同,蛋白质组学是以细胞内全部蛋白质的存在及其活动方式为研究对象,并对生命的复杂活动进行全面和深入的研究[1]。鉴于膜蛋白的重要性,其组学的研究成为热点。膜蛋白通过许多疏水氨基酸残基锚定在膜结构中,不易溶解于水性缓冲液系统中。因此,膜蛋白的制备和获得是研究膜蛋白组学的关键技术难点,所提取蛋白纯度的高低会直接影响最终的实验结果。制备膜蛋白样品时,传统的方法是使用去污剂,根据其明显的疏水性特点,常选用离子型SDS和非离子型Triton-X等。SDS会使多数蛋白完全变性[2],限制了很多下游分析。非离子型去污剂较为温和,但是对于膜蛋白,特别是具有多个跨膜区膜蛋白的抽提效果往往很差。本研究中选用的Novagen ProteoExtract 跨膜蛋白抽提试剂盒(简称TM-PEK),是将离子型和非离子型去污剂按照一定比例配制而成[3],提高了对膜蛋白的提取效果,并对下游分析的影响较小。
本研究建立了用 TM-PEK 对微量(约50 mg)大鼠脑皮质组织进行膜蛋白提取,经FASP法酶解,再依据肽段的色谱保留行为进行NanoLC分离,通过Orbitrap Fusion高分辨质谱采集数据,PD分析鉴定所提取到蛋白的方法;并用本法研究了出生2~3 d SD乳鼠与SD♂成年鼠脑皮质膜蛋白的差异蛋白组学。
1 材料
1.1实验动物健康♂1月龄SD大鼠(约100 g)、SD乳鼠(2~3 d)、3月龄健康♂成年SD鼠(约300 g),由河北省实验动物中心提供。实验期间,饲以河北省实验动物中心提供的固体饲料,自由饮食饮水。
1.2试剂Novagen膜蛋白试剂盒(提取溶液1、提取溶液2、TM-PEK试剂A、TM-PEK试剂B、蛋白酶抑制剂 Ⅲ),德国Merck公司;碘代乙酰胺、脲素,美国Sigma-Aldrich公司;二硫苏糖醇,生工生物工程(上海)股份有限公司;蛋白酶抑制剂PMSF,索莱宝(北京)科技有限公司;BCA工作液(试剂A、试剂B、牛血清蛋白BSA),天根生化科技(北京)有限公司;胰酶,普洛麦格(北京)生物技术有限公司。
1.3仪器纳升型超高效液相色谱EASY-nLC1000、Orbitrap Fusion高分辨质谱仪(美国Thermo公司);恒温混匀仪(杭州奥盛仪器有限公司);Vivacon 500超滤浓缩管(德国Sartorius公司);细胞超声破碎仪(宁波新芝生物有限公司)。
2 方法
2.1纳升液相色谱分离条件色谱柱:Acclaim PepMap RSLC 75 μm×15 cm,nanoViper C18;流动相A:0.1%甲酸水溶液;流动相B:0.1%甲酸-乙腈溶液。梯度:0~3 min,2%~5%流动相B;3~58 min,5%~22%流动相B;58~68 min,22%~30%流动相B;68~73 min,30%~90%流动相B;73~78 min,90%流动相B。
2.2质谱方法离子源:NSI电喷雾源[4];喷雾电压:2.1 kV;离子传输管温度:300℃;射频透镜(RF-lens):60%。扫描模式:速度模式(top-speed);循环时间:3 s;动态排除:60 s。一级OT扫描:质量分析器,静电场轨道阱;扫描范围,质核比350~1 550;分辨率,120 000;最大注入时间,60 ms;自动增益控制(automatic gain control,AGC):2e5。二级OT扫描:离子选择,四级杆;选择窗口,2 u;质量分析器,静电场轨道阱;分辨率,30 000;最大注入时间,70 ms;AGC:1e5;碎裂模式,高能碎裂(higher-energy collisional dissociation,HCD);碎裂能量,37 %。质谱数据由Xcalibur软件采集。
2.3膜蛋白的初提取将实验鼠分为3组,包括健康♂1月龄SD大鼠、SD乳鼠(2~3 d)、健康♂3月龄成年SD大鼠,每组3只。取3只健康♂1月龄SD大鼠颞叶皮层,混合后匀浆(其他两组同法提取膜蛋白,并进行质谱分析及生物信息学分析),分别取2份50 mg左右的匀浆组织,各加入2 mL冰提取溶液1和5 μL 蛋白酶抑制剂Ⅲ,在超声细胞破碎仪中超声5 s,共3个循环。冰上孵育10 min并温和搅拌,4℃条件下,1 000×g离心5 min。将上清液(胞质蛋白部分)移至新管中,冰上储存。加入5 mL冰PBS溶解沉淀,4℃条件下,1 000×g离心5 min,弃上清。复溶沉淀,其中一份加入0.2 mL提取缓冲液2A(0.1 mL提取溶液2与0.1 mL TM-PEK试剂A混合)和5 μL蛋白酶抑制剂Ⅲ;另一份加入0.2 mL提取缓冲液2B(0.1 mL提取溶液2与0.1 mL TM-PEK试剂B混合)和5μL蛋白酶抑制剂Ⅲ,4℃孵育15 min并温和搅拌。4℃条件下,16 000×g离心15 min,将富集膜蛋白的上清液移至新管中,用BCA法测定蛋白浓度。
2.4样品蛋白浓度测定根据标准品和样品数量,按BCA试剂A与试剂B为50 ∶1的比例配制适量BCA工作液,充分混匀。取2 g·L-1BSA(-20℃保存),室温融化后,按BCA法制作蛋白标准曲线。标准品和样品中分别加入BCA工作液200 μL,充分混匀后,于37℃孵育30 min,冷却至室温后,测定其在562 nm处的吸收值,并与标准曲线对比,即可计算蛋白的浓度。
2.5还原烷基化和FASP酶解[5]蛋白提取液中加入DTT,使终浓度为10 mmol·L-1,于37℃震荡1 h。再加入碘乙酰胺,使终浓度为50 mmol·L-1,于室温避光震荡45 min。将上述蛋白样品约100 μg加入到Vivacon 500浓缩超滤管中,离心15 min(14 000×g,20℃;下述未作说明时,同此条件),弃滤液。继续加入200 μL脲素至上述超滤管中,离心15 min弃滤液。再加入50 mmol·L-1NH4HCO3200 μL,再次离心15 min弃滤液;更换新的接收套管,在浓缩超滤管中加入50 mmol·L-1NH4HCO3100 μL,并在200 μg蛋白样品中加入20 μL胰酶(浓度为0.1 g·L-1),质量比100 ∶1,37℃酶切2 h。继续加入20 μL胰酶,37℃酶切12 h。离心15 min,收集肽段,再次加入50 mmol·L-1NH4HCO3200 μL,收集肽段,合并两次的收集物。将上述合并后的肽段溶液低温冷冻旋干后,用100 μL的0.1%甲酸水复溶,离心15 min,取上清20 μL放入进样小瓶中,操作流程见Fig 1。
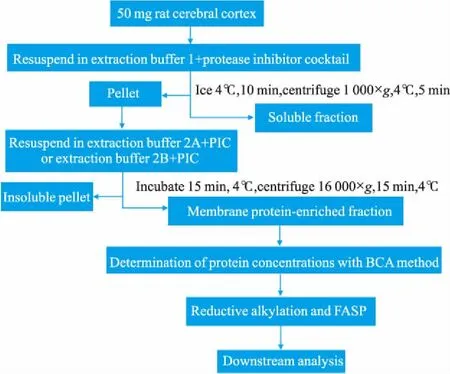
Fig 1 The membrane protein extraction procedure
2.6数据分析方法
2.6.1质谱数据分析 数据使用Proteome Discoverer 2.1软件搜库鉴定,搜索引擎:SEQUEST;数据库:Uniprot大鼠全蛋白数据库(www.uniprot.org)20170608;蛋白酶:胰蛋白酶(full);最大漏切位点:2;母离子质量精度:10 ppm;子离子质量精度:0.02 u(OT);固定修饰:脲甲基化(+57.021 u);可变修饰:N端乙酰化(+42.011 u);N,Q脱氨基化(+0.984 u),M氧化(+15.995 u)。
2.6.2物理化学性质及生物学分析 计算所鉴定到蛋白的GRAVY(http://www.gravy-calculator.de)值,预测蛋白的疏水性;用TMHMM预测蛋白的跨膜区域(http://phobius.binf.ku.dk/index.html),计算其跨膜结构域(transmembrane domains,TMDs)。利用DAVID(https://david.ncifcrf.gov/)[6]进行细胞定位(cellular component)、分子功能(molecular function)和生物学过程(biological process)的基因本体(gene ontology,GO)分析。
3 结果
3.1肽段图谱的采集膜蛋白样品经过胰蛋白酶酶解,经纳升液相分离、Orbitrap Fusion数据采集,得到肽段的一级质谱谱图和二级质谱谱图,典型的肽段谱图见Fig 2。
3.2两种膜蛋白提取液的NanoLC-MS/MS鉴定结果根据Proteome Discoverer 2.1软件搜库,提取缓冲液2A共鉴定出489个蛋白,1 108个肽匹配图谱(peptide matched spectra,PMSs)。提取缓冲液2B共鉴定出2 590个蛋白,8 322个PMSs。如Fig 3所示,提取缓冲液2A与提取缓冲液2B共同鉴定的蛋白有387个,与提取缓冲液2A相比,提取缓冲液2B在蛋白数量上多鉴定出2 101个,PMSs多出7 214个。
3.3比较两种提取液提取蛋白的物理化学性质首先,我们分析比较了被鉴定蛋白的分子量(MW)及等电点(pI)的分布情况[7]。如Fig 4A、4B所示,两种提取液所提取蛋白的MW和pI的整体分布没有明显区别。大部分被鉴定蛋白的MW分布在20~40 ku,pI分布在5~7和8~9。与提取缓冲液2A相比,提取缓冲液2B鉴定的蛋白广泛分布于各MW和pI组中;一些具有特殊性能的蛋白,如过酸蛋白或高分子量蛋白,仅由提取缓冲液2B中鉴定得到,如pI为12.15的40S核糖体蛋白S30(P62864)。
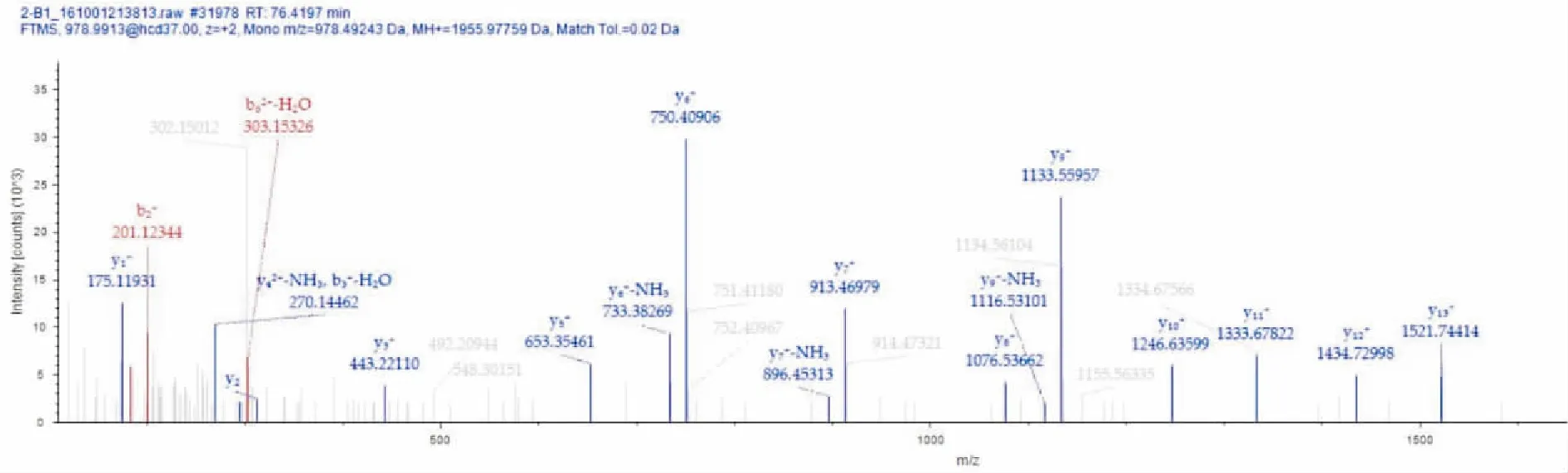
Fig 2 The representative MS2 spectrum for peptide
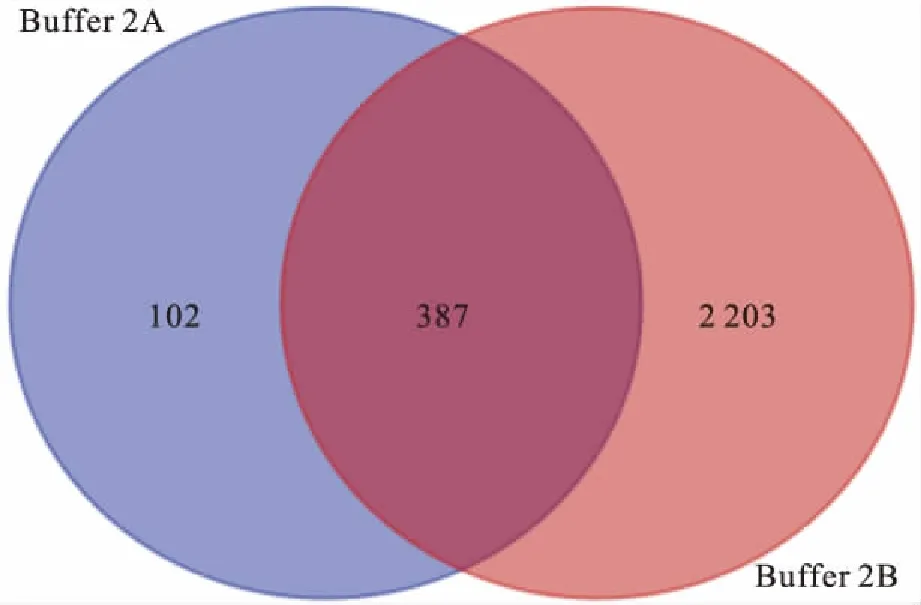
Fig 3 Difference in cytoplasmic membrane proteins betweenextraction buffer 2A and extraction buffer 2B
另外,我们依据计算出的GRAVY值[8]和预测出的TMDs,分析比较了两种提取液对不同疏水性蛋白的抽提效率,如Fig 4C、4D所示。GRAVY值是测定蛋白或肽段亲水性的常用参数,通常认为GRAVY值为正值时,肽段和蛋白为疏水性,负值则为亲水性。依据GRAVY值的大小,将所有鉴定的蛋白分为6组:<-1.5、-1.5~-1、-1~-0.5、-0.5~0、0~0.5、0.5~1组。结果发现,提取缓冲液2A和提取缓冲液2B所鉴定GRAVY值为正值的蛋白数量分别是30(6%)和272(11%)个。与提取缓冲液2A相比,提取缓冲液2B在各组中鉴定出更多的蛋白,两种提取缓冲液所提取蛋白数均在-0.5~0组中最多,其次为-1~-0.5组,但为无显著性差别增多,表明提取液2B对不同疏水性蛋白有更高的鉴定效率。
通过TMHMM对所抽提蛋白的TMDs进行预测,提取缓冲液2A与提取缓冲液2B分别有48和618个蛋白具有跨膜区域,其中有21个(43.8%)和304个(49.2%)蛋白不止1个TMDs;大部分蛋白含有1~4个跨膜区域,其次为5~8个跨膜区域。两种提取液所抽提蛋白的TMDs分布有明显区别,提取缓冲液2B抽提出含有更多跨膜区域的蛋白,尤其是TMDs>14的蛋白只在提取缓冲液2B中存在。例如,提取缓冲液2B鉴定出烟酰胺核苷酸转氢酶(Q5BJ23)和NADH-泛醌氧化还原酶链5(P11661)都含有14个TMDs。这些数据更进一步表明,与提取缓冲液2A相比,提取缓冲液2B更适用于酶解和鉴定含有高度疏水性多重跨膜区域的蛋白。
3.4两种提取液提取蛋白的GeneOntology分析我们利用https://david.ncifcrf.gov/分析工具,根据Gene Ontology数据库的注释[9],对大鼠脑组织皮层蛋白质表达谱中鉴定出的蛋白质进行了细胞定位、分子功能和生物学过程的分析。
提取缓冲液2A鉴定的489个蛋白中,331个(68%)蛋白可进行GO分析。细胞定位分析结果表明:细胞器(organelle)蛋白303个(91%),胞外区蛋白(extracellular region)202个(61%),大分子复合物(macromolecular complex)蛋白181个(55%),细胞内的膜封闭腔(membrane-enclosed lumen)蛋白101个(31%),突触(synapse)蛋白73个(22%),细胞连接(cell junction)蛋白66个(20%)(Fig 5A)。分子功能分析结果表明:涉及结构分子活性(structural molecule activity)和结合(binding)有关的蛋白分别是41个(12%)和301个(91%),与抗氧化活性(antioxidant activity)和转运活性(transporter activity)相关的蛋白分别是10个(3%)和36个(9%)(Fig 5B)。生物学过程分析结果表明:278个(84%)蛋白与单一生物过程(single-organism process)相关,223个(67%)蛋白参与生物过程调节(regulation of biological process),194个(59%)蛋白与细胞成分的组织或生物合成(cellular component organization or biogenesis)有关,156个(50%)蛋白与定位(localization)有关,153个(46%)蛋白参与发育过程(developmental process)(Fig 5C)。
提取缓冲液2B鉴定出2 590个脑皮质蛋白,其中1 720个(66%)蛋白可进行GO分析。在细胞定位的分析结果中,膜蛋白1 164个(68%),膜部分蛋白790个(46%),细胞器蛋白1 473个(86%),胞外区蛋白748个(43%),细胞连接蛋白393个(23%)(Fig 5A)。在分子功能分析中,241个(14%)和1 326个(77%)蛋白分别与结构分子活性和结合有关,195个(11%)和624个(36%)蛋白分别与转运活性和催化活性相关,149个蛋白(8%)与分子功能调节(molecular function regulator)相关(Fig 5B)。在生物学过程分析中,840个(49%)蛋白与细胞成分的组织或生物合成相关,788个(46%)蛋白与定位有关,685个(40%)蛋白参与发育过程,1 359个(79%)蛋白参与单一生物过程,1 507个(88%)蛋白参与细胞内变化(cellular process)(Fig 5C)。
3.5应用两种膜蛋白提取液研究♂成年SD鼠和乳鼠的脑皮层膜蛋白如Fig 6所示,提取缓冲液2A对SD乳鼠共鉴定出461个蛋白,对♂成年SD鼠共鉴定出1 806个蛋白;提取缓冲液2B对SD乳鼠共鉴定出2 488个蛋白,对♂成年SD鼠共鉴定出2 383个蛋白。
2A提取溶液提取并鉴定到的♂成年SD鼠的膜蛋白数量(1 233个)明显多于乳鼠的膜蛋白(277个),♂成年SD鼠的胞外区蛋白(P=1.6E-72)、突触蛋白(P=4.3E-70)明显多于乳鼠,且得到明显富集;化学性突触中参与突触前膜过程(presynaptic process involved in chemical synaptic transmission,P=2.2E-15)的蛋白也明显多于乳鼠。KEGG通路分析显示,♂成年SD鼠的蛋白富集到蛋白酶体(proteasome, P=1.2E-21)、突触囊泡循环(synaptic vesicle cycle, P=4.0E-13)、碳代谢(carbon metabolism, P=1.6E-13)通路和丙酮酸代谢(pyruvate metabolism, P=7.0E-8)通路,而乳鼠的蛋白则富集到剪接体(spliceosome,P=3.4E-11)、核糖体(ribosome,P=1.7E-6)通路中。通过本实验,证实大鼠皮层在发育过程中,以突触为代表的细胞间的联系发生了明显变化,乳鼠蛋白的合成较成年鼠旺盛。如在成年鼠中提取到轴突蛋白-1(Q63372)可影响突触和内分泌细胞的功能,在体内触发突触前结构的新生;而富集到的神经细胞囊泡循环蛋白-1 (Q62876) 和突触小泡蛋白(P07825)则参与短期和长期突触可塑性的调控。
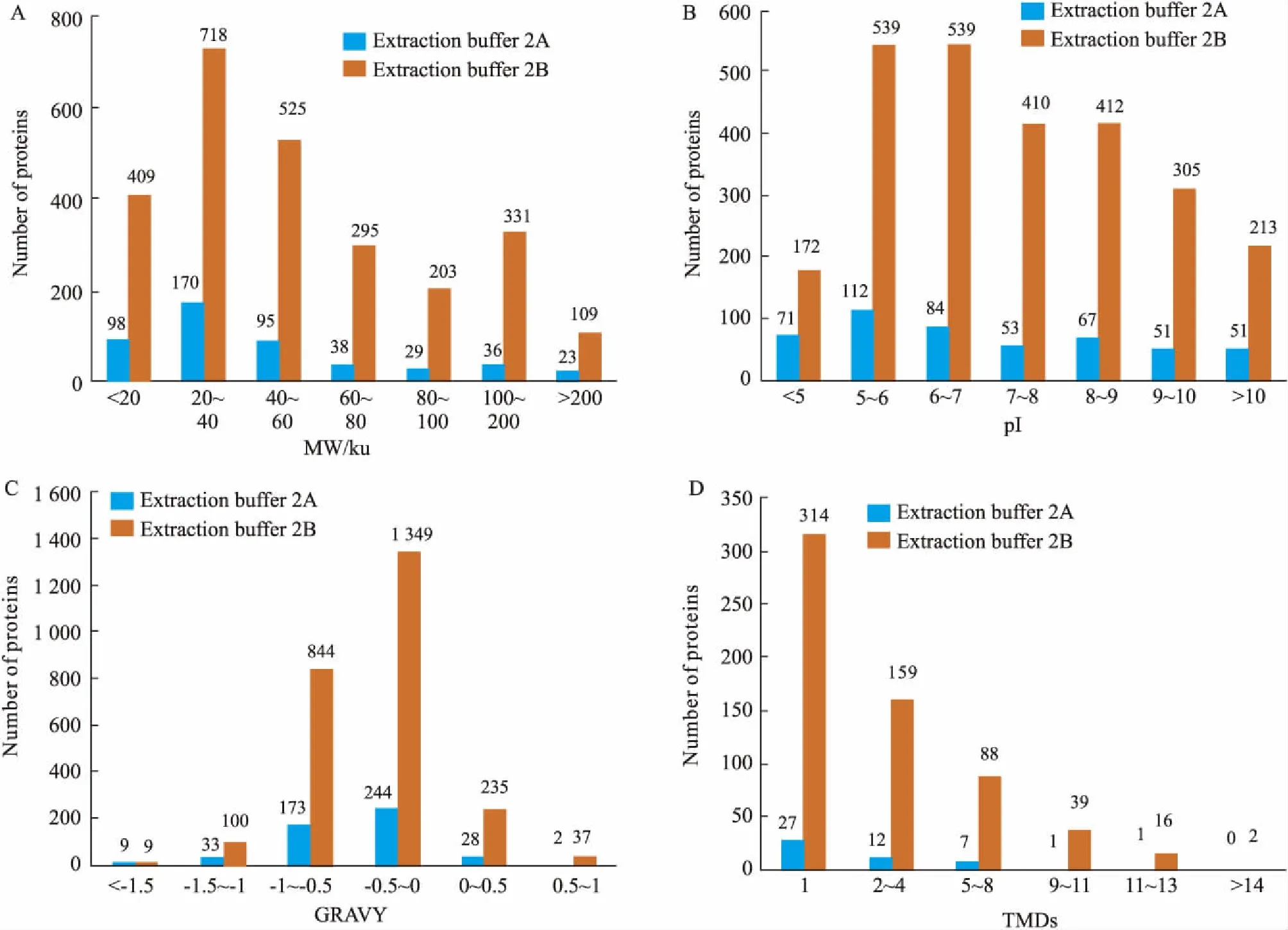
Fig 4 Comparison of distribution of membrane proteins identified based on two different extraction buffers
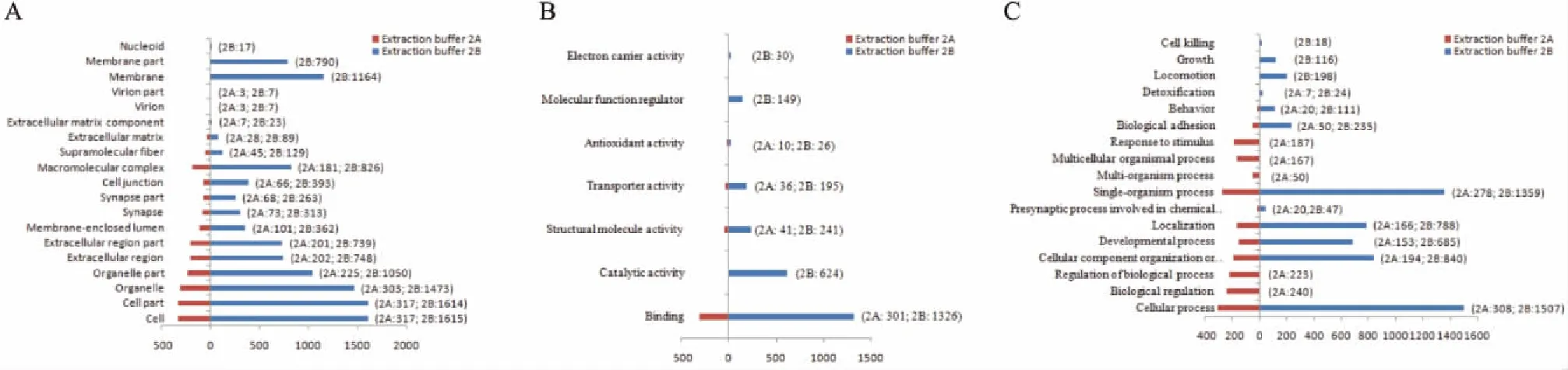
Fig 5 The GO analysis of cortex membrane proteins in rat cerebral cortex compared between two different extractions
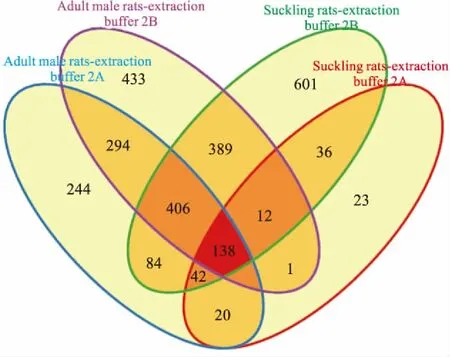
Fig 6 Difference in cytoplasmic membrane proteinsbetween suckling rats and adult male rats usingextraction buffer 2A(extraction buffer 2B)
2B提取溶液鉴定到的♂成年SD鼠的膜蛋白数量为1 679个,乳鼠的膜蛋白为1 708个,膜蛋白总数接近,但♂成年SD鼠的胞外区蛋白(P=1.5E-25)、突触蛋白(P=8.7E-48)与乳鼠相比得到明显富集。与催化活性相关(P=2.0E-14)的蛋白明显多于乳鼠。KEGG通路分析显示,♂成年SD鼠的蛋白富集到GABA氨基丁酸突触(GABAergic synapse,P=2.6E-7)、谷氨酸能突触(glutamatergic synapse,P=8.0E-7)、多巴胺能突触(dopaminergic synapse,P=1.8E-5)、谷胱甘肽代谢(glutathione metabolism,P=8.3E-6)及逆行神经信号 (retrograde endocannabinoid signaling,P=6.6E-7)、催产素信号传导通路 (oxytocin signaling path,P=3.1E-4)、磷脂酰肌醇信号系统(phosphatidylinositol signaling system,P=3.6E-4)。乳鼠蛋白则富集于剪接体(P=4.2E-56)、RNA转运(RNA transport,P=4.4E-14)、内质网蛋白加工(protein processing in endoplasmic reticulum,P=7.0E-6)、真核细胞的核糖体生物合成(ribosome biogenesis in eukaryotes,P=6.0E-4)等与蛋白质合成相关的通路中。与提取液2A所得结论相同,成年大鼠皮层在发育过程中,以突触为代表的细胞间的联系发生了明显变化,乳鼠蛋白的合成较成年鼠旺盛。
4 讨论
根据膜蛋白在膜中的位置,可分为外在膜蛋白(extrinsic membrane proteins)和内在膜蛋白(integral membrane proteins,IMPs)。外在膜蛋白约占膜蛋白的20%~30%,分布在膜的内外表面,为水溶性蛋白,它通过离子键、氢键与膜脂分子的极性头部相结合,或通过与内在蛋白的相互作用,间接与膜结合;内在蛋白约占膜蛋白的70%~80%,可不同程度地嵌入脂双层分子中,具有较强的疏水性[10]。基于膜蛋白的这种疏水性差异,可应用不同的提取溶剂进行抽提,不同抽提溶剂的组合可使疏水性不同的膜蛋白得到富集。Heo等[3]用6-氨基乙酸从小鼠脑组织海马体中提取膜蛋白,利用Nano-LC-ESI-MS/MS 技术,鉴定出1 878个蛋白,其中28.39%为质膜蛋白。Kang等[11]用1.5 mol·L-1羟基乙酸从C57BL/6J鼠脑组织海马体中提取膜蛋白,然后进行SDS-PAGE分离、Nano-LC-MS/MS鉴定,大部分膜蛋白MW分布在450~1 236 ku。虽然传统的非离子性表面活性剂SDS可以使多数膜蛋白变性溶解,但SDS在后续样品处理过程中不容易除去[12],抑制质谱的离子响应,反而不利于肽段的检出;而非离子表面活性剂Triton-X的临界胶束浓度(CMC)较低[13],单独使用对于膜蛋白的溶解并不理想。
本文建立了基于TM-PEK试剂盒提取、NanoLC-MS/MS分析鉴定大鼠皮层膜蛋白的方法。我们对比分析了TM-PEK试剂盒中的两种提取缓冲液(提取缓冲液2A和提取缓冲液2B)对1月龄青年大鼠脑皮质膜蛋白的抽提效果,经质谱分析提取缓冲液2A共鉴定出489个蛋白,提取缓冲液2B共鉴定出2 590个蛋白。与提取缓冲液2A相比,提取缓冲液2B多鉴定出2 101个蛋白,提取缓冲液2B对蛋白的抽提效率是提取缓冲液2A的5倍;用提取缓冲液2B能够得到更多的MW>100 ku的蛋白,能鉴定出更多的GRAVY值为正值的蛋白。通过TMHMM对所抽提蛋白的TMDs进行分析,两种提取缓冲液对只含有1个TMDs的蛋白数量相对最多,而提取缓冲液2B在富集具有多个TMDs的蛋白时具有明显优势。GO分析也提示,提取缓冲液2B所抽提的蛋白在膜、膜部分和拟核中得到明显富集,而提取缓冲液2A无此类蛋白的富集。
用本法研究大鼠乳鼠及成年鼠的皮层膜蛋白,2A提取溶液鉴定到乳鼠、成年鼠的皮层膜蛋白数量分别为277个、1 233个;2B提取溶液鉴定到乳鼠、成年鼠的皮层膜蛋白数量分别为1 708个、1 679个。结果表明,2A提取溶液在提取膜蛋白时具有明显的选择性;对所鉴定到的蛋白进一步进行生物信息学分析,提示成年鼠以突触为代表的细胞间的联系发生了明显变化,而乳鼠蛋白的合成较成年鼠旺盛。