基于模型认知与建构的元素化学教学设计探析
李灵敏
[摘 要]新课程标准提出了要发展学生的化学学科核心素养,核心素养的获得关键靠课堂教学。以《镁的提取及应用》教学设计为例,从模型认知与建构的角度对元素内容进行教学设计与探析,结合情景引入、层层设问、分组实验、联系实际、深入推进等环节,逐步实现学生核心素养的发展。
[关键词]镁的提取;实验探究;模型认知;教学设计
[中图分类号] G633.8 [文献标识码] A [文章编号] 1674-6058(2018)35-0060-02
一、教学与评价目标
1.教学目标
(1)通过海水中镁的提取过程,认识含镁物质及其转化关系,建立物质性质与物质用途的关联;
(2)通过实验探究镁的主要化学性质,初步形成基于物质类别、元素价态和原子结构对物质的性质进行预测和检验的认知模型;
(3)了解镁及其化合物的重要用途,深刻认识化学对满足人们日益增长的生活需要的重大贡献。
2.评价目标
(1)通过自主预习预测镁的性质,诊断学生基于前期所学经验使用模型认识物质的水平(经验水平、系统水平);
(2)通过对含镁物质及其转化关系的讨论和点评,诊断并发展学生对物质及其转化思路的认识水平(孤立水平、系统水平);
(3)通过镁的提取过程中试剂的选择、加热方法的确立等,诊断学生根据已知信息解決实际问题的能力水平(孤立水平、系统水平)及其对化学价值的认识水平(学科价值视角、社会价值视角)。
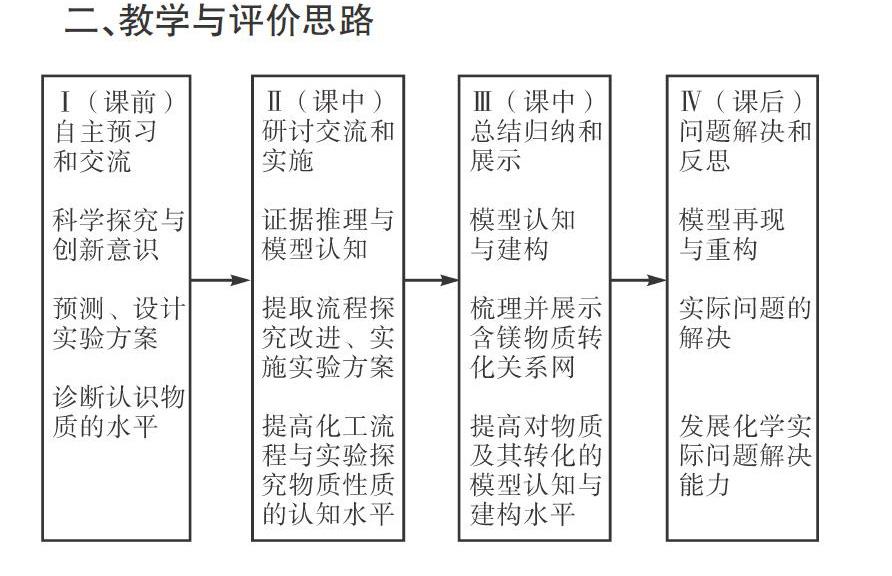
二、教学与评价思路
三、教学过程
1.情景引入,学生尝试,激发兴趣,引出主题
【情景】观看《野外生存与挑战》节目——点火工具“打火棒”的使用,并请一位学生自愿上讲台来试一试。
【学生】根据视频介绍,利用打火棒引燃一张白纸。
【提问】打火棒是什么材料做的,如何提炼?
设计意图:联系生活实际,让学生感受化学魅力,培养学生的科学态度与社会责任感;同时激发学生学习兴趣,引发学生对“打火棒主体材料是什么,如何提炼”等问题的积极思考,为本堂课接下来的探究奠定基础。
2.层层设问,分组实验,遭遇困惑,不断优化
【教师】介绍镁在地壳和海水中的存在形式和含量。
【设问1】从矿石中提取镁与从海水中提取镁,哪个更合适?为什么?
【学生】从海水中提取镁更合适。因为原料来源丰富,而且矿石作业容易产生粉尘。
【设问2】我们该如何从海水中分离出Mg2+ 呢?(每个小组面对自己桌上放着的那瓶海水进行讨论)
【学生】讨论之后,各组代表回答:①先加NaOH溶液再过滤;②先加Ca(OH)2溶液再过滤;③先加Na2CO3溶液再过滤;等等。
【学生】分组实验,发现海水中直接加NaOH溶液,加得再多也没有明显的沉淀。(学生心中充满困惑)
【教师】我们通过实验发现,直接往海水中加试剂,效果非常不明显,现在用浓缩海水试试。
【学生】再次分组实验,看到明显沉淀。
【设问3】为什么海水直接加NaOH试剂没有沉淀产生?有没有必要专门对海水进行浓缩?
【学生】因为海水中镁离子的浓度太低,所以有必要将海水浓缩成母液。
设计意图:“学起于思,思源于疑。”富含思考性是课堂生命力所在,学生若能够积极思考,主动质疑,就能变“被动接受”为“主动发现”,从而实现自主学习。本实验看似非常简单,就是让海水中的Mg2+沉淀下来以便分离,但实验结果却出乎意料,学生肯定会产生疑惑,会去思考,于是就有了思考的空间,进而培养“科学探究”与“创新意识”之化学核心素养。
3.联系实际,捕捉信息,迎难而上,获取新知
【设问4】那么实际生产中,我们应该选择什么作为沉淀剂?
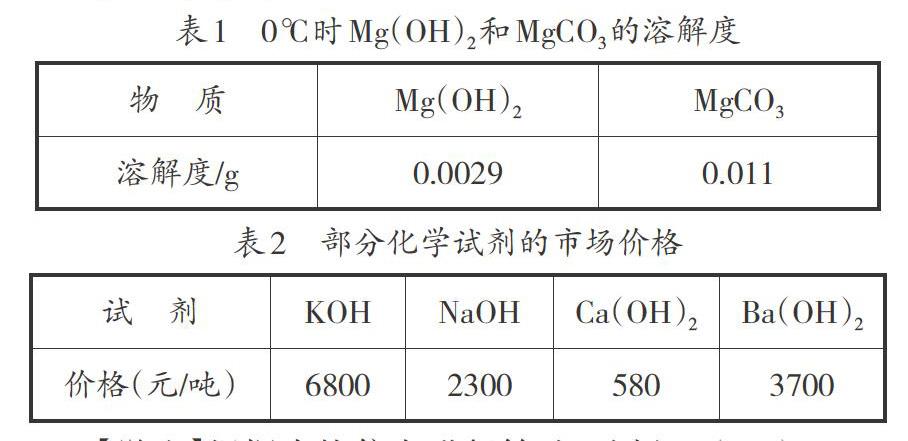
【PPT投影】
【学生】根据表格信息进行筛选,选择Ca(OH)2。
【设问5】实际生产中我们选择物美价廉的石灰乳,使镁离子转化为Mg(OH)2,那么又如何实现从Mg(OH)2到Mg的生产呢?
【学生】分组讨论,各组代表发言,最终汇总出以下几个方案:
①加热氢氧化镁,制得氧化镁,用C等置换Mg;②加盐酸,制得氯化镁,再用钾或钠来置换镁;③加盐酸,制得氯化镁,然后电解(教材上有);④加热氢氧化镁,制得氧化镁,再电解。
【追问】现在我们来看看方案①行不行得通?
【教师】演示实验
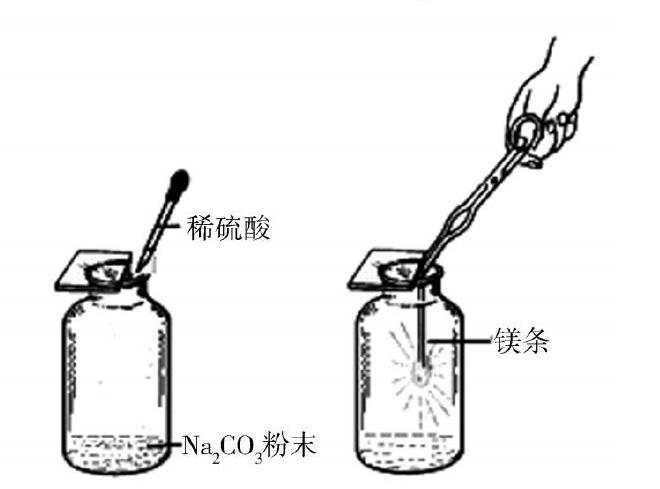
步骤:(1)向一定量的装有碳酸钠粉末的集气瓶中加入稀硫酸;
(2)用燃着的木条检验CO2是否已经收集满;
(3)点燃镁条并插入收集满CO2的集气瓶中。<E:\教育学院杂志社\中学教学参考\中学教学参考2018年12月(理科中旬)\h2.tif>
【学生】描述现象,得出结论: 2Mg+CO2=2MgO+C。
【设问6】通过实验事实我们发现存在上述反应,接下来请大家判断该反应的还原剂和还原产物,并结合还原性强弱规律分析C能否置换出Mg。
【学生】还原剂是Mg,还原产物是C;根据“还原剂的还原性大于还原产物”这一规律,C不可能置换出Mg。
【教师】实验事实告诉我们用C置换镁是行不通的,选择用K的确可以,但是K比较贵,所以我们只能考虑用电解法来制取Mg。那么是电解MgCl2 好,还是电解MgO好呢?
【PPT投影】
表3 几种物质的熔点
[物 质 MgO MgCl2 MgSO4 熔点/℃ 2825 714 1327 ]
【学生】结合表中信息选择电解MgCl2。
【追问】是电解MgCl2 溶液,还是电解熔融的MgCl2?
【学生】思考讨论,并结合电解饱和食盐水和电解熔融的NaCl的情况,得出应该选择电解熔融的MgCl2 。
设计意图:联系工业生产实际,沿着学生已有知识与思维模型,层层设问,逐个突破,建构新的模型认知:建立认识事物的一般认知模型,根据已有经验进行假设,通过实验或推理进行证伪。此外,本环节还通过多张图表数据,来引导学生对信息进行筛选、类比、分析、推理,并得出结论,逐步发展他们的思维能力和创新素养。
4.深入推进,交流讨论,展示自我,提升能力
【教师】通过电解熔融的MgCl2,我们终于得到了单质镁,那么镁还有哪些化学性质呢?
【学生】结合预习学案,根据镁的原子结构预测镁的化学性质。
【教师】点评学生的预测情况,完善镁的化学性质。
【设问7】从海水到镁,再到镁的性质,这整个过程大家是否可以用流程图来表示?请设计海水到镁以及镁及其化合物转化关系的整体框架图,并进行展示、交流与评价。
【学生】展示分享与交流成果。
设计意图:学生在交流与讨论中绘制出镁的提取流程图,并认识镁及其化合物的相互转化关系,建立起元素化合物学习的一般认知模型,并能将这种认知模型推广到其他元素及其化合物的学习中去。
四、教学反思
本节课的课堂主线明确、条理清晰,围绕如何从海水中提取镁这一过程,通过层层设问、实验操作、分组討论、信息提示与处理等形式把中间遇到的小难关一个个攻破,顺利完成本节课新知识的学习。整堂课的设问有梯度,符合学生从感性到理性的认知过程,并通过元素化合物学习的一般认知模型,建构海水到镁以及镁及其化合物转化关系的知识网络图,有效促进学生的认知发展,不断完善学生的整体思维,提高学生的化学学科核心素养。
[ 参 考 文 献 ]
[1] 王祖浩.普通高中课程标准实验教科书:化学1(必修)[M].南京:江苏教育出版社,2009.
[2] 中华人民共和国教育部.普通高中化学课程标准(2017年版)[S].北京:人民教育出版社,2018.
[3] 付勇,房寿高,吴星.简析化学文化与化学教育[J].化学教育,2006(6):12-14.
(责任编辑 罗 艳)

