XELOX与FOLFOX4方案治疗进展期胃癌疗效及安全性
周 娓, 陈泉全, 罗红梅
(湖北省鄂州市中医医院 肿瘤科, 湖北 鄂州, 436000)
XELOX与FOLFOX4方案治疗进展期胃癌疗效及安全性
周娓, 陈泉全, 罗红梅
(湖北省鄂州市中医医院 肿瘤科, 湖北 鄂州, 436000)
摘要:目的评价奥沙利铂联合卡培他滨(XELOX)方案与奥沙利铂联合5-氟尿嘧啶、亚叶酸钙(FOLFOX4)方案治疗进展期胃癌的疗效及安全性。方法将78例进展期胃癌患者随机分为XELOX组和FOLFOX4组,各39例,分别采取XELOX方案和FOLFOX4方案进行规范治疗,比较2组临床疗效及不良反应。结果XELOX组总有效率(ORR)为56.41%,疾病控制率(DCR)为87.18%,中位肿瘤进展时间(TTP)6.3个月,中位生存时间(MST)13.9个月;FOLFOX4组ORR为51.28%,DCR为84.62%,中位TTP 6.1个月,MST 13.5个月。2组ORR、DCR、中位TTP及MST比较,差异均无统计学意义(P>0.05)。XELOX组白细胞减少,恶心、呕吐,腹泻及口腔黏膜炎发生率显著低于FOLFOX4组(P<0.05或P<0.01),仅手足综合征发生率显著高于FOLFOX4组(P<0.05)。结论XELOX方案和FOLFOX4方案对进展期胃癌均有近55%的有效率,远期疗效也相近,但XELOX方案安全性更高。
关键词:进展期胃癌; 卡培他滨; 奥沙利铂; 氟尿嘧啶; 亚叶酸钙
胃癌的发病率居于各类恶性肿瘤之首,早期发现较为困难。约70%胃癌患者就诊时已处于III、IV期,此类患者手术切除率低,获得根治性切除的比例小,术后复发率、转移率高,总体预后不良,因此积极提高手术切除率成为改善胃癌患者预后的一大目标[1]。随着新的辅助性治疗理论和技术的完善,术前对进展期胃癌患者开展辅助化疗可缩小肿瘤,降低临床分期,提高根治性切除率,延长生存时间,降低术后复发转移率,明显改善预后[2-3]。由于化疗方案复杂多样,患者对其敏感性不同,所以目前对局部进展期胃癌新辅助化疗方案的选择尚无统一标准[4]。本研究比较了奥沙利铂联合卡培他滨联合(XELOX)方案与奥沙利铂联合5-氟尿嘧啶(5-FU)、亚叶酸钙(FOLFOX4)方案治疗胃癌的临床疗效和安全性,现报告如下。
1资料与方法
1.1一般资料
选取2012年3月—2015年9月湖北省鄂州市中医医院肿瘤科收治的进展期胃癌患者78例,均符合国际抗癌联盟(UICC)第7版胃癌分期中的诊断及临床分期标准[5],排除残胃癌、有上腹部手术史以及腹腔、肝、脑等器官转移者。所有患者均签署知情同意书。其中男38例,女40例;平均年龄(55.0±6.7)岁。随机分为XELOX组和FOLFOX4组,各39例。2组性别、年龄、病理类型、转移情况等一般资料比较无显著差异(P>0.05),具有可比性。
1.2方法
XELOX组:奥沙利铂130 mg/m2, 静脉滴注2 h,第1天;卡培他滨1 000 mg/m2, 口服, 2次/d,第1~14天;每21 d为1个周期, 2个周期后评价疗效。FOLFOX4组:奥沙利铂85 mg/m2, 静脉滴注2 h,第1天;亚叶酸钙200 mg/m2, 静脉滴注2 h, 第1~2天; 5-FU 400 mg/m2, 快速静脉推注,600 mg/m2,持续静脉滴注22 h, 第1~2天;每2周为1个周期,4个周期后评价临床疗效。每个疗程治疗前检查血尿常规、肝肾功能、肿瘤标记物、腹部B超或计算机断层扫描(CT)检查,同时给予相应支持治疗,比如予以格拉司琼止吐,粒细胞集落刺激因子预防白细胞减少等。
1.3评价标准
采用实体瘤疗效评价标准(RECIST)[6]进行近期疗效评估,分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)和疾病进展(PD)。总有效率(ORR)=(CR+PR)例数/总例数×100%,疾病控制率(DCR)=(CR+PR+SD)例数/总例数×100%。不良反应参照世界卫生组织(WHO)抗癌药物急性及亚急性毒性分级标准[7]评定,分为0度(无)、Ⅰ度(轻度)、Ⅱ度(中度)、Ⅲ度(重度)、Ⅳ度(威胁患者生命)。
1.4统计学方法
采用SPSS 19.0统计学软件进行数据分析,计数资料以百分比表示,采用χ2检验,P<0.05为差异有统计学意义。
2结果
2.12组近远期疗效比较
XELOX组CR 3例,PR 19例,SD 12例,PD 5例,ORR为56.41%,DCR为87.18%;FOLFOX4组CR 2例,PR 18例,SD 13例,PD 6例,ORR为51.28%,DCR为84.62%。2组ORR及DCR比较,差异均无统计学意义(P>0.05)。
XELOX组中位肿瘤进展时间(TTP)6.3个月,中位生存时间(MST)13.9个月;FOLFOX4组中位TTP 6.1个月,MST 13.5个月。2组中位TTP、MST比较无显著差异(P>0.05)。
2.22组不良反应比较
2组不良反应以Ⅰ、Ⅱ度为主,Ⅲ、Ⅳ度较为少见。XELOX组白细胞减少,恶心、呕吐,腹泻及口腔黏膜炎发生率明显低于FOLFOX4组(P<0.05或P<0.01),而手足综合征发生率显著高于FOLFOX4组(P<0.05)。2组血小板减少、外周神经毒性、转氨酶升高及高胆血红素升高等发生率比较,差异无统计学意义(P>0.05)。见表1。
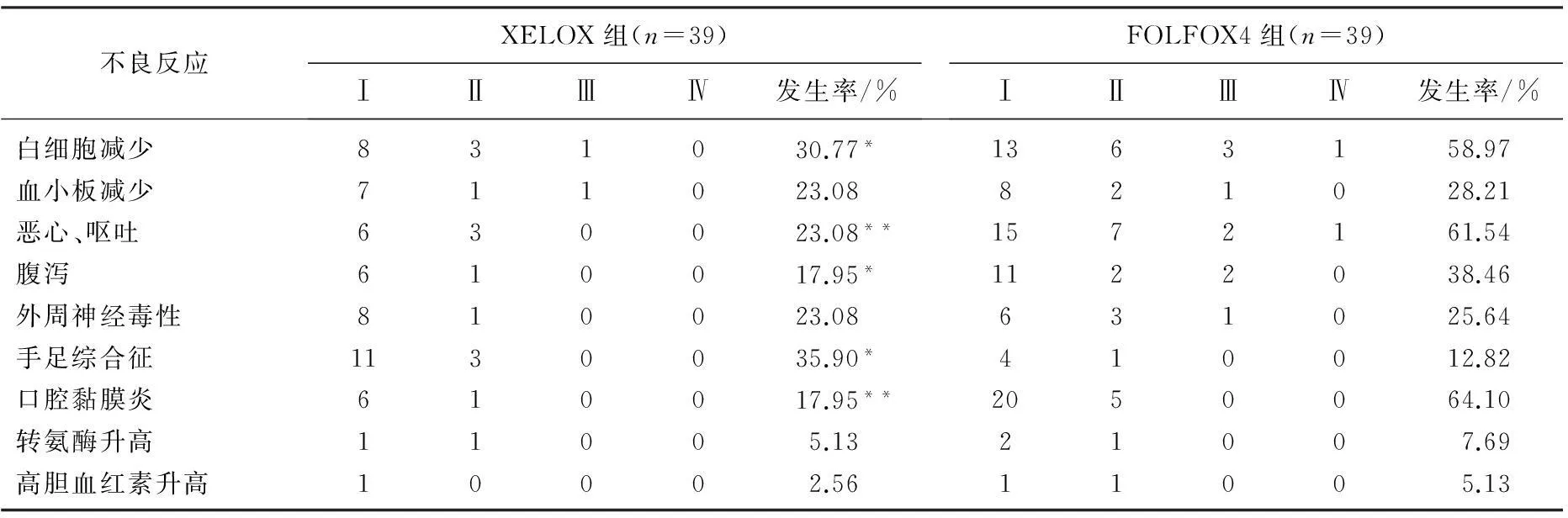
表1 2组不良反应比较
与FOLFOX4组比较, *P<0.05, **P<0.01。
3讨论
胃癌早期以手术切除为主,但多数进展期胃癌患者无法进行手术[8]。新辅助治疗在局部晚期乳腺癌的成功经验使其在进展期胃癌的治疗中得以开展[9]。胃癌新辅助化疗又称术前化疗,可使患者肿瘤降期,从而接受手术,并提高手术切除率,改善治疗效果[10]。近年来,对于进展期胃癌的化疗方案比较多,必须从患者自身身体状况、化疗方案的疗效及毒副作用等多方面综合考虑,选择既安全又有效的化疗方案。目前,XELOX方案与FOLFOX4方案在胃癌术后辅助治疗中的有效性已被美国国立综合癌症网络(NCCN)列为2A级证据[11],但其作为新辅助化疗方案的疗效及安全性如何尚无确切结论。
新辅助化疗早期多以顺铂及5-FU为主,奥沙利铂作为第3代铂类抗癌药物,通过铂化作用抑制DNA的合成和修复,且与顺铂和卡铂药物无交叉耐药性,不良反应轻[12]。卡培他滨是一种新型的口服氟尿嘧啶氨甲酸酯类抗肿瘤药物,属于5-FU的前体药物,可被肿瘤组织内特有的胸苷磷酸化酶激活转化为活性物质,而对正常的组织和细胞几乎无作用,口服方便、有效,抗肿瘤作用已经超过了5-FU类药物,且应用广泛。奥沙利铂与5-FU具有协同作用,且对5-FU耐药者也有效[13]。研究[11,14]发现,晚期胃癌辅助治疗中FOLFOX4方案的有效率为55%,XELOX方案的有效率高达63%。本研究结果显示,XELOX组ORR为56.41%,DCR为87.18%,中位TTP为6.3个月,MST为13.9个月;FOLFOX4组ORR为51.28%,DCR为84.62%,中位TTP为6.1个月,MST为13.5个月。由于2种方案的基本作用原理类似,故2者近远期疗效相当,与陈绍俊等[12]研究结果相似。
2组不良反应主要为恶心、呕吐,骨髓抑制,神经毒性反应,手足综合征及肝功能异常等。骨髓抑制主要以白细胞减少为主,其次是血小板减少;神经毒性反应主要表现为指端感觉迟钝;肝功能检查中转氨酶和高胆血红素升高,但不明显。所有不良反应均以Ⅰ、Ⅱ度为主,Ⅲ、Ⅳ度较为少见。本研究结果显示,XELOX组仅手足综合征发生率高于FOLFOX4组,通过口服维生素B6并局部涂抹防护油膏后逐渐缓解。XELOX组白细胞减少,恶心、呕吐,腹泻及口腔黏膜炎发生率明显低于FOLFOX4组,予以对症支持治疗后均可缓解,不影响治疗,与樊志明等[15]研究报道一致。
参考文献
[1]王婧, 田劭丹, 陈信义. 晚期胃癌治疗进展[J]. 中国肿瘤临床, 2010, 37(3): 171-175.
[2]郑积华, 周娟, 谢波, 等. 不同化疗方案治疗老年晚期胃癌患者的疗效和安全性比较[J]. 实用医学杂志, 2014, 30(13): 2086-2087.
[3]Fontana E, Smyth E C. Novel targets in the treatment of advanced gastric cancer: a perspective review[J]. Ther Adv Med Oncol, 2016, 8(2): 113-125.
[4]Tian S B, Yu J C, Kang W M, et al. Effect of neoadjuvant chemotherapy treatment on prognosis of patients with advanced gastric cancer: a retrospective study[J]. Chin Med Sci J, 2015, 30(2): 84-89.
[5]Edge S B, Compton C C. The American Joint Committee on Cancer: the 7thedition of the AJCC cancer staging manual and the future of TNM[J]. Ann Surg Oncol, 2010, 17(6): 1471-1474.
[6]Nishino M, Jackman D M, Hatabu H, et al. New Response Evaluation Criteria in Solid Tumors (RECIST) guidelines for advanced non-small cell lung cancer: comparison with original RECIST and impact on assessment of tumor response to targeted therapy[J]. AJR Am J Roentgenol, 2010, 195(3): W221-W228.
[7]龚子永, 杨成轩. 转移性乳腺癌化疗后卡培他滨维持治疗疗效观察[J]. 中国实用医药, 2015, 10(7): 31-32.
[8]齐素兰, 邓祖丽蕊, 岳大成. 腹腔镜胃癌根治性切除联合生物免疫治疗对预后的影响[J]. 中国普通外科杂志, 2015, 24(6): 910-913.
[9]Yoshikawa T, Sasako M, Yamamoto S, et al. Phase II study of neoadjuvant chemotherapy and extended surgery for locally advanced gastric cancer[J]. Br J Surg, 2009, 96(9): 1015-1022.
[10]Xiong B H, Cheng Y, Ma L, et al. An updated meta-analysis of randomized controlled trial assessing the effect of neoadjuvant chemotherapy inadvanced gastric cancer[J]. Cancer Invest, 2014, 32(6): 272-284.
[11]靖昌庆, 李乐平, 王金申, 等. XELOX和FOLFOX4新辅助化疗方案对不能手术切除的局部进展期胃癌的疗效比较[J]. 中华消化外科杂志, 2010, 9(6): 430-433.
[12]陈绍俊, 黄海欣, 李桂生. 卡培他滨与氟尿嘧啶/亚叶酸钙联合奥沙利铂治疗晚期胃癌的随机对照临床研究[J]. 中国癌症杂志, 2007, 17(6): 483-486.
[13]Kang H, Chang H T, Ryu M, et al. A phase II study of paclitaxel and capecitabine as a first-line combination chemotherapy for advanced gastric cancer[J]. Br J Cancer, 2008, 98(2): 316-322.
[14]Sumpter K, Harper-Wynne C, Cunningham D, et al. Report of two protocol planned interim analyses in a randomized multicenter phase III study comparing capecitabine with fluorouracil and oxaliplatin with cisplatin in patients with advanced oesophagogastric cancer receiving ECF[J]. Br J Cancer, 2005, 92(11): 1976-1983.
[15]樊志明, 贺鸿桂, 黄超红, 等. FOLFOX4和XELOX治疗进展期胃癌的临床疗效比较[J]. 实用癌症杂志, 2013, 28(4): 396-398.
Efficacy and safety of XELOX and FOLFOX4 regimens in the treatment of patients with advanced gastric carcinoma
ZHOU Wei, CHEN Quanquan, LUO Hongmei
(DepartmentofOncology,EzhouHospitalofTraditionalChineseMedicine,Ezhou,Hubei, 436000)
ABSTRACT:ObjectiveTo evaluate the efficacy and safety of oxaliplatin plus capecitabine (XELOX) and oxaliplatin plus 5-fluorouracil and calcium folinate (FOLFOX4) regimens in the treatment of patients with advanced gastric carcinoma. MethodsSeventy-eight patients with advanced gastric carcinoma were randomly divided into XELOX group (n=39) treated with XELOX regimen and FOLFOX4 group (n=39) treated with FOLFOX4 regimen. The clinical efficacy and adverse reactions were compared in two groups. ResultsThe overall response rate (ORR), disease control rate (DCR), median time to tumor progression (TTP) and median survival time (MST) in XELOX group were 56.41%, 87.18%, 6.3 months and 13.9 months. The ORR, DCR, median TTP and MST in FOLFOX4 group were 51.28%, 84.62%, 6.1 months and 13.5 months. There were no significant differences in the ORR, DCR, median TTP and MST between two groups (P>0.05). Compared with FOLFOX4 group, the incidence rates of leucopenia, nausea, vomiting, diarrhea and oral mucositis in XELOX group were lower significantly (P<0.05 or P<0.01), but incidence rate of hand-foot syndrome was significantly higher (P<0.05). ConclusionThe response rates of XELOX and FOLFOX4 regimens are close to 55% in the treatment of advanced gastric carcinoma, and their long-term efficacy is similar. However, XELOX regimen has higher safety.
KEYWORDS:advanced gastric carcinoma; capecitabine; oxaliplatin; fluorouracil; calcium folinate
中图分类号:R 735.2
文献标志码:A
文章编号:1672-2353(2016)09-064-03
DOI:10.7619/jcmp.201609018
收稿日期:2016-01-26

