毛细管气相色谱法测定达沙替尼原料药中6种残留溶剂
郭旭光,郑子栋,郭毅
(河南省食品药品检验所,郑州 450003)
毛细管气相色谱法测定达沙替尼原料药中6种残留溶剂
郭旭光,郑子栋,郭毅
(河南省食品药品检验所,郑州 450003)
目的 建立毛细管气相色谱测定达沙替尼原料药中吡啶、二氯甲烷、甲醇、N,N-二甲基甲酰胺、二甲亚砜、乙醇6种有机溶剂残留量的方法。方法 采用DB-624 (30 m×0.53 mm,3 μm)毛细管柱;氢火焰离子化检测器;程序升温:初始温度25 ℃(维持13 min),再以15 ℃·min-1升至150 ℃(维持5 min),再以40 ℃·min-1升至220 ℃(维持5 min);载气为氮气;柱流速为2.0 mL·min-1;进样口温度:230 ℃;检测器温度:250 ℃;分流直接进样,以N,N-二甲基乙酰胺为溶剂,进样体积为0.5 μL。结果 6组分均能良好分离,6组分峰面积与浓度均呈良好的线性关系,其中吡啶、二氯甲烷、甲醇、N,N-二甲基甲酰胺、二甲亚砜、乙醇的线性范围分别为4.16~31.21 μg·mL-1(r=0.999 8),12.12~90.92 μg·mL-1(r=0.999 4),59.98~449.85 μg·mL-1(r=0.999 8),18.16~136.19 μg·mL-1(r=0.999 3),100.25~751.87 μg·mL-1(r=0.999 1),100.30~752.28 μg·mL-1(r=0.999 9),平均回收率为98.4%~101.3%(RSD=2.8%~5.0%)。结论 该方法简单、灵敏、准确,可用于测定达沙替尼原料药中的残留溶剂。
达沙替尼;残留溶剂;色谱法,毛细管气相
达沙替尼是一种新型ABL和Scr家族酪氨酸激酶抑制药[1],为对伊马替尼耐药的BCR/ABL阳性白血病患者提供了一个有效的治疗选择[2]。本品在合成过程中溶剂有二氯甲烷和甲醇,结晶过程中溶剂有二甲亚砜和乙醇,起始原料还可能含有甲醇、吡啶、二甲基甲酰胺等残留溶剂[3-6]。其中吡啶、二氯甲烷、甲醇、N,N-二甲基甲酰胺为第二类有机剂,二甲亚砜和乙醇为第三类有机溶剂,按《中华人民共和国药典》标准的规定均应控制其残留量[7]。气相色谱同时测定达沙替尼原料药中的上述6种残留溶剂的方法未见报道,笔者参考相关文献采用毛细管气相色谱直接进样测定了达沙替尼原料药中上述6种残留溶剂[8-12]。方法简单灵敏,快速准确,结果可靠。
1 仪器与试药
1.1 仪器 Agilent 6890N气相色谱仪(美国安捷伦公司),氢火焰离子化检测器,DB-624毛细管柱(30 m×0.53 mm,3 μm)。AL104分析天平(梅特勒-托利多公司,感量:0.1 mg)。
1.2 试药 吡啶、 二氯甲烷、二甲亚砜、甲苯(分析纯,均购于天津市风船化学试剂科技有限公司),N,N-二甲基乙酰胺(分析纯,天津市瑞金特化学品有限公司),乙醇(分析纯,北京化工厂),甲醇(色谱纯,默克公司),N,N-二甲基甲酰胺(DMF)(色谱纯,美国VBS公司)。达沙替尼原料药(新乡双鹭药业有限公司,批号:20130701,20130702,20130703)。
2 方法与结果
2.1 色谱条件 色谱柱:DB-624 (30 m×0.53 mm,3 μm)毛细管色谱柱;载气为高纯氮;柱流速为2.0 mL·min-1;分流比:2:1;进样口温度:230 ℃;氢火焰离子化检测器温度:250 ℃;程序升温,初始温度25 ℃(维持13 min),再以15 ℃·min-1的升温速率升至150 ℃(维持5 min),再以40 ℃·min-1的升温速率升至220 ℃(维持5 min);进样量0.5 μL,自动进样。
2.2 溶液的制备
2.2.1 内标溶液的制备 精密称取甲苯约100 mg,置100 mL量瓶中,加N,N-二甲基乙酰胺稀释至刻度,摇匀。
2.2.2 对照品储备液制备 精密称取吡啶208.07 mg、二氯甲烷606.10 mg、甲醇2 999.01 mg、N,N-二甲基甲酰胺907.93 mg、二甲亚砜5 012.43 mg和乙醇5 015.17 mg置50 mL量瓶中,加N,N-二甲基乙酰胺稀释至刻度,摇匀,再精密量取1 mL,置20 mL量瓶中,加N,N-二甲基乙酰胺稀释至刻度,摇匀作为对照品储备液。
2.2.3 对照品溶液制备 精密量取对照品储备液1 mL、内标溶液1 mL置同一10 mL量瓶中,加N,N-二甲基乙酰胺稀释至刻度,摇匀。
2.2.4 供试品溶液的制备 精密称取本品1 g,置10 mL量瓶中,加N,N-二甲基乙酰胺适量,超声使溶解,加内标溶液1.0 mL,加N,N-二甲基乙酰胺稀释至刻度,摇匀。
2.3 系统适用性实验 精密量取对照品溶液和供试品溶液各0.5 μL,注入气相色谱仪,记录色谱图,测定各有机溶剂的分离度和柱效,结果见图1,溶剂N,N-二甲基乙酰胺对各被测溶剂无干扰,被测溶剂的理论板数均应>5 000,相邻溶剂的分离度均>1.5。
2.4 精密度实验 精密量取“2.2.3”项下的对照品溶液0.5 μL,连续进样6次,测定各被测溶剂的峰面积,结果吡啶、二氯甲烷、甲醇、N,N-二甲基甲酰胺、二甲亚砜和乙醇峰面积的RSD分别为1.85%,1.16%,0.58%,1.04%,0.69%,1.47%。
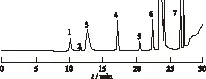
1.甲醇;2.二氯甲烷;3.乙醇;4.甲苯;5.吡啶;6.N,N-二甲基甲酰胺;7.二甲亚砜
图1 系统适用性实验各待测溶剂分离色谱图
2.5 线性关系考察 精密量取“2.2.2”项下的对照品储备液0.2,0.5,0.8,1.0,1.2,1.5 mL,分别置10 mL量瓶中,各加内标液1.0 mL,加N,N-二甲基乙酰胺稀释至刻度,摇匀,得线性范围系列标准溶液。取系列标准溶液,分别进样0.5 μL,记录色谱图,以溶液浓度X(μg·mL-1)为横坐标,对照品和内标峰面积比值(Y)为纵坐标绘制标准曲线,计算回归方程,结果见表1。
2.6 检测限与定量限 取“2.2.2”项下对照品储备液适量,用N,N-二甲基乙酰胺分别稀释制成系列浓度的溶液,照上述的色谱条件分别进样测定,以S/N约为3计算检测限,结果吡啶、二氯甲烷、甲醇、N,N-二甲基甲酰胺、二甲亚砜、乙醇的检测限分别为0.042,1.21,0.05,0.004 5,0.05,0.09 μg·mL-1;以S/N≥10计算定量限,结果吡啶、二氯甲烷、甲醇、N,N-二甲基甲酰胺、二甲亚砜、乙醇定量限分别为0.2,4.6,1.2,0.007,0.1,1.5 μg·mL-1。
2.7 重复性实验 精密称取本品(批号:20130701)适
量,照“2.2.4”项下制备供试品溶液,共6份,按“2.1”项下的色谱条件进行分析,检出本品中含吡啶、N,N-二甲基甲酰胺、二甲亚砜和乙醇分别为:0.001 72%,0.038%,0.054%,0.1%,RSD分别为:0.9%,1.1%,0.2%,0.8%。二氯甲烷和甲醇均未检出。
2.8 稳定性实验 取“2.2.3”项下的对照品溶液,在室温下分别于0,2,4,6,12,24 h后,按上述色谱条件,进样测定,吡啶、二氯甲烷、甲醇、N,N-二甲基甲酰胺、二甲亚砜、乙醇峰与内标物质的峰面积比值RSD分别为:0.3%,0.8%,1.4%,1.3%,2.4%,1.2%。表明溶液在24 h内稳定。
2.9 耐用性实验 分别对载气流速、初始温度、进样口及检测器温度进行了考察,实验结果表明载气流速、初始温度、进样口及检测器温度微小变动对残留溶剂的测定没有影响,残留溶剂峰的分离度均符合要求,该色谱条件耐用性良好。
2.10 加样回收率实验 分别精密称取本品(批号:20130701)9份(约1.0 g),分别置10 mL量瓶中,加N,N-二甲基乙酰胺适量使溶解,再分别加“2.2.1”项下的内标溶液1.0 mL;取3份分别加“2.2.2”项下对照品储备液的0.5 mL,再加N,N-二甲基乙酰胺稀释至刻度,摇匀,作为残留溶剂限量浓度的50%;另取3份加“2.2.2”项下对照品储备液的1.0 mL溶液,再加N,N-二甲基乙酰胺稀释至刻度,摇匀,作为残留溶剂限量浓度的100%溶液;另取3份加“2.2.2”项下对照品储备液的1.5 mL溶液,再加N,N-二甲基乙酰胺稀释至刻度,摇匀,作为残留溶剂限量浓度的150%溶液。取上述溶液,照“2.5”项下的方法测定含量,计算回收率和RSD,结果测得各溶剂的平均回收率分别为:吡啶98.4%、二氯甲烷99.4%、甲醇100.5%、N,N-二甲基甲酰胺101.3%、二甲亚砜99.7%、乙醇98.8%,RSD分别为3.9%,4.1%,3.2%,5.0%,4.7%,2.8%。
2.11 样品测定 分别取“2.2.3”项下的对照品溶液和“2.2.4”项下供试品溶液,按“2.1”项下色谱条件进行测定,按内标法以峰面积比计算,结果见表2,样品图见图2。
表1 线性范围与回归方程n=6

表2 达沙替尼样品中残留溶剂检测结果 %,n=2


1.乙醇;2.甲苯;3.吡啶;4.N,N-二甲基甲酰胺;5.二甲亚砜
图2 供试品溶液气相色谱图
3 讨论
3.1 溶剂的选择 达沙替尼在水中为极微溶,在二甲基乙酰胺中易溶,且二甲基乙酰胺能与本研究被测溶剂混溶,本研究色谱条件下二甲基乙酰胺峰与上述被测溶剂峰分离完好,故选择二甲基乙酰胺作为溶剂。
3.2 气化温度的选择 本实验被测残留溶剂中甲醇、二氯甲烷和乙醇沸点较接近,均在50 ℃左右,甲苯、吡啶、二甲亚砜、N,N-二甲基甲酰胺和N,N-二甲基乙酰胺沸点较高均在100~200 ℃之间,选择230 ℃为进样口温度使待测组分能够迅速气化,预防拖尾改善峰形,且不会分解,达到较好的分离效果。
3.3 柱温的选择 笔者曾考察柱温初始为35 ℃保持12 min,以35 ℃·min-1的速度升温至220 ℃,保持8 min,其他色谱条件不变,结果乙醇和二氯甲烷的分离度小于1.5,调整初始温度为25 ℃保持13 min,以15 ℃·min-1的速度升温至150 ℃,保持5 min,再以40 ℃·min-1的速度升至220 ℃,保持5 min,结果各被测溶剂峰的分离度均>1.5,符合要求。
3.4 色谱柱的选择 本实验所测残留溶剂种类较多,极性和沸点范围跨度都相对较大,为了获得较好的分离度,分别试用了极性的DB-WAX,DB-FFAP,弱极性的DB-624、DB-1301和中等极性的DB-35,HP-35等6种型号的石英毛细管柱,结果发现以弱极性的色谱柱分离效果最好,极性柱的色谱图二氯甲烷峰和乙醇峰合为一个峰,分析比较后以弱极性的DB-624色谱柱各被测溶剂峰的分离度最好,且峰形对称性较好,故最终
选用DB-624石英毛细管柱。
总之,因本实验所测溶剂种类较多,沸点范围跨度大,且二甲亚砜沸点较高,通过程序升温分流直接进样,无造成对柱子的污染,使各被测溶剂达到完好分离,理论板数均>5 000。该方法切实可行可以用于本品残留溶剂的测定。
[1] 王杨,王京华.酪氨酸激酶抑制剂治疗慢性髓系白血病的现状及进展[J].临床血液学杂志,2013,26(2):214-216.
[2] 朱雨,潘良琴,钱思轩,等.达沙替尼治疗伊马替尼耐药的BCR/ABL阳性白血病的临床研究[J].中国实验血液学杂志,2013,21(3):581-586.
[3] 张少宁,魏红涛,吉民.达沙替尼的合成[J].中国医药工业杂志,2010,41(3):161-163.
[4] 王伟,翟鑫,王刚,等.达沙替尼的合成工艺研究[J].中国药物化学杂志,2009,19(1):36-38.
[5] 刘晓宇,陈旭冰,陈光勇.达沙替尼合成图解[J].化工时刊,2011,25(6):38-40.
[6] 安康,关建宁,杨浩,等.达沙替尼合成工艺改进[J].精细化工中间体,2011,41(2):42-44.
[7] 国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:附录61.
[8] 徐力昆,张东娜,郭永建,等.GC法测定达沙替尼原料药残留溶剂[J].解放军药学学报,2013,29(2):162-164.
[9] 李园,于捷飞,徐箐,等.毛细管气相色谱法测定盐酸吉西他滨中5种有机溶剂残留量[J].中国医院药学杂志,2013,33(14):1199-1201.
[10] 余春梅,郑小锋,杨秀丽,等.直接进样气相色谱法测定硫酸氢氯吡格雷中的有机残留溶剂[J].中国药业,2013,22(14):67-68.
[11] 谢赞,史颖,耿佳,等.毛细管GC法测定头孢地尼中5种残留溶剂的有机溶剂[J].华西药学杂志,2012,27(1):96-97.
[12] 董瑞,任东,杨婧威,等.毛细管气相色谱和HPLC法测头孢美唑中的残留溶剂[J].中国抗生素杂志,2011,36(2):139-142.
DOI 10.3870/yydb.2015.08.025
2014-05-04
2014-08-06
郭旭光(1972-),男,河南襄城人,主管药师,硕士,研究方向:食品药品质量控制。电话:0371-63388290,E-mail:gxg0371@126.com。
R973;R927.1
B
1004-0781(2015)08-1081-03

