医院制剂微生物限度检查方法的重新验证
黄依玲
药品微生物试验易受样品成分、试验条件等多种因素的影响,其结果不能真实反映样品污染的微生物状况。中国药典2005版开始规定当建立药品的微生物限度检查法时,应进行检验方法的验证,以确认所采用的方法适合于该药品的细菌、霉菌及酵母菌数的测定,若药品的组分或原检验条件发生改变可能影响到检验结果时,计数方法应重新验证[1]。本实验针对由于医院由于整体搬迁,制剂生产、检验场所及配制制剂的原料生产厂家发生改变,对该院自制制剂的微生物限度检查方法进行重新验证,并与原来的检验方法进行比较和改进,结果总结如下。
1 试验材料
1.1 样品 氨茴香合剂、水合氯醛合剂、ORS-Ⅱ颗粒、10%氯化钾溶液、33%和50%硫酸镁溶液、复方硫酸镁灌肠液、呋喃西林溶液、鼻软膏、鱼肝油软膏、硫磺霜、复方苯酚含漱水、复方硫磺洗剂、痱子水、0.25%氯霉素溶液、炉甘石散剂、30%氧化锌油、链霉素液状石蜡滴鼻液(简称链石液)、呋喃西林麻黄素滴鼻液(O/W乳剂)、麻黄素滴鼻液、碳酸氢钠滴耳液,共计21个品种,每个制剂品种均实验3个批号。制剂的处方成分按中国医院制剂规范及本院制剂规范。
1.2 试验菌株 大肠埃希菌[CMCC(B)44102-1]、金黄色葡萄球菌[CMCC(B)26003-1]、枯草芽胞杆菌[CMCC(B)63501-1]、铜绿假单孢菌[CMCC(B)10104-1]、白色念珠菌[CMCC(F)98001-1]、黑曲霉[CMCC(F)98001-1]由广西食品药品检验所提供,验证试验用菌株传代次数为3~4代。
1.3 试剂 营养琼脂培养基、玫瑰红钠琼脂培养基、营养肉汤培养基、胆盐乳糖培养基(BL)、曙红亚甲蓝琼脂培养基(EMB)、甘露醇氯化钠培养基、十六烷三甲基溴化铵琼脂培养基、改良马丁培养基(以上培养基由广西食品药品检验所提供),蛋白胨(广东环凯生物科技公司),氯化钠、磷酸二氢钾、磷酸氢二钠均为分析纯。
2 方法
实验操作按中国药典2010版二部附录微生物限度检查法[1]中细菌、霉菌及酵母菌计数方法和控制菌检查方法的验证规定进行。每样品分别进行3次以上独立的平行试验,并分别计算各次试验的回收率。
2.1 菌液制备 取实验用菌,临用前用0.9%氯化钠溶液分别制备成每毫升含菌数为50~100cfu的菌悬液和孢子菌液,每次预计数。
2.2 供试液制备 用1∶10供试液进行实验,需要特殊制备供试液的供试品如下:水溶媒的混悬剂如炉甘石散剂、复方硫磺洗剂,取样品放置使充分沉降后,小心取上清液10 ml,加pH7.0无菌氯化钠-蛋白胨缓冲液至100 ml,混匀,制成1∶10的供试液。油性混悬制剂如30%氧化锌油、链霉素石腊油滴鼻液放置使自然沉降后,小心取上层澄清油液10 g,加聚山梨酯10 g,加pH7.0无菌氯化钠-蛋白胨缓冲液适量,搅拌使乳化,逐次加pH7.0无菌氯化钠-蛋白胨缓冲液至100 ml,混匀,制成1∶10的供试液,放置使溶液稳定,取上清液待测。抑菌作用强乳膏剂如硫磺霜,取样品5 g,加聚山梨酯5,卵磷酯1 g,充分搅均,逐次加pH7.0无菌氯化钠-蛋白胨缓冲液至100 ml,搅均,放置使充分沉降后,取上清液以500转/min离心3 min,取上层离心液作为1∶20供试液。
磺胺类软膏剂如鼻软膏,取样品10 g,加45℃的乳化剂(5 g司盘80、3 g单硬脂酸甘油酯、10 g聚山梨酯80),搅拌后,逐次加入45℃的 pH7.0无菌氯化钠-蛋白胨缓冲液至100 ml,加1%PABA5 ml,制成1∶10 供试液,放置使自然沉降后取上清液待测。乳化剂和稀释剂已做稀释剂对照组实验,回收率均>70%。
2.3 验证试验
2.3.1 细菌、霉菌及酵母菌计数方法验证 试验组:取按2.2制备的供试液1 ml和50~100cfu试验菌,分别注入平皿中,倾入琼脂培养基,每株实验菌平行制备2个平皿,按平皿法测定其菌数。
菌液组:用平板法分别测定所加各菌株的试验菌数。供试品对照组:取与实验组同一供试液测定供试品本底菌数。计算回收率(试验组的平均菌落数减去供试品对照组的平均菌落数的值占菌液组的平均菌落数的百分率)应不低于70%。
实验结果21个品种中有10%氯化钾溶液等9个品种用常规方法试验,对6个实验菌均无抑菌作用,回收率均>70%,与上次验证的实验方法无变化;而有些品种的有些试验菌回收率低于70%,有些品种的实验操作方法需作改进,见表1。
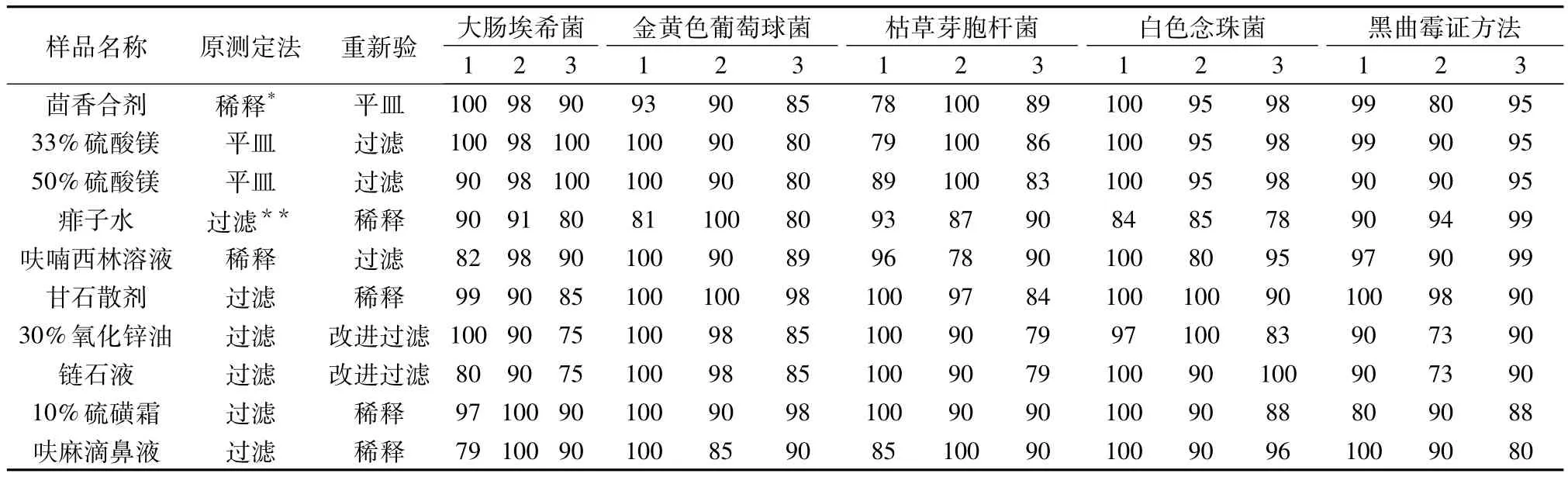
表1 计数验证各试验菌回收率(n=3,%)
2.3.2 控制菌检验方法的验证 试验组:取按2.2制备的供试液10 ml及50~100cfu试验菌加入增菌培养基中,依相应控制菌检查法检查,应检出试验菌。
阴性对照组:方法同试验组,验证大肠埃希菌的阴性对照用金黄色葡萄球菌,铜绿假单孢菌、金黄色葡萄球菌的阴性对照均用大肠埃希菌,阴性对照菌应不得检出,以验证该控制菌检查方法的专属性。
结果大多数品种按常规法检查无抑菌作用,少数制剂通过培养基稀释和延长增菌培养时间即可排除实验干扰,见表2。
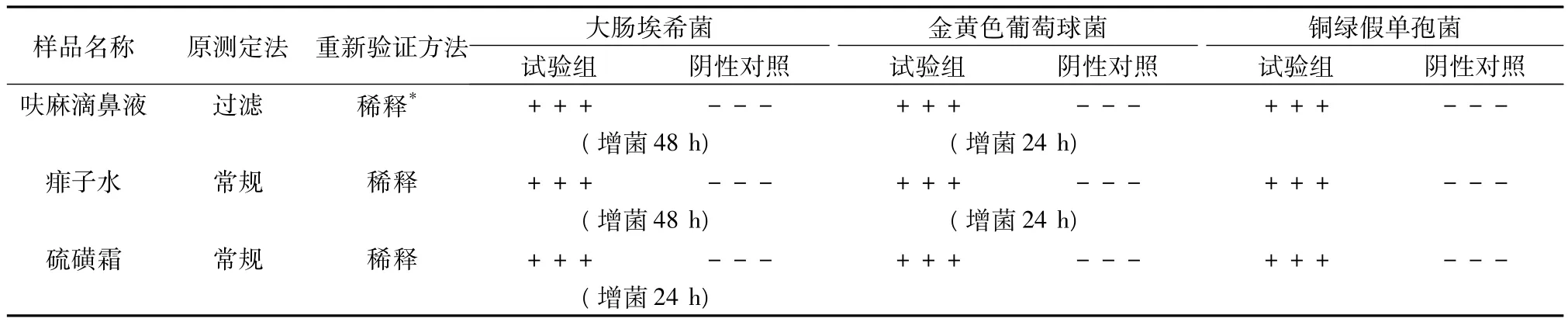
表2 控制菌检查方法验证结果
3 讨论
3.1 与原方法结果比较,部分制剂微生物检验方法有所变化,如氨茴香合剂原来用培养基稀释法,重新验证后用常规平皿法即可使实验菌达到规定的回收率,而33%、50%硫酸镁溶液原来用常规平皿法培养,重新验证结果3次平行实验中有的批次枯草杆菌回收率不能达到70%,因此采用薄膜过滤法。这说明了重新验证的必要性。
3.2 经实验摸索,将原有些剂型的实验方法做有效的改进,使操作更加简便易行,各实验菌得到最稳定的回收率。如有抑菌作用的水溶性制剂如硫酸镁溶液等,或制备成水溶性的供试液如30%氧化锌油,无论抑菌作用强弱,一律用薄膜过滤法,此法比培养基稀释法使用平皿少,实验结果稳定,器皿易清洗,熟练后操作简便易行;对于混悬液的样品如30%氧化锌油、链石液等,在制备1∶10供试液前,取数瓶足量的样品混合后,静置使充分沉降,小心吸取上清油液,加聚山梨酯80进行乳化,再加pH7.0无菌氯化钠-蛋白胨缓冲液至100 ml,制成充分分离不溶性成分的1∶10供试液,使在薄膜过滤时快速易冲洗,避免了原来的检验方法中将样品摇匀后取样制备成1∶10供试液,再进行沉降和低速离心,这样不能将混悬液中不溶性成分充分分离,无法有效进行薄膜过滤和冲洗;对于沉降及低速离心均不易分离的制剂如硫磺霜、呋喃西林麻黄素滴鼻液(乳液),以及含乙醇制剂如痱子水在用水稀释制备1∶10供试液时由于樟脑等成分析出产生少量混浊的样品,不溶性成分不能完全分离,原来用的薄膜过滤法因堵塞不能有效过滤,应用培养基稀释法。
3.3 控制菌检查中因有增菌培养,很多在细菌计数时有抑菌的品种,在控制菌检查中能检出试验菌。除了对抑菌活性较强的抗生素品种用薄膜过滤法外,其余制剂用培养基稀释法延长增菌时间能有效排除抑菌作用。
[1] 国家药典委员会.中华人民共和国药典(二部)2010版,北京:化学工业出版社,2006:附录107-116.

