香草醛/聚乙烯醇/κ-卡拉胶交联薄膜的制备及其性能研究
王秀超,刘保栋,张帅,郭传燕,郭红革
香草醛/聚乙烯醇/κ-卡拉胶交联薄膜的制备及其性能研究
王秀超,刘保栋,张帅,郭传燕,郭红革*
(齐鲁工业大学 轻工学部,济南 250353)
以安全无毒的方式提高聚乙烯醇薄膜的耐水性,用海洋植物来源的κ-卡拉胶材料与聚乙烯醇共混,以部分取代石油基材料成为新的包装材料。以聚乙烯醇为基材,通过共混占聚乙烯醇不同质量分数(2.5%、5%、7.5%、10%、12.5%)的κ-卡拉胶,以确定力学性能最优的共混膜配方。再以最佳共混配方为基础,添加占聚乙烯醇不同质量分数的(12.5%、25%、37.5%)香草醛为交联剂,在pH=2的酸性条件下制备香草醛/聚乙烯醇/κ-卡拉胶交联薄膜。通过傅里叶红外变换光谱、X射线衍射研究薄膜的化学结构,扫描电镜表征薄膜的微观形貌,拉伸强度和断裂伸长率评估薄膜的力学性能,吸湿性测试、水蒸气透过系数以及水接触角表征薄膜的耐水性能、琼脂盘扩散试验表征薄膜的抗菌性能。傅里叶变换红外光谱表明,香草醛的醛基与聚乙烯醇和κ-卡拉胶的醇羟基之间存在羟醛缩合反应,证明发生了交联反应。当聚乙烯醇质量分数为4%、κ-卡拉胶、香草醛分别为的聚乙烯醇质量的7.5%、25%时,共混薄膜的拉伸拉强度达到44.02 MPa;吸湿率(相对湿度为100%)、水蒸气透过系数比纯聚乙烯醇薄膜的分别提升了17.91%、15.18%。抗菌圈实验表明添加香草醛提高了共混薄膜的抗菌性。香草醛的加入改善了聚乙烯醇/κ-卡拉胶共混薄膜的耐水性能、力学性能和抗菌性能,克服了聚乙烯醇薄膜耐水性差的缺点,拓展了其应用范围。
聚乙烯醇;κ-卡拉胶;香草醛;交联;耐水性
在过去的十年间,以石油基为代表的不可降解的塑料废物造成了严重的环境污染[1]。对这一问题的关注使全球范围内利用可再生资源开发环保型可生物降解聚合物成为趋势[2]。聚乙烯醇(Polyvinyl Alcohol,PVA)是一种可生物降解的合成聚合物,具有良好的拉伸强度、柔韧性和热稳定性[3]。它已被广泛地应用于涂料、纺织品、纸张加工助剂和塑料制品等领域[4]。但由于PVA膜过于柔软,且结构中含有大量羟基导致其耐水性能差[5],极大地限制了其应用,无法满足在实际应用中的使用需求。因此,需要对PVA薄膜进行改性,既可以提高其力学和耐水等应用性能,也可以拓宽其应用范围。化学交联改性可以在PVA薄膜的高分子链之间形成化学键交联的网络[6],从而提高PVA膜的力学性能和耐水性[7]。
卡拉胶是一类线性、含有硫酸酯基团的高分子水溶性非均一多糖,由D-半乳糖和3,6-脱水-D-半乳糖单元组成,主要从海洋红藻中提取[8]。根据硫酸酯基团数量和位置的不同,卡拉胶可分为多种类型,其中kappa (κ)、lambda (λ)、Iota (ι)类型应用最为广泛[9]。一般来说,κ-卡拉胶(κ-carrageenan,KC)表现出最强的胶凝能力,因为它含有约25%~30%的硫酸基团和28%~35%的3,6-脱水半乳糖含量[10]。KC具有良好的凝胶性与成膜性,但KC单独成膜脆性大,无法满足使用需求。与传统的石油基薄膜材料相比,KC具有很大的优势,因为它不仅无毒可生物降解,且价格低廉[11],是新型可降解塑料薄膜无可争议的新材料。KC是水溶性的,因为其结构中含有羟基[12],所以KC分子上的羟基既可以与PVA形成分子内和分子间氢键,又可以与PVA分子上大量的羟基发生化学交联反应,从而提升交联膜的耐水性。
本文采用化学交联法,在酸性条件下,通过添加交联剂使PVA发生化学交联反应从而改善薄膜的综合性能。选择恰当的交联剂可使PVA得到更好的交联,否则PVA交联不完全可能会影响薄膜的性能。目前,有采用PVA甲醛化[13]、肉桂醛交联[14]、硼砂改性[15]等方法对PVA薄膜进行改性,但由于存在甲醛具有刺激性气味及毒性、肉桂醛在水中的溶解度低且有异味、硼砂改性难以控制等弊端,使他们应用范围受到限制。在此背景下,无毒、溶解度高的交联剂受到了更多的关注[16]。存在于香子兰(Vanilla Planifolia)种子中的香草醛(Vanillin,Van)是常用的添加剂之一,并且在诸如食品、饮料、香料和制药工业的实际应用中广泛用作调味剂和防腐剂[17]。它具有香甜、浓烈的奶香气味[18],可有效掩盖KC本身的腥味。PVA分子上的羟基既可以与KC分子上的羟基形成氢键,又可以与Van分子上的醛基发生羟醛缩合反应[19]。因此,本文采用Van作为交联剂,柠檬酸(CA)为pH调节剂,添加KC改性PVA薄膜,以提高薄膜的综合性能。
1 实验
1.1 材料与仪器
主要材料:聚乙烯醇(PVA 2488型),上海英佳工业发展有限公司;κ-卡拉胶,青岛德惠卤科技有限公司;甘油(分子摩尔质量为92.09 g/mol)和香草醛,国药化学试剂有限公司;柠檬酸,上海麦克林生化有限公司;水,试验中所用水均为去离子水。
主要仪器:DF-101S恒温水浴锅,河南予华仪器有限公司;BDZF-55鼓风干燥箱,山东博科科学仪器有限公司;Regulus 8100扫描电子显微镜,日立高新技术公司;SmartLab X射线衍射仪,日本理学;NICOLET iS10傅里叶红外分光光谱仪,美国Massachusetts公司;TGAQ50热重分析仪,沃特世科技(上海)有限公司;XLW(EC)电子拉力试验机,济南兰光机电技术有限公司;CT-7005-T恒温恒湿箱,高铁检测仪器(东莞)有限公司;BKQ-BXX Ⅱ高温高压灭菌锅,山东博科消毒设备;THZ-100恒温培养摇床,上海一恒科学仪器;SPL-250生化培养箱,天津莱铂特瑞。
1.2 方法
1.2.1 成膜液的制备
将4 g PVA粉末分散到含有100 mL去离子水的锥形瓶中并用保鲜膜覆盖瓶口,充分溶胀后制成质量分数为5%的PVA水溶液,分别将占PVA不同质量分数(2.5%、5%、7.5%、10%、12.5%)的KC分散到PVA溶液中,并在90 ℃油浴锅中搅拌2 h制成PVA/KC共混成膜液。在PVA/KC共混成膜液中,加入一定量的CA将pH值调至2,随后加入占PVA不同质量分数(12.5%、25%、37.5%)的Van继续在90 ℃下搅拌2 h,最后将1 g甘油与上述复配体系混合得到PVA/KC/Van/CA共混成膜液,静置消泡后备用。
1.2.2 薄膜的制备
取相同体积的上述成膜液在20 cm×20 cm规格的玻璃板上流延,并在60 ℃烘箱中干燥12 h,揭膜后于温度为25 ℃、相对湿度为53%的恒温恒湿箱中保存48 h后测试性能。
1.3 测试与表征
1.3.1 力学性能测试
参考Vanjeri等[20]的方法,在室温下使用万能电子拉力试验机测试薄膜的力学性能。夹距为80 mm,拉伸速度为50 mm/min,每个样品设置5组平行试验。
1.3.2 薄膜的微观结构表征
选取无杂质和气泡的薄膜,平衡后在液氮中浸泡后破碎,经真空溅射喷金处理后,用扫描电子显微镜研究薄膜横截面的形态。
1.3.3 傅里叶红外光谱测试
采用傅里叶红外光谱(FTIR)分析薄膜各组分基团的变化情况。参数设定:分辨率为4 cm−1,扫描波数为600~4 000 cm−1,扫描次数为64。
1.3.4 X-射线衍射分析
使用X-射线衍射仪(X-ray Diffraction,XRD)对薄膜的结晶性进行分析,采用CuKa射线为辐射源,入射线波长0.154 nm,扫描角度2为5°~60°,扫描速度为2(°)/min。加速电压和电流分别为40 kV和40 mA,扫描范围为5°~60°,扫描速度为20(°)/min。
1.3.5 吸湿性测试
参考GB/T 1034—2008[21]塑料吸湿性的测试。在25 ℃条件下将薄膜放置在存有无水硅胶颗粒的干燥器中平衡48 h,并将其裁剪为20 mm×20 mm的样品进行称量;然后将样品平铺在表面皿上,在温度为25 ℃,相对湿度分别为53%、100%的恒温恒湿箱中放置48 h后,取出称量。根据吸湿前和吸湿后薄膜的质量,利用式(1)计算出吸湿程度。
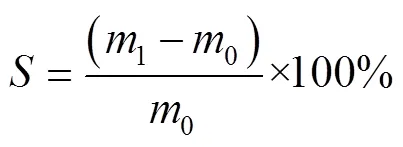
式中:0和1分别为吸湿前后薄膜的质量,g。
1.3.6 水蒸气透过性测试
根据GB/T 1037—2021[22]测试薄膜的水蒸气渗透性。将样品固定在烧杯瓶口,瓶内装有无水硅胶,置于温度为25 ℃、相对湿度为53%的恒温恒湿箱中24 h。水蒸气透过率(WVP)利用式(2)计算。
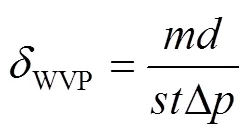
式中:为烧杯质量的增加量,g;为薄膜的厚度,cm;为水蒸气透过薄膜的有效面积,cm2;为测定时间,h;Δ为膜两侧水蒸气压差,kPa。
1.3.7 水接触角测试
使用接触角测量仪对贴在载玻片上的样品(1 cm× 1 cm)进行接触角测量。将去离子水(2 μL)滴落并与样品薄膜接触,拍摄并记录液滴滴落在样品膜上第10 s 内的水接触角。
1.3.8 抗菌性测试
参考标准EN ISO 20645—2004[23],采用琼脂盘扩散法评价薄膜的抗菌活性。对样品上的大肠杆菌()以及金黄色葡萄球菌()进行检测。将细菌悬液均匀地分布在琼脂盘表面,将圆形的薄膜样品与琼脂表面接触,在温度为37 ℃的生化培养箱中培养24 h。结束后,观察并拍摄琼脂盘表面的抑制圈。
2 结果与分析
2.1 PVA/KC共混膜的力学性能分析
图1中反映了不同KC添加量对PVA薄膜拉伸强度(Tensile Strength,TS)和断裂伸长率(Elongation at Break,EB)的影响。实验结果显示,当KC的添加量为2.5%、5.0%、7.5%时,PVA/KC共混薄膜的拉伸强度与纯PVA薄膜相比逐渐升高;当KC添加量为7.5%时,共混膜的TS值最高,为44.02 MPa。这是因为在PVA/KC共混薄膜中,PVA分子与KC分子间存在氢键作用。共混薄膜的断裂伸长率随着KC添加量的增加而降低,并且当KC的添加量达到10.0%时,薄膜的拉伸强度也开始降低。这是因为过高浓度的KC导致共混薄膜之间的相容性减弱,打破了原本致密的结构,使PVA结构变得松散,导致其断裂伸长率下降。因此,选取7.5%的KC作为最佳添加量。
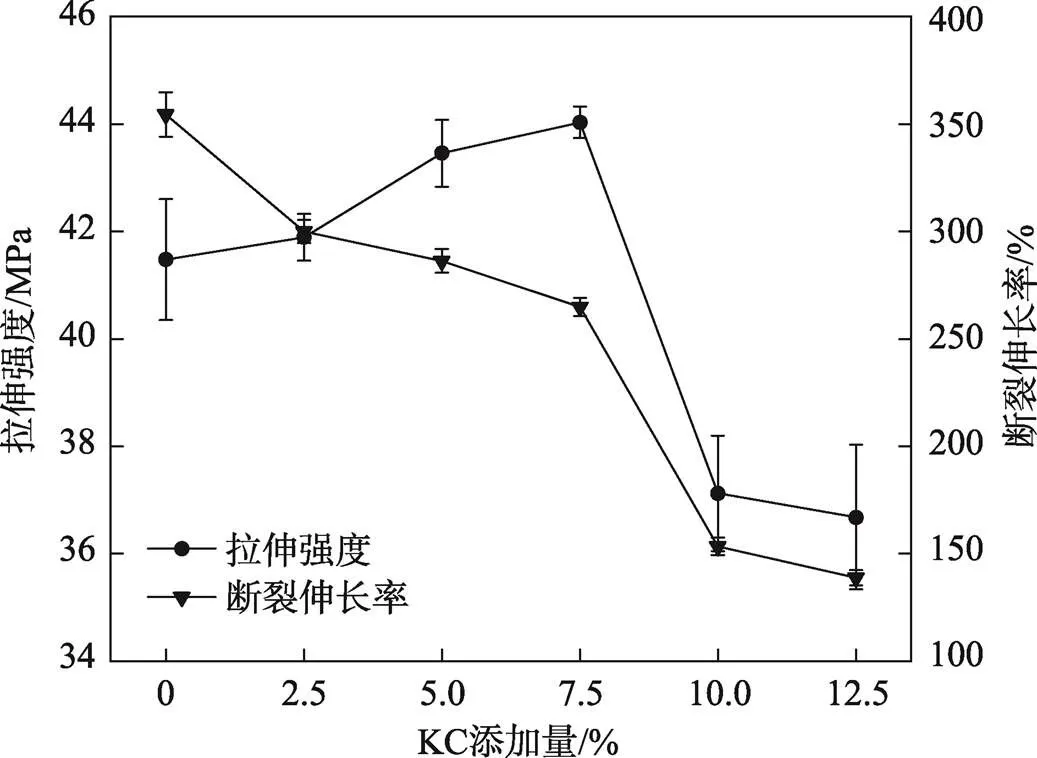
图1 不同KC添加量对PVA薄膜力学性能的影响
2.2 Van/PVA/KC交联膜力学性能分析
图2为不同添加量的Van对PVA/KC共混薄膜的拉伸强度和断裂伸长率的影响。实验结果显示,与PVA/KC共混薄膜相比,在酸性条件下添加Van的PVA/KC共混薄膜的拉伸强度均得到进一步提高,同时断裂伸长率显示出下降趋势。这是因为Van的加入可能使PVA和KC分子链间发生化学交联,使得PVA聚合物线性链迁移比较困难,可以承受更大的力,同时交联反应可能导致三维网络结构的形成[24],这也可以限制分子间的相对滑动,从而进一步提高了薄膜的拉伸强度。PVA/KC共混薄膜在Van添加量达到25.0%和37.5%时薄膜的拉伸强度达到最高且两者差别不大。因此,选取25%作为Van的最佳添加量。
2.3 Van/PVA/KC交联膜的断面形貌分析
图3显示了纯PVA薄膜、PVA/KC共混薄膜、Van/PVA/KC薄膜的断面微观结构。PVA/KC共混薄膜出现了糯状的突起痕迹,这可能是KC凝胶引起的,但是整体断面较为均匀,这说明KC与PVA的相容性良好;断裂处有明显分层,这说明KC的加入导致PVA薄膜的脆性变大,从而造成薄膜的断裂伸长率降低。添加Van的PVA/KC共混薄膜与未添加Van的薄膜相比,其横截面更致密、更光滑且连续,甚至出现鱼鳞状的断痕,这可能是由于发生了交联反应,从而改变了薄膜的结构,其拉伸性能得到进一步增强。
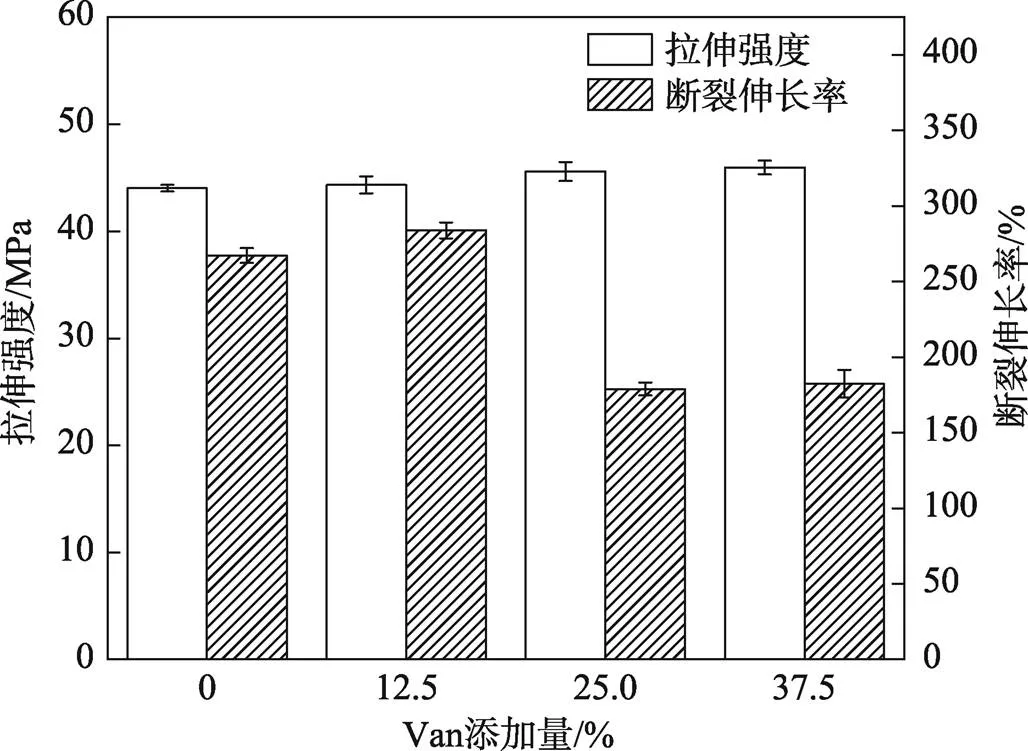
图2 不同Van添加量对PVA/KC共混膜力学性能的影响
2.4 Van/PVA/KC交联膜的微观结构分析
2.4.1 FTIR表征分析
如图4所示,分别测定了纯PVA膜、PVA/KC共混薄膜、PVA/KC/Van/CA共混薄膜、KC、CA以及KC/CA的KBr压片的红外光谱图。KC的红外光谱图显示,在3 700~3 100 cm−1的特征峰来自于KC上羟基的伸缩振动,在1 224、920和838 cm−1处的吸收峰分别归属于硫酸酯的S=O基团、3,6-脱水-D-半乳糖和D-半乳糖-4-硫酸酯基团,1 031 cm−1处的峰是3,6-脱水-D-半乳糖中C—O—C键引起的。在纯PVA光谱中,3 700~3 100 cm−1间较大的谱带是羟基的伸缩振动形成的。

图3 PVA/KC共混薄膜和PVA/KC/Van/CA共混薄膜的截面扫描电子显微镜图
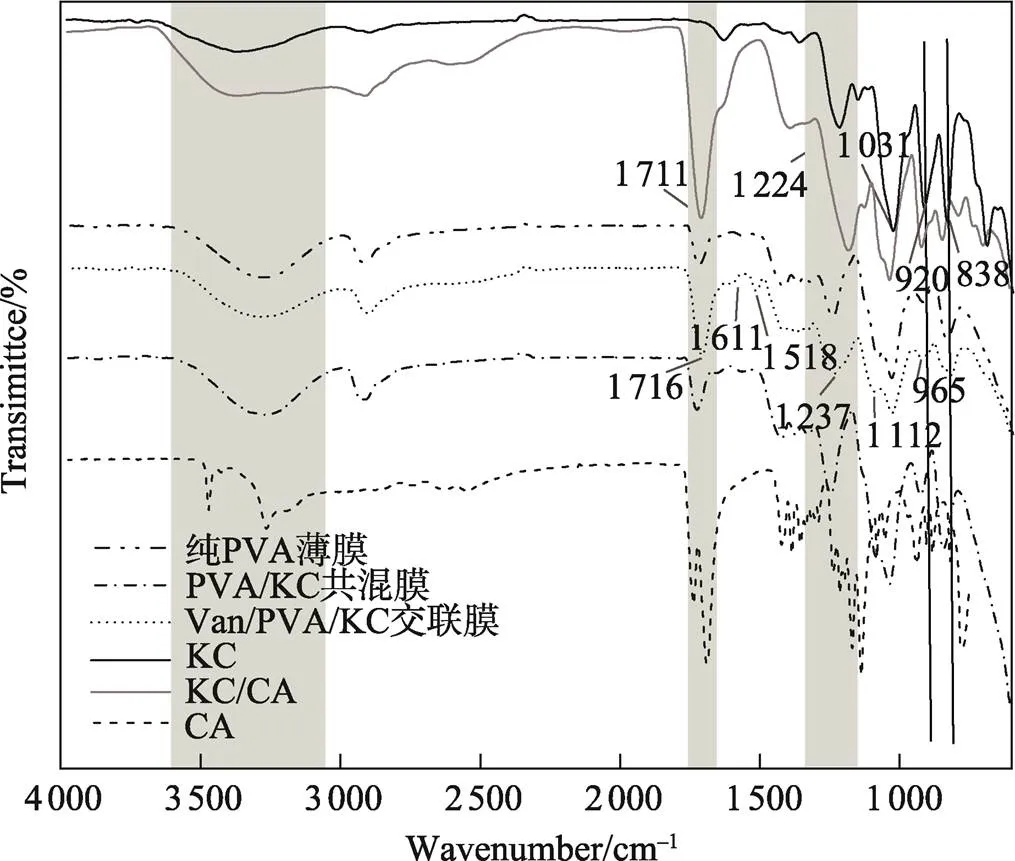
图4 纯PVA薄膜、PVA/KC混合膜、 Van/KC/PVA交联膜、KC和KC/CA的 KBr压片的红外光谱图
PVA/KC共混薄膜表现出与纯PVA薄膜类似的光谱,但显示出D-半乳糖-4-硫酸酯基团、3,6-脱水-D-半乳糖的特征峰。3 600~3 000 cm−1处PVA的醇羟基(氢键缔合)吸收峰变小,纯PVA薄膜中1 035 cm−1处醇C—OH基团的C—O弯曲振动结合引起的吸收峰变得更尖锐,并且向右偏移,证明PVA与KC之间存在氢键作用,这与Chan等[25]使用淀粉与PVA共混测试结果一致。KC/CA红外图谱中显示838、920 cm−1的D-半乳糖-4-硫酸酯基团、3,6-脱水-D-半乳糖的特征峰变小,并且新增1 711 cm−1处C=O的伸缩振动峰。这可能是由于CA受热使其分子内脱水生成酸酐,柠檬酸酐与KC发生化学反应,说明成功引入了柠檬酸酐基团,与徐坤等[26]使用CA与淀粉制备柠檬酸双酯淀粉的测试结果一致。在PVA/KC/Van/CA交联膜红外图谱中显示出Van的特征峰(1 518、1 611 cm−1),羟基峰变小,并且1 100~1 000 cm−1处C−OH基团的C−O吸收峰变小。证明在成膜过程中PVA的羟基与Van的醛基之间可能发生了羟醛缩合反应[7]。Van与PVA可能发生的化学反应机理如图5所示。综上所述,PVA/KC/Van/CA体系内发生了交联反应,并同时存在多种交联反应产物。
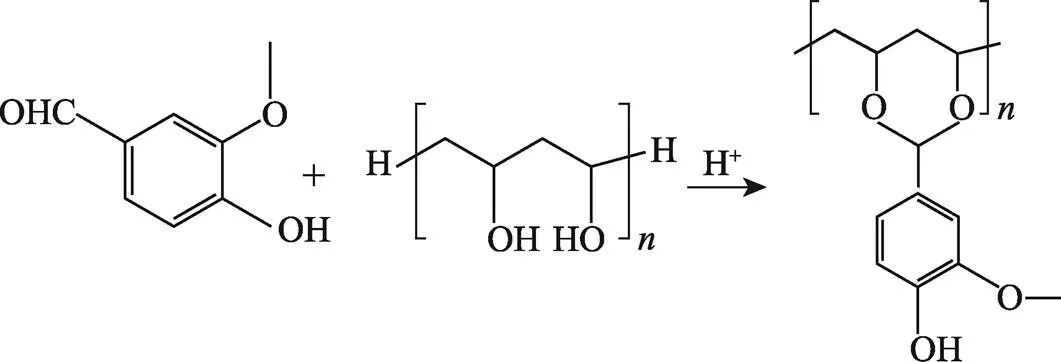
图5 PVA与Van的化学反应过程
2.4.2 X射线衍射表征分析
纯PVA薄膜、PVA/KC共混薄膜、PVA/KC交联薄膜、纯KC薄膜的XRD曲线如图6所示。图6a显示出卡拉胶薄膜在2=19.8°处有一个宽峰,表明它基本上具有无定形结构[27]。图6b显示的3条曲线相似,PVA衍射的主要特征峰为2=19.6°,纯PVA薄膜的结晶度为19.47%,PVA/KC共混薄膜的结晶度为17.57%。PVA与KC混合后薄膜的结晶度降低,这是因为KC与PVA组分之间的强相互作用会抑制PVA大分子排列并破坏晶体结构,导致结晶度降低。这与Tian等[28]制备的聚乙烯醇共混淀粉薄膜结晶度变化相一致。Van/PVA/KC交联膜的结晶度为14.67%,与PVA/KC共混薄膜相比,Van/PVA/KC交联膜的结晶度降低。这可能是由于交联作用,使PVA的羟基与Van的醛基之间发生了化学键合作用,形成了网状结构[7],限制了PVA分子的运动,Van/PVA/KC交联膜的结晶度降低。
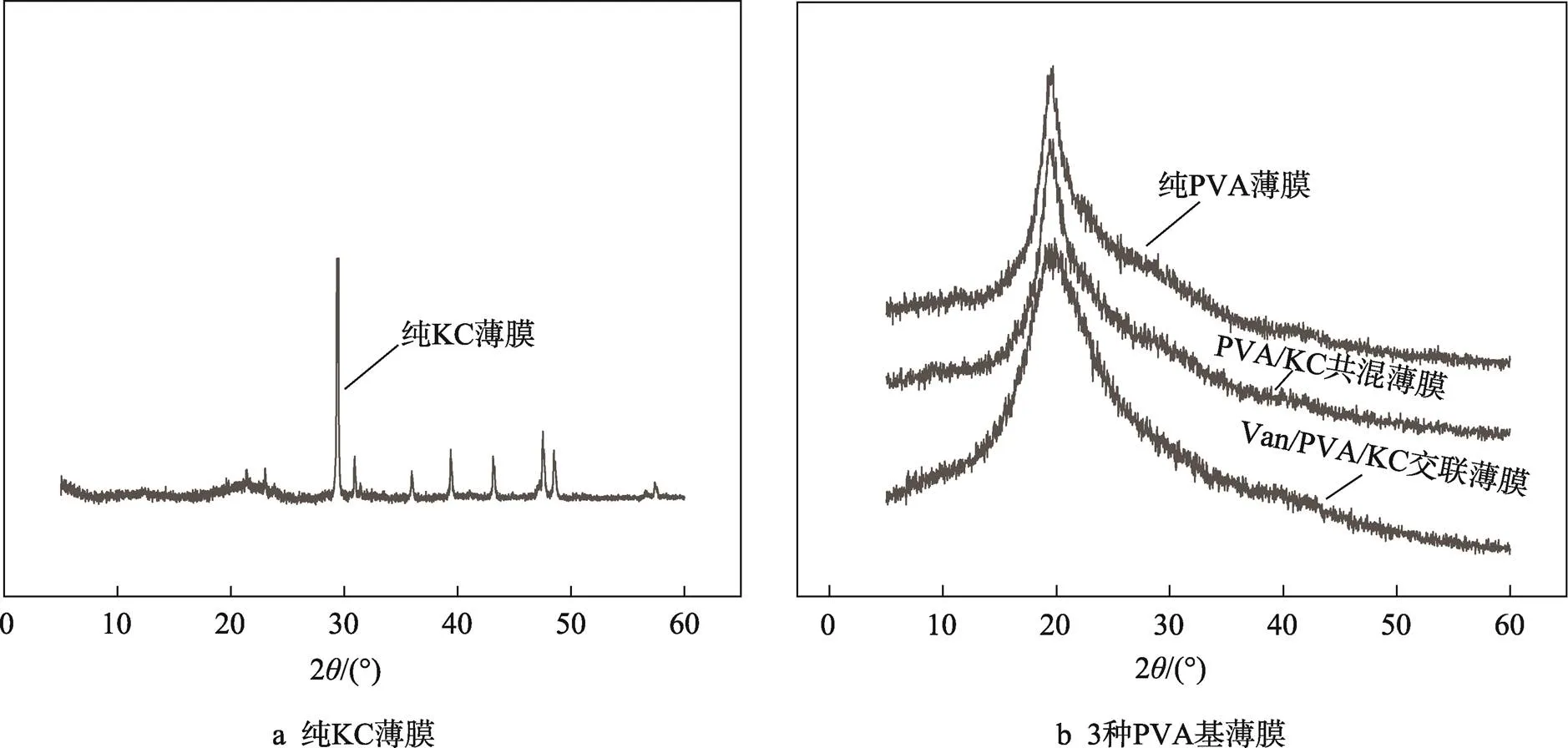
图6 X射线衍射图谱
2.5 Van/PVA/KC交联膜的亲水性分析
2.5.1 吸湿率分析
图7为不同Van添加量条件下PVA/KC交联薄膜吸湿率的变化。由于PVA、KC均具有亲水性,所以薄膜对环境湿度有着高敏感度。当相对湿度从53%提高到100%时,不同Van添加量的PVA/KC交联薄膜的吸湿率变化趋势相同且都相应提高。随着Van 添加量的增多,PVA/KC交联薄膜的吸湿率呈下降趋势。这是因为交联反应消耗掉分子链中亲水的羟基基团,减小了对水的亲合作用[29]。
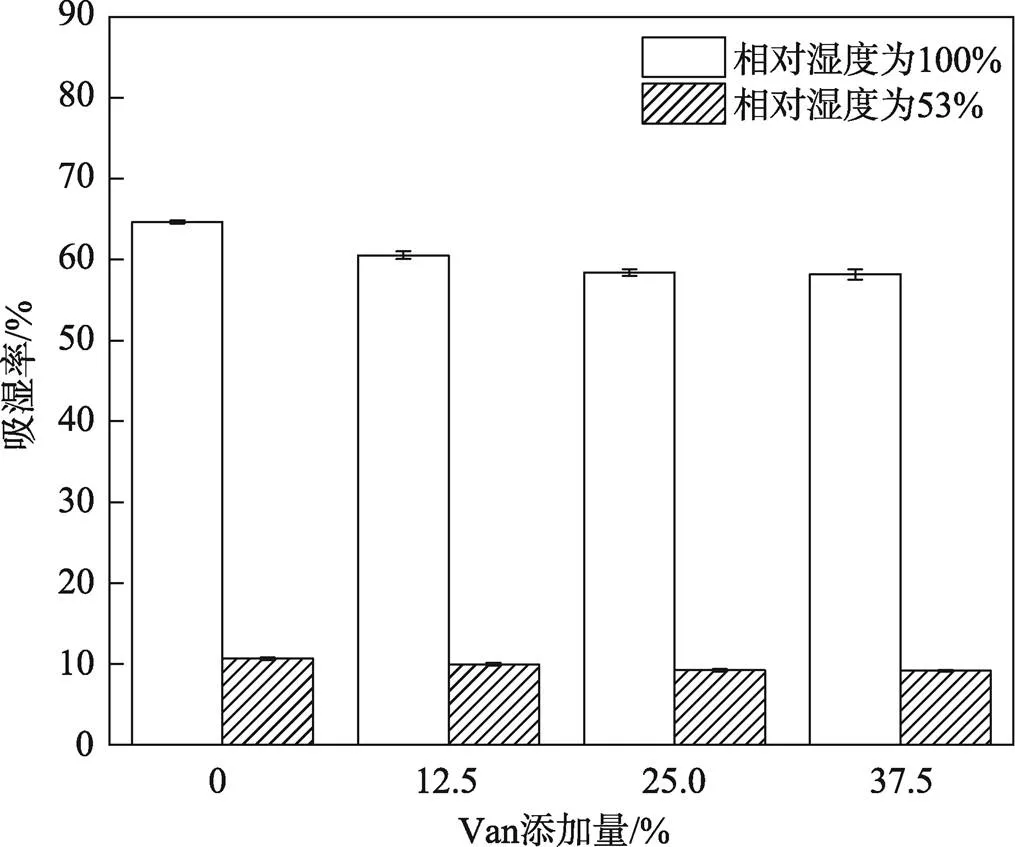
图7 不同Van添加量对Van/PVA/KC交联膜吸湿率的影响
2.5.2 水蒸气透过系数分析
表1中为纯PVA薄膜以及不同Van添加量的PVA/KC交联薄膜的水蒸气透过系数。所有PVA/KC交联薄膜的水蒸气透过系数均比纯PVA薄膜的更低,且随着Van添加量的增多,薄膜的水蒸气透过系数变化不大。这是因为含羟基的CA和Van,不仅可以与PVA和KC形成氢键,还可以发生酯化反应[30]和羟醛缩合反应,形成的化学键使结构更加致密,对水的亲和作用更低,从而导致水分子不易通过。
表1 薄膜的水蒸气透过系数
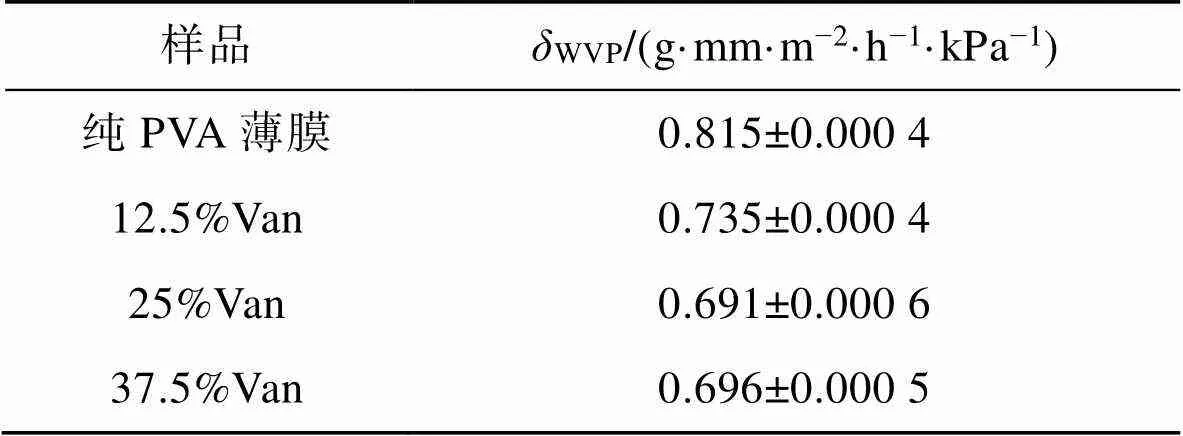
Tab.1 WVP of films
2.5.3 水接触角分析
水接触角是表征薄膜表面的耐水性的重要指标之一。图8为纯PVA薄膜以及不同Van添加量的PVA/KC交联薄膜的水接触角图像。结果表明,纯PVA薄膜以及PVA/KC交联薄膜均为亲水性膜。与纯PVA膜相比,PVA/KC交联薄膜的表面亲水性随着Van添加量的增加呈先下降后上升的趋势。这可能是因为KC与PVA共混后产生的强氢键作用以及Van参与的交联反应使薄膜中的羟基数量减少,故亲水性下降。水接触角的最大值为59°,较纯PVA薄膜约提升23%。但加入过量的Van会导致PVA/KC共混薄膜亲水性上升。这是因为过量的Van打破了PVA内部羟基的氢键联接,暴露出更多的游离羟基与水亲合,导致亲水性提高。

图8 薄膜的水接触角
2.6 Van/PVA/KC交联膜的抗菌性能分析
图9为纯PVA薄膜、PVA/KC共混薄膜、PVA/KC交联薄膜的抑菌圈试验结果。纯PVA薄膜与PVA/KC共混薄膜并没有显示出抗菌特性,而添加了Van、CA的PVA/KC交联薄膜显示出明显的抗菌圈,证明了Van/PVA/KC交联膜具有抗菌特性。这是因为Van的抑菌基团为醛基,醛基的极性效应使醛基碳带正电荷,醛基氧带负电荷,醛通过带正电荷的碳与带孤对电子的氨基(−NH4+,细菌蛋白质的氨基)或细菌酶系统的巯基(−SH)等发生亲核加成反应,使细菌失去复制能力,引起代谢系统紊乱,达到杀菌抑菌的目的[31]。CA的加入既可以为交联反应提供酸性环境,也可以提升Van/PVA/KC交联膜的抗菌性能[32]。
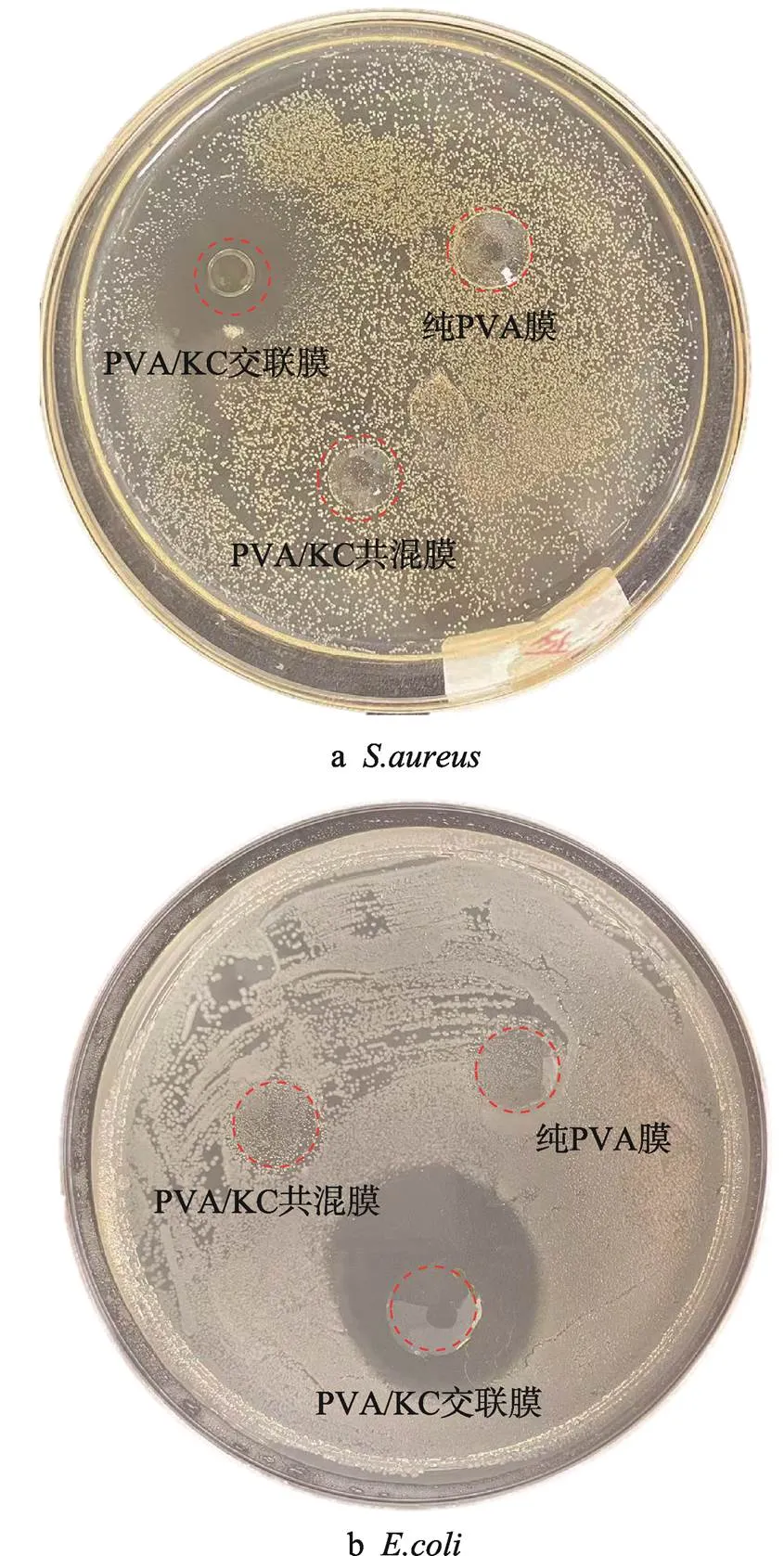
图9 薄膜的抑菌圈图像
3 结语
通过化学交联法成功制备了具有抗菌活性的PVA/KC耐水膜。FTIR与XRD分析证实了PVA、KC与Van间以化学键形式进行连接,形成交联结构;PVA结晶度下降表明交联作用消耗了其分子上的羟基,可以有效提高PVA的耐水性。SEM显示出Van/PVA/KC交联膜的断面更光滑、结构更致密。当KC添加量为7.5%、Van添加量为25%时,Van/PVA/KC交联膜显示出更高的抗拉强度以及较低的断裂伸长率,其拉伸强度为44.02 MPa,断裂伸长率为178.9%。Van/PVA/KC交联薄膜的吸湿性、水蒸气透过系数、表面亲水性均低于纯PVA薄膜,证明耐水性能得到提升。虽然部分Van参与了交联反应,但游离的Van使Van/PVA/KC交联膜表现出良好的抗菌性能。综上所述,KC与Van的加入改善了PVA薄膜的理化性质与功能特性,可作为一种包装材料用于延长食品的货架寿命。
[1] SATTI S M, SHAH A A. Polyester-Based Biodegradable Plastics: an Approach Towards Sustainable Development[J]. Lett Appl Microbiol, 2020, 70(6): 413-430.
[2] SÁNCHEZ C. Fungal Potential for the Degradation of Petroleum-Based Polymers: An Overview of Macro- and Microplastics Biodegradation[J]. Biotechnology Advances, 2020, 40: 107501.
[3] CHEN W, DING J, YAN X, et al. Plasticization of Cottonseed Protein/Polyvinyl Alcohol Blend Films[J]. Polymers 2019, 11(12): 2096.
[4] GAUTAM L, WARKAR S G, AHMAD S I, et al. A Review on Carboxylic Acid Cross-Linked Polyvinyl Alcohol: Properties and Applications[J]. Polymer Engineering & Science, 2021, 62(2): 225-246.
[5] ASADPOUR S, RAEISI VANANI A, KOORAVAND M, et al. A Review on Zinc Oxide/Poly(Vinyl Alcohol) Nanocomposites: Synthesis, Characterization and Applications[J]. J Cleaner Prod, 2022, 362: 132297.
[6] KUMAR A, RYPAROVá P, HOSSEINPOURPIA R, et al. Hydrophobicity and Resistance Against Microorganisms of Heat and Chemically Crosslinked Poly(Vinyl Alcohol) Nanofibrous Membranes[J]. Chem Eng J, 2019, 360: 788-796.
[7] GAO H, YANG H. Characteristics of Poly(Vinyl Alcohol) Films Crosslinked by Cinnamaldehyde with Improved Transparency and Water Resistance[J]. J Appl Polym Sci, 2017, 134:37-38.
[8] FIRDAYANTI L, YANTI R, RAHAYU E S, et al. Carrageenan Extraction from Red Seaweed (Kappaphycopsis Cottonii) Using the Bead Mill Method[J]. Algal Res, 2023, 69: 102906.
[9] SEDAYU B B, CRAN M J, BIGGER S W. Reinforcement of Refined and Semi-Refined Carrageenan Film with Nanocellulose[J]. Polymers, 2020, 12(5): 1145-1145
[10] WANG X, ZHOU D, GUO Q, et al. Textural and Structural Properties of a Kappa-Carrageenan-Konjac Gum Mixed Gel: Effects of Kappa-Carrageenan Concentration, Mixing Ratio, Sucrose and Ca(2+) Concentrations and Its Application in Milk Pudding[J]. J Sci Food Agric, 2021, 101(7): 3021-3029.
[11] EL-FAWAL G. Preparation, Characterization and Antibacterial Activity of Biodegradable Films Prepared from Carrageenan[J]. Journal of Food Science and Technology, 2014, 51(9): 2234-2239.
[12] CROITORU C, POP M A, BEDO T, et al. Physically Crosslinked Poly (Vinyl Alcohol)/Kappa-Carrageenan Hydrogels: Structure and Applications[J]. Polymers, 2020, 12(3):560.
[13] CHEN L, QIANG T, CHEN X, et al. Tough and Biodegradable Gelatin-Based Film via the Synergistic Effect of Multi-Cross-Linking[J]. ACS Appl Polym Mater, 2022, 4(1): 357-368.
[14] KARDAM S K, KADAM A A, DUTT D. Retention of Cinnamaldehyde in Poly(Vinyl Alcohol) Films Intended for Preservation of Faba Beans through Vapor-Phase Antimicrobial Effect[J]. Food Packag Shelf Life, 2021, 29: 100704.
[15] TANPICHAI S, OKSMAN K. Crosslinked Poly(Vinyl Alcohol) Composite Films with Cellulose Nanocrystals: Mechanical and Thermal Properties[J]. J Appl Polym Sci, 2018, 135(3): 1-11.
[16] PARK C, LEI J, SHIN H, et al. Polydopamine-Vanillin Surface-Modified Thin-Film Composite Membrane to Mitigate Bacterial Growth[J]. J Environ Chem Eng, 2022, 10(5): 108307.
[17] DAS S, VISHAKHA K, BANERJEE S, et al. Antibacterial and Antibiofilm Effectiveness of Bioactive Packaging Materials from Edible Sodium Alginate and Vanillin: Assessment on Lettuce[J]. J Food Process Preserv, 2021, 45(9): 15668.
[18] KUNDU A. Vanillin Biosynthetic Pathways in Plants[J]. Planta, 2017, 245(6): 1069-1078.
[19] ZHANG Z H, HAN Z, ZENG X A, et al. Enhancing Mechanical Properties of Chitosan Films Via Modification with Vanillin[J]. Int J Biol Macromol, 2015, 81: 638-643.
[20] VANJERI V N, GOUDAR N, KASAI D, et al. Thermal and Tensile Properties Study of 4-Hydroxycoumarin Doped Polyvinyl Alcohol/Chitosan Blend Films[J]. Chem Data Collect, 2019, 23: 100257.
[21] GB/T 1034—2008, 塑料吸水性的测定[S].
GB/T 1034-2008,Plastics—Determination of Water Absorption[S].
[22] GB/T 1037—2021, 塑料薄膜与薄片水蒸气透过性能测定杯式增重与减重法[S].
GB/T 1037-2021,Test Method for Water Vapor Transmission of Plastic Film and sheet—Desiccant Method and Water Method[S].
[23] EN ISO 20645—2004, 纺织织物.抗菌活性的测定.琼脂扩散木片试验[S].
EN ISO 20645-2004, Textile Fabrics-Determination of Antibacterial Activity-Agar Diffusion Plate Test[S].
[24] 李昂, 郭建华, 王燕, 等. 双醛淀粉交联大豆蛋白/聚乙烯醇复合膜的制备及微观结构表征[J]. 齐齐哈尔大学学报(自然科学版), 2023, 39(4): 52-55.
LI Ang, GUO Jian-hua, WANG Yan, et al. Preparation and Microstructure Characterization of SPI/PVA Composite Membrane Crosslinked with Dialdehyde Starch[J]. Journal of Qiqihar University (Natural Science Edition), 2023, 39(4): 52-55.
[25] CHAN M K, TANG T H. The Properties of Starch/Cellulose/ Polyvinyl Alcohol Composite as Hydrodegradable Film[J]. Polym Polym Compos, 2022, 30: 1-8.
[26] 徐坤, 李文婷, 刘青明, 等. 柠檬酸甘油共混热塑性淀粉的制备及性质研究[J]. 中国粮油学报, 2012, 27(1): 38-42.
XU Kun, LI Wen-ting, LIU Qing-ming, et al. The Preparation and Nature of Citric Acid/Glycerine Blending Thermoplastic Glutinous Rice Starch[J]. Journal of the Chinese Cereals and Oils Association, 2012, 27(1): 38-42.
[27] RONG L, ZHANG T, MA Y, et al. An Intelligent Label Using Sodium Carboxymethyl Cellulose and Carrageenan for Monitoring the Freshness of Fresh-Cut Papaya[J]. Food Control, 2023, 145: 109420.
[28] TIAN H, YAN J, RAJULU A V, et al. Fabrication and Properties of Polyvinyl Alcohol/Starch Blend Films: Effect of Composition and Humidity[J]. Int J Biol Macromol, 2017, 96: 518-23.
[29] 任世学, 倪海月, 田金玲, 等. 碱木质素交联PVA共混啶虫脒缓释薄膜的制备及性能[J]. 北京林业大学学报, 2015, 37(12): 116-121.
REN Shi-xue, NI Hai-yue, TIAN Jin-ling, et al. Preparation and Performance of Alkali Lignin-PVA Crosslinked Blend Slow-Release Acetaniprid Film[J]. Journal of Beijing Forestry University, 2015, 37(12): 116-121.
[30] 邹国享, 邹新良, 瞿金平. 淀粉/PVA降解塑料耐水性能的研究[J]. 塑料科技, 2008, 36(2): 54-58.
ZOU Guo-xiang, ZOU Xin-liang, QU Jin-ping. Study on Water Resistance of Starch/PVA Biodegradable Plastics[J]. Plastics Science and Technology, 2008, 36(2): 54-58.
[31] MATEI A, PUSCAS C, PATRASCU I, et al. On the Stability of Glutaraldehyde in Biocide Compositions[J]. International Journal of Molecular Sciences, 2020, 21(9): 3372.
[32] VERDEGUER P, GIL J, PUNSET M, et al. Citric Acid in the Passivation of Titanium Dental Implants: Corrosion Resistance and Bactericide Behavior[J]. Materials, 2022, 15(2): 545.
Preparation and Properties of Vanillin/Poly(Vinyl Alcohol)/κ-carrageenan Cross-linked Films
WANG Xiu-chao, LIU Bao-dong, ZHANG Shuai, GUO Chuan-yan,GUO Hong-ge*
(Faculty of Light Industry, Qilu University of Technology, Jinan 250353, China)
The work aims to improve the water resistance of polyvinyl alcohol films in a safe and non-toxic manner and blend the κ-carrageenan materials from marine plant with polyvinyl alcohol to partially replace petroleum-based materials as a new packaging material. Firstly, poly(vinyl alcohol) was used as the base material to determine the blended film formulation with optimal mechanical properties by blending κ-carrageenan with different mass fractions of poly(vinyl alcohol) (2.5%, 5%, 7.5%, 10%, and 12.5%). Then, the vanillin/polyvinyl alcohol/κ-carrageenan films were prepared based on the optimal blending formulation after added with different mass fractions of (12.5%, 25%, and 37.5%) vanillin as a cross-linking agent under acidic conditions at pH=2. The chemical structures of the films were investigated by Fourier Transform Infrared Spectroscopy (FTIR) and X-ray Diffraction (XRD), the microscopic morphologies of the films were characterized by Scanning Electron Microscopy (SEM), the mechanical properties of the films were evaluated based on Tensile Strength (TS) and Elongation at Break (EB), the water resistance of the films was characterized by the hygroscopicity test, Water Vapor Permeation Coefficient (WVP), and Water Contact Angle, and the antimicrobial properties of the films were characterized by the agar disc diffusion test. FTIR spectroscopy showed hydroxyaldol condensation among the aldehyde group of vanillin and the alcohol hydroxyl group of polyvinyl alcohol and κ-carrageenan, proving that cross-linking reaction occurred. When the mass fraction of polyvinyl alcohol was 4%, κ-carrageenan and vanillin were 7.5% and 25% of the mass of polyvinyl alcohol, respectively, the tensile strength of the blended film reached 44.02 MPa. Compared with the pure poly(vinyl alcohol) film, the moisture adsorption (100% RH) and water vapor transmission coefficient were improved by 17.91% and 15.18%, respectively. Antimicrobial circle experiments showed that the addition of vanillin improved the antimicrobial properties of the blended films. In summary, the addition of vanillin improves the water resistance, mechanical properties and antimicrobial properties of the polyvinyl alcohol/ κ-carrageenan blended films, overcoming the drawbacks of poor water resistance of polyvinyl alcohol films and expanding their applications.
polyvinyl alcohol; κ-carrageenan; vanillin; cross-linking; water resistance
TB484
A
1001-3563(2023)23-0036-08
10.19554/j.cnki.1001-3563.2023.23.005
2023-09-27
齐鲁工业大学(山东省科学院)国际合作研究专项基金(QLUTGJHZ2018028)
责任编辑:曾钰婵

