核心素养视域下观念建构为本的概念教学
车铭妍









摘要: 化学键的教学要实现概念向能力素养的转化,发展学生对物质构成的认知,需基于化学学科观念的建构,建立概念模型。利用化学键发展史与“太空天梯”材料的寻找两条情景线,认识化学键在物质构成、能量变化、化学反应本质中的作用,建构微粒观与元素观、化学价值观、“结构决定性质”的思想观念,打造素养统领、观念统摄、情景统一、认知发展合理进阶的课堂,达成能力与素养的培育目标。
关键词: 核心素养; 观念建构; 化学键; 概念教学; 认知发展
文章编号: 1005-6629(2023)09-0046-05 中图分类号: G633.8 文献标识码: B
1 研究背景
化学键的概念和原理对于元素化合物、化学反应原理及有机化学的教学起到起承转合的作用,可以有效促进学生形成“结构决定性质”的思想观念,是理解化学反应实质的根本,也是培养“宏观辨识与微观探析”“证据推理与模型认知”核心素养的重要知识生长点。
在课堂教学中,一般教师轻化学键而重离子键和共价键,没有充分发挥化学键概念、原理的教育功能。本文基于鲁科版教材必修第二册第二章第一节“化学键与物质构成”的第1课时“化学键”的教学设计,以化学键的发展史为情景,揭示其概念意义;在第2课时再进行共价键和离子键的教学,更符合建构主义思想和学生认知发展规律,着重从化学键的视角认识物质结构和化学反应实质,建立起解释与分析物质的性质的意识[1]。
2 学情分析
高中学生已经建立起了初步的微粒观:了解原子的基本结构,知道原子是由带正电的原子核和带负电的核外电子构成的,了解微粒之间存在一定的作用力,了解保持物质化学性质的最小微粒是分子,化学反应中的最小微粒为原子。但这种微粒观只是对微粒自身、微粒和物质构成、微粒和化学变化的认识,尚未建立起微粒之间的作用和变化、微粒的结构与化学性质的关联等认识。
同时,学生也形成了一定的化学变化观:对化学反应中的物质变化有一定的认识,认识到化学反应的本质是分子分解成原子、原子重新组合成新的分子的过程,对燃烧等放热反应也有较深的印象。
在鲁科版高中化学必修第二册第一章已经学习了“原子结构与元素周期律”,对原子的构成有了更深入的了解,已经建立起了“原子核外电子排布对元素性质会产生影响”的基本认知,形成了“结构决定性质”观念的初步意识,但仍然是停留在性质的宏观认知层面,对于原子之间如何结合成新分子、离子之间如何形成新物质尚未完全了解。
3 教学思路
3.1 教学框架
化学键的概念和原理抽象且不易理解,高中教学应立足于微观粒子之间的作用,进一步建构微粒观、“结构决定性质”的观念(后面简称“构性观”)、变化观、化学价值观等学科核心观念。从物质构成到反应实质以及能量变化逐步揭示化学键的概念本质与意义,建立观点、证据、结论之间的合理逻辑。整节课的教学设计围绕以下兩种情境展开。
情境1:通过化学键发展史,模拟科学探究发展过程以认识化学键。从“分子间作用力”到相邻原子、离子之间的作用,从“亲和力”到“库仑力”,不断挖掘微粒之间的作用力的过程中,形成概念模型,逐步构建微粒观、元素观和构性观(见图1)。
情境2:嫦娥五号登月。从宏观应用认识物质,将宏观情景转化为微观探索欲。以“嫦娥五号”探月为背景,探求“太空天梯”材料,从“力”的角度寻找材料,必然从“力”的方向认识物质,引入化学键概念。利用长征五号的发动机燃料不同,构建化学键与能量模型。揭示神秘材料“碳纳米管”,导入碳的同素异形体,构建化学键与物质构成关系模型。因为化学键的断裂和形成带来了能量变化,使得“长征五号”不同部位的发动机燃料选择有了数据依据,揭示化学反应的三个特征:物质变化、能量变化与化学键变化,形成化学反应的微观角度模型,提升学生对化学反应的认知,推动变化观的建构。
两条情境线交织,形成了宏观认知与理论发展的交替生长线。素养的发展与观念的建构相辅相成,基于宏观情景,探讨微观本质,转化旧思维,形成新思想(见图2)。
3.2 教学基本流程
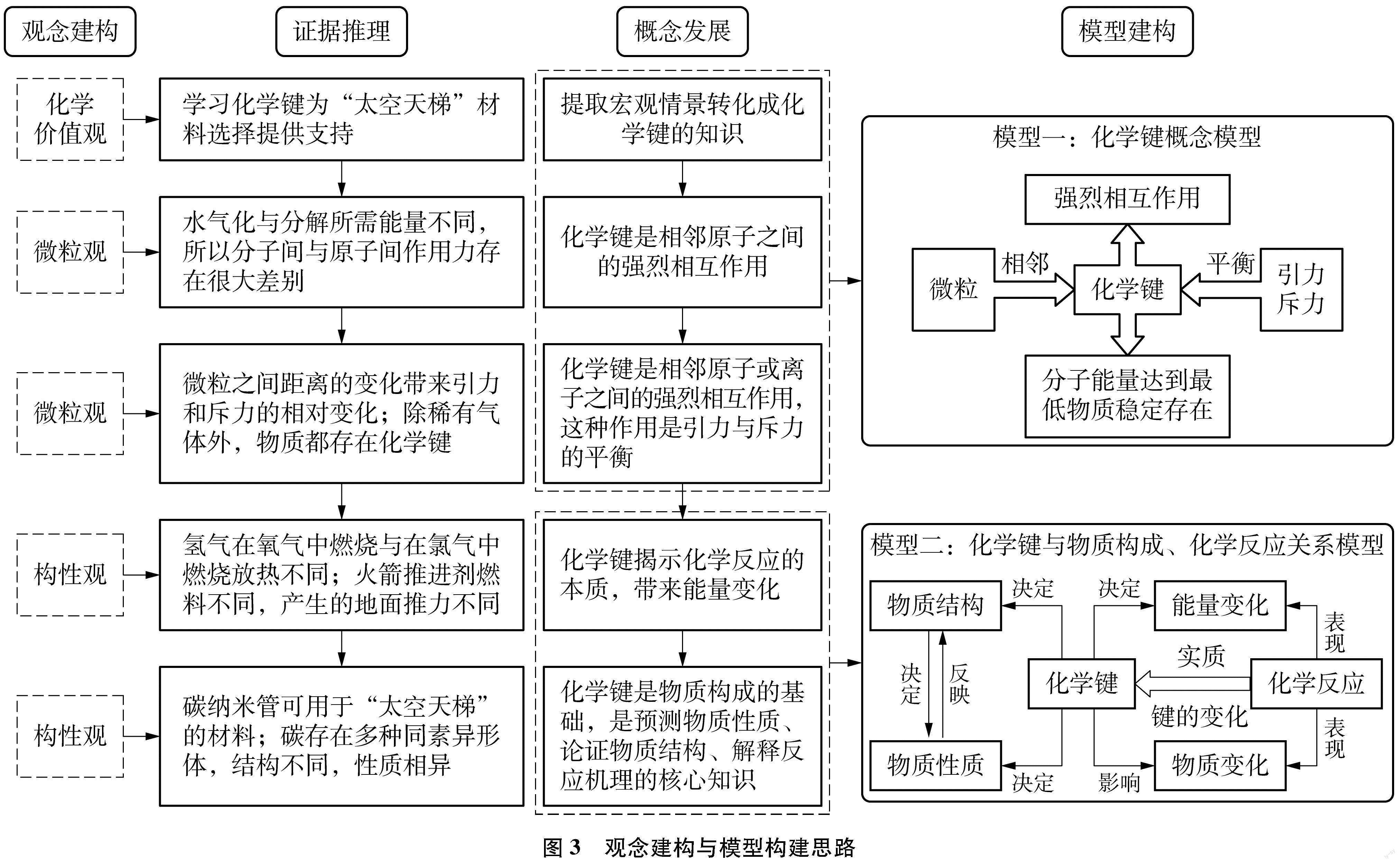
教学流程见图3。
4 化学键的概念教学设计
4.1 建构化学键概念模型
[教师]嫦娥五号顺利登月,长征五号功不可没。是否存在建立“太空天梯”的材料,让普通人也有机会登月?选择“太空天梯”材料的关键是什么?
[学生]选择材料的关键——微粒之间作用力要强!
[质疑]播放视频:零下20℃的肥皂泡,产生漂亮的雪花。问:为什么肥皂泡不散落?
[学生]水分子间存在作用力。
[深度质疑]加热至100℃时,水会沸腾变成水蒸气。加热至2200℃以上时,水会分解(见图4)。
(1) 在这两个变化过程中,外界提供的能量的作用是什么?使水分解和使水沸腾温度不同说明什么?
(2) 你对“微粒之间是否存在着相互作用”这一问题有了哪些新的认识?
[学生]把水气化,需外界提供44kJ·mol-1的能量,用于克服水分子间的作用力,把水分解,需外界提供918kJ·mol-1的能量,用于克服水分子内氢原子和氧原子之间的作用力。水分子内部氢原子与氧原子之间的作用力远大于水分子间作用力,原子间存在强烈的相互作用(见图5)。
[教师]水分子间与水分子内的氢氧原子之间作用力是否相同?你如何理解化学键?
[学生](1) 不直接相邻,作用力弱;直接相邻,作用力强。
(2) 化学键是直接相邻原子之间强烈的相互作用(见图6)。
[教师](1) 十七、十八世纪的一些自然科学家把牛顿力学推广到化学领域,把化学元素能够互相结合的能力单纯看作引力。你同意他们的观点吗?
(2) 从原子结构的角度分析,HCl分子内H、 Cl之间存在哪些作用力?NaCl中Na+、 Cl-之间存在哪些作用力?你如何理解“化学键”与“作用力”的关系?
[学生]化学键是引力与斥力的平衡,不是单纯的引力。化学键广泛存在于分子内原子之间和相邻离子之间。
[教师]“直接相邻”与“强烈相互作用”是否存在关联呢?
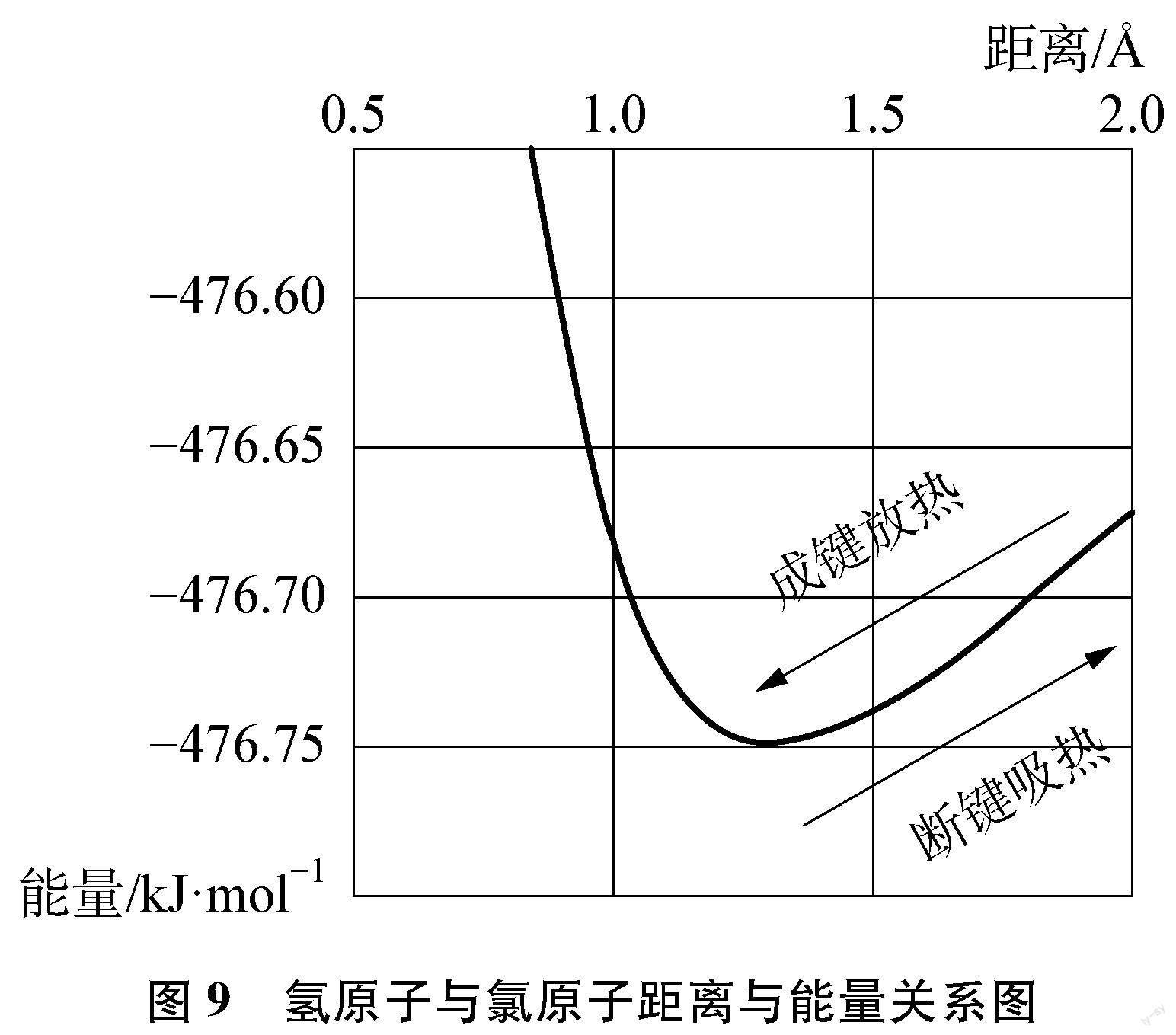
[提供信息]H、 Cl之间“距离与能量关系图”(见图7)。
[学生]能量越低越稳定,化学键越牢固。H、 Cl之间距离较远或者距离太近均能量高,不稳定。只有达到“直接相邻”能量最低,化学键稳定。化学键是直接相邻的微粒之间引力与斥力达到平衡时的强烈的相互作用。形成化学键,可以使分子稳定性增强(见图8)。
[教师]所有的物质中都存在化学键吗?
[提供信息]破坏两氦气相邻原子之间的作用力只需要0.167kJ·mol-1的能量[3],遠小于断裂化学键所需能量100~600kJ·mol-1的能量。
[学生]并非所有物质都存在化学键,稀有气体相邻原子间不存在化学键。
[小结]化学键概念模型:化学键是直接相邻的微粒之间当引力与斥力达到平衡时产生的作用力。化学键的存在使分子能量降低,是构成物质、使物质稳定存在的本质原因。
4.2 建构化学键与化学反应关系模型
[教师]请描述H2在O2中燃烧和H2在Cl2中燃烧的现象,说出两个化学方程式中化学键的变化。
[学生]不同化学反应中化学键的变化不同。
[教师](1) 室温下,1mol H2在O2中完全燃烧生成液态水放出256kJ能量,1mol H2在Cl2中完全燃烧生成HCl放出185kJ能量。为什么不同的反应,释放的能量不同?
(2) 化学键的断裂和形成对化学反应的能量变化有什么影响?
[提供信息]展示H、 Cl之间“距离与能量关系图”(见图9)。
[学生](1) 当两原子由稳定状态逐渐远离,能量升高,说明断开化学键需要吸收能量;两原子从较远向稳定状态变化,能量逐渐降低,说明形成化学键要释放能量。
(2) 化学变化的特征之一是生成新的物质,在反应过程中必然伴随着旧化学键的断裂和新化学键的形成。当断裂旧化学键吸收能量与形成新化学键释放能量不相等时,化学反应就表现为对外吸收或释放能量。这就是化学反应的实质(见图10)。
[提供信息]长征五号芯级发动机采用地面推力50吨级的液氢—液氧燃料;助推器采用地面推力为120吨级的液氧—煤油发动机。为什么不同的燃料燃烧,放出的能量不同,对地面的推力不同。
[学生]有效利用化学键的断裂与形成带来的能量变化,给航空航天带来燃料的多种选择。化学键的研究对人类探索能源提供了结构上的依据。
4.3 探索化学键研究意义
[提供信息](1) 视频——碳纳米管可用作“太空天梯”登月的材料,目前清华大学对碳纳米管的科研与生产技术已经居于世界前列,相关成果发表于2020年8月28日《Science》。
(2) 金刚石坚硬、碳60有优良的光电磁性能、石墨滑润且有导电性、石墨烯和碳纳米管强韧。碳所形成的多种同素异形体,结构与性质均不相同。
[教师](1) 视频中,碳纳米管为什么可以做“太空天梯”?它的元素组成和化学键有什么特殊性?
(2) 碳的多种同素异形体化学性质不同的根本原因是什么?
(3) 经过本节课的学习,请你谈一谈,你对化学键有了哪些新的认识?
[学生](1) 同样的元素通过化学键形成了不同的物质且性质各异,说明化学键是物质结构不同的根本原因,物质结构决定了物质性质。
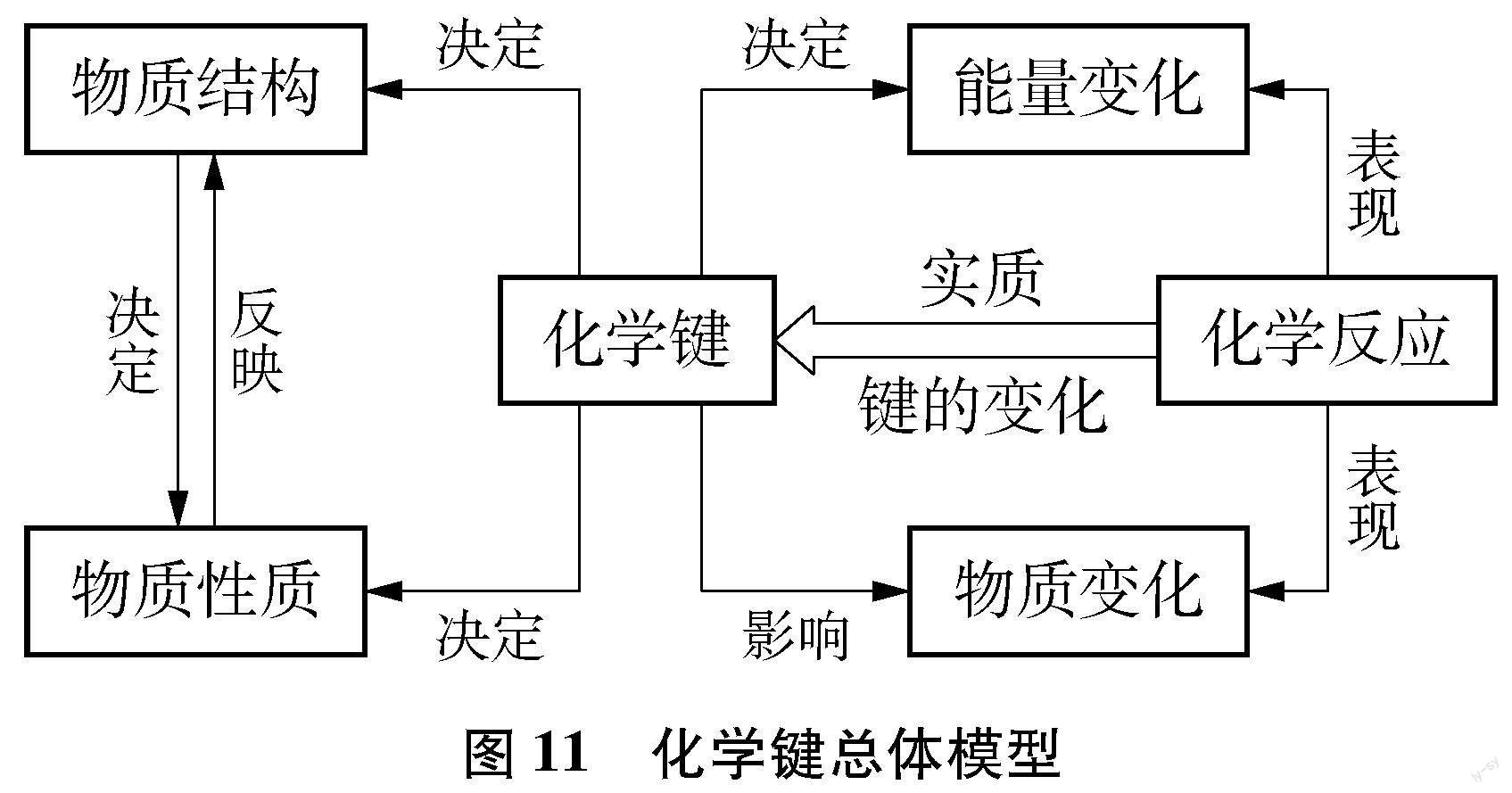
(2) 化学键决定了物质构成的多样性,决定了化学反应的能量变化,是化学反应的本质(见图11)。
[提供信息](1) 化学键理论的发展历程(见图12)。
(2) 2012年北京大学成功实现了化学键的选择性操控。对化学键的操控,可以对单电子分子设备、纳米机电系统、化学合成和药物输送产生很大的影响。
[教师](1) 你对化学键的发展史有哪些感受?对北京大学选择性操控化学键有怎样的认识?
(2) 中国科学院白春礼院士说,化学的发展支撑了人类社会的可持续发展。通过本节课的学习,你对这句话有了怎样的感悟?
[学生](1) 对化学键的选择性操控,让我们认识到化学键不是虚拟的,而是真实存在于物质内部,影响着物质构成。
(2) 我们用一节课了解的科学,是无数科学家百年薪火相传的成果。化学键的发展史,就是人类对物质结构认知的发展史。我们要遵循事物发展的一般规律,尊重科学事实,继承并发扬科学家们的探索精神。
(3) 通过化学键的学习,认识化学对人类社会发展的重大贡献,学好化学、用好化学,发展科学事业,创造更美好的生活!
5 教学反思
从学习的视角出发,化学基本观念是学生对化学学习进行深入反思和体验的结果,这种反思和体验包括对物质的组成、结构和变化规律等知识的概括性认识、对化学探究过程和方法的反思、对化学科学本质及其在社会发展中作用的认识和反思[5]。对于抽象概念的教学,更要立足观念建构,渗透学科素养。在化学键的教学中,不仅要教会学生领会概念本身的含义,还要在微粒观基础上发展构性观,揭示化学反应的本质,理解概念深层次的意义,认识化学键与物质结构、物质性质、能量变化、化学反应本质之间的关联。
参考文献:
[1]何彩霞. 在多重关联中探寻知识的意义——以高中《化学2》“化学键”单元教学为例[J]. 化学教学, 2014, (8): 46~49.
[2]廖正衡. 化学键理论发展的四个阶段[J]. 化学教育, 1986, (6): 54~57.
[3]夏泽吉. 关于范德华力本质的定量探索[J]. 川东学刊(自然科学版), 1997, (4): 84.
[4]王磊, 陈光巨. 普通高中教科书·化学必修第二册[M]. 济南: 山东科技出版社, 2019: 7.
[5]毕华林, 万延岚. 化学的魅力与化学教育的挑战[J]. 化学教学, 2015, (5): 4.

