2,4,6-三芳基吡啶(TAPs)的合成研究进展
曾 闽
(温州大学化学与材料工程学院,浙江 温州 325000)
由于热稳定性好及优良的π-堆积能力,2,4,6-三芳基吡啶作为制备荧光小分子[1]﹑聚合物[2]﹑超分子[3]以及用于离子检测的荧光传感器[4]的通用起始材料而备受关注。此外,得益于其对各种金属中心的优异配位能力,2,4,6-三芳基吡啶还可以用于先进催化剂的设计以及有机发光二极管(OLEDs)的制备[5],这使得其实际意义得到进一步增强。值得注意的是,2,4,6-三芳基吡啶不仅是有机合成化学中常见的活性中间体[6],还是医药化学中常用的抗癌剂[7]。本文着重介绍了2,4,6-三芳基吡啶(TAPs)近期的合成研究进展,根据氮源的不同,其合成方法大致可分为以下4 种:1)由乙酸铵合成2,4,6-三芳基吡啶;2)由苄胺合成2,4,6-三芳基吡啶;3)由乙酸肟酯合成2,4,6-三芳基吡啶;4)其他合成方法。
1 由乙酸铵合成2,4,6-三芳基吡啶
1906 年,前苏联化学家Aleksey Chichibabin通过醛与氨的热缩合制备了取代吡啶[8]。43 年之后,Frank 和Seven 对该反应进行了改良,通过添加乙酸铵,使得反应之后的产物组成相对简单[9]。在那之后,醛与烯醇化的酮在氨源存在下的缩合,便成为合成TAPs 最流行的方法之一。2007 年,Hervavi 课题组[10]报道了一种无溶剂条件下,杂多酸作为催化剂的2,4,6-三芳基吡啶的高效合成。在H14[NaP5W30O110]介导下,芳香醛﹑苯乙酮及其衍生物与乙酸铵经一步缩合得到产物。

图1 杂多酸催化合成2,4,6-三芳基吡啶(TAPs)Fig. 1 The synthesis of TAPs catalyzed by heteropolyacid.
2009 年,Ren 等人[11]开发了一种分子碘催化的芳香醛﹑苯乙酮﹑乙酸铵三组分的一锅反应,在无溶剂情况下,以中等产率获得了2,4,6-三芳基吡啶。该方法有效避免了使用金属﹑有机溶剂及有毒试剂,操作简单。
2015 年,Wang 等人[12]以苯乙酮﹑芳香醛和乙酸铵为氨源,在130℃下实现了无需溶剂和催化剂的三组分一锅法制备2,4,6,-三芳基吡啶。在该方案中,富电子和缺电子的芳香醛都能顺利得到相应的产物,并且后者所需的反应时间相对较短。
为了缩短反应时间,Zarnegar 等人[13]将纳米晶镁铝尖晶石作为催化剂,与超声波辐射相结合,以乙酸为反应溶剂,在90℃下成功地在70min 之内合成了2,4,6-三芳基吡啶。这是多相催化剂和超声辐射协同作用的结果。前者作为Lewis 酸,可促进反应过程中的每一步,后者则产生局部热点,并通过空化现象促进向表面的传质。
2020 年,Li 等人[14]报道了在DBU/乙酸催化体系中,通过吡啶盐﹑β-硝基苯乙烯与乙酸铵的多组分反应,制备了2,4,6-三芳基吡啶。他们指出,三芳基吡啶的组装是通过向β-硝基苯乙烯中加入氨开始的,随后历经数次C−C 和C−N 键的形成,产生关键中间体二硝基全氢吡啶。
Lewis 酸﹑Brønsted 酸和Brønsted 碱,是催化合成2,4,6-三芳基吡啶常用的催化剂。相较于传统催化体系,固体负载型催化剂拥有制备简单﹑后处理操作简便﹑可重复使用等明显优势,因此在该领域中,固体催化剂成为最受欢迎的选择之一。Tabrizian 及其同事[15]用纳米二氧化钛负载磺酸(n-TSA)并将其用作合成TAP 的催化剂。以2,4,6-三苯基吡啶的合成为例,该催化剂可以在多达6 个连续反应中重复使用,同时保持了高催化活性(90%~93%产率)和相同的粒度(平均粒度为35~60 nm 的球形粉末)。后来,这种方法被用于制备新型的四配位硼发射体,以修饰可用于热激活延迟荧光OLED 的三齿螯合配体。
由于醛在储存过程中容易发生氧化,并且多官能化的醛一般依赖于特殊的合成手段来获得,因此近年来,科研工作者们尝试在齐齐巴宾反应合成2,4,6-三芳基吡啶时,使用其他试剂来代替醛。2017年,陈保华课题组[16]使用铜催化苯乙酮与甲苯衍生物的sp3C-H 键氧化偶联,实现了2,4,6-三芳基吡啶的制备。在该方案中,叔丁基过氧化氢作为原位生成醛的选择项氧化剂。除了4-硝基苯乙酮﹑3-乙酰基吡啶﹑2-甲基吡啶和2-甲基喹啉等少数典型底物,其他不同取代基的甲基芳烃和芳基甲酮均可适用于该方案。
苄基衍生物被认为是醛的另一类替代物。Mohammadi 采用氢氧化钠和等物质的量的γ 型二氧化锰作为催化剂,在微波辅助下实现了苯甲醇﹑苯乙酮﹑乙酸铵的无溶剂一锅缩合制备2,4,6-三芳基吡啶[17]。
2016 年,Adib 等人[18]首次报道了使用苄基卤化物作为醛的替代试剂,合成2,4,6-三芳基吡啶的方法。供电子或是吸电子取代的苄基卤化物,都可以通过该方法,以优秀产率获得相应的2,4,6-三芳基吡啶。美中不足的是,只有在高温条件下,苄基卤化物才能与乙酸铵相互作用转化为对应的醛或亚胺,进而参与之后的反应过程。
2019 年,Doan 等人[19]合成了一种新型铁有机骨架(VNU-22),并将其用作苯乙酮﹑乙酸铵以及苯乙酸之间级联合成2,4,6-三芳基吡啶的多相催化剂。实验结果显示,VNU-22 在级联反应中的活性比众多的均相和多相催化剂更高。同时,将VNU-22 催化剂重复多次用于合成三芳基吡啶,其催化活性和形态不会发生明显劣化。该方法为2,4,6-三芳基吡啶的合成提供了新思路。
2 由苄胺合成2,4,6-三芳基吡啶
如上所述,苄基衍生物可在齐齐巴宾反应合成吡啶中充当醛的替代试剂。如果苄基衍生物是苄胺,则不需要引入任何氮源,这在某些情况下可能是合成上的优点。2013 年,Huang 等人[20]发展了一种铜催化芳香甲基胺的C−N 键裂解的策略,用于吡啶类化合物的组装。使用三氟甲磺酸铜作为催化剂,在有氧氛围下,苯乙酮及其衍生物与苄胺在100℃下反应20h,即得到2,4,6-三芳基吡啶。当使用2-氨甲基吡啶作为底物时,反应更倾向于酮的α-烷基化,此时得到的产物为β-(2-吡啶基)酮。
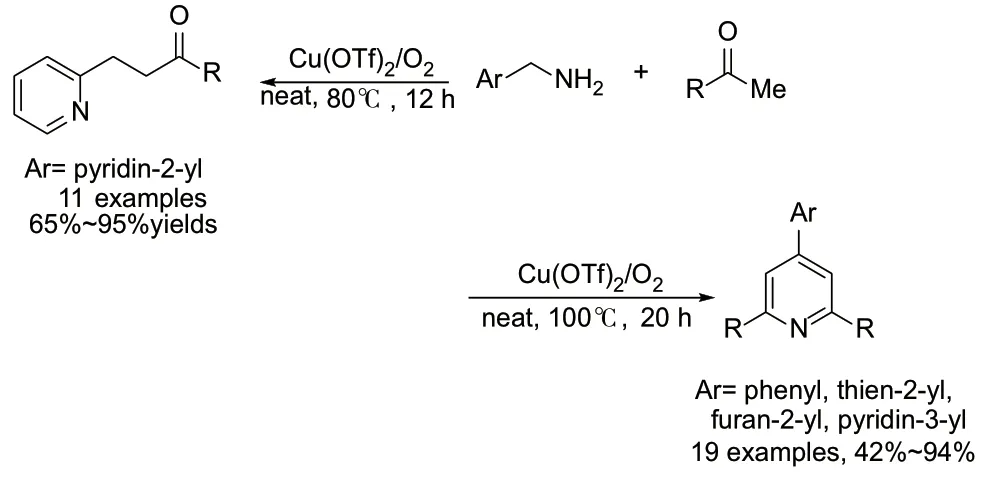
图2 三氟甲磺酸铜催化苄胺与苯乙酮合成2,4,6-三芳基吡啶Fig. 2 Cu(OTf)2 catalyzed synthesis of TAPs from benzylamine and acetophenone
2016 年,Zhang 等人[21]报道了通过三氟甲磺酸催化苯乙酮和苄胺的无溶剂缩合,简单高效地合成了2,4,6-三芳基吡啶。该反应开始于空气条件下,三氟甲磺酸催化苄胺的氧化C−N 键裂解,产生相应的醛和三氟甲磺酸铵,后者随着反应的进行被分解为游离的氨和三氟甲磺酸。尽管反应条件相对苛刻(120℃,12h),但是该方法能高产率地由各种芳基和杂芳基酮与胺合成2,4,6-三芳基吡啶。
类似地,Lin 等人[22]于2018 年报道了三(五氟苯基)硼烷催化苄胺和苯乙酮的氧化脱氨/环化级联反应,在无金属及无溶剂情况下得到了2,4,6-三芳基吡啶。
最近,Gopalaiah 及其同事[23]发展了铁催化芳基乙炔与苄胺的氧化级联环化合成2,4,6-三芳基吡啶。该反应无法在极性有机溶剂如DMSO 或DMF中进行,此外,氧气是该反应不可或缺的存在。在缺少分子氧参与时,仅能获得微量产物,替换为空气氛围也会导致反应产率有所降低。
3 由乙酸肟酯合成2,4,6-三芳基吡啶
另一种避免在齐齐巴宾反应合成吡啶中引入额外氮源的方法,是将氮原子结合到苯乙酮上,比如采用苯乙酮肟乙酸酯。2011 年,Ren 等人[24]首次报道了铜催化苯乙酮肟乙酸酯和醛的偶联反应,高效合成了2,4,6-三芳基吡啶。该反应使用溴化亚酮作为催化剂,亚硫酸氢钠用于调节反应的pH,使得苯乙酮肟乙酸酯的水解被抑制,120℃下在二甲基亚砜中反应2.5h,能以中等至优秀的产率得到产物。
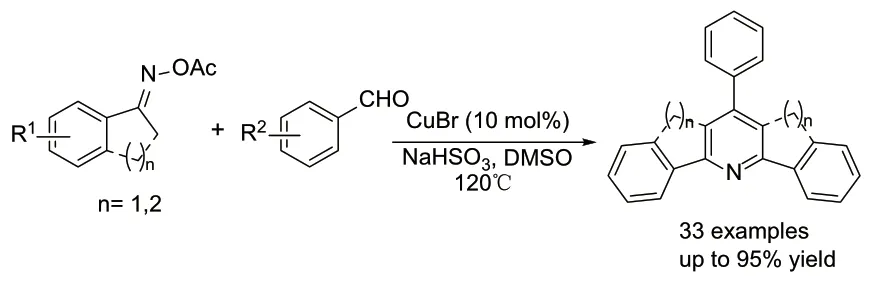
图3 铜催化苯乙酮肟乙酸酯和醛偶联合成2,4,6-三芳基吡啶Fig. 3 Copper-Catalyzed Coupling of Oxime Acetates with Aldehydes to access TAPs.
2018 年,Gao 等人[25]开发了碘诱导的芳基酮肟乙酸酯与3-甲酰基吲哚的[3+2+1]环化反应,用于合成2 号位吲哚连接的2,4,6-三芳基吡啶化合物。该反应的优势是起始原料易于制备,反应操作简单方便,兼具良好的官能团耐受性和高度的区域选择性。
类似于齐齐巴宾反应合成三芳基吡啶,近期有研究者用苄基衍生物替代醛,与乙酸肟酯发生反应。2016 年,Fu 等人[26]报道了一种通过铜催化的乙酸肟酯与甲基芳烃的sp3C−H 键偶联,合成2,4,6-三芳基吡啶的新方案。众多富电子和缺电子的甲苯衍生物都可以顺利参与该反应,不过,可能是电子效应对该反应的影响较大,强吸电子(如硝基)取代的芳烃底物不能得到相应的偶联产物。
2019 年,Thu N. M. Le 等人[27]首次报道了由苯乙酸和苯乙酮肟乙酸酯经氧化环化合成2,4,6-三苯基吡啶。通过凝胶煅烧制备了锶掺杂钴酸镧钙钛矿,并将其作为多相催化剂,用于苯乙酸和苯乙酮肟乙酸酯的氧化环化反应。加热条件下,使用二叔丁基过氧化物作为氧化剂时,仅需要极低负载量的催化剂,反应可以在氯苯中平稳进行,能以中等至优良的产率得到2,4,6-三苯基吡啶。
2020 年,Jiang 等人[28]报道了三氟甲磺酸铁催化乙酸肟酯和硝酮的亲核加成/氧化环化反应,构建了一系列2,4,6-三芳基吡啶。值得一提的是,硝酮在该反应中被当作一种新型的C1 合成单元。
4 其他方法合成2,4,6-三芳基吡啶
2008 年,Mehdi 等人[29]报道了在微波辐射条件下,查尔酮与盐酸胍无溶剂合成2,4,6-三芳基吡啶。作者筛选了多种尿素衍生物,其中盐酸胍可以提供最高的产率。尽管该方法高效快捷,但180℃的反应温度,在一定程度上限制了该反应更深层次的应用。
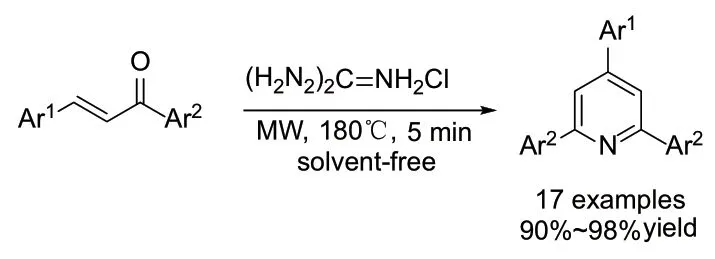
图4 微波辅助查尔酮和盐酸胍合成2,4,6-三芳基吡啶Fig. 4 Microwave-assisted synthesis of TAPs from Chalcone and guanidine hydrochloride.
2016 年,Xiang 等人[30]使用分子碘作为串联催化剂,实现了从天然氨基酸出发,化学选择性合成2,4,6-三芳基吡啶。机理研究表明,该反应涉及氨基酸的脱羧-脱氨基过程。
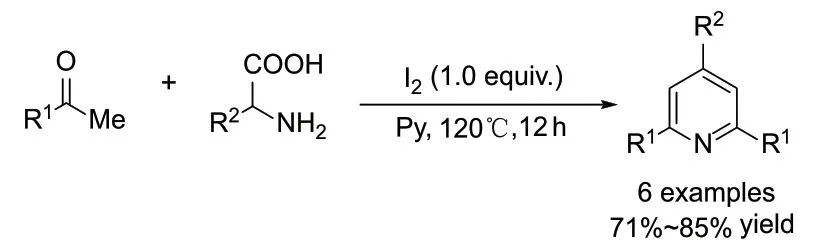
图5 碘诱导天然氨基酸选择性合成2,4,6-三芳基吡啶Fig. 5 Iodine induces the selective synthesis of TAPs fromNatural Amino Acids.
2018 年,Zhang 等人[31]通过碱促进的查尔酮与烯胺酮的级联Michael 加成/芳构化反应,在无过渡金属条件下,温和高效地获得了2,4,6-三芳基吡啶。查尔酮中苯环取代基的空间位阻对反应的影响显著,相比苯环对位取代,苯环间位取代的查尔酮底物能够以更高的产率得到相应的产物。
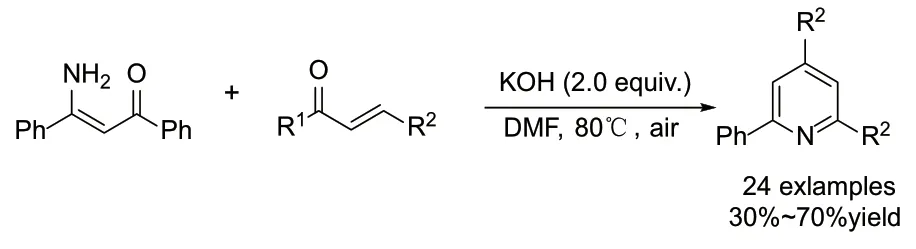
图6 碱促进查尔酮与烯酮胺级联合成2,4,6-三芳基吡啶Fig. 6 Base-promoted cascade synthesis TAPs between Enaminones and Chalcones.
2020 年,Guin 等人[32]首次报道了DABCO 促进的乙烯基/二烯基取代对醌甲基化合物,与环状磺酰亚胺1,6-加成消除-6π-氮-电环化-芳构化反应,能以良好至优秀的产率,合成各种对称及非对称﹑具有空间位阻酚部分的2,4,6-三芳基吡啶。
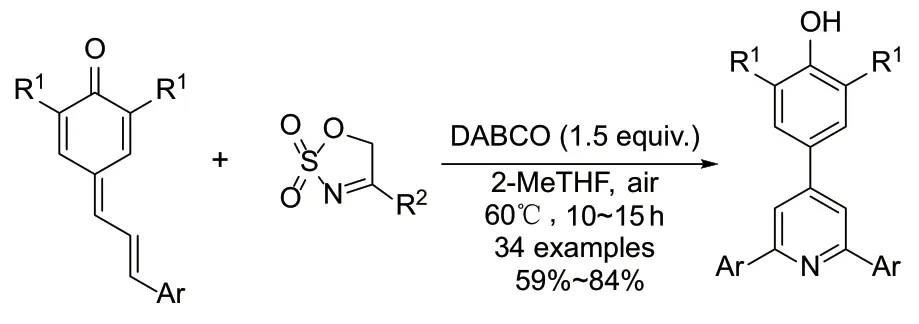
图7 DABCO 介导对醌甲基化合物和环状磺酰亚胺合成2,4,6-三芳基吡啶Fig. 7 DABCO-mediated TAPs synthesis from p-quinone methides and cyclic sulfamidate imines.
之后,该课题组还报道了乙酸铵介导的苯乙酮﹑醛和环状磺酰亚胺的多米诺合成含羟基取代的非对称2,4,6-三芳基吡啶[33]。该方法无需加入金属﹑氧化剂及溶剂。这种中性条件足够温和,一系列官能团都可以耐受,从而为2,4,6-三芳基取代吡啶的合成开辟了一条便捷道路。
5 总结与展望
综上所述,研究者们已经掌握了多种方法来制备2,4,6-三芳基吡啶。不过,该领域所面临的挑战仍旧不容小觑。新方法尤其需要解决以下问题:1)在非对称2,4,6-三芳基吡啶的合成方面,需要开发具有高度区域选择性的策略;2)连有金属锚定基团(如羟基﹑氨基﹑羧基等)的 2,4,6-三芳基吡啶的合成方法,还有待进一步探索;3)基于绿色化学的发展理念,探索温和高效的催化体系,从而降低对环境的负面影响。

