双石清热合剂指纹图研究及5种成分含量测定
宋奇,王隆隆,杨忠杰,陈恒文,刘菊,黄霞,于晓涛*(.漯河市中心医院,河南 漯河 600;.中国中医科学院广安门医院,北京 00000;.郑州市中医院,郑州 50000;.河南省食品药品检验所,郑州 50000)
双石清热合剂(SQM)是以经典名方“银翘散”为基础,在长期临床应用中形成的临床经验方,全方由金银花、黄芩、知母等14 味中药组成。本方中金银花清热解毒、疏散风热,为君药,黄芩、知母清热燥湿、泻火解毒、滋阴润燥,为臣药,佐以栀子、大青叶等清泻三焦火热、凉血解毒,共奏清热解毒之功。常用于肺胃实热、口舌生疮、牙龈肿痛及上呼吸道感染等症。目前,双石清热合剂的质量控制标准比较简单,仅包含《中国药典》2020年版合剂项下的鉴别项和检查项,不能反映制剂的整体概貌及进行有效的质量控制。
中药制剂发展的难点在于中药饮片的来源及批次不同对复方制剂中物质基础影响较大,不利于质量控制[1-3]。指纹图谱从“整体”上全面反映中药饮片及制剂内在物质基础的特征,可作为质量控制研究的有效方法[4]。化学模式识别能够对指纹图谱信息进行数字化识别、处理和评估,已广泛应用于中药饮片及制剂的质量控制研究[5-8]。
本研究采用高效液相色谱法(HPLC)建立12 批双石清热合剂的指纹图谱,通过相似度评价,结合聚类分析(CA)、主成分分析(PCA)及正交偏最小二乘法-判别分析(OPLS-DA)法筛选批次间差异贡献较大的主要成分基础,同时测定5 种成分的含量,从定性与定量两方面,为双石清热合剂的质量控制研究提供参考[9]。
1 仪器与试药
1.1 仪器
高效液相色谱仪(日本岛津LC-20AD 型,包括二元泵,全波长紫外检测器,柱温箱,自动进样器,工作站);SB25-12D 超声波清洗机(宁波新芝生物科技有限公司);AUW-120D 型十万分之一电子天平(日本Shimadzu 公司);Milli-Q 超纯水机(美国Millipore 公司);5810R 高速离心机(美国Eppendorf 公司)。
1.2 试药
SQM 样品(S1 ~S12,医院自制,批号分别为20191205、20200312、20200506、20200710、20200925、20201122、20201230、20210111、20210115、20210306、20210507、20210625)。绿原酸(批号:110753-201817,纯度:96.8%)、栀子苷(批号:110749-201718,纯度:97.6%)、芒果苷(批号:111607-201704,纯度:98.1%)、黄芩苷(批号:110715-201821,纯度:95.4%)、牛蒡苷(批号:110819-201812,纯度:95.0%)、汉黄芩苷(批号:112002-201702,纯度:98.5%)、黄芩素(批号:111514-201706,纯度:98.9%)(对照品,中国食品药品检定研究院);乙腈、甲醇(色谱纯,美国Fisher 公司),甲酸(色谱纯,天津科密欧化学试剂有限公司),水为饮用水或超纯水。
2 方法
2.1 色谱条件
色谱柱为Agilent SB-C18(4.6 mm×250 mm,5 μm),以0.05%甲酸-水(A)-乙腈(B)为流动相进行梯度洗脱(0 ~17 min,7%B;17 ~28 min,7% ~13%B;28 ~32 min,13%B;32 ~37 min,13% ~17%B;37 ~42 min,17%B;42 ~48 min,17% ~23%B;48 ~63 min,23%B;63 ~75 min,23% ~48%B;75 ~95 min,48%B;95 ~96 min,48%~7%B;96 ~110 min,7%B);柱温40℃;进样量10 μL;流速1.0 mL·min-1;检测波长239 nm[10-11]。
2.2 溶液的制备
2.2.1 对照品溶液 精密取绿原酸、栀子苷、芒果苷、黄芩苷、牛蒡苷、汉黄芩苷及黄芩素对照品适量,加甲醇分别制成质量浓度为1.86、1.92、1.75、2.14、2.02、1.96、1.42 mg·mL-1的对照品储备液;精密取各储备液适量,混匀,制得含绿原酸、栀子苷、芒果苷、黄芩苷、汉黄芩苷、黄芩素分别为25.76、57.30、20.98、234.24、25.82、34.47、59.86 μg·mL-1的混合对照品溶液,密封保存。
2.2.2 供试品溶液制备 精密取 12 批SQM 各1 mL,加甲醇1 mL,超声10 min,混匀,13 000 r·min-1离心,取上清液为供试品溶液。
2.2.3 单味饮片供试品溶液制备 参照SQM 制备工艺(10 倍量水,浸泡40 min,煎煮3 次,每次100 min),制备金银花、黄芩、知母等14 味中药的单味饮片溶液,按“2.2.2”项下方法制备各单味饮片的供试品溶液。
2.3 方法学验证
2.3.1 精密度试验 取SQM(S1)供试品溶液,连续进样6 次,以黄芩苷为参照峰,结果各共有峰相对保留时间的RSD均≤1.0%,相对峰面积RSD均≤1.1%,表明仪器精密度良好。
2.3.2 重复性试验 取SQM(S1)样品,平行制备供试品溶液6 份,进样测定,以黄芩苷为参照峰,结果各共有峰相对保留时间的RSD均≤1.0%,相对峰面积RSD均≤1.9%,表明方法重复性良好。
2.3.3 稳定性试验 取SQM(S1)供试品适量,分别在0、3、9、24、48 h 进样测定,以黄芩苷为参照峰,结果各共有峰相对保留时间的RSD均≤0.9%,相对峰面积的RSD均≤1.5%,表明供试品在48 h 内稳定。
2.4 指纹图谱研究
按“2.2.2”项下方法制备12 批SQM 供试品(S1 ~S12),进样测定,记录各色谱图。
2.4.1 参照峰的选定 在12 批SQM 供试品色谱图中黄芩苷特征峰面积较大、分离度较高且保留时间适中,可作为参照峰。
2.4.2 相对保留时间和相对峰面积 计算12 批SQM 指纹图谱中各共有峰的相对保留时间和相对峰面积的RSD值。结果各共有峰保留时间的RSD均小于1.1%,表明12 批样品共有峰的出峰时间相对稳定;峰面积RSD相差较大,说明SQM 存在批次间差异。
如图3所示,漂烫温度与切片厚度之间交互作用显著,切片厚度和漂烫温度分别为4 mm和90 ℃时,标准化综合得分达到最大值。当切片厚度大于4 mm样品厚度越大,内部淀粉颗粒为糊化,使得产品破碎力增加,脆度降低。在一定漂烫温度和时间下,样品中引起褐变的为完全失活,有利于产品色泽的提高。
2.4.3 指纹图谱的建立及相似度评价 取S1 ~S12的SQM 样品建立指纹图谱,采用“中药色谱指纹图谱相似度评价系统(2012版)”计算相似度。结果,各SQM 谱图与对照图谱相似度均大于0.97,共标定22 个共有峰,占总峰面积的83.48%,可以代表色谱图概况。以黄芩苷为参照峰,12 批SQM 供试品各共有峰保留时间的RSD均小于1.2%,峰面积RSD在7.11%~59.16%,相差较大,说明SQM 批次间存在差异(见图1 及表1)。
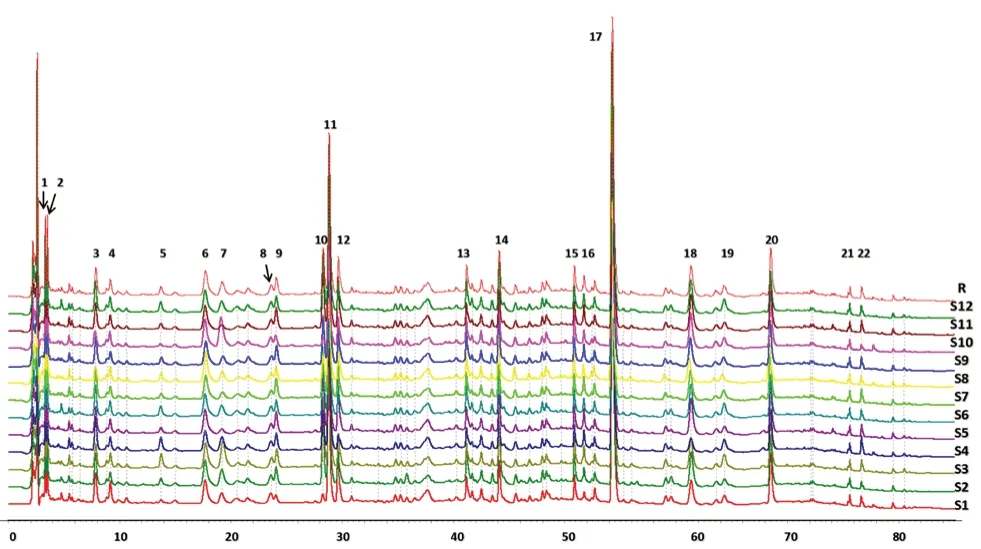
图1 HPLC 指纹图谱和对照指纹图谱(R)Fig 1 HPLC fingerprint and control fingerprint (R)

表1 相似度评价结果Tab 1 Similarity evaluation
2.4.4 共有峰化学成分指认 取混合对照品液、SQM 供试品(S1)溶液及单味饮片供试品溶液、进样分析,结果见图2。通过混合对照品、SQM供试品(S1)及单味饮片色谱比较共指认了20 个共有峰,分别为峰8、峰11(栀子苷)归属于栀子,峰13 归属于玄参,峰18(牛蒡苷)归属于牛蒡子,峰7、峰12(芒果苷)归属于知母,峰17(黄芩苷)、峰19、峰20(汉黄芩苷)、峰21(黄芩素)归属于黄芩,峰5、峰10 归属于龙胆草,峰2 ~3、峰14 归属于连翘,峰4、峰6(绿原酸)、峰9、峰15 归属于金银花,其中峰1 在玄参、大青叶、地黄及地丁中均有出现。
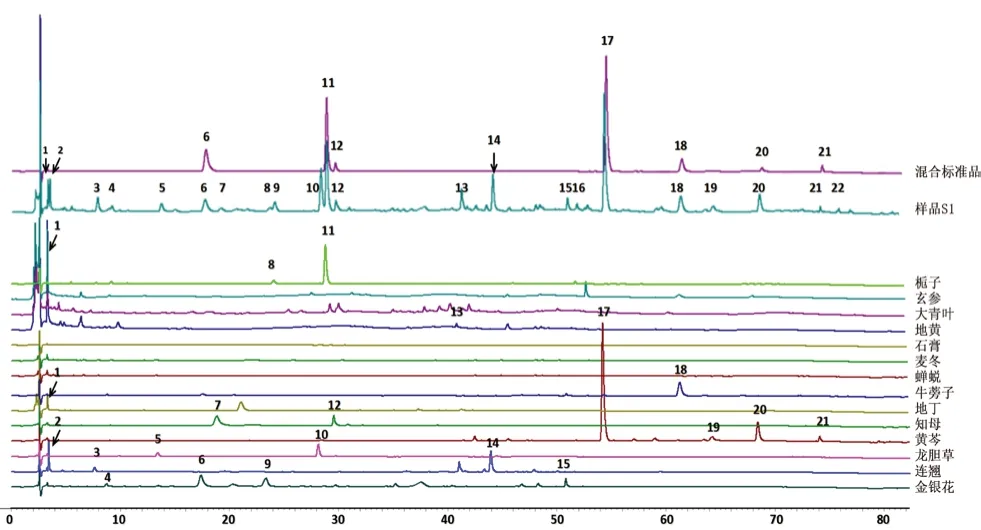
图2 SQM 共有峰化学成分指认及归属HPLC 图Fig 2 HPLC of common peak chemical composition identification and attribution for SQM
2.5 化学模式识别
2.5.1 CA 采用z-score 标准化法将12 批SQM供试品22 个共有峰的峰面积进行数据处理,通过SPSS 20.0 软件进行聚类分析(见图3)。聚类结果表明,在欧氏平方距离为10 时,可将12 批SQM分为两类,其中S3、S6、S7、S9、S12聚合为一类,其余样品为一类。说明批次间SQM 存在差异,这可能与饮片的产地、厂家、批次等差异有关,提示应保持SQM 饮片来源的均一性和稳定性。
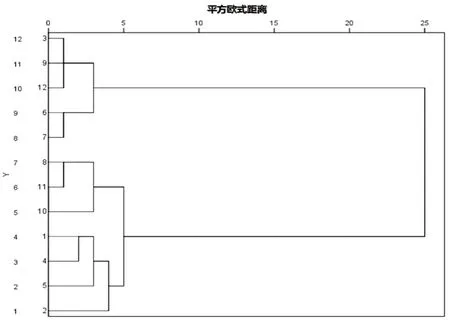
图3 12 批双石清热合剂聚类分析图Fig 3 Cluster analysis of 12 batches of Shuangshi Qingre mixture
2.5.2 PCA 12 批SQM 共有峰峰面积z-score 标准化处理后的数据导入SPSS 20.0 和SIMCA 14.1软件,进行PCA[12]。以特征值>1 为提取标准,得到5 个主成分,累积方差贡献率86.7%,能概括色谱图绝大部分信息。由结果可知,12 批SQM 分为两类,S3、S6、S7、S9、S12 聚合为一类,其余样品为一类,与CA 结果一致(见图4)。
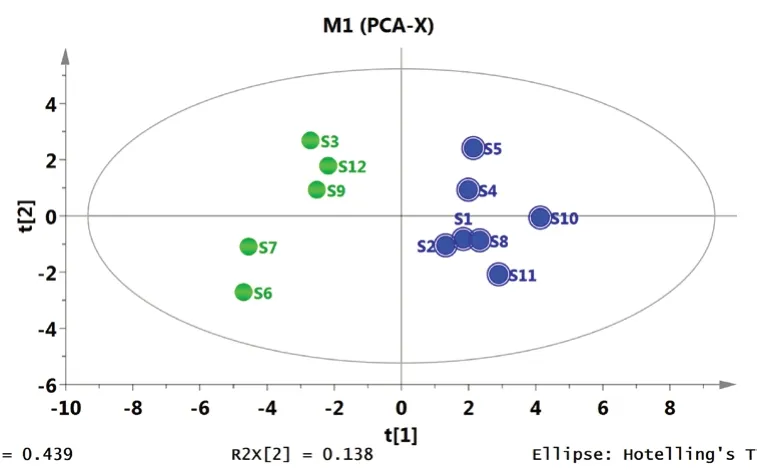
图4 主成分分析得分图Fig 4 Principal component analysis score chart
2.5.3 OPLS-DA 12 批SQM 的22 个共有峰峰面积标准化处理后的数据导入SIMCA 14.1 软件,以OPLS-DA 建模分析,得分矩阵图、载荷散点图和变量重要投影值图(见图5)[13-14]。结果,在置信区间(95%)内,12 批样品存在差异,可分为两类,样品S3、S6、S7、S9、S12 为一类,其余样品为一类。OPLS-DA 载荷散点图,每个点表示一个共有峰自变量,距离原点越远,对样品的差异性贡献越大。VIP 图可筛选出对样品差异贡献较大的成分,以VIP值>1.0 为参考,共提取出6 个特征峰,分别为峰17(黄芩苷)、峰11(栀子苷)、峰20(汉黄芩苷)、峰18(牛蒡苷)、峰14、峰6(绿原酸),说明这6种成分可能是12 批SQM 分类的差异性标志物。

图5 OPLS-DA 分析结果图Fig 5 OPLS-DA analysis
2.6 4 种指标成分含量测定
2.6.2 线性关系考察 精密量取“2.2.1”项下混合对照品溶液,用甲醇稀释成不同质量浓度的系列混合对照品溶液,进样测定,记录峰面积。以质量浓度为横坐标(X),以峰面积为纵坐标(Y),进行线性拟合,结果见表2。
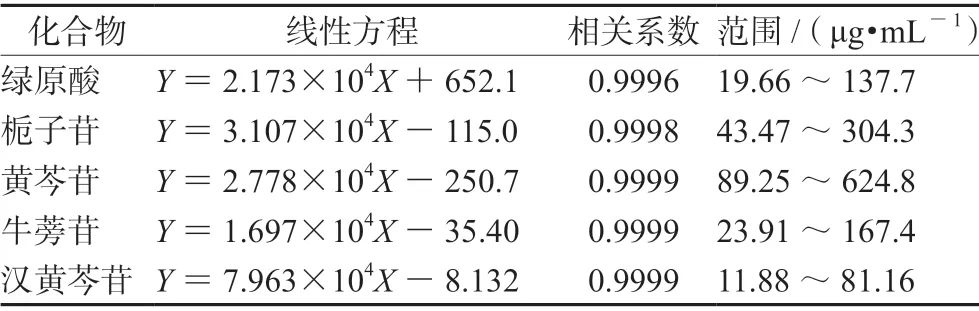
表2 各化学成分的回归方程、相关系数和线性范围Tab 2 Regression equation,correlation coefficient and linearity
2.6.3 精密度试验 取“2.2.1”项下混合对照品溶液,连续进样6 次,记录峰面积。结果绿原酸、栀子苷、黄芩苷、牛蒡苷、汉黄芩苷峰面积的RSD均小于1.5%,表明仪器精密度良好。
2.6.4 重复性试验 取供试品溶液(S1)适量,进样分析,记录峰面积。结果绿原酸、栀子苷、黄芩苷、牛蒡苷、汉黄芩苷峰面积RSD均小于1.6%,表明该方法重复性良好。
2.6.5 稳定性试验 取供试品溶液(S1)适量,室温下存放 0、6、12、24、48 h,进样分析,结果绿原酸、栀子苷、黄芩苷、牛蒡苷、汉黄芩苷峰面积的RSD均小于1.8%,表明供试品48 h 内稳定。
2.6.6 加样回收试验 取已知含量的样品(S11)适量,制备供试品溶液9 份。取“2.2.1”项下对照品储备液适量,配制与样品含量相同的混合对照品溶液,精密加入各成分质量分数的50%、100%、150%的混合对照品溶液,混匀,进样测定。结果绿原酸、栀子苷、黄芩苷、牛蒡苷、汉黄芩苷平均回收率在98.90%~101.42%,RSD均小于2.6%,表明方法准确度良好。
2.6.7 样品含量测定 取12 批SQM 供试品溶液,进样测定,结果绿原酸、栀子苷、黄芩苷、牛蒡苷、汉黄芩苷含量分别为0.075 ~0.096、0.126 ~0.159、0.496 ~0.586、0.075 ~0.093、0.071 ~0.098 mg·g-1(见表3)。由结果分析可知,12 批SQM 的化学成分种类和数目基本一致,但5 种指标成分含量存在一定差异,这可能与饮片的来源、产地及批次间差异有关。
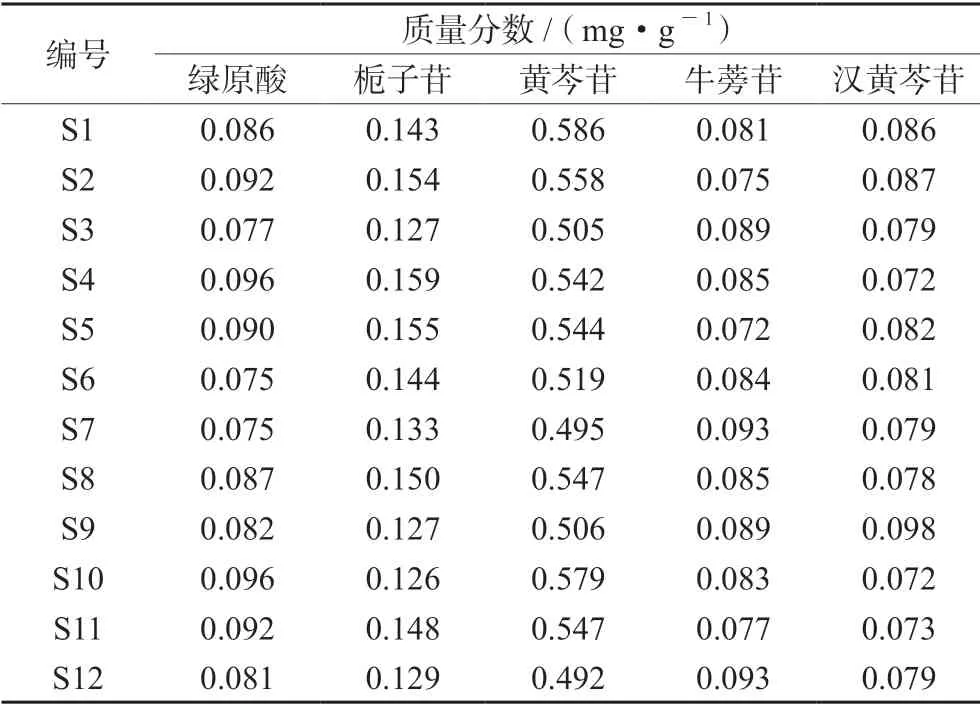
表3 双石清热合剂中5 种成分的含量Tab 3 Content of 5 ingredients in Shuangshi Qingre mixture
3 讨论
3.1 色谱方法考察
本研究考察了不同色谱柱(Agilent、YMC、Phenomenex、GL Sciences),不同流动相[乙腈-水、乙腈-(0.1%磷酸-水)、乙腈-(0.1%甲酸-水)、乙腈-(0.05%甲酸-水)],不同流量体积(0.8、1 mL·min-1),不同柱温(35、40℃)及不同检测波长(230、239、276 nm)对色谱图的影响,最终确定为本文色谱条件。
3.2 含量测定指标成分选定
本研究指认了20 个色谱峰的归属,确认了绿原酸、栀子苷、芒果苷、黄芩苷、牛蒡苷、汉黄芩苷及黄芩素7 种化学成分的特征峰;在OPLSDA 试验中,以VIP 值>1 为特征,筛选出6 个成分,峰17(黄芩苷)、峰11(栀子苷)、峰20(汉黄芩苷)、峰18(牛蒡苷)、峰14 及峰6(绿原酸)。结合文献资料当归中药理活性成分的综合研究,发现绿原酸在抗菌、抗炎等方面有较强药理活性[15],栀子苷有抗感染和免疫调节作用[16],黄芩苷及汉黄芩苷具有清热泻火、抗炎、抗病毒等药理活性[17],牛蒡苷具有抗炎、抗氧化、抗流行性感冒、抗菌等药理活性作用[18],均与本方治疗肺胃实热、口舌生疮、牙龈肿痛及上呼吸道感染等功效联系紧密,故选择作为差异性标志物进行含量测定,以期为SQM 质量标准研究提供参考。
——评析绿原《幸福》

