芩连胶囊中重金属及其胶囊壳中铬元素的含量测定及安全风险评估
周娟娟,吴 莉,冯有龙,张妤琳,吴嫣艳
江苏省食品药品监督检验研究院,南京 210019
芩连胶囊由黄芩、连翘、黄连、黄柏、赤芍、甘草等中药组成,具有清热解毒、消肿止痛等功效[1],临床上用于脏腑蕴热、头痛目赤、口鼻生疮、热痢腹痛、湿热带下、疮疖肿痛等[2]。目前对芩连胶囊的报道多为化学成分、临床药理作用等,鲜有对其安全性的研究,尤其对中成药及胶囊壳中的重金属含量及安全评估尚未见报道。
由于土壤污染及中药自身蓄积等方面的原因,目前中药材中重金属残留的现象普遍存在,主要涉及的有铅、镉、砷、汞、铜等,这不仅会对人体产生潜在的影响和威胁,还影响其药效发挥和用药安全[3,4]。铬是明胶空心胶囊壳中的重金属成分之一,过量摄入会造成中毒,及时准确地监测胶囊壳中铬的含量尤为重要[5]。因此,采用电感耦合等离子体质谱法(ICP-MS)对芩连胶囊中5 种重金属元素铅(Pb)、镉(Cd)、砷(As)、汞(Hg)、铜(Cu)同时进行定量检测,并利用原子吸收分光光度法(AAS)对其胶囊壳中的铬元素进行含量测定,且依据相关法规[6,7],对其进行安全风险评估,以期为芩连胶囊和其他中药制剂的安全评价和制订重金属及有害元素残留限度提供参考。
1 材 料
1.1 仪器
Agilent 7700 电感耦合等离子体质谱仪(美国安捷伦公司);PE 900Z 原子吸收仪(美国珀金埃尔默有限公司);Mars 6 微波消解仪(美国CEM 公司);BS21S 型电子天平(北京赛多利斯天平有限公司)。
1.2 标准物质与试剂
铅、镉、砷、汞、铜单元素对照品溶液(浓度均为1000 μg·mL-1,物质批号为GBW08619、GBW08612、GBW08611、GBW08617、GBW08615)均来自中国计量科学研究院;锗、铟、铋、铬单元素对照品溶液(浓度均为1000 μg·mL-1,物质批号为GSB04-1728-2004、GSB04-1731-2004、GSB04-1719-2004、GSB04-1723-2004),均购自国家有色金属及电子材料分析测试中心。硝酸为色谱纯,水为去离子水。
1.3 样品
芩连胶囊为国家评价性抽验样品,共计16 批次,样品信息见表1。
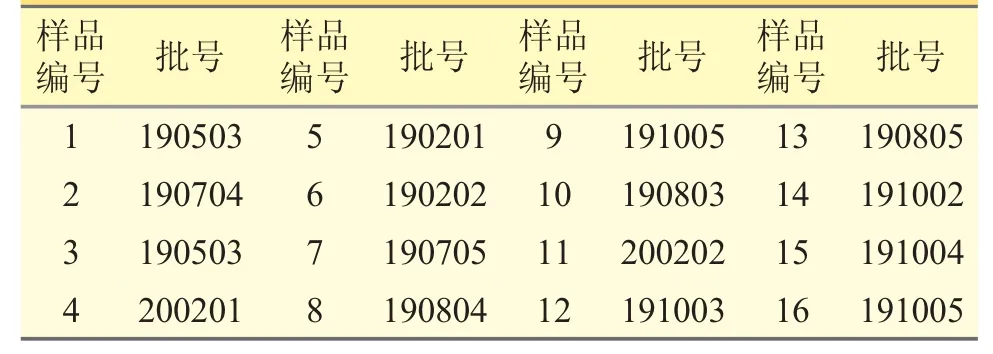
表1 样品信息
2 方法与结果
2.1 铅、镉、砷、汞、铜的测定方法
2.1.1 ICP-MS 仪器工作条件通过仪器设置的调谐程序,采用氦气碰撞反应池模式,用调谐液对仪器质量轴、分辨率、灵敏度、双电荷、氧化物进行优化,所得参数:射频功率1550 W;雾化气流速0.99 L·min-1;等离子气体流速15 L·min-1;辅助气流速1.0 L·min-1;蠕动泵转速0.1 r·s-1;等离子体模式为He 模式;重复次数3 s。
2.1.2 溶液的制备
2.1.2.1 对照品系列溶液及内标溶液:精密吸取Pb、Cd、As、Cu 各对照品溶液,用2%硝酸逐级稀释制成相应多元素质量浓度的混合对照品系列溶液。
精密吸取Hg 单元素对照品储备液适量,用2%硝酸逐级稀释制成Hg 对照品系列溶液。级别及浓度见表2。
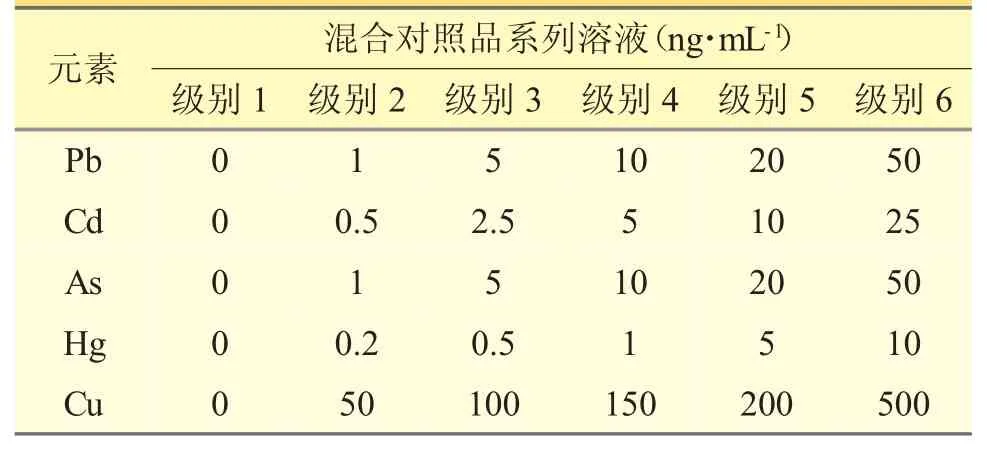
表2 混合对照品系列溶液浓度
2.1.2.2 供试品溶液:取本品0.5 g,精密称定,置聚四氟乙烯微波消解罐中,加硝酸5 mL,混匀,置微波消解仪中,开始样品消解。在0~5 min,由初始温度升至120 ℃,维持5 min;在5~8 min 由120 ℃升至150 ℃,维持2 min;在8~13 min 由150 ℃升至180 ℃;在13~23 min 由180 ℃升至190 ℃。消解完全后,冷却消解液至60 ℃以下,取出消解罐,在通风橱中放冷,将消解液转入50 mL 聚四氟乙烯量瓶中,用少量水洗涤消解罐数次,合并洗液于量瓶中,用水定容后摇匀,即得。
除不加样品外,同法制备空白溶液。
2.1.3 含量测定测定选取同位素为208Pb、114Cd、75As、202Hg、63Cu,其中208Pb 和202Hg 以209Bi 作为内标,114Cd以115In 作为内标,75As 和63Cu 以72Ge 作为内标。采用在线内标法用蠕动泵与样品混合后进入ICP-MS仪,按“2.1.1”项下仪器条件进行测定。
2.1.4 线性关系考察和检测限将“2.1.2.1”项下系列对照品溶液分别进样分析,以对照品浓度X 为横坐标,以对照品峰强与相应的内标元素峰强比值Y为纵坐标,绘制标准曲线,得各元素对照品的回归方程、相关系数以及检测限(见表3)。5 种元素线性关系均良好。
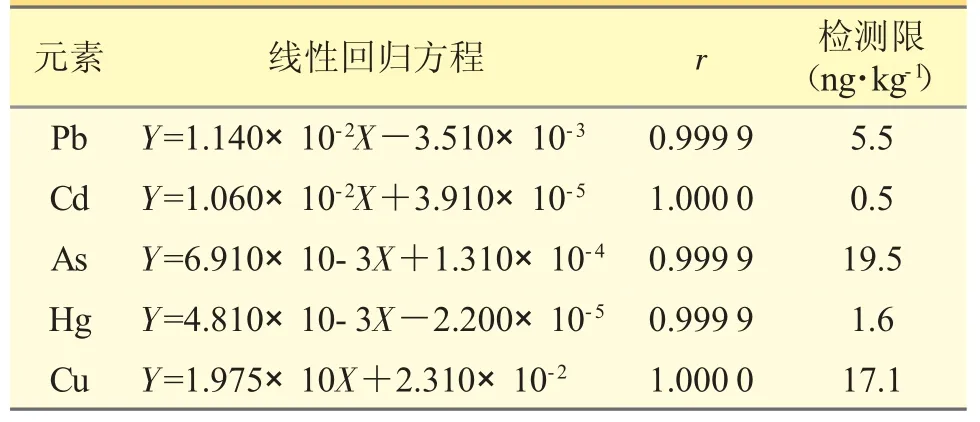
表3 铅、镉、砷、汞、铜各元素的线性关系结果
2.1.5 精密度试验取标准曲线范围内同一浓度的混合对照品溶液和汞对照品溶液,重复测定6次,记录测量值,结果Pb、Cd、As、Hg、Cu 测量值的RSD 分别为1.2%、0.6%、1.1%、0.8%、1.5%(n=6),表明仪器精密度良好。
2.1.6 重复性试验取批号为190704 的样品,按“2.1.2.2”项下方法制备6 份供试品溶液,按“2.1.1”仪器条件进样测定,结果铅、镉、砷、汞、铜的平均值(n=6)分别为1.8430、0.2984、0.5351、0.0070、1.8798 mg·kg-1,RSD 分别为1.6%、1.9%、1.9%、1.5%、0.9%。结果表明方法重复性良好。
2.1.7 稳定性试验取已知含量的供试品溶液(批号:190704)适量,分别放置0、2、4、8、16、24 h 测定,结果Pb、Cd、As、Hg、Cu 5 种元素 的RSD 分别为1.1%、0.9%、0.8%、1.0%、1.2%,表明5 种元素溶液在24 h 内稳定性良好。
2.1.8 加样回收率试验取同一批已知含量的样品(批号:190704)6 份,每份约0.25 g,精密称定,置聚四氟乙烯消解罐内,加“2.1.2.1”项下多元素混合对照品溶液(级别6)1.0mL,按“2.1.2.2”项下方法制备样品,按“2.1.3”项下测定条件进行测定,通过线性回归方程得到加样样品中的各元素含量,计算回收率,铅、镉、砷、汞、铜的平均加样回收率分别为92.3%、95.6%、97.5%、95.0%、99.3%,RSD(n=6)分别为2.3%、1.9%、2.2%、1.6%、1.8%。结果表明本方法具有良好的准确性。
2.1.9 样品含量测定按“2.1.2.2”项下方法平行制备2 份样品,按“2.1.3”项下测定条件进行测定,以回归方程分别计算样品中各元素的含量,结果见表4。
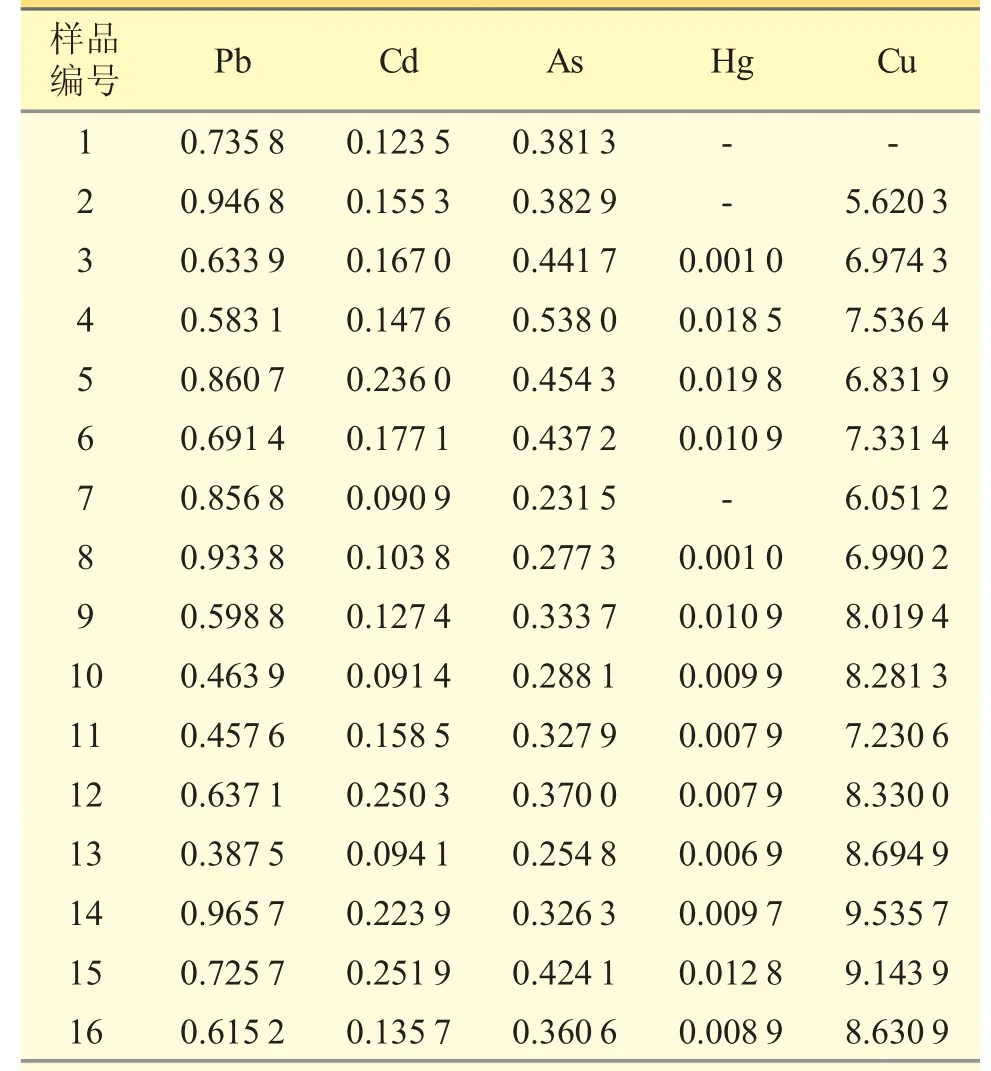
表4 样品中Pb、Cd、As、Hg、Cu 的含量(mg·kg-1,n=2)
2.2 铬的测定方法
2.2.1 AAS 仪器工作条件配备石墨炉自动进样器。铬空心阴极灯,波长357.9 nm,狭缝0.7 nm,灯电流22 mA,石墨炉原子化器,氩气为保护气,背景校正为塞曼校正。石墨炉工作条件升温程序:①干燥温度以150 ℃保持30 s;②灰化温度以1200 ℃保持20 s;③原子化温度以2300 ℃保持5 s;④净化温度以2450 ℃保持3 s。
2.2.2 溶液的制备
2.2.2.1 对照品系列溶液:精密量取铬元素对照品溶液适量,用2%硝酸溶液逐级稀释成每毫升含铬25 ng 的溶液,再由自动进样系统稀释成0、5、10、15、20、25 ng·mL-1的系列标准溶液。
2.2.2.2 供试品溶液:精密称定本品0.25 g,置聚四氟乙烯微波消解罐中,加硝酸5 mL,混匀,预消解30 min(100 ℃),置微波消解仪中,开始样品消解:0~5min,由初始温度升至120℃,维持10min;15~20min由120 ℃升至190 ℃,维持20 min。消解完全后,消解液冷至60 ℃以下,取出消解罐置电热板上缓缓加热至红棕色蒸汽挥尽并近干,用水转移至25 mL 聚四氟乙烯量瓶中,以少量水洗涤消解罐数次,洗液合并同一量瓶中,水稀释至刻度,摇匀,即得。
2.2.3 含量测定取供试品溶液和对照品溶液适量,以石墨炉为原子化器,照原子吸收分光光度法[8](《中国药典》2020 年版四部通则0406 第一法),在357.9 nm 波长处测定,计算,即得。
2.2.4 线性关系和检测限将“2.2.2.1”项下对照品系列溶液进样分析,以吸光度(A)为纵坐标、浓度(C)为横坐标绘制标准曲线,得铬元素的回归方程:Y=1.756×10-2X+1.010×10-3,r=0.999 9,表明铬元素浓度在0~25 ng·mL-1范围内与吸光度具有良好的线性关系。检测限为0.4 mg·kg-1。
2.2.5 精密度试验取标准曲线范围内同一浓度的对照品溶液,重复测定6 次,结果RSD 为1.8%(n=6),表明仪器具有良好的精密度。
2.2.6 重复性试验取同一批次样品(编号2)适量,按“2.2.2.2”项下方法制备6 份供试品溶液,按“2.2.1”仪器条件测定,结果平均值(n=6)为0.3 mg·kg-1,RSD 为1.3%。表明方法的重复性良好。
2.2.7 稳定性试验取已知含量的供试品溶液(编号2)适量,分别放置0、2、4、8、16、24 h 测定,结果RSD 为1.1%,表明该元素溶液在24h 内稳定性良好。
2.2.8 加样回收率试验取同一批次已知含量的样品(编号2)6 份,每份约0.12 g,精密称定,分别精密加入各测定元素相应的对照品溶液适量,按“2.2.2.2”项下方法制备样品,按“2.2.3”项下测定条件进行测定,通过线性回归方程得到加样样品中的铬元素含量,计算回收率,结果铬的平均加样回收率为98.1%,RSD(n=6)为1.9%。表明本方法具有良好的准确性。
2.2.9 样品含量测定以“2.2.2.2”项下方法平行制备样品2 份,按“2.2.3”项下仪器条件测定,结果见表5。
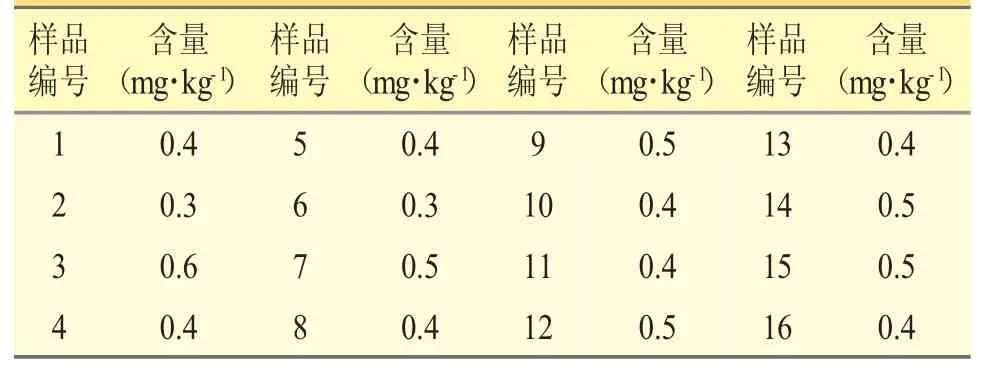
表5 样品中Cr 的含量(mg·kg-1,n=2)
2.3 风险评估
实验分别参照《ICH 指导原则Q3D 元素杂质指南》和《中国药典》2020 年版四部9302“中药有害残留物限量制定指导原则”建立有害元素风险评估模型。
评估模型①:参考ICH Q3D,按公式1 计算最大允许浓度,PDE 为每日允许暴露量;根据芩连胶囊说明书最大服用剂量为每日口服一次4 粒,一日3 次,每粒为0.44 g,日最大服用剂量为5.28 g 计算,结果见表6。
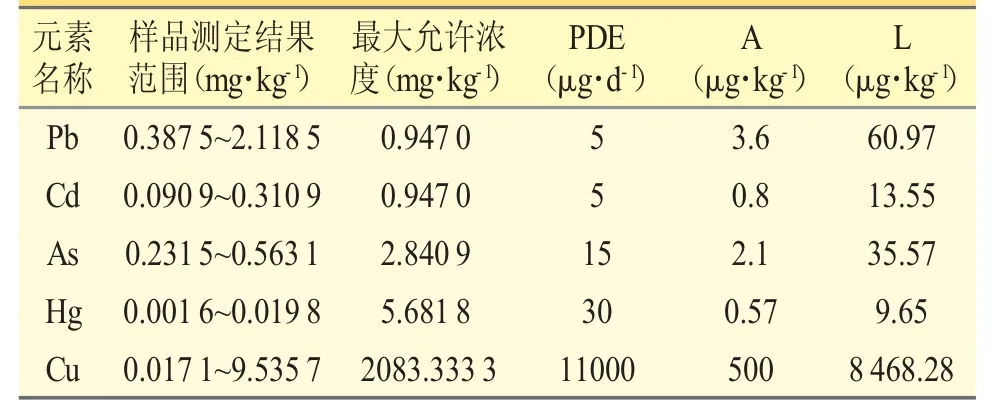
表6 风险评估结果

评估模型②[6,7]:参照《中国药典》2020 年版,按公式2 计算。

L 为最大限量理论值(mg·kg-1);A 为每日允许摄入量(μg·kg-1);W 为人体平均体质量(kg),一般按63 kg 计;M 为每日人均可服用的最大剂量(kg),芩连胶囊M 按日最大服用剂量为5.28 g;TA为平均寿命天数,一般为365 d×70 年;EF为中药服用频率(d/年),设为每年90 d;ED为一生服用中药的暴露年限,设为20 年;t 为重金属元素的转移率(%),中成药t 为100%;10 为安全因子,表示每日由中药材及其制品中摄取的重金属量不大于日总暴露量(包括食物和饮用水)的10%。
由表6 显示,芩连胶囊中重金属元素Pb、Cd、As、Hg、Cu 和Cr 的含量均低于《中国药典》2020 年版和《ICH 指导原则Q3D 元素杂质指南》规定的限度,此方法为厂家产品进行重金属有害元素风险评估提供参考。
3 讨论
重金属问题已经成为中药出口和阻碍中医药发展的主要问题。有研究表明,重金属元素具有积累性、食物链传递性和不易降解性,易在人体内蓄积,当达到一定含量时,可导致各种疾病发生[8]。
重金属及有害元素风险评估旨在科学、合理研究中药用药安全性。《中国药典》中仅对芩连胶囊处方中的甘草[6]重金属及有害元素含量作出了规定。由于芩连胶囊为复方制剂,单纯采用此标准对其进行安全评价不尽合理。《ICH 指导原则Q3D 元素杂质指南》中的风险评估模型通俗易懂,使用简便,多适用于化学药品,对于中药及其相关制品可能存在一定的评价风险偏差;《中国药典》2020 年版的风险评估模型计算相对复杂,但评估元素的每日允许摄入量不易获得;采用2 种模型相结合的方式进行风险评估,可呈扬优补缺之效。
对本次检测的16 批芩连胶囊进行分析评价,表明部分样品中Pb、Cd、As 仍有较多的残留,说明仍需持续加强中药材种植中对土壤、化肥等的选择和管理,严控重金属超标,提高中药质量,力求达到以环保标准为基础的绿色认证制度要求。

