以“合成氨”为中心的大单元教学设计
盛烨锋

关键词:大单元设计;合成氨;化学反应和能量;复习课
化学学科核心素养能够引领化学教学,彰显育人价值,核心素养既关注学生关键能力的提升,也注重必备品格的培育。关键能力是一种在特定的情境中,调动多种资源,以满足复杂需要的能力,是个体在解决现实复杂问题过程中表现出来的综合品质。本文是作者参加直属高中优质课比赛实录。
一、化学问题解决的教学模型
二、采用单元整体教学设计
将相关的知识点组织起来,成为有结构的知识体系。备课从知识点到单元,标志着教师备课的站位的提升:立足单元,上接学科核心素养,下连知识点的目标要求。
单元整体教学设计:
三、基于问题解决的教学实施
课堂引入:一个人解决了半个中国的温饱问题——袁隆平爷爷。一个化学反应解决几十亿人的吃饭问题——合成氨。从两个角度认识:从能量变化和化学反应速率和限度的视角认识合成氨。
【教师】我们首先来看探析合成氨的热量变化,请问化学反应的本质是什么?
【学生】旧键断裂,新键生成。
【教师】化学反应有吸放热的原因是什么?
【学生】旧键断裂吸热,新键生成放热。
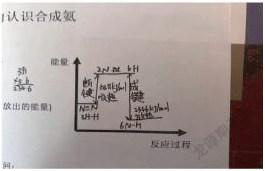
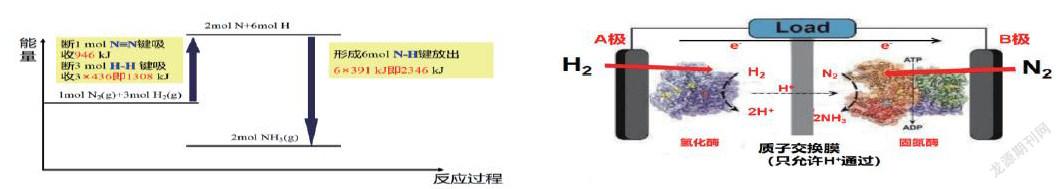
【教师】接下来我们来看合成氨的吸放热,请同学们根据任务一完成能量变化示意图。
【教师】投影学生完成情况
【教师】请同学点评。
【学生】断键的能量出现了问题,应当是1 mol氮氮三键和3 mol氢氢键的能量。
【教师】请问该反应的热效应?
【学生】应当是放热反应,因为反应物断键所需要的能量小于生成物成键放出的能量。
【教师】展示正确答案。
【教师】能否从宏观的角度解释放热反应。
【学生】宏观上反应物的总能量大于生成物的总能量,因而为放热反应。
设计意图:键能的角度绘制反应过程和能量的曲线,再从宏观的角度解释放热反应,从两个角度解释了反应能量的变化原因,绘制曲线也能提升热量变化识图能力,提升学生宏观辨识和微观探析的素养。
【教师过渡】我们再来看合成氨的另外一种方法。犹他大学的Minteer教授通过构筑H2/N2生物燃料电池,真的就是以氮气和氢气为原料,在合成氨的同时还能获得电能。
【教师】复习原电池的构成条件,如何判断该原电池的正负极?
【学生】可以通过氢离子,跑向正极。通过电子移动方向,还可以根据化合物。
【教师】请写出A、B电极的电极反应式以及总反应,请同学上台板书。
设计意图:通过燃料电池的模型复习原电池的工作原理,提高学生的模型建构的化学素养。
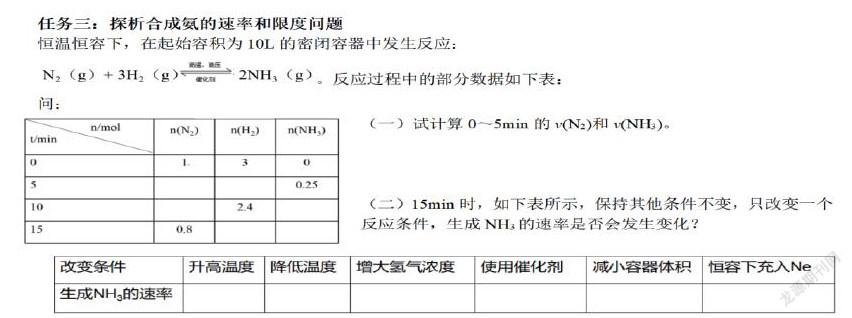
【教师过渡】通过生物燃料电池生成氨还只是停留在实验室,我们还是要工业合成氨,那么如何又快又多的合成氨呢?接下来解决任务三:探析合成氨的速率和限度问题。
【学生】反应速率的计算公式为浓度除时间,因而可以计算出速率。还可以发现速率之比等于系数之比。
【教师】强调单位的正确书写,请同学回答第二个问题。
【学生】改变温度可以改变反应速率,升高温度加快反应速率,降低温度减慢反应速率。
增大氢气浓度可以加快反应速率,使用催化剂可以加快反应速率,减小容器体积可以加快反应速率,恒容下充入Ne不改变容器体积,故浓度不变,因而不改变反应速率。
设计意图:参考学考卷中的题型,利用合成氨中的数据将速率及其影响因素结合其中,利用定义计算化学反应速率,外界条件变化速率变化情况,提升学生变化观念。
【教师】试判断10分钟时,反应是否达到平衡状态,说出判断依据。
【学生】因为浓度不变,故已达平衡。
【教师】复习平衡状态的特征。请完成后续问题。
下列能說明达到平衡状态的是
(1)H2的正反应速率等于N2的逆反应速率
(2)容器内压强保持不变
(3)容器内密度保持不变
(4)容器内平均摩尔质量保持不变
【学生】第一个不能,应当成系数之比。第二个能说明,压强和n成正比。
第三个容器体积和气体质量都不变,故不能说明。第四个气体的物质的量在变化,因而可以说明达到平衡状态。
【教师】总结变量不变因而可以说明达到化学平衡状态。
设计意图:根据化学平衡的特征进行平衡状态的判断的复习,提升学习的平衡思想。
四、基于问题解决的教学反思
认真准备展示课,对教师的专业成长帮助很大,一线教师不仅要认真学习新课标,更要能将新课标的课程理念落实在每一节的课堂教学中,要具备这种能力就必须将理论学习与实践研究相结合。
参考文献:
[1]孙艳霞.高中化学“反应与能量”课题教学目标认识与教学设计[J].数理化解题研究,2019(7):2.
[2]贺阳.基于项目化学习的化学反应与能量单元复习课--社会性议题“燃油车会消失吗”[J].化学教与学,2022(2):3

