原发性纵隔卵黄囊瘤肺内转移1例并文献复习
吴红剑,冯玉莲(通讯作者)
(曲靖市中医医院放射科 云南 曲靖 655000)
原发性纵隔卵黄囊瘤(primary mediastinal yolk sac tumor)又称纵隔内胚窦瘤(endodermal sinus tumour),是由卵黄囊发生的高度恶性生殖细胞肿瘤,好发于儿童及青年,多数位于前纵隔。本文就我科诊断1例患者,现将该疾病影像学、检验、病理特征,报道如下,以提高对本病的早期诊断及治疗水平。
1 病例资料
1.1 病例
患者,男,23岁,农民,入院日期:2018年9月25日,主因“胸骨后疼痛1个月”入院。血生化:甲胎蛋白(AFP):>1 100 ug/L。
1.2 术前影像表现
胸部CT见前上纵隔不规则囊实性肿块,密度不均匀,增强后不均匀强化,分隔及实性部分轻度至中度强化,坏死区及囊变区无强化(图1、图2)。
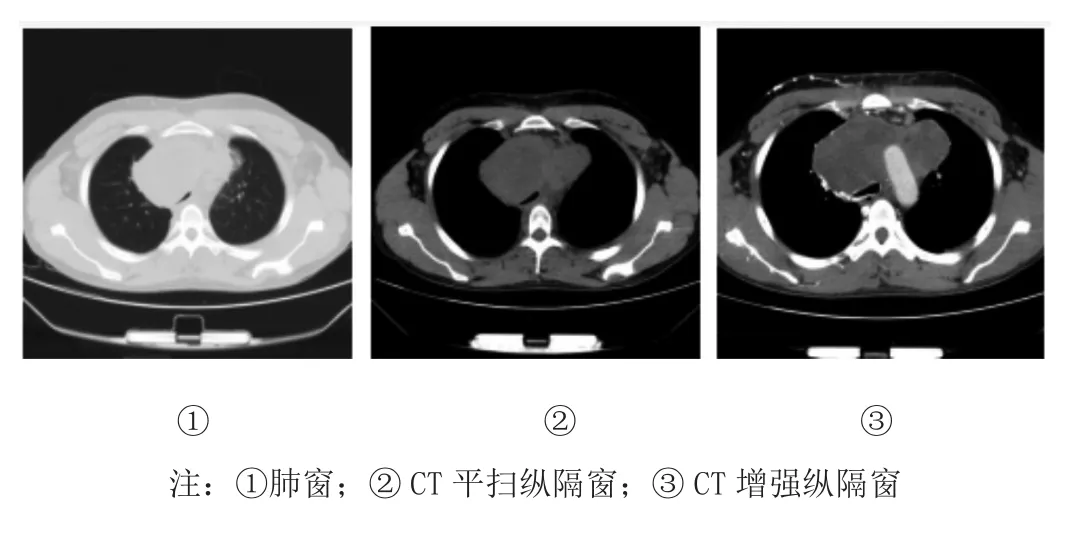
图1 术前胸部CT检查肿瘤表现

图2 CT冠状位重建④ CT增强冠状位重建⑤
1.3 术中所见
肿块位于前上纵隔,呈灰白灰黄囊实性,质软,肿块包绕纵隔大血管,气管受压。
1.4 病理诊断
术后病理(前上纵隔恶性肿瘤),结合免疫组化符合卵黄囊瘤。
免疫组化:Villin(+), AFP(+),CD117(部分+),SALL4(+), Pan CK(+), p40(-), p63(-), HCG(-),CK20(-),CD30(-),D2-40(-),EMA(-),PLAP(-),CK7(-),Vim(-),(图 3)。
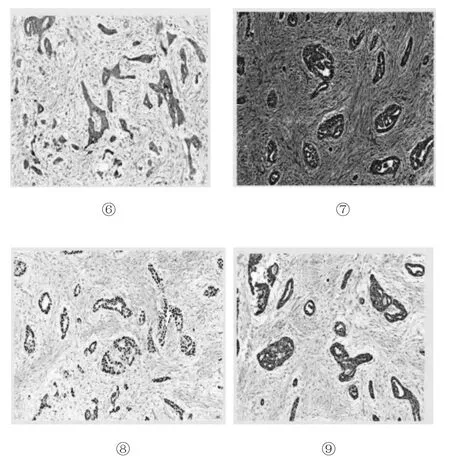
图3 免疫组化:Villin(+)⑥,AFP(+)⑦SALL4(+)⑧,Pan CK(+)⑨
1.5 治疗过程
患者确诊后,行手术治疗,术后多次周期辅助化疗,半年后复查胸部CT示肿瘤复发并肺内多发转移性病灶(图4)。间隔半年后复查胸部CT示肿瘤较前进展,双肺多发炎性病灶,双肺内多发转移灶,右侧胸腔及心包大量积液(图5)。患者于三月后因肿瘤术后复发并肺内多发转移、肺部感染及心力衰竭、呼吸衰竭死亡。
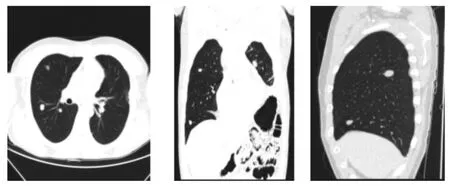
图4 双肺多发转移灶
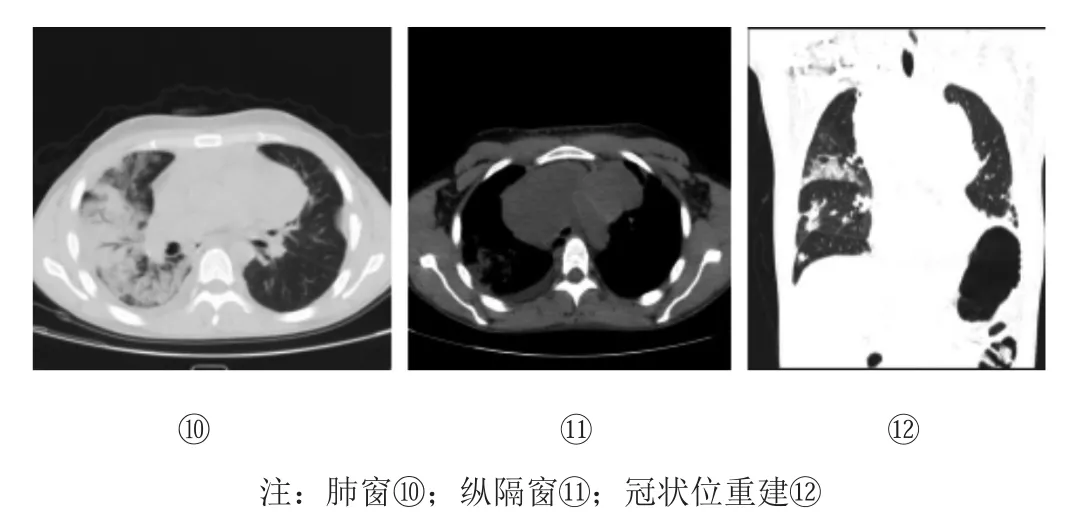
图5 右肺阻塞性肺炎
2 讨论
2.1 临床特点
卵黄囊瘤好发于儿童及青年,多发于性生殖腺发育过程的中线区域,也可发生在鞍区、纵隔、骶尾椎等。纵隔多发生于前、上纵隔。该病易复发、易转移,常见的转移部位有脑、肺、肝、骨等。纵隔卵黄囊瘤需要与发生于纵隔的其他恶性肿瘤鉴别[1]:①纵隔淋巴瘤,好发于前、中纵隔,以20~30岁及60~80岁两个年龄段多发,多伴有全身其他部位的淋巴结肿大,不易累及肺或胸膜;②侵袭性胸腺瘤,好发于40岁以上的中年人,临床典型者有重症肌无力,经常并发胸腔及心包积液;③胸腺癌,好发于中年男性,很少伴发重症肌无力,其恶性程度较侵袭性胸腺瘤更高,易发生肺、骨转移及纵隔侵犯;④其他AFP升高的肺部疾病,常见的有:肺母细胞瘤、肺大细胞神经内分泌癌等。
2.2 影像学特点
纵隔卵黄囊瘤多发生于前纵隔,体积较大的囊实性肿块,增强动脉期出现瘤内新生血管、静脉期新生血管增多,实性部分不均匀渐进性强化,尤其是瘤灶大片坏死、囊变与瘤内新生血管丰富的矛盾性的特点,再结合AFP、β-HCG及CA125等升高的实验室指标,则该病可能性极大,确诊仍需结合病理检查及免疫组化[2]。CT检查有利于临床医生对肿瘤进行术前评估、制定诊疗计划及疗效监测[3]。
2.3 病理学结构及免疫组化特点
卵黄囊瘤有特征性病理学结构:网状结构、Schiller-Duval小体、嗜酸性小体及PAS染色阳性的透明小体。术后大体病理诊断是确诊纵隔卵黄囊瘤的金标准[4]。免疫组织化AFP、CK呈阳性时诊断具有特异性[5]。免疫组化FISH检测12p对于鉴别纵隔原发肿瘤:胸腺瘤、淋巴瘤、间叶源性肿瘤等非常有价值[6]。
2.4 实验室检查特点
血清AFP在卵黄囊瘤诊断、治疗和疗效的评判中具有重要价值[7],AFP和β-HCG结合可用于精原细胞瘤的分型和分期。血清AFP明显升高是卵黄囊瘤的特异性诊断指标,而血β-HCG升高则要考虑精原细胞瘤或绒毛膜癌[8]。胸腺癌和淋巴瘤AFP和β-HCG则无异常。
2.5 治疗及预后
根治性手术+化疗仍是目前最重要的治疗手段[9]。卵黄囊瘤的恶性程度较高,生长速度快,且易较早发生转移,多数患者难以完整切除肿瘤,易复发,预后极差。但是通过早期诊断及手术、化疗等多学科联合治疗手段,患者仍存在改善生存期的希望。
综上所述,综合分析患者的临床表现、影像特点,结合血清AFP明显升高,病理学Schiller-Duval小体、嗜酸性小体及PAS染色阳性的透明小体,免疫组化AFP、CK阳性等,可以提高卵黄囊瘤的诊断符合率,通过合理治疗来改善患者生存期。

