4-硝基苯基-β-D-纤维二糖苷的合成
胡亚丹,常新林,钟 婷,张贺延昊,苏 进,张园园*
(1.北京中医药大学药学院有机化学教研室,北京 100049;2.复旦大学药学院天然药物化学教研室,上海 201203)
糖苷酶又称糖苷水解酶,是水解酶家族中的一大类,也隶属于糖基酶,是所有可水解糖苷键的酶类的总称。糖苷酶根据催化作用机制的不同分为构型翻转酶和构型保持酶两种[1]。近年来,随着糖类物质在生物学领域内的重要性越发凸显,关于糖苷酶的研究与应用也变得越发重要。糖苷酶的活性一般采用具有生色基团的物质与糖类形成的缀合物进行测定,称为速率检测法,目前对硝基苯基作为发色基团较为常见[2]。随着工业社会的进步,能源问题越发严峻。固定化的太阳能生物质能资源是最为丰富的碳来源,其中纤维素占比高达一半。但是纤维素较难被降解利用,这成为能源发展的难题。对硝基苯基纤维二糖苷作为纤维寡糖的结构类似物,广泛用于专一性测定纤维素系列酶的活性[3]。因此,该酶底物的合成具有较为重要的意义,但其合成工艺鲜有报道。目前,仅可查阅到一些文献关于与其相似结构的化合物的合成[4-6]。本研究通过相转移催化法合成了4-硝基苯基-β-D-纤维二糖苷,可为其高效制备及酶催化机制的研究提供依据。
1 材 料
1.1 仪器 RE-201D旋转蒸发器(巩义市予华仪器有限责任公司);78-1磁力搅拌器(江苏荣华仪器制造厂);2695高效液相色谱仪(美国Waters公司);核磁共振仪[1H-NMR (400 MHz),13C-NMR (125 MHz),瑞士Bruke公司]。
1.2 试剂 纤维二糖、对硝基苯酚钠(美国Sigma-Aldrich公司);甲醇(色谱纯,美国Tedia公司);水为纯净水(杭州娃哈哈集团有限公司);乙酸酐、二氯甲烷、甲醇、乙醇、浓硫酸(分析纯,北京化工厂);33%的氢溴酸-乙酸溶液、无水乙酸钠、甲醇钠、四丁基溴化铵(北京伊诺凯科技有限公司)。
2 方法和结果
目标化合物4-硝基苯基-β-D-纤维二糖苷的合成路线见图1。
2.1 1,2,3,6,2′,3′,4′,6′-O-八乙酰基纤维二糖(化合物A)的合成 在500 ml圆底烧瓶中加入270 ml(2.86 mol)乙酸酐,冰浴下加入100.00 g(0.29 mol)纤维二糖、100.00 g无水乙酸钠,常温搅拌4 h,薄层色谱法(TLC)监测至反应完成。将反应液倒入冰水中,析出白色固体,抽滤,冷水洗涤,无水乙醇重结晶,得白色固体(化合物A)195.41 g,收率98.6%。
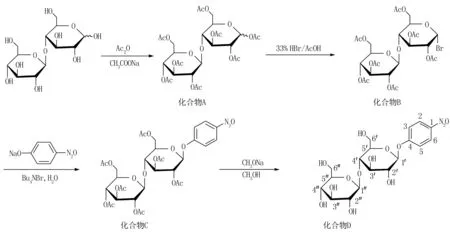
图1 4-硝基苯基-β-D-纤维二糖苷的合成路线Figure 1 Synthetic route of 4-nitrophenyl-β-D-cellobioside化合物A:1,2,3,6,2′,3′,4′,6′-O-八乙酰基纤维二糖;化合物B:2,3,6,2′,3′,4′,6′-O-七乙酰基-α-D-溴代纤维二糖; 化合物C:2,3,6,2′,3′,4′,6′-O-七乙酰基-4-硝基苯基-β-D-纤维二糖苷; 化合物D:4-硝基苯基-β-D-纤维二糖苷
2.2 2,3,6,2′,3′,4′,6′-O-七乙酰基-α-D-溴代纤维二糖(化合物B)的合成 在1000 ml圆底烧瓶中加入195.41 g (0.29 mol)化合物A、600 ml二氯甲烷、75 ml 33%的氢溴酸-乙酸溶液(0.41 mol)于室温下搅拌反应。高效液相色谱-蒸发光散射(HPLC-ELSD)法监测反应,4 h后停止搅拌。依次用水、饱和碳酸氢钠、饱和食盐水洗涤,分取二氯甲烷层,浓缩后乙醚结晶,得白色固体(化合物B)142.10 g,收率71.0%。
2.3 2,3,6,2′,3′,4′,6′-O-七乙酰基-4-硝基苯基-β-D-纤维二糖苷(化合物C)的合成 将142.10 g(0.20 mol)化合物B溶于400 ml二氯甲烷,加入50.00 g(0.31 mol)对硝基苯酚钠、23.00 g(0.07 mol)四丁基溴化铵作为相转移催化剂,加入400 ml纯水,32 ℃下用恒压漏斗滴加饱和碳酸钠溶液使pH值保持在8左右,反应10 h。分取二氯甲烷层,减压浓缩析出淡黄色结晶。乙醇重结晶,得白色固体(化合物C)82.08 g,产率54.2%。
2.4 4-硝基苯基-β-D-纤维二糖苷(化合物D)的合成 取82.08 g(0.11 mol)化合物C置1000 ml圆底烧瓶中,加入700 ml甲醇,加适量甲醇钠调节pH值至9,室温下反应3 h,TLC监测至反应完全。冰浴搅拌3 h析出固体,过滤,乙酸乙酯重结晶,得白色固体(化合物D)48.58 g,产率95.3%。
化合物D的结构鉴定结果如下。1H-NMR(500 MHz,D2O) δ: 8.17(d,J=7.5 Hz,2H,Ar-H),7.16(d,J=7.5 Hz,2H,Ar-H),5.21(d,J=7.0 Hz,1H,H-1′),4.70(m,7H,OH;2H,H-2′,H-2″),4.46(d,J=7.5 Hz,1H,H-1″),2.90~3.10(m,10H,H-2′~H-6′,H-2″~H-6″)。13C-NMR(125 MHz,D2O)δ:161.64(C-1″),142.61(C-4″),126.09(C-3″,C-5″),116.45(C-2″,C-6″),102.56(C-1′),99.22(C-1),78.14(C-4),75.98(C-5′),75.47(C-3),75.07(C-5),73.96(C-3′),73.14(C-2′),72.50(C-2),69.44(C-4′),60.56(C-6),59.72(C-6′)。
2.5 4-硝基苯基-β-D-纤维二糖苷(化合物D)的纯度测定 色谱条件: Prevail C18色谱柱(250 mm×4.6 mm,5 μm),柱温30 ℃,流动相为甲醇-水(30∶70,V/V),流速1 ml/min,进样量20 μl,漂移管温度85 ℃,氮气流速2 L/min,进样浓度500 μg/ml。
记录色谱图和峰面积,用峰面积归一化法进行纯度测定,纯度约为99.87%。4-硝基苯基-β-D-纤维二糖苷(化合物D)的HPLC谱图见图2。
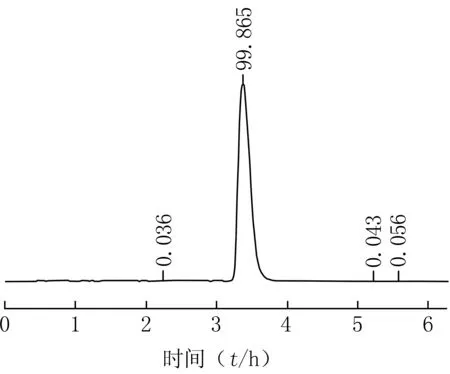
图2 4-硝基苯基-β-D-纤维二糖苷(化合物D)的HPLC谱图Figure 2 HPLC chromatogram of 4-nitrophenyl-β-D-cellobioside(compound D)
3 讨 论
3.1 化合物B的合成 由于产物的热力学性质原因,化合物B的绝对构型为热力学稳定的α构型。该反应会有多种副产物生成,其中最具有代表性的副产物为二糖水解生成的2,3,4,6-O-四乙酰基-α-D-溴代葡萄糖,另外随着反应的继续还有可能生成不同位置取代或者多取代的溴代葡萄糖、溴代纤维二糖,所以探索适宜的反应条件尤为重要。在化合物B的合成之前,先用1.00 g原料进行预实验,筛选合适的合成条件。通过对温度(0 ℃、室温25 ℃)及时间(2、4、6 h)的筛选,发现室温下反应效率较高,反应4 h后产率升高不明显,且副产物开始积累,故选择室温反应4 h为最佳合成条件。
3.2 化合物C的合成 此步反应经历了一个双分子亲核取代反应(SN2)历程,产物发生了构型的转化(Walden转化),选择性地由α构型变成了β构型。本研究考察了以碘化钾为催化剂,丙酮-水为溶剂体系进行成苷反应,20 h未见产物生成。在相转移催化剂四丁基溴化铵作用下,得到了目标产物,反应10 h的产率为54.2%。但反应过程中需注意使用弱碱碳酸氢钠调节溶液的pH值,若使用强碱氢氧化钠则易造成溴代糖变质及二糖链的水解。另外,反应温度不宜过高,否则易造成溴代糖变质。
3.3 化合物D的合成 该反应的原理是酯交换反应,甲醇钠作为催化剂,易与水反应生成氢氧化钠而失去醇解能力,所以反应过程中应保持无水。另外,应注意甲醇钠的用量,使体系pH值控制在9即可,若碱性过强则易造成糖苷键及二糖链水解。
本研究以较为廉价的D-八乙酰纤维二糖、对硝基苯酚钠为底物,经乙酰化、溴代、相转移催化成苷、脱保护4个步骤,优化溴代纤维二糖制备工艺和成苷反应条件,最终简单、高效地合成了酶底物4-硝基苯基-β-D-纤维二糖苷,可为其进一步广阔应用提供原料储备和技术支持。

