分散液液微萃取/高效液相色谱法测定水样中的苯胺类物质
, ,,, ,,, , ,,
(1.广州大学环境科学与工程学院,广东广州 510006;2.珠江三角洲水质安全与保护教育部重点实验室,广州大学,广东广州 510006;3.广东省放射性核素污染控制与资源化重点实验室,广州大学,广东广州 510006;4.四川大学华西第二医院妇产科,四川成都 610041)
苯胺类物质是染料、化妆品、制药、橡胶、煤气等工业领域的原料,而由于工业废水的不合理排放对环境造成了严重的污染[1 - 3]。苯胺类物质可通过吸入、食入或通过皮肤渗入人体,对肝脏、血液系统、神经系统等造成严重损伤,还具有潜在的致癌、致突变等作用[4 - 5]。中国、美国和欧盟等均将其列入常规监测和优先监测的污染物名单[2]。
目前检测苯胺类化合物的主要分析方法有分光光度法[6]、气相色谱法[5,7 - 8]、液相色谱法[9 - 10]、气相色谱-质谱法[11 - 12]、液相色谱-质谱法[3 - 4]和电化学法[13 - 14]等。水中苯胺类物质常用的预处理方法有固相萃取或液-液萃取法,但这两种方法操作繁琐、耗时,且需使用大量有毒有害的有机溶剂。分散液液微萃取(DLLME)是由REZAEE等[15]于2006年提出的一种环保、高效、简单、经济的分离富集技术。目前,DLLME已被广泛应用于不同基质样品的痕量分析。本研究对DLLME过程中的各种影响因素进行条件优化,结合高效液相色谱法,成功将其应用于不同水样中苯胺、4-硝基苯胺、2-硝基苯胺和2,4-二硝基苯胺这4种物质的同时测定。
1 实验部分
1.1 主要仪器与试剂
Agilent1200型高效液相色谱仪(美国,Agilent公司),配备二极管阵列检测器(DAD);TDL-4台式离心机(上海安亭科学仪器厂);氮吹仪(北京腾云博海科技有限公司);电子分析天平(德国,Sartorius集团);PB-10标准型pH计(德国,Sartorius集团);超声波清洗仪(美国,Cole-Parmer公司);SK-1快速混匀器(江苏金坛市荣华仪器制造有限公司);AL-01型溶剂过滤器(天津奥特塞恩斯仪器有限公司);25μL微量进样器(美国,Hamilton公司);0.45μm水性滤膜(上海安普公司)。
1000.0μg/mL的苯胺(A)、4-硝基苯胺(4-NA)的甲醇标准储备溶液,均购自国家环境保护总局标准样品研究所,2,4-二硝基苯胺(2,4-NA)(纯度≥99.0%)购自德国Dr.Ehrenstorfer化学材料公司,2-硝基苯胺(2-NA)(纯度≥99.0%)购自美国AccuStandard集团有限公司;色谱纯乙腈购自上海安普公司;1-丁基-3-甲基咪唑六氟磷酸盐([C4MIM][PF6])离子液体购自上海成捷化学有限公司,纯度99%;其他所用试剂均为分析纯。
1.2 样品处理
水样经0.45μm水性滤膜过滤后,用稀NaOH溶液调节试液pH值为11,接着加入NaCl固体,使其在水溶液中的浓度为0.3g/mL。取2mL水样于5mL离心试管中(如果是加标回收实验,需加入苯胺类混合标准),快速加入一定量的三氯甲烷(萃取剂),在快速混匀器上混匀1min后,以2000r/min的转速离心3min;用进样针取出离心管底下的沉积相于内插管中,用氮吹仪吹至近干;然后加入20μL甲醇溶解,取10μL进行高效液相色谱分析。
1.3 色谱条件
色谱柱:AgilentExtend-C18色谱柱(250×4.6mm,5μm);流动相:乙腈-水=36∶65(V/V);流速:1.0mL/min;柱温:室温;进样量:10μL。苯胺和2-硝基苯胺的检测波长为230nm,4-硝基苯胺和2,4-二硝基苯胺检测波长为360nm。
2 结果与讨论
2.1 检测波长的选择
通过扫描苯胺、4-硝基苯胺、2-硝基苯胺和2,4-二硝基苯胺的紫外-可见吸收光谱,发现苯胺和2-硝基苯胺在波长230nm附近有最大的吸收,4-硝基苯胺在波长360nm附近有最大吸收,2,4-二硝基苯胺在波长360nm附近有个很大的吸收峰。因此,为了获得更高的灵敏度,在DAD上设置了不同的波长进行比较,最终选择苯胺和2-硝基苯胺的检测波长为230nm,4-硝基苯胺和2,4-二硝基苯胺的检测波长为360nm。
2.2 分散液液微萃取条件的优化

图1 萃取剂种类对萃取效率的影响Fig.1 Effects of the type of extraction solvent on extraction efficiency
2.2.1萃取剂的选择萃取剂是影响分散液液微萃取萃取效果的重要因素。本实验分别选取了1,2-二氯乙烷、三氯甲烷、四氯化碳、二氯甲烷以及离子液体[C4MIM][PF6]这5种物质作为分离富集水样中4种目标苯胺类物质的萃取剂,结果见图1。从图中可以看出三氯甲烷和1,2-二氯乙烷的萃取效果较佳,但前者的毒性低于后者。后续实验选择三氯甲烷作为萃取剂。
2.2.2萃取剂体积的选择萃取剂体积越大,对目标组分的萃取量越大,但萃取剂体积过大会造成目标组分浓度的稀释,从而降低萃取效率。本实验考察了萃取剂三氯甲烷体积分别为20、30、40、50、60、70、80 μL对萃取效率的影响,结果见图2。当萃取剂三氯甲烷体积从20 μL增加到60 μL时,萃取效率逐渐增大,到体积60 μL时,萃取效率最高,继续加大萃取剂的体积,萃取效率反而有所降低。因此,选取60 μL作为最佳萃取剂体积。
2.2.3水样pH值的影响实验考察了水样pH值在6至12对萃取效率的影响(图3)。当pH值从6增加到10时,三氯甲烷对苯胺类化合物的萃取效率随着pH值的增大而增大;pH值在10~12之间,萃取效率无明显变化。这是因为在pH值为10~12时,苯胺类物质主要以分子形式存在,在水中的溶解度相对较小,有利于被三氯甲烷萃取。因此,为了减少实验的误差,本实验调节水溶液的pH值为11。

图2 萃取剂体积对萃取效率的影响Fig.2 Effect of the volume of extraction solvent on extraction efficiency

图3 溶液pH值对萃取效率的影响Fig.3 Effect of pH value of solution on extraction efficiency

图4 NaCl浓度对萃取效率的影响Fig.4 Effect of NaCl concentration on extraction efficiency
2.2.4盐度的影响盐效应对萃取的影响有双方面:(1)盐析作用,增加溶液的离子强度,降低目标组分在溶液中的溶解度,提高萃取效率;(2)样品中的极性物质与盐离子的静电作用,会降低萃取效率。本实验考察了水样中0、0.1、0.2、0.3 g/mL的NaCl对苯胺类物质萃取效率的影响,实验结果见图4。三氯甲烷萃取苯胺类物质,盐析效应占主导地位,即随着盐度的增加,萃取效率也在增加。因此,本实验采用0.3 g/mL的NaCl来调节水样的盐度。
2.3 方法的评价
2.3.1方法的线性范围、检出限和重现性以优化后含盐水溶液(pH=11)为介质,配制一系列不同浓度苯胺、4-硝基苯胺、2-硝基苯胺和2,4-二硝基苯胺的混合标准溶液,在优化的条件下进行分散液-液微萃取/高效液相色谱法测定,每个浓度至少重复3次。4种目标苯胺类物质在2~1 000 μg/L浓度范围内呈现良好的线性关系,相关系数(r)为0.9991~0.9997;以3倍信噪比(S/N=3)得出苯胺类物质的检出限为0.3~0.5 μg/L。对浓度为10 μg/L苯胺类物质溶液进行6次的平行测定,得相对标准偏差(RSD)为3.2%~5.3%,重现性良好。
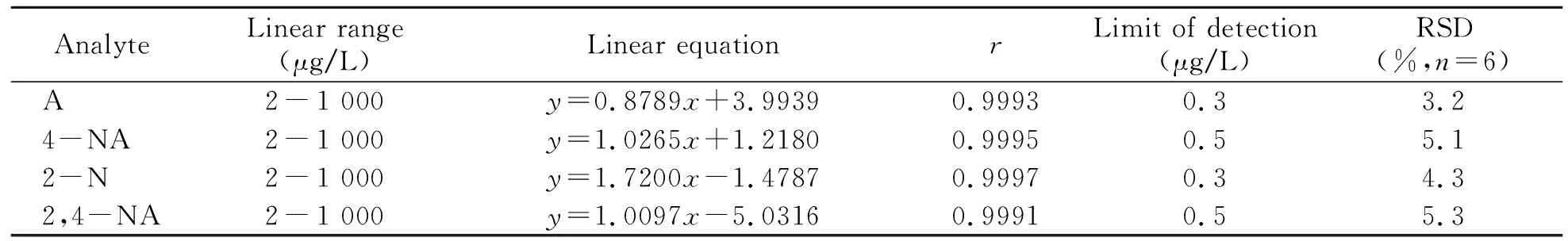
表1 4种苯胺的线性范围、线性方程、检出限及精密度
y:peak area;x:mass concentration,μg/L.
2.3.2样品分析及加标回收率实验在优化的实验条件下,测定了实验室自来水、珠江江水(广州大学河段)、广州沥滘污水处理厂的污水和广州南沙海水中的4种目标苯胺类物质,他们的含量均低于本方法的检出限。为了考察基质效应的影响,对这些实际水样进行两个浓度(10 μg/L和100 μg/L)的加标回收实验,测定其回收率,结果见表2。从表中可知实际水样的加标回收率在87.6%~101.8%之间,RSD为4.1%~6.5%,说明受基质效应的影响小,重现性良好。图5为蒸馏水加标、污水空白和加标水样的分散液-液微萃取后的色谱图。
2.4 本方法与其他方法的比较
将本实验所建立的方法与其他方法进行比较,见表3。虽说近几年有方法采用直接进样测定水中苯胺类物质,但需采用液相色谱-串联质谱法才能达到比较好的灵敏度[3 - 4,17]。而液相色谱-串联质谱法,由于使用的仪器贵,目前还不普及。陈昀[20]使用分散液-液微萃取的方法富集环境水样中的硝基苯胺类物质,方法的检出限跟本方法类似,使用了75 μL三氯甲烷做萃取剂,1 mL的乙腈做分散剂,采用3次反复抽取注射的方式来达到萃取的效果,回收率只有53.6%,没有本方法好,使用的有机溶剂也比本方法多。我国现行实施的《污水综合排放标准》测定苯胺的方法是N-(1-萘基)乙二胺偶氮分光光度法,此方法测定的是芳香族伯胺类化合物的总和,不是具体的各个苯胺类化合物的含量,水样的体积为25 mL,对于苯胺最低检出浓度为30 μg/L[21 - 22]。《地表水环境质量标准》中测定苯胺的方法是气相色谱-氢火焰离子化检测法(GC-FID),样品的前处理使用GDX-502高分子微球吸附10 L水中微量苯胺,用二氯乙烷洗脱,方法的最低检测浓度为2 μg/L[23 - 24],但此法操作繁琐、耗时、所需水样量大。

图5 蒸馏水加标(a)、 污水空白(b)和加标水样(c)的色谱图Fig.5 Chromatograms of distilled water spiked with the anilines(100 μg/L)(a),waste water(b) and waste water spiked with the anilines(100 μg/L)(c)1.aniline;2.4-nitroaniline;3.2-nitroaniline;4.2,4-dinitroaniline.

AnalyteSpiked(μg/L)Tap waterRiver waterWaste water Sea waterRecovery(%)RSD (%)Recovery(%)RSD(%)Recovery(%)RSD (%)Recovery(%)RSD (%)A10100.66.390.94.494.54.594.45.410093.65.899.55.590.84.989.56.12-NA1099.65.891.74.296.25.087.66.010092.35.397.94.197.94.790.25.84-NA1092.56.091.24.696.36.293.26.1100101.85.394.25.895.45.694.95.72,4-NA1096.76.192.35.292.45.590.16.510097.34.995.35.497.45.394.86.3
本实验采用高效液相色谱法,根据4种苯胺类物质的最大吸收波长来分别设置检测波长从而提高仪器检测的灵敏度。另外,本实验采用分散液-液微萃取的方法分离富集水样中苯胺类物质,所需萃取剂三氯甲烷只要60 μL,不需要分散剂,水样也只需2 mL,萃取快速,操作简单,灵敏度和重现性都得到了较好的结果,满足《污水综合排放标准》[21]和《地表水环境质量标准》[23]中规定的苯胺一级标准最高限量值分别为1 000、100 μg/L的要求,适用于污水及地表水源中苯胺、4-硝基苯胺,2-硝基苯胺和2,4二硝基苯胺的测定。

表3 本方法与其他测定苯胺类物质方法的比较
(续表3)

MethodRef.Linear range(μg/L)Extraction time(min)Sample volume(mL)Recovery(%)RSD(%)Detection of limit(μg/L)A2-NA4-NA2,4-NATC-IL-DLLME-UPLC-MS/MS j[18]0.5-503887.4-95.78.3-13.60.005---DI-HPLC-FLDk[9]50-200 000--91-109.91.6518---OL-SPE-HPLCl[10]--56-98-0.50.10.2-UA-IL-DLLME-HPLCm[19]100-1 500121090.5-1130.3-4.20.5-73-ECDn[13] 931-93 100--96-1013.83563---DLLME-HPLC o[20]2-200-553.6-1111.1-5.8-0.140.210.26Our method2-1 0001284.9-95.84.0-6.90.30.50.30.5
aSimultaneous derivatization-dispersive liquid liquid microextraction-GC-FID;bSimultaneous derivatization-ultrasound assisted emulsification microextraction-GC-FID;cNeedle trap-GC-NPD;dMicrowave assisted-headspace-solid phase microextraction-GC-FID;eHeadspace-solid phase microextraction-GC-MS;fSolid phase microextraction-GC-MS;gDirect injection-LC-MS/MS;hDirect injection-HPLC-MS/MS;iDirect injection-LC-MS/MS;jTemperature controlled-ionic liquid-dispersive liquid liquid microextraction-UPLC-MS/MS;kDirect injection-HPLC-FLD;lOn line-solid phase extraction-HPLC;mUltrasound assisted-ionic liquid-dispersive liquid liquid microextraction-HPLC;nElectrochemical detection;oDispersive liquid liquid microextraction-HPLC.
3 结论
采用了分散液-液微萃取/高效液相色谱-二极管阵列检测法,建立了测定水样中苯胺、4-硝基苯胺、2-硝基苯胺和2,4-二硝基苯胺的分析方法。该方法操作简单、所需溶剂少、环保、回收率高、检出限低、重现性好,适合用于实际水样中这4种苯胺类物质的分析检测。

