高效液相色谱法测定四神片中吴茱萸碱和吴茱萸次碱含量
潘瑞玲,韩慧琴
(1.内蒙古医学院第二附属医院,内蒙古 呼和浩特 010030; 2.河北省张家口市食品药品检验中心,河北 张家口 075000)
四神片由煨肉豆蔻、盐补骨脂、醋五味子、制吴茱萸、大枣(去核)和干姜6味中药组方,《国家药品标准》[1]中设置了吴茱萸的薄层色谱鉴别项,但未对其进行定量检验。国内相继有对吴茱萸碱、吴茱萸次碱、吴茱萸内酯含量测定的报道[2-6],但未见用1种流动相同时测定四神片中吴茱萸碱和吴茱萸次碱含量的报道。为此,本研究中采用高效液相色谱(HPLC)法(二极管阵列检测器),利用1种流动相,同时测定四神片中吴茱萸碱和吴茱萸次碱的含量,旨在为有效控制四神片的质量提供依据。
1 仪器与试药
Mettler AE163型电子天平(瑞士);Shimadzu UV-2450型紫外-可见分光光度计(日本);Waters 2695-2996型高效液相色谱仪(美国)。吴茱萸碱对照品(供含量测定用,中国药品生物制品检定所,批号为110802-200606);吴茱萸次碱对照品(供含量测定用,中国药品生物制品检定所,批号为110801-201006);四神片(陕西永寿制药有限责任公司,批号分别为120601,120806,120609);阴性样品(自制);甲醇、乙腈为色谱纯;十二烷基硫酸钠、磷酸为分析纯;水为去离子水。
2 方法与结果
2.1 色谱条件[7]
色谱柱:Capcell PAK-C18柱(150 mm ×4.6 mm,5 μm);流动相:0.1%磷酸溶液(含十二烷基硫酸钠0.2%)-甲醇-乙腈(50 ∶20 ∶30);流速:1.0 mL /min;吴茱萸碱检测波长:225 nm;吴茱萸次碱检测波长:343 nm;柱温:25 ℃;进样量:10 μL。
2.2 溶液制备
取吴茱萸碱对照品、吴茱萸次碱对照品适量,精密称定,加无水乙醇制成每1 mL各含2.5 μg的混合溶液,即得对照品溶液。取供试品 10片,精密称定,研细,取 1.2 g(2片的质量),精密称定,置具塞锥形瓶中,精密加入1%浓氨水无水乙醇25 mL,密塞,称定质量,超声处理(功率400 W,频率40 kHz)30 min,放冷,再称定质量,用无水乙醇补足减失的质量,摇匀,滤过,精密量取续滤液 10 mL,加入中性氧化铝柱(120~150目,5 g,内径 1.5~2 cm,湿法装柱)上,用无水乙醇10 mL洗脱,收集洗脱液,置25 mL容量瓶中,用无水乙醇稀释至刻度,摇匀,即得供试品溶液[8]。按处方比例制备缺吴茱萸饮片的吴茱萸阴性四神片制剂,再按供试品溶液制备方法制成阴性对照品溶液。
2.3 方法学考察
专属性考察:取对照品溶液、供试品溶液和阴性对照品溶液各10 μL注入高效液相色谱仪,依法测定。结果对照品溶液色谱有较好的峰形,供试品溶液色谱中吴茱萸碱和吴茱萸次碱能与其他杂质获得较好分离,分离度大于1.5,其色谱峰的纯度角度均小于纯度阈值,且阴性无干扰。色谱图见图1和图2。
线性关系考察:精密量取质量浓度为0.003 75 g/L的吴茱萸碱和 0.002 5 g /L 的吴茱萸次碱对照品溶液 1,2,5,10 μL,精密量取质量浓度为0.075 g/L的吴茱萸碱和0.05 g/L的吴茱萸次碱对照品溶液 1,2,5,10 μL,分别注入高效液相色谱仪,按拟订色谱条件测定,以峰面积积分值(Y)为纵坐标、对照品进样量(μg,X)为横坐标进行线性回归,得吴茱萸碱回归方程 Y=10 469 353X-2 857,r=0.999 9;吴茱萸次碱回归方程 Y =8 239 439 X-4 820,r=0.999 9。结果表明,吴茱萸碱进样量在 0.003 8 ~0.750 0 μg、吴茱萸次碱进样量在0.002 5~0.500 0 μg范围内与峰面积积分值线性关系良好。
精密度试验:取供试品10片,精密称定,研细,取1.2 g(2片的质量),精密称定,按2.2项下方法制备供试品溶液,精密吸取供试品溶液10 μL,连续进样5次,测定吴茱萸碱和吴茱萸次碱的峰面积。结果的 RSD分别为0.36%和0.62%(n=5),表明仪器精密度良好。
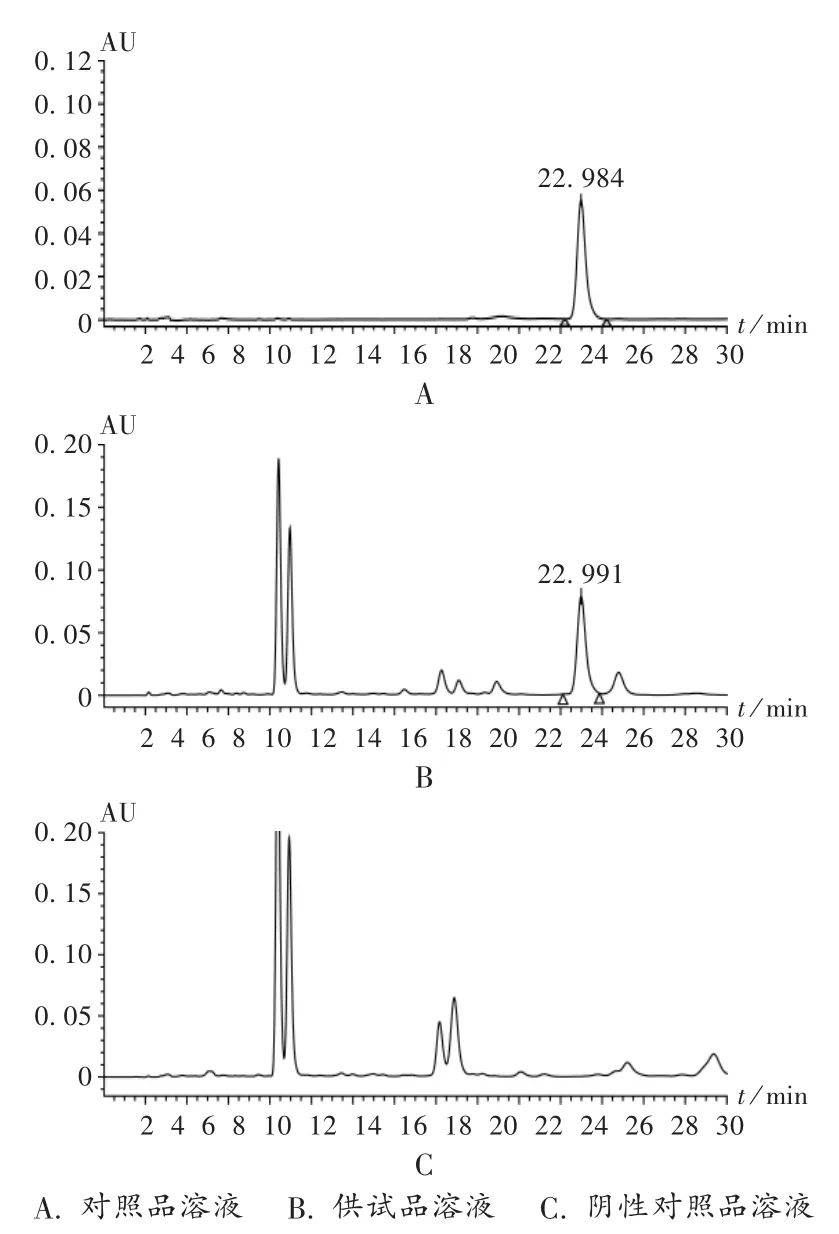
图1 吴茱萸碱高效液相色谱图
稳定性试验[9]:取同一供试品(批号为 120601)溶液,分别于0,8,12,16,20,24 h 按拟订色谱条件各进样 10 μL 测定,记录吴茱萸碱和吴茱萸次碱峰面积积分值。结果的 RSD分别为0.68%和0.73%(n=6),表明供试品溶液在24 h内稳定。
重复性试验:取同一批供试品(批号为120601)适量,研细,混匀,取 0.96,1.20,1.44 g 各 3 份,精密称定,按拟订方法制备供试品溶液,依法进样测定。结果供试品中吴茱萸碱的平均含量为 74.58 μg/g,RSD 为 0.89% (n =9);吴茱萸次碱的平均含量为 106.2 μg/g,RSD 为 0.96%(n =9)。
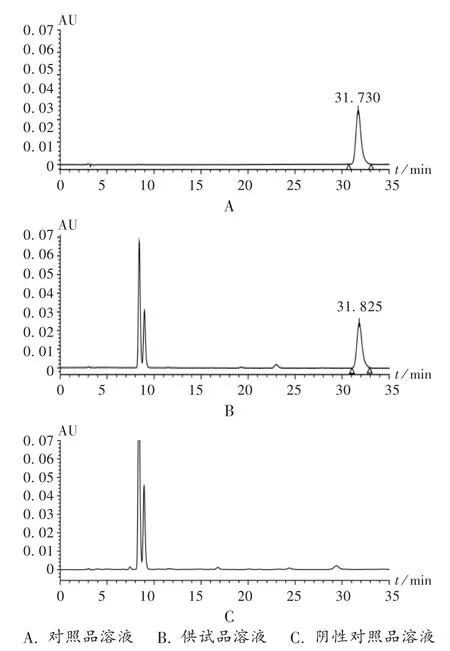
图2 吴茱萸次碱高效液相色谱图
加样回收试验:取已知含量的四神片(批号为120601),研细,混匀,取6份,每份约0.6 g,精密称定,每2份为1组,分别用以1%浓氨水无水乙醇为溶剂制备的3种吴茱萸碱和吴茱萸次碱对照品混合溶液(质量浓度分别为 1.432 μg/mL 和 2.039 μg/mL,1.788 μg /mL 和 2.529 μg/mL;2.147 μg /mL 和 3.058 μg /mL)代替1%浓氨水无水乙醇,按2.2项下方法制备供试品溶液,依法进样测定,计算回收率。结果见表1。
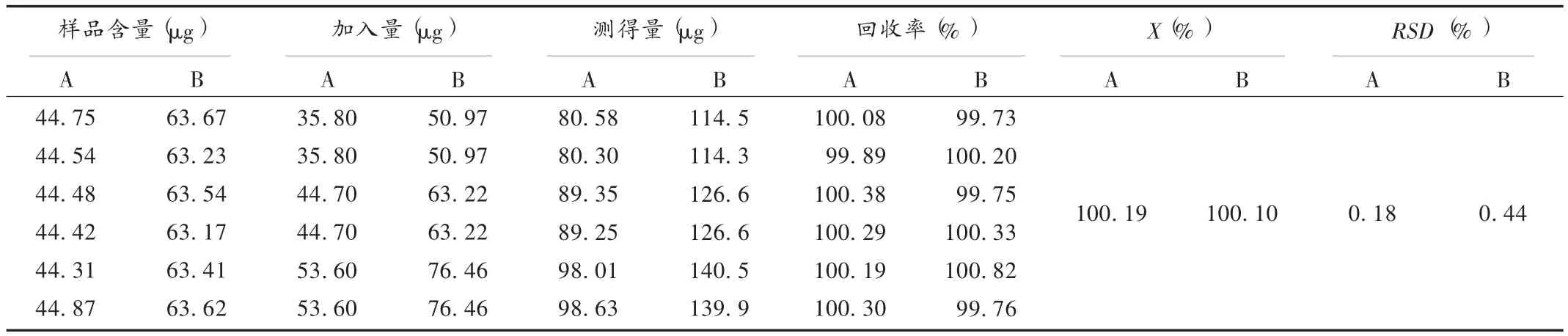
表1 吴茱萸碱和吴茱萸次碱加样回收试验结果(n=6)
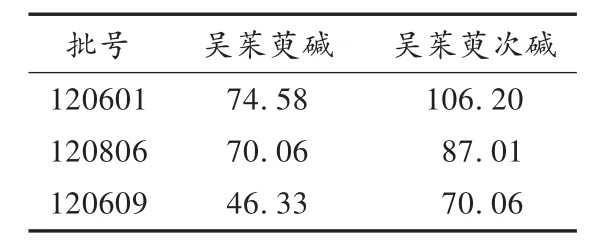
表2 样品含量测定结果(μg/片,n=2)
2.4 样品含量测定
取3批四神片,按拟订方法进样测定,计算样品含量,结果见表2。
3 讨论
2010年版《中国药典(一部)》吴茱萸药材含量测定项下的流动相为乙腈-水-四氢呋喃 - 冰醋酸(41∶59∶1 ∶0.2)[10]。采用该流动相时,四神片中吴茱萸碱和吴茱萸次碱色谱峰与其他杂质峰重叠,反复调整比例仍无法达到基线分离。后采用0.1%磷酸溶液(含十二烷基硫酸钠0.2%)-甲醇-乙腈为流动相,通过调整比例为(50∶20∶30)后,得到分离度良好、出峰时间适宜的色谱图。提取溶剂的考察曾采用环己烷、三氯甲烷、乙酸乙酯、丙酮作溶剂制备供试品溶液,均未使待测峰的分离得到改善,改用无水乙醇后试验结果良好。试验过程中,对超声时间、所加溶剂的量、中性氧化铝的量和洗脱液的量都进行了考察,最后确定了文中的提取方法。
吴茱萸碱和吴茱萸次碱虽为生物碱,但不易溶于酸水中,因此,供试品溶液的前处理净化不能采用酸水。
本方法简便,准确,高效,并有较高的重复性,可作为四神片的质量控制方法。
参考文献:
[1]WS3-B-1524-93-2011,国家药品标准 [S].
[2]胡晓艳,陈 乐,熊 彝,等.HPLC法测定吴茱萸超微速溶饮片中吴茱萸碱、吴茱萸次碱及柠檬苦素的含量[J].中国医药科学,2013,3(1):108-110.
[3]魏璐雪,徐艳春,周玉新,等.HPLC测定黄连与吴茱萸配伍前后吴茱萸碱及吴茱萸次碱的含量[J].中国中药杂志,2001,26(12):846.
[4]洪玉梅,蔡 嵩,王维皓,等.HPLC测定吴茱萸及其炮制品中吴茱萸内酯的含量[J].中国中药杂志,2006,31(20):1 726-1 727.
[5]罗 君,张丽艳.贵州余庆栽培吴茱萸的质量对比研究[J].时珍国医国药,2008,19(12):3 001-3 002.
[6]袁金成,罗习珍,肖锡林,等.HPLC法测定吴茱萸中吴茱萸碱和吴茱萸次碱的含量[J].现代生物医学进展,2008,2(12):2 536-2 537.
[7]李 丽,贾 英,陈晓辉,等.HPLC法同时测定吴茱萸中吴茱萸苦素和柠檬苦素的含量[J].中国天然药物,2003,9(3):158-160.
[8]史万忠,李世芳,刘 瑾,等.复方灵通胶囊稳定性试验中吴茱萸碱和吴茱萸次碱的含量变化[J].中成药,2011,33 (8):1 356-1 360.
[9]张敏娟,黄秀梅,姜世贤.HPLC和UPLC法测定复方黄连素片中吴茱萸碱、吴茱萸次碱含量的方法比较[J].药物分析杂志,2012,32(11):2 077-2 081.
[10]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:141.
——以吴茱萸为例

