多西他赛联合顺铂方案在二线治疗晚期非小细胞肺癌中的应用价值
多西他赛联合顺铂方案在二线治疗晚期非小细胞肺癌中的应用价值
祝子明1, 李凌云2, 张年宝1
(安徽省宣城市人民医院, 1. 药学部; 2. 肿瘤科, 安徽 宣城, 242000)
关键词:多西他赛; 顺铂; 晚期非小细胞肺癌; 无进展生存期; 生存率
肺癌是世界范围内的医学难题,其发病率和病死率在各种恶性肿瘤中居高不下,约80%新确诊的肺癌患者被诊断为非小细胞肺癌(NSCLC)[1]。由于起病隐匿、进展迅速,有2/3以上的患者在初诊时即为中晚期,缺乏手术指证而失去根治性手术机会[2]。循证医学证据支持2种不同细胞毒性的化疗药物联合应用作为晚期NSCLC患者的一线治疗,其中以含铂类化疗药为基础的联合方案广受推荐[3]。然而,晚期NSCLC患者治愈希望渺茫,一线治疗后的疾病进展不可避免。在Karnofsky活动状态(KPS)评分较好的一线治疗失败的患者中,施行合理有效的二线治疗方案,对延长生存期、改善生存质量具有重要意义[4]。美国临床肿瘤学会(ASCO)推荐的二线化疗药物为多西他赛、培美曲塞、厄洛替尼及吉非替尼等。本研究通过观察多西他赛联合顺铂双药方案二线治疗晚期NSCLC患者,取得了较好疗效,现报告如下。
1资料与方法
1.1 一般资料
选取2011年2月—2013年2月安徽省宣城市人民医院收治的晚期NSCLC患者72例。入选标准: ① 经病理组织学或细胞学检查确诊为NSCLC; ② 经CT或PET-CT检查有可测量病灶; ③ KPS评分≥60分; ④ TNM临床分期为Ⅲ~Ⅳ期; ⑤ 以往接受以含铂类药物为基础的一线化疗或分子靶向药物治疗,治疗期间疾病进展或结束后6个月内疾病进展; ⑥ 预计生存期>3个月; ⑦ 血常规、心肺肝肾功能基本正常,无重要器官功能障碍; ⑧ 签署知情同意书。排除标准: ① 妊娠及哺乳期妇女; ② 神经症状或控制不佳的脑部转移者; ③ 伴有其他恶性肿瘤,严重感染,出血性或精神疾病者; ④ 严重药物过敏者。将患者随机分为双药组37例和单药组35例,双药组男22例,女15例;年龄39~78岁,中位年龄52.5岁;鳞癌13例,腺癌21例,其他3例;TNM分期:ⅢB期16例,Ⅳ期21例。单药组男21例,女14例;年龄39~77岁,中位年龄51.7岁;鳞癌11例,腺癌21例,其他3例; TNM分期: ⅢB期14例,Ⅳ期21例。2组患者性别、年龄、TNM分期等一般资料比较差异无统计学意义(P>0.05), 具有可比性。
1.2 方法
单药组给予多西他赛注射液(江苏奥赛康药业股份有限公司)75 mg/m2, 静脉滴注,第1天。双药组给予多西他赛注射液75 mg/m2,静脉滴注,第1天; 顺铂注射液(江苏豪森药业股份有限公司)75 mg/m2, 水化后分3 d静脉滴注,第1~3天。21 d为1个周期, 2组至少接受2个周期的化疗。静脉滴注多西他赛前30 min, 给予异丙嗪25 mg, 肌肉注射;地塞米松10 mg和甲氰咪呱0.6 g, 静脉注射。化疗前,给予盐酸昂丹司琼预防呕吐,必要时给予粒细胞集落刺激因子(G-CSF)升白细胞治疗及营养支持等对症治疗。化疗前后,进行血常规、血生化、心电图、肝肾功能、CT或PET-CT等检查。
治疗2个周期后评价近期疗效,此后继续治疗,直至患者死亡或随访结束。随访采用门诊及住院复查、电话、信件等方式,随访截止于2014年5月。
1.3 疗效观察
治疗2个周期后评价近期疗效,并观察毒副反应的发生情况。至随访结束,观察患者无进展生存期(PFS)、生存期及1年生存率。
1.4 疗效评价
根据实体瘤的评价标准(RECIST)进行总体最佳疗效评价[5], 包括完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)。以至少治疗4周确认的(CR+PR)计算客观缓解率(ORR),以至少治疗4周确认的(CR+PR+SD)计算临床受益率(CBR)。按通用不良事件术语标准4.0版(CTCAE v4.03)评价不良反应[6]。
2结果
2.1 近期疗效
所有患者均完成2个周期治疗。单药组CR 0例,PR 13例,SD 12例,PD 10例,ORR为37.1%(13/35), CBR为71.4%(25/35)。双药组CR 1例,PR 14例,SD 14例,PD 8例,ORR为40.5%(15/37), CBR为78.4%(29/37)。2组ORR及CBR比较,差异均无统计学意义(P>0.05)。
2.2 远期疗效
双药组随访4.2~39.1个月,中位随访时间15.8个月;单药组随访3.5~38.8个月,中位随访时间14.4个月。双药组和单药组中位PFS分别为4.1个月和2.2个月,2组比较差异有统计学意义(P<0.05),而中位生存期(10.9个月、9.1个月)和1年生存率(37.8%、37.1%)比较差异均无统计学意义(P>0.05)。2组生存曲线比较见图1。

图1 2组Kaplan-Meier生存曲线比较
2.3 毒副反应
2组毒副反应主要包括贫血、中性粒细胞减少、血小板减少、发热性中性粒细胞减少、恶心、呕吐、腹泻、乏力和周围神经病变。双药组除腹泻总发生率显著高于单药组外(P<0.01),其余毒副反应发生率与单药组比较差异均无统计学意义(P>0.05)。见表1。
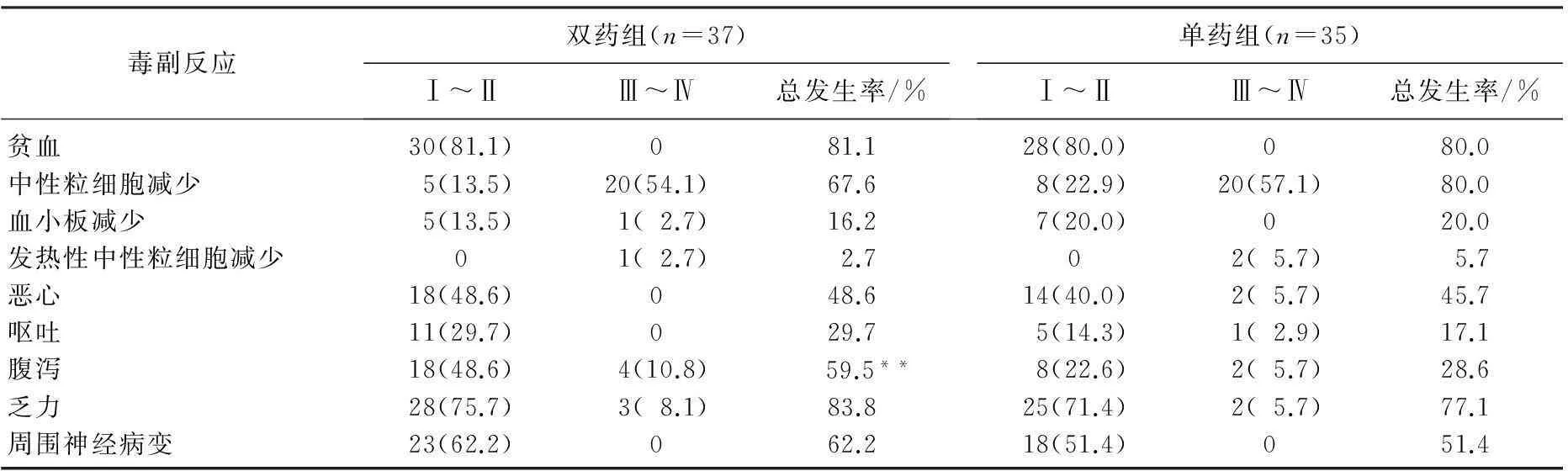
表1 2组毒副反应比较[n(%)]
与单药组比较,**P<0.01。
3讨论
目前,临床对于晚期NSCLC患者标准的一线治疗方案为以含铂类药物为基础的双药联合方案,疗效已被证实,且可明显改善患者预后,提高生存质量。但对于手术不可切除的晚期NSCLC患者,临床治愈希望渺茫,患者经过一线治疗后仍会出现PD。对于一线治疗后或治疗过程中发生病情进展的患者,是否接受二线治疗是决定预后的关键因素。多西他赛用于晚期NSCLC患者的二线治疗优于最佳支持治疗,且在目前标准的二线治疗方案中费用最低[7]。目前国内关于多西他赛用于二线治疗晚期NSCLC的研究较多,但关于联合铂类双药或单药方案的疗效及不良反应方面的研究较为有限。
多西他赛属于紫杉类抗肿瘤药物,其作用靶点为微管,通过结合微管蛋白来促进微管蛋白二聚物聚合,组成微管并抑制微管解聚,使肿瘤细胞分裂受阻,并停滞于G2和M期,从而抑制肿瘤增长[8]。有研究表明,多西他赛与微管蛋白结合的能力高出紫杉醇2倍,且与紫杉醇有不完全交叉耐药,即紫杉醇方案治疗失败的患者,应用多西他赛仍可有效[9-10]。铂类药物在NSCLC的治疗中有着重要地位,其通过与DNA单链内两点交叉联结,抑制DNA复制过程促使细胞凋亡[11]。大量临床试验已证实以铂类为基础的化疗方案的有效性,目前以普遍用于NSCLC一线化疗中。一项Meta分析纳入8项研究,以观察双药联合方案较单药方案在NSCLC二线治疗中的疗效,结果显示,双药方案较单药方案能显著提高ORR, 延长PFS, 但总生存期无显著改变[12]。但上述研究纳入的化疗方案包含多种形式,例如伊立替康、吉西他滨、培美曲塞等,可能存在较大的异质性。而国内的一项Meta分析纳入4项随机对照研究,将范围缩小为多西他赛/培美曲塞联合铂类双药对比多西他赛/培美曲塞单药用于晚期NSCLC二线治疗,结果显示双药方案能显著延长患者总生存期及PFS[13]。一项Ⅲ期随机对照研究表明,在NSCLC的二线治疗中,多西他赛联合卡铂方案较多西他赛单药方案能显著延长PFS,而在总生存期改善中并不显著[14]。本研究结果显示,双药组和单药组中位PFS分别为4.1个月和2.2个月, 2组比较差异有统计学意义,而中位生存期和1年生存率比较差异均无统计学意义,这与Athanasios等研究结果相似[14]。目前的研究均证实,双药方案并不能明显增加毒副反应[15]。本研究结果显示,双药组除腹泻总发生率显著高于单药组外,其余毒副反应发生率与单药组比较差异均无统计学意义,说明多西他赛联合顺铂双药方案并不能明显增加毒副反应。虽然临床已有较完善的化疗药物进行预处理,但在二线治疗中毒副反应仍是影响治疗进度及预后的一项重要因素。因此在治疗中要规范操作,及时发现并处理相关毒副反应。
参考文献
[1]胡兴胜, 焦顺昌, 张树才, 等. 培美曲塞及吉西他滨分别联合顺铂治疗初治晚期非小细胞肺癌安全性和有效性的随机对照研究[J]. 中国肺癌杂志, 2012, 15(10): 569.
[2]曹子昂. 2010年肺癌外科进展评述[J]. 中国医学前沿杂志: 电子版, 2011, 3(1): 42.
[3]Azzoli C G, Temin S, Aliff T, et al. 2011 Focused Update of 2009 American Society of Clinical Oncology Clinical Practice Guideline Update on Chemotherapy for Stage IV Non-Small-Cell Lung Cancer[J]. J Clin Oncol, 2011, 29(28): 3825.
[4]Garon E B, Ciuleanu T E, Arrieta O, et al. Ramucirumab plus docetaxel versus placebo plus docetaxel for second-line treatment of stage IV non-small-cell lung cancer after disease progression on platinum-based therapy (REVEL): a multicentre, double-blind, randomised phase 3 trial[J]. Lancet, 2014, 384(9944): 665.
[5]Nishino M, Jackman D M, Hatabu H, et al. New response evaluation criteria in solid tumors (RECIST) guidelines for advanced nonsmall cell lung cancer: comparison with original RECIST and impact on assessment of tumor response to targeted therapy[J]. AJR Am J Roentgenol. 2010, 195(3): 221.
[6]皋文君, 刘砚燕, 袁长蓉. 国际肿瘤化疗药物不良反应评价系统—通用不良反应术语标准4.0版[J]. 肿瘤, 2012, 32(2): 142.
[7]王泽阳, 侯梅, 王海燕, 等. 多西他赛单药与多西他赛联合顺铂二线治疗晚期非小细胞肺癌的疗效观察[J]. 现代预防医学, 2011, 38(9): 1754.
[8]刘睿, 宋文广, 张志, 等. 奈达铂联合多西他赛二线治疗晚期非小细胞肺癌的临床疗效观察[J]. 中国全科医学, 2013, 16(6): 670.
[9]Ramlau R, Gorbunova V, Ciuleanu T E, et al. Aflibercept and Docetaxel Versus Docetaxel Alone After Platinum Failure in Patients With Advanced or Metastatic Non-Small-Cell Lung Cancer: A Randomized, Controlled Phase III Trial[J]. J Clin Oncol, 2012, 30(29): 3640.
[10]Reck M, Kaiser R, Mellemgaard A, et al. Docetaxel plus nintedanib versus docetaxel plus placebo in patients with previously treated non-small-cell lung cancer (LUME-Lung 1): a phase 3, double-blind, randomised controlled trial[J]. Lancet Oncol, 2014, 15(2): 143.
[11]Petrelli F, Coinu A, Cabiddu M, et al. Platinum rechallenge in patients with advanced NSCLC: a pooled analysis[J]. Lung Cancer, 2013, 81(3): 337.
[12]Di Maio M, Chiodini P, Georgoulias V, et al. Meta-analysis of single-agent chemotherapy compared with combination chemotherapy as second-line treatment of advanced non-small-cell lung cancer[J]. J Clin Oncol, 2009, 27(11): 1836.
[13]赵晗君. 多西他赛/培美曲塞联合铂类双药方案对比单药方案二线治疗非小细胞肺癌的Meta分析[D]. 河北医科大学, 2014.
[14]Belvedere O, Follador A, Rossetto C, et al. A randomised phase II study of docetaxel/oxaliplatin and docetaxel in patients with previously treated non-small cell lung cancer: An Alpe-Adria Thoracic Oncology Multidisciplinary group trial (ATOM 019)[J]. Eur J Cancer, 2011, 47(11): 1653.
[15]贺建宇, 李士英, 徐卫明, 等. 多西他赛联合奥沙利铂、联合顺铂对晚期非小细胞肺癌化疗的临床研究[J]. 同济大学学报: 医学版, 2010, 31(6): 83.
基金项目:中国高校医学期刊临床专项资金(11520855)
收稿日期:2014-12-16
中图分类号:R 734.2
文献标志码:A
文章编号:1672-2353(2015)11-123-03
DOI:10.7619/jcmp.201511042

