碳基固体酸的制备及其催化合成碳酸甲丙酯
倪邦庆,贾国亮,范明明,王 辉
(江南大学化学与材料工程学院,江苏 无锡 214122)
不对称烷基碳酸酯被广泛应用在有机合成、化学溶剂、医药和农药等方面[1],碳酸甲丙酯(methyl propyl carbonate,MPC)是其中重要的一种不对称碳酸酯[2]。与同系列对称碳酸酯相比,MPC具有更高的闪点和极性,应用于锂离子电池的电解质溶剂时,其性能显著优于其它烷基碳酸酯[3]。研究者目前主要通过酯交换法合成不对称碳酸酯[4-9],其中碳酸二甲酯(dimethyl carbonate,DMC)与正丙醇酯交换法合成 MPC,生产路线绿色、清洁。原料DMC是一种无毒无腐蚀性的绿色环保原料,副产物甲醇可以循环利用合成 DMC,反应过程无三废产生。醇-酯酯交换法合成不对称碳酸酯的反应多为碱性物质催化的液相反应,碱催化通常可得到较高的原料转化率,却往往很难获得较好的选择性。文献报道高温气相的反应条件利于合成不对称碳酸酯,却存在反应设备复杂、原料汽化环节能耗较大等弊端,一定程度上使其应用受到限制[10-11]。
碳基固体酸催化剂是一种新兴的固体酸材料,主要应用在酯化、重排、水解和烷基化等反应[12-17]。与传统的固体酸催化剂比较,其原料价廉,制备过程简单,且具有酸密度高、耐热性好、结构稳定等优点,因此在绿色合成中具有很好的应用前景。目前,碳基固体酸催化剂在酯交换反应领域的研究鲜见报道。本文作者研究了碳基固体酸对DMC与正丙醇酯交换反应的催化活性,考察了 MPC合成工艺条件对催化剂活性的影响,用FT-IR、TGA等方法对催化剂进行了表征。
1 实验部分
1.1 主要试剂及仪器
无水葡萄糖、浓硫酸(质量分数为95%~98%,下同)、碳酸二甲酯、正丙醇、无水乙醇、丙酮(分析纯,国药集团化学试剂有限公司)。SX2-8-10型马弗炉(宜兴市精益电炉有限公司);FALA 2000-104傅里叶变换红外光谱仪(加拿大 Boman公司);C-9790型气相色谱仪(浙江温岭福立分析仪器有限公司)。
1.2 催化剂的制备
称取一定量的无水葡萄糖,在N2氛围中不完全碳化。对碳化产物进行粉碎过筛,与浓硫酸一并加入反应器中,N2保护下磺化,将磺化产物冷却至室温加去离子水稀释,冷却、抽滤、洗涤至滤液无SO42−检出。采用无水乙醇(60 ℃)洗涤滤饼至滤液无色,得到黑色固体粉末,在110 ℃下烘干即得磺化碳固体酸催化剂。
1.3 催化剂的表征
采用红外光谱仪对催化的结构进行鉴定;采用瑞士Mettler Toledo公司TGA/DSC1/1100SF型梅特勒热重分析仪对催化剂的热稳定性进行分析,升温速率为10 ℃/min。
1.4 碳酸二甲酯与正丙醇的酯交换反应
在装有温度计和回流装置的反应器中,按计量依次加入催化剂、DMC、正丙醇,升温至指定温度开动搅拌并计时。反应结束降温,将反应混合液离心处理后取上层清液准备气相色谱分析。
1.5 产物的分析检测
色谱柱为PEG-20M色谱柱,直径0.32 mm,长30 m,膜层0.3 μm。氢火焰离子化检测器,载气为工业用氮气,柱前压力0.1 MPa,分流比50∶1。汽化室温度250 ℃,检测器温度250 ℃。柱温采取程序升温:初温50 ℃,保持0.5 min,以20 ℃/min的速度升温至200 ℃,保持1 min,然后自然降温。进样量 0.2 µL。
2 结果与讨论
2.1 催化剂的表征
碳化材料和磺化材料的FT-IR光谱见图1。由图1可知,碳化材料经磺化后,在3386.7 cm−1附近出现一个宽吸收峰,这是—SO3H基团与C—H的吸收峰耦合形成。出现在 1716.52 cm−1、1606.58 cm−1处加强的吸收峰说明磺化过程使得碳材料的碳架结构发生变化。在1186.13 cm−1附近的吸收峰为—SO2—的不对称伸缩振动吸收峰,1033.77 cm−1处出现 S—O的伸缩振动吸收峰,在 621.03 cm−1处出现C—S的吸收峰,这些特征峰表明所制备的碳基固体酸催化剂具有—SO3H的结构[18]。
热稳定性分析结果如图2所示,催化剂在低于100 ℃时失重明显,主要原因是催化剂脱水所致。在100~200 ℃之间质量几乎不变,在200~300 ℃之间曲线平缓下降,这说明催化剂开始缓慢分解。由此说明200 ℃以下催化剂热力学性质较稳定。
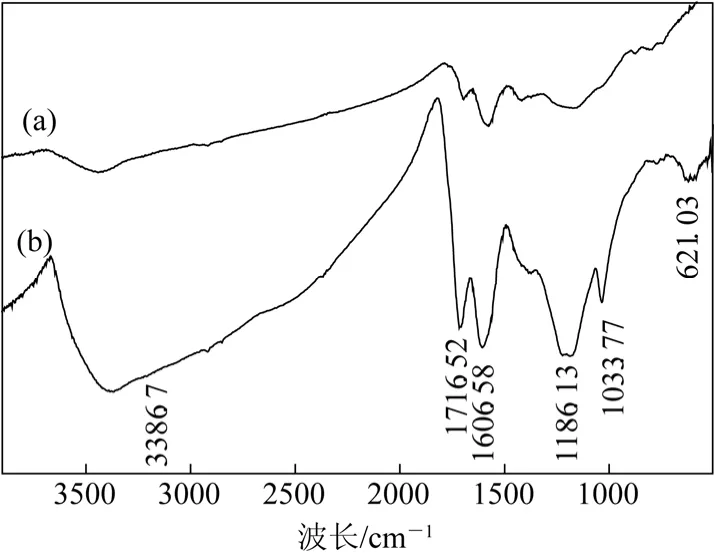
图1 碳化材料(a)和固体酸(b)的红外光谱图

图2 固体酸的TG曲线
2.2 催化剂制备条件对其活性的影响
催化剂活性通过催化碳酸二甲酯与正丙醇的酯交换反应的结果来评价,以碳酸甲丙酯的收率为指标。固定酯交换反应条件n(丙醇)∶n(DMC)=3∶1,反应温度90 ℃,反应时间8 h,催化剂用量占原料总质量10%不变,考察催化剂制备条件,如碳化温度、碳化时间、磺化温度、磺化时间、硫酸用量等因素对催化剂活性的影响。
2.2.1 碳化温度的影响
考察碳化温度对催化剂活性的影响,结果如图3所示。从图3中可以看出,碳化温度低于300 ℃或者高于350 ℃时,MPC的收率均较低。这是因为碳化温度过低,碳架结构不能充分地形成,导致碳材料在磺化反应后进行洗涤时与水和乙醇相溶;随着碳化温度的升高,碳架结构逐渐生成;碳化温度太高,碳材料易被过度碳化,使之后的磺化反应无法充分进行。碳化温度在300~350 ℃,MPC的收率和选择性变化不大,300 ℃条件下碳化产物的洗涤过程耗费过多乙醇,故选择碳化温度为350 ℃。
2.2.2 碳化时间的影响
考察碳化时间对催化剂活性的影响,结果如图4所示。由图4可知,当碳化时间为2 h时,MPC的收率达到最大;在此之后,随着碳化时间的延长,MPC的收率逐渐下降。碳化时间过短易导致碳材料的碳架结构形成不完全,在洗涤过程中部分流失;碳化时太长不利于后继磺化反应的进行。因此,选择碳化时间为2 h。
2.2.3 磺化温度的影响

图3 碳化温度对催化剂活性的影响
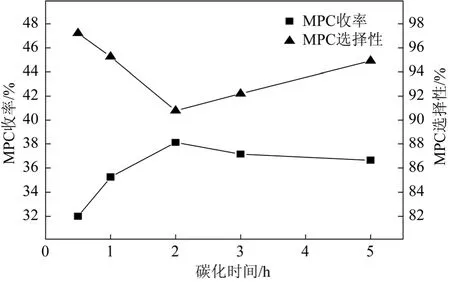
图4 碳化时间对催化剂活性的影响
考察磺化温度对催化剂活性的影响,结果如图5所示。可以看出,当磺化温度低于130 ℃时,随着磺化温度的逐渐升高,MPC的收率不断增大;磺化温度在130~150 ℃范围内,MPC的收率变化甚微;温度高于 150 ℃时,MPC的收率有明显的下降。这可能是因为磺化温度低于130 ℃时,温度升高磺化反应可以更充分地进行;但硫酸与碳载体接触时产生热量,温度过高阻碍了磺酸基团在碳架结构上的吸附,影响催化活性;当温度高于160 ℃会导致碳材料进一步发生碳化,干扰磺化反应的进行。最终选择磺化温度为130 ℃。
2.2.4 磺化时间的影响
考察磺化时间对催化剂活性的影响,结果如图6所示。由图6可知,随着磺化反应时间的延长,MPC的收率逐渐增加,而MPC的选择性逐渐下降。在磺化时间为10 h时,MPC的收率达到最大。图6中出现的变化趋势可能是因为磺化反应进行 10 h时,负载在碳架结构上的磺酸基团基本饱和,催化剂的酸密度基本不变。继续延长磺化时间,碳基固体酸催化剂的催化活性不会得到大幅度的提高。确定最佳的磺化时间为10 h。

图5 磺化温度对催化剂活性的影响
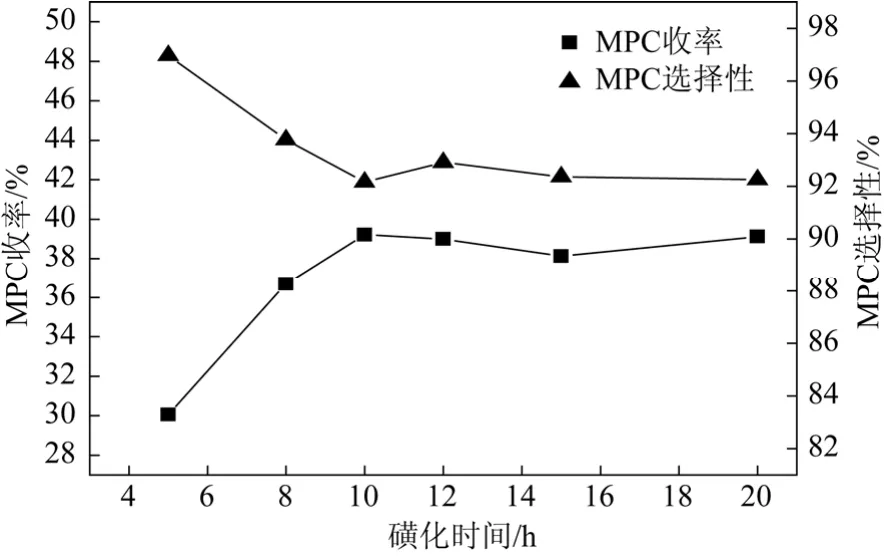
图6 磺化时间对催化剂活性的影响
2.2.5 浓硫酸用量的影响
考察浓硫酸用量对催化剂活性的影响,结果如图7所示。随着硫酸用量的增加,MPC的收率有大幅度地提高,当浓硫酸与碳化材料质量比达100∶1并继续增大时,MPC的收率几乎不变。原因可能是磺化过程中,加入的硫酸量越大,亲电基团越多,发生磺化反应的概率也越大,制备的碳基固体酸催化剂的酸密度也越大,催化活性就越好。当质量比达到100∶1以后,MPC的收率变化微小,表明制备的催化剂催化活性趋于稳定。实验表明,适宜的硫酸用量即浓硫酸与碳化材料质量比为100。
2.3 酯交换反应条件的优化
固定催化剂制备条件,如碳化温度350 ℃、碳化时间2 h、磺化温度130 ℃、磺化时间10 h、浓硫酸与碳材料的质量比100∶1等因素不变,优化碳酸二甲酯与正丙醇的酯交换反应工艺条件。以碳酸甲丙酯收率为评价指标,考察反应物摩尔比、反应温度、反应时间、催化剂用量、催化剂重复使用性能等因素对催化剂活性的影响。
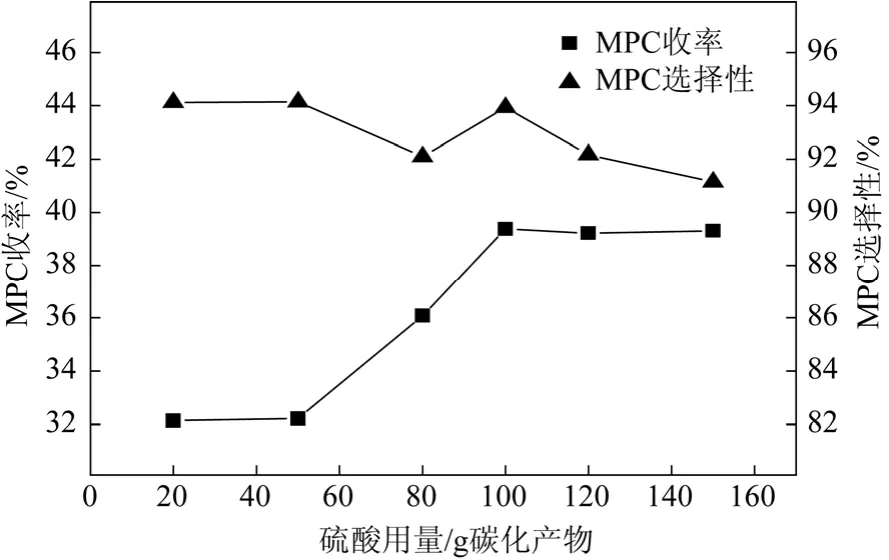
图7 硫酸用量对催化剂活性的影响
2.3.1 物料摩尔比的影响
考察物料摩尔比对催化剂活性的影响,结果如图8所示。当DMC和正丙醇的摩尔比高于1∶2时,MPC的收率随着物料摩尔比的增加而增大;当物料摩尔比达1∶4时,MPC的收率有所下降。造成这种变化趋势是由于合成 MPC的酯交换反应是一个平衡可逆反应,增加正丙醇的量有利于促进反应正向进行,从而提高MPC的收率;此外,生成的MPC继续与正丙醇反应生成碳酸二丙酯的反应,同样是平衡可逆反应,继续增加丙醇的量,MPC选择性下降,导致 MPC收率降低。结果表明,适宜的反应原料配比为n(DMC)∶n(正丙醇)=2∶1。
2.3.2 反应温度的影响
考察反应温度对催化剂活性的影响,结果如图9所示。当反应温度由60 ℃升至90 ℃,MPC的收率逐渐升高;当温度达到90 ℃时,MPC的收率达到最大;温度高于90 ℃,MPC的收率及其选择性均出现下降的趋势,适宜的反应温度为 90 ℃。分析可能的原因是:一方面反应温度的升高加快了反应平衡的移动,MPC收率上升;另一方面,温度高于 90 ℃时,较多 DMC被汽化回流,在液相中与催化剂接触的DMC的量开始减少,导致在高于DMC沸点的反应温度下,MPC的收率开始下降。
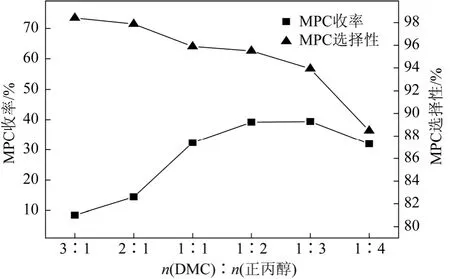
图8 原料摩尔比n(DMC)∶n(正丙醇)对酯交换反应的影响

图9 反应温度对酯交换反应的影响
2.3.3 反应时间的影响
考察反应时间对催化剂活性的影响,结果如图10所示。由图10可知,DMC的转化率随反应时间的增加而逐渐升高,而MPC的选择性则逐渐降低。反应从2 h进行到4 h过程中,MPC的收率增加明显,同时 MPC的选择性快速下降。这可能是由于反应初期反应物浓度较大,有利于主反应的正向进行,随着反应的推进,生成的 MPC部分与正丙醇进一步反应或相互歧化生成了副产物碳酸二丙酯,从而导致选择性下降。反应5 h后,MPC收率在略微下降后几乎保持不变,这可能是因为此时生成和消耗 MPC的速率达到平衡,继续反应可能会造成MPC选择性的下降。因此反应时间选择5 h。
2.3.4 催化剂用量的影响
考察催化剂用量对催化剂活性的影响,结果如图11所示。如图11所示,催化剂用量对酯交换反应中 MPC的收率及其选择性影响较显著。催化剂的用量从2%(基于总反应物质量,下同)升至4%的过程中,MPC的收率不断增加,选择性则先下降后上升,当加入催化剂的质量占总反应物质量的4%时,MPC的收率较高,超过4%以后,MPC的收率增加有限,故确定较适宜的催化剂用量为4%。
2.3.5 催化剂的稳定性

图10 反应时间对酯交换反应的影响

图11 催化剂用量对酯交换反应的影响

表1 催化剂重复使用性能
考察催化剂的重复使用性能。将回收的催化剂多次洗涤、烘干参与反应,结果如表1所示。催化剂使用4次后,MPC的收率开始下降,而MPC的选择性则逐步加强。出现这种变化可能的原因是在反应过程中,催化剂中的—SO3H的损失,使得催化剂的活性位减少,催化剂的催化性能下降,从而导致 MPC的收率下降。实验结果证明,将反应后的液体浓缩后进行红外分析,发现有—SO3H的特征吸收峰,对失活的催化剂再次进行磺化,催化剂基本恢复催化活性,从而验证了—SO3H流失的猜想。
3 结 论
以葡萄糖为碳化材料、浓度为95%~98%的浓硫酸为磺化试剂,制备出了碳基固体酸催化剂。将其应用于DMC与正丙醇的酯交换反应,表现出了有较优的催化性能。
(1)采用单因素实验优化得到适宜的碳基固体酸催化剂的制备条件为:碳化温度为350 ℃、碳化时间为2 h、磺化温度为130 ℃、磺化时间为10 h、浓硫酸与不完全碳化物的质量比为100∶1。
(2)将制备的碳基固体酸催化剂用于DMC与正丙醇的酯交换合成 MPC的反应,当反应原料正丙醇与DMC摩尔比为2∶1、反应温度为90 ℃、反应时间为5 h及催化剂用量为4%的条件下,MPC的收率达到40%左右,选择性超过90%。
(3)由红外结构表征和热分析结果可知,所制备的碳基固体酸催化剂具有—SO3H的结构,200℃以下催化剂热力学性质较稳定。催化剂循环利用实验表明,催化剂失活的主要原因是反应过程中—SO3H结构的部分流失,再次磺化处理后,催化剂基本恢复活性。
[1] 姚杰,王越,曾毅,等. 合成碳酸甲丙酯的研究进展[J]. 天然气化工,2004,29(1):57-59.
[2] Ein-Eli Y,Mc Devitt S Y,Aurbach D,et a1.Methyl propyl carbonate:A promising single solvent for li-ion battery electrolytes[J].Electrocute Soc.,1997,144(7):180-184.
[3] Gan H,Marcus J P,Esther S T. Method of synthesizing unsymmetric organic carbonates and preparing nonaqueous electrolytes for alkali ion electrochemical cells:US,5962720[P].1999-10-05.
[4] Inaba Masashi,Hasagawa Katsuaki,Suzuki Takemichi. Production of asymmetric carbonate compound:JP,10237026[P]. 1998-09-08.
[5] 赵春香,陈兴权,赵天生. 气相酯交换法合成碳酸甲丙酯负载型催化剂的研究[J]. 高等化学工程学报,2006,20(3):374-378.
[6] 陈英,韩金玉,刘艳平. 固体碱催化剂上碳酸甲乙酯的洁净合成[J]. 天津大学学报,2007,40(3):285-288.
[7] 柳娜,薛冰,李永昕,等. K2CO3/MgO催化合成碳酸乙丙酯[J]. 石油化工,2009,38(9):989-993.
[8] Abbas-Alli G S. Swaminathan & organic carhonstes[J].Chem. Rev.,1996,96(3):1951-976.
[9] 宋军超,赵天生,马清祥,等. MgO/γ-Al2O3催化酯交换合成碳酸甲丁酯[J]. 精细石油化工,2007,24(6):8-10.
[10] 赵春香,赵天生,丁永杰. DMC和丙醇酯交换合成MPC反应的热力学分析[J]. 天然气化工,2008,33(3):19-25.
[11] Kim W B,lee J S.A new process for the synthesis of dipenyl carbonate from dimethy1 carbonate and phenol over heterogeneous catalysts[J].Catal. Lett.,1999,59(1):83-88.
[12] Takagaki A,Toda M,Okamura M,et al. Esterification of higher fatty acids by a novel strong solid acid[J].Catal. Today,2006,116(2):157-161.
[13] Toda M,Takagaki A,Okamura M,et al. Biodiesel made with sugar catalyst[J].Nature,2005,438(10):178-179.
[14] Hara M,Yoshida T,Takagaki A. A carbon material as a strong protonic acid[J].Angewandte Chemie InternationalEdition,2004,43(22):2955-2958.
[15] Nakajima K,Tomita I,Hara M,et al. A stable and highly active hybrid mesoporous solid acid catalyst[J].Adv. Mater.,2005,17(15):1839-1842.
[16] Nakajima K,Tomita I,Hara M,et al. Development of highly active SO3H-modified hybrid mesoporous catalyst[J].Catal. Today,2006,116(2):151-156.
[17] Toda M,Takagaki A,Okamura M,et al. Biodiesel made with sugar catalyst[J].Nature,2005,438(10):178-179.
[18] 王艺娟. 新型固体酸制备与应用中的红外光谱表征[D]. 湖南:湖南师范大学,2007.

