系统性硬化症肺部受累患者临床及影像学特点分析
周晓明,侯 刚,叶 蕊,冯学威,赵 立
系统性硬化症(systemic sclerosis,SSc)是以细胞外基质过度沉积、微血管闭塞、体液免疫和细胞免疫异常为特征的系统性结缔组织病[1]。呼吸系统常受累,主要表现为间质性肺疾病和肺动脉高压,这二者是SSc患者主要的死亡原因[2-3]。尽管随着诊治手段的提高SSc患者的生存期有所延长,但由于肺纤维化所导致的病死率从6%增长到33%[4]。因此,及早发现肺脏受累对SSc患者的早期干预及改善预后具有重要的价值。为此,本研究通过总结SSc肺部受累患者的临床及影像学特点,提高临床医生对SSc肺间质及肺血管受累的认识。
1 资料与方法
1.1一般资料收集我院2009—2011年呼吸内科及风湿免疫科明确诊断的SSc患者43例,均符合1980年美国风湿病学会关于SSc的诊断标准[5]。其中女34例,男9例,女∶男为3.78∶1;平均年龄(59.7±18.8)岁。
1.2方法回顾性分析43例患者的临床表现,包括SSc的临床表现及肺部受累的表现,根据临床表现对SSc进行分型:(1)弥漫型SSc(弥漫性硬皮病):对称性的四肢、面部皮肤变紧,变硬,变厚,可累及四肢近端、颈部及躯干,同时伴有胃肠道、肾脏、肺部、心脏等内脏损害;(2)局限型SSc(肢端硬化症):皮肤改变局限于肢体远端如手指、前臂、下肢远端及颜面,出现上述部位对称性的皮肤变紧,变硬,变厚,伴有雷诺现象[1]。然后结合肺高分辨体层扫描(high resolution computed tomography,HRCT)及心脏超声检查评估肺间质及肺动脉受累情况,并比较弥漫型和局限型SSc患者肺间质及肺动脉受累情况的差异,总结SSc患者肺部受累的临床及影像学特点。
肺HRCT采用Siemens Definition 64排螺旋CT平扫,自肺底向肺尖扫描,扫描间距8 mm,层厚2 mm。采用Philip 2D经胸心脏超声(S5-1探头)进行超声心动图检查,肺动脉高压严重程度判断标准:轻度,35 mm Hg(1 mm Hg=0.133 kPa)<肺动脉收缩压(PASP)≤50 mm Hg;中度,50 mm Hg
1.3统计学方法采用SPSS 17.0软件进行统计检验。计数资料用百分率表示,两组间率的比较采用四格表χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1临床表现43例患者中,局限型SSc 22例(51.2%),弥漫型SSc 21例(占48.8%)。
2.1.1呼吸系统症状43例患者中,19例(44.2%)出现呼吸系统症状,以活动后气促(19例)和咳嗽(10例)最常见,其次为咳痰(8例)、呼吸困难(8例)、胸痛(1例)。7例(16.3%)以呼吸道症状为首发症状就诊。
2.1.2周身表现43例(100.0%)均有肢端硬化症状,21例(48.8%)有躯干皮肤硬化症;32例(74.4%)出现雷诺现象;1例(2.3%)出现CREST综合征。
2.2肺间质和肺动脉受累情况以及影像学表现43例患者中,肺HRCT检查证实30例(69.8%)存在间质性肺疾病,其中40.0%(12/30)的患者无呼吸系统症状。
HRCT表现以磨玻璃影(51.2%)和网格影(37.2%)最常见(见表1);分布以双下肺(48.8%,21/43)及胸膜下(55.8%,24/43)分布为主,弥漫性分布14例(32.6%)。
43例患者中,心脏超声检测出10例(23.3%)并发肺动脉高压,其中轻度肺动脉高压1例,中度肺动脉高压5例,重度肺动脉高压4例。
2.3弥漫型和局限型SSc患者肺部受累情况比较弥漫型和局限型SSc患者雷诺现象、肺动脉高压的发生率比较,差异均无统计学意义(P>0.05);而间质性肺疾病的发生率间差异有统计学意义(P<0.05,见表2)。
有雷诺现象的患者其肺动脉高压的发生率(31.2%,10/32)高于无雷诺现象者(0),差异有统计学意义(χ2=4.48,P<0.05)。
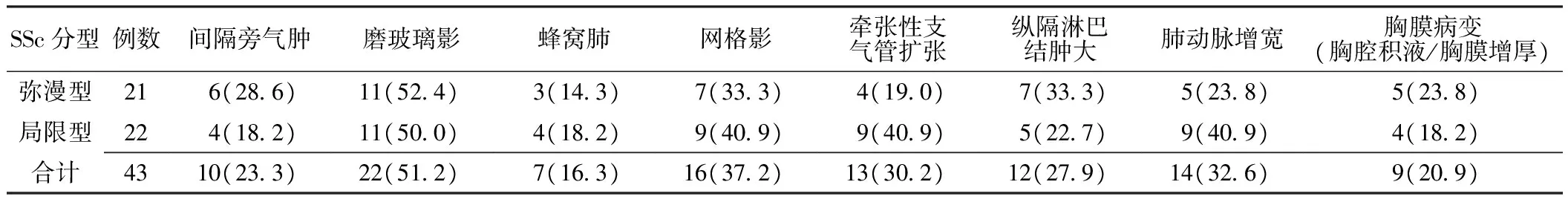
表1 弥漫型和局限型SSc患者肺HRCT表现〔n(%)〕Table 1 High resolution computerized tomography manifestations of systemic sclerosis in patients with diffusive or limited systemic sclerosis
表2弥漫型和局限型SSc患者肺部受累情况比较〔n(%)〕
Table2Comparison of the pulmonary involvement in patients with diffusive or limited systemic sclerosis
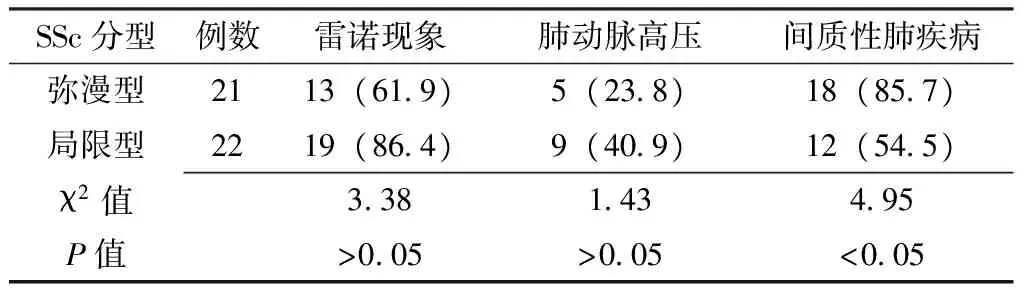
SSc分型例数雷诺现象肺动脉高压间质性肺疾病弥漫型2113(61 9)5(23 8)18(85 7)局限型2219(86 4)9(40 9)12(54 5)χ2值3 381 434 95P值>0 05>0 05<0 05
3 讨论
SSc是一类多系统受累的自身免疫性疾病,目前病因不清楚,女性发病率高,女∶男为(3~6)∶1[2]。本病起病隐匿,当出现典型的皮肤受累时往往丧失了早期治疗的最佳时机。另外,肺部受累也是SSc常见的临床表现,其中间质性肺疾病的发生率在19%~47%[2,7],肺动脉高压的发生率为9.9%[7]。肺部受累是SSc患者病死的重要影响因素,但肺部受累患者的呼吸系统症状也较隐匿。本研究结果显示,30例影像学证实肺间质受累的患者中有40.0%的患者无呼吸系统症状,与以往研究结果相似[2,7],因此早期诊断SSc和发现肺部受累对早期治疗和改善患者预后具有重要的意义。
对于SSc的早期诊断应重视雷诺现象,本研究中74.4%的患者具有雷诺现象,但弥漫型和局限型SSc患者雷诺现象发生率间无显著差异,这与Akesson等[8]的研究相一致。另外,本研究结果显示,具有雷诺现象的患者其肺动脉高压的发生率显著高于无雷诺现象的患者,说明一旦出现雷诺现象,则提示全身微血管受累。有研究报道无论是SSc伴随继发性雷诺现象还是原发性雷诺现象时,SSc患者体内内皮素-1(ET-1)水平均显著升高,提示微血管受累,且继发性雷诺现象的病程与机体ET-1水平增高呈正相关[9]。另外,前瞻性研究显示雷诺现象的出现可早于皮肤改变,有雷诺现象者数年后可出现典型的SSc皮肤改变[10]。基于上述情况,雷诺现象是早期诊断SSc的重要指标。2010年欧洲硬皮病组织提出早期诊断硬皮病的指标中雷诺现象是主要标准,且雷诺现象的病程是SSc重要的死亡预测因子之一[11]。
早期评估肺部受累主要依靠客观检查,因为呼吸系统症状是非特异性的,而且很多肺部受累者并无相应的呼吸系统症状。本组资料显示,43例SSc患者中仅44.2%的患者出现呼吸系统症状,而肺HRCT检查出69.8%的患者存在间质性肺疾病。本研究中弥漫型SSc患者间质性肺疾病发生率显著高于局限型,但两种类型的患者雷诺现象、肺动脉高压的发生率间无显著差异。这与2009年德国学者基于1 200例SSc患者所得出的研究结果相一致,他们发现无论患者皮肤受累情况是弥漫型还是局限型,患者的肺动脉高压发生情况是一致的,但该研究未评价肺间质受累情况[11]。本研究结果显示,肺部受累患者的HRCT最常见表现为磨玻璃影和网格影,主要出现在双下肺和胸膜下,还可出现牵张性支气管扩张、索条影及蜂窝肺,这与多项研究的结果相一致[12-13]。而胸膜下分布的磨玻璃影及网格影常提示患者存在非特异性间质性肺炎(non-specific interstitial pneumonia,NSIP)[14]。故应该对肺HRCT出现磨玻璃影给予重视,因为肺HRCT存在磨玻璃影也是早期诊断SSc的指标之一。磨玻璃影提示病变存在可逆转的可能,对糖皮质激素或细胞毒药物的敏感性高[15]。因此,对有雷诺症状的患者检测肺HRCT有利于早期诊断SSc,而对确诊的SSc患者定期检查肺HRCT有利于早期发现肺脏受累,尤其是弥漫型SSc患者,因为弥漫型SSc患者更易并发间质性肺炎[16]。此外,定期进行肺功能检查也是必要的,有研究显示肺功能检查对肺间质受累的诊断具有较高的敏感性,而且该项检查无创、无辐射,简单易行,应作为SSc患者随访的常规检查项目[13]。
肺动脉高压是临床工作中重点关注的另一个肺部受累的表现,肺动脉高压一旦出现将严重影响患者的预后,而且治疗支出可能大幅度增加。肺动脉高压可出现于疾病的任一时期,且与其他结缔组织病相关的肺动脉高压相比,SSc相关性肺动脉高压的脑钠肽(brain natric peptide,BNP)水平最高,1年后生存率最低,是一种相对独立的肺动脉高压类型。本研究采用超声心动图检查发现23.3%的SSc患者存在肺动脉高压,但需要注意的是如果条件允许,对患者进行有创的肺动脉压检测的同时进行急性血管反应试验,以确诊和评估肺动脉高压的严重程度及对钙离子拮抗剂的治疗反应,而超声心动图只是作为该人群肺动脉高压的筛查工具。
综上所述,SSc患者的肺部受累多见,尤其在弥漫型患者中,其症状隐匿且不具备特异性。雷诺现象是SSc的常见症状,可先于皮肤改变出现,是早期诊断SSc的重要指标。肺HRCT较呼吸系统症状更灵敏地发现肺部受累,而且对评价疾病严重程度及判断治疗反应有一定的帮助,是早期发现SSc肺部受累的重要手段。另外,定期的心脏超声检测有利于早期发现肺动脉高压。故重视SSc患者的临床及影像系统评估,将使SSc的早期诊断成为可能,有利于患者的及时诊治。
1Wollheim FA.Classification of systemic sclerosis.Visions and reality[J].Rheumatology(Oxford),2005,44(10):1212-1216.
2Wells AU,Steen V,Valentini G.Pulmonary complications:one of the most challenging complications of systemic sclerosis[J].Rheumatology(Oxford),2009,48(Suppl 3):40-44.
3Le Pavec J,Humbert M,Mouthon L,et al.Systemic sclerosis-associated pulmonary arterial hypertension[J].Am J Respir Crit Care Med,2010,181(12):1285-1293.
4Ioannidis JP,Vlachoyiannopoulos PG,Haidich AB,et al.Mortality in systemic sclerosis:an international meta-analysis of individual patient data[J].Am J Med,2005,118(1):2-10.
5American Rheumatism Association.Preliminary criteria for the classification of systemic sclerosis(scleroderma).Subcommittee for scleroderma criteria of the American Rheumatism Association Diagnostic and Therapeutic Criteria Committee[J].Arthritis Rheum,1980,23(5):581-590.
6Nakanishi N,European Society of Cardiology,European Respiratory Society.2009 ESC/ERS pulmonary hypertension guidelines and connective tissue disease[J].Allergol Int,2011,60(4):419-424.
7Vonk MC,Broers B,Heijdra YF,et al.Systemic sclerosis and its pulmonary complications in the Netherlands:an epidemiological study[J].Ann Rheum Dis,2009,68(6):961-965.
8Akesson A,Wollheim FA.Organ manifestations in 100 patients with progressive systemic sclerosis:a comparison between the CREST syndrome and diffuse scleroderma[J].Br J Rheumatol,1989,28(4):281-286.
9Sulli A,Soldano S,Pizzorni C,et al.Raynaud′s phenomenon and plasma endothelin:correlations with capillaroscopic patterns in systemic sclerosis[J].J Rheumatol,2009,36(6):1235-1239.
10Czirják L,Matucci-Cerinic M.Beyond Raynaud′s phenomenon hides very early systemic sclerosis:the assessment of organ involvement is always mandatory[J].Rheumatology(Oxford),2011,50(2):250-251.
11Tyndall AJ,Bannert B,Vonk M,et al.Causes and risk factors for death in systemic sclerosis:a study from the EULAR Scleroderma Trials and Research(EUSTAR) database[J].Ann Rheum Dis,2010,69(10):1809-1815.
12Hanitsch LG,Burmester GR,Witt C,et al.Skin sclerosis is only of limited value to identify SSc patients with severe manifestations-an analysis of a distinct patient subgroup of the German Systemic Sclerosis Network(DNSS) Register[J].Rheumatology,2009,48(1):70-73.
13彭敏,许文兵,施举红,等.系统性硬化症的肺部表现[J].中国呼吸与危重监护杂志,2011,10(4):386-390.
14Goldin JG,Lynch DA,Strollo DC,et al.High-resolution CT scan findings in patients with symptomatic scleroderma-related interstitial lung disease[J].Chest,2008,134(2):358-367.
15De Lauretis A,Veeraraghavan S,Renzoni E.Review series:aspects of interstitial lung disease:connective tissue disease-associated interstitial lung disease:how does it differ from IPF? How should the clinical approach differ?[J].Chron Respir Dis,2011,8(1):53-82.
16Roth MD,Tseng CH,Clements PJ,et al.Predicting treatment outcomes and responder subsets in scleroderma-related interstitial lung disease[J].Arthritis Rheum,2011,63(9):2797-2808.

