谷胱甘肽包被的CdTe量子点作为荧光探针测定微量银
董微,王莹,宋有涛,董焱,周巳琪,曹智星
(1.沈阳医学院基础医学院化学教研室,辽宁 沈阳 110034;2.辽宁大学生命科学院动物资源与疫病防治重点实验室;3.沈阳药科大学中药学院实验中心;4.沈阳医学院奉天医院重症医学科;5.沈阳医学院沈洲医院医保科)
金属离子的高灵敏检测一直是离子探针领域研究的热点。目前已经有很多有机染料成功应用于金属离子的检测。但是有机染料自身具有局限性,如激发光谱窄、发射光谱宽、容易光漂白等缺点[1]。量子点(quantum dots,QDs)是一种半径小于或接近于激子玻尔半径的新型半导体纳米材料,与传统有机荧光染料相比,QDs具有量子产率高,抗漂白能力强,光化学稳定性好等优良特性[2-3],是一种很有发展潜力的荧光探针。
目前应用于银离子检测的方法有原子吸收分光光度法、电感耦合等离子体发射光谱法(inductively coupled plasma atomic emission spectrometry,ICP-AES)、电感耦合等离子体质谱法(inductively coupled plasma mass spectrometry,ICP-MS)[4-6]等。本文采用谷胱甘肽包被的水溶性CdTe QDs,基于银离子对其荧光有猝灭作用,建立了一种以CdTe QDs为离子探针测定微量银的新方法,并成功应用于实体水样中银离子的检测报告如下。
1 实验部分
1.1 仪器与试剂 LS-55 荧光光度计(Perkin Elmer);DF-101S集热式恒温加热磁力搅拌器(巩义市英峪予华公司);D-37520 型高速冷冻离心机(Sorvall Biofuge Stratos);Sartorius 普及型pH计(北京赛多利斯仪器系统有限公司);TH-500A梯度混合器(上海青浦沪西仪器厂)。
碲粉(Te 99.999%,国药化学试剂公司);硼氢化钠(NaBH4,96%国药集团化学试剂有限公司);氯化镉(CdCl2·2.5H2O)(国药化学试剂公司);还原型谷胱甘肽(国药集团化学试剂有限公司);磷酸和Tris缓冲溶液。
Ag+标准储备液:精密称定AgNO3适量,用去离子水溶解,转移至容量瓶中,定容,摇匀,用时稀释至所用浓度。
水样:沈阳医学院实验室自来水。
1.2 实验方法
1.2.1 CdTe QDs的合成 利用硼氢化钠的强还原性,将碲粉还原成碲氢化钠。将氯化镉和谷胱甘肽溶于三蒸水中,调节混合液的pH值使其在9~10,通入氮气脱氧30 min。然后加入1 ml新制备的碲氢化钠溶液,加热搅拌温度达到100 ℃时,回流2 h,得到橙色QDs溶液,并对其进行荧光性能的表征。
1.2.2 Ag+检测方法 向5 ml比色管中加入一定体积合适浓度的QDs溶液和一定浓度的缓冲溶液,再分别加入不同体积的Ag+标准液,用去离子水定容,摇匀,待反应完全,为待测液,用荧光光度计测定其荧光强度(I)。另准备试剂空白,不加Ag+标准液,测定其荧光强度(I0)。
2 结果与讨论
2.1 CdTe QDs的表征 本实验采用谷胱甘肽作为稳定剂,而谷胱甘肽分子上具有多个可以与纳米粒子表面的Cd2+离子配位的位点,在CdTe QDs表面具有很强的配位作用,为在水溶液中合成具有较高量子效率的QDs提供了可能。图1可见,所合成的CdTe QDs在575 nm具有窄而对称的荧光发射峰,其紫外可见吸收光谱在395 nm具有明显的吸收峰,表明所合成的QDs粒径分布比较均一。
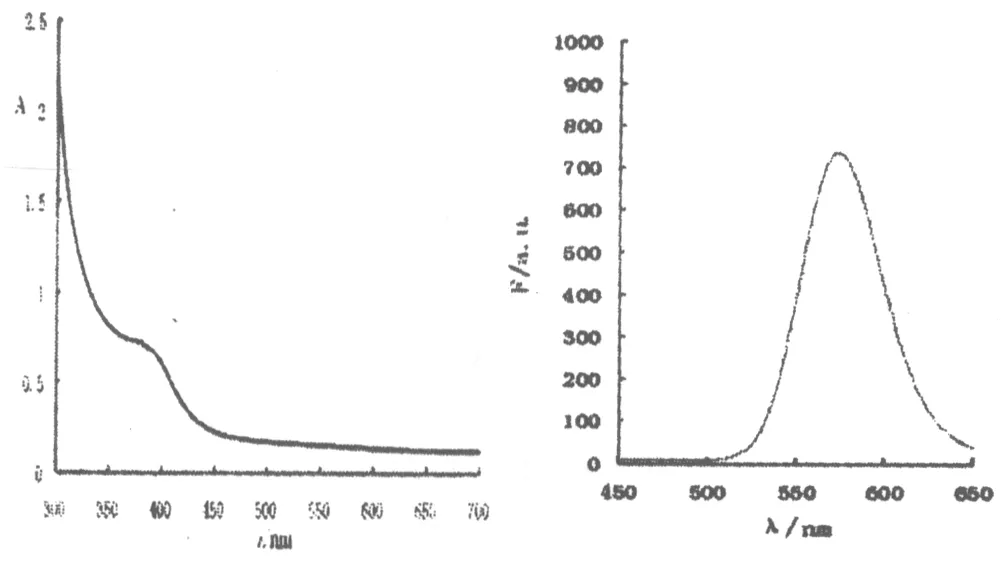
图1 CdTe QDs的吸收(左)和荧光(右)光谱图
2.2 QDs浓度的选择 QDs浓度是影响本方法灵敏度和线性范围的关键因素。当反应体系中QDs浓度过高时,加入少量Ag+,体系的荧光强度有较小程度的猝灭,分析的灵敏度低;当反应体系中QDs浓度过低时,体系的荧光强度猝灭程度变大,灵敏度较高,但线性范围窄。如图2所示,本实验考察了相同浓度Ag+溶液对不同浓度QDs的荧光猝灭情况,综合考虑,选取最佳的QDs浓度为0.004 g/L,在此浓度下,荧光的猝灭程度较大,线性范围较宽。
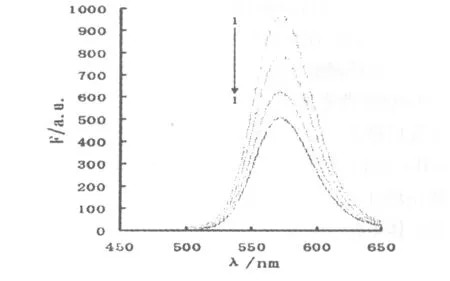
图2 QDs浓度的影响
曲线1~4QDs浓度分别为0.006,0.004,0.003,0.002 g/L
2.3 缓冲溶液种类、pH值和浓度的选择 本文考察了2种缓冲体系,即磷酸缓冲溶液(PBS,Na2HPO4+KH2PO4)和Tris缓冲溶液(Tris+HCl)对QDs荧光强度的影响。结果表明,PBS缓冲溶液更适合作为缓冲介质。由于水相合成的CdTe QDs表面性质与pH值的变化紧密相关,实验进一步探讨了不同pH值(5.5~9.0)的磷酸缓冲液对体系荧光强度的影响。结果表明,随着pH值的升高,QDs的荧光强度逐渐增强,当pH值达到7.0左右时,体系的荧光强度最强且趋于稳定,这为QDs与Ag+作用提供了宽而稳定的pH范围。为方便配制,本实验选择在pH值为7.4的PBS缓冲体系中进行测定。同时进一步考察了PBS缓冲液浓度对体系荧光强度的影响,结果如图3所示,在不同浓度的PBS缓冲溶液 (0.000 1~0.000 7 mol/L)中体系的荧光强度存在明显差异。当缓冲液浓度增大时,体系的荧光强度减小,所以本实验选择的PBS缓冲液浓度为0.000 1 mol/L。
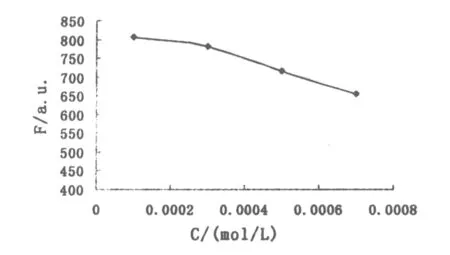
图3 PBS缓冲溶液浓度的影响
2.4 反应温度及反应时间的选择 结果表明反应温度对体系荧光强度的影响不大,本实验选择在室温条件下进行测定。在室温条件下研究了反应时间对体系的荧光强度稳定性的影响,实验结果表明,Ag+与CdTe QDs的作用在5 min后趋于稳定,可保持40 min,说明该体系反应快速且稳定,因此选择反应5 min后进行测定。
2.5 Ag+浓度对CdTe QDs荧光强度的影响 如图4所示,CdTe QDs的荧光强度随Ag+浓度的增大而减小,并伴随有9 nm左右的发射峰位的红移。这种CdTe QDs荧光强度逐渐下降的趋势在Ag+达到一定浓度后停止。CdTe QDs荧光猝灭可能是由于Ag+与CdTe表面的结合位点发生配位导致的,其发射峰位置出现红移则可能是由于Ag+与CdTe QDs结合之后,体系的总能量低于单独的CdTe QDs所致[7]。

图4 Ag+浓度对CdTe量子点荧光强度的影响
曲线1~5的Ag+浓度分别为0,25.06,49.68,74.30,98.60 μg/L
2.6 共存离子的影响 考察了多种干扰离子对Ag+测定结果的影响。结果表明,在测定的相对误差为±5%范围内,下列离子(倍数):K+、Na+、Mg2+、Mn2+、Zn2+(200),Ca2+、Co3+、Al3+(50)对测定无干扰,Fe3+、Cu2+对测定有干扰;Fe3+、Cu2+可加入F-和氨水加以掩蔽。
2.7 线性范围和检出限 在最佳的实验条件下,当Ag+浓度在25.06~98.60 μg/L范围内时,体系的荧光猝灭程度与Ag+浓度呈现良好线性关系,结果如图5所示。其线性方程为ΔI=I0-I=26.07+7.01c(c为Ag+的质量浓度,单位为μg/L),线性相关系数为0.995 7。根据公式:LOD=3S0/K(其中LOD为检出限;S0为空白对照的相对标准偏差;K为校准标准曲线的斜率)算出此方法检测Ag+的检出限为0.15 μg/L。分别对浓度为25.06,49.68,74.30 μg/L的Ag+标准溶液平行测定6次,相对标准偏差分别为0.97%,0.82%,1.06%,表明本方法精密度良好。

图5 Ag+的标准曲线
3 样品分析
取采集的实验室用自来水代替Ag+标准液加入体系中,按照上述Ag+测定方法,进行加标回收实验,取2 500 μl样品溶液于5 ml比色管中,再分别加入20 μl,25 μl,30 μl上述Ag+溶液,测定荧光强度,平行测定6次,计算相对标准偏差。实验结果显示(表1),本法测定的精密度和回收率均符合微量分析要求。
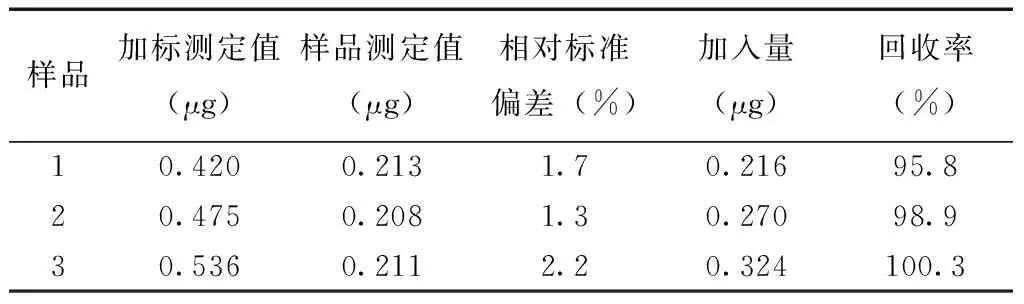
表1 样品分析结果
参考文献:
[1]Mattoussi H,Mauro JM,Goldman ER,et al.Self-assembly of CdSe-ZnS quantum dots bioconjugates using an engineered recombinant protein[J].Am Chem Soc,2000,122:12142-12150.
[2]Li MY,Ge YX,Chen QF,et al.Hydrothermal synthesis of highly luminescent CdTe quantum dots by adjusting precursors’ concentration and their conjunction with BSA as biological fluorescent probes[J].Talanta,2007,72:89-94.
[3]Bruchez M J,Moronne M,Alivisatos A P,et al.Semiconductor nanocrystals as fluorescent biological labels[J].Science,1998,281(5385): 2013-2016.
[4]金宜纫,马荣生.原子吸收分光光度法测定抗癌新药卡铂中痕量元素银的含量[J].微量元素与健康,1993,10(3):34-35.
[5]李光俐,徐光,何姣,等.ICP-AES法测定抗癌药物奥沙利铂中微量银、钯、镉[J].贵金属,2009,30(3):34-36.
[6]童成举,刘涛,魏振宏.ICP-MS测定污水中银的含量[J].光谱实验室,2010,27(5): 1844-1846.
[7]Kim YJ ,Johnson RC ,Hupp JT.Gold nanoparticle based sensing of “spectroscopically silent ”heavy metal ions [J].Nano Lett,2001,1 : 165-167.

