首发未服药的精神分裂症患者多导睡眠图特征
王俊清 林以环 江丽芸 翁壁兰 许崇涛 卓永宁 章杰 陈曲亮
首发未服药的精神分裂症患者多导睡眠图特征
王俊清*林以环*江丽芸*翁壁兰*许崇涛*卓永宁*章杰*陈曲亮*
目的 探索首次发病的精神分裂症患者多导睡眠图(Polysomnography PSG)的特征。方法 对22例首发精神分裂症患者和18名正常对照进行整夜PSG监测,采用匹兹堡睡眠质量指数量表评估主观睡眠,比较两组PSG及主客观睡眠的差异。结果 与对照组比较,患者组表现入睡潜伏期延长[(67.26±13.02)min vs(28.73±10.47)min],总睡眠时间减少[(271.46±25.14)min vs(357.81±22.83)min]、睡眠效率下降[(61.58±11.62)vs(89.71±9.44)]、睡眠期觉醒时间[(67.84±13.76)min vs(26.94±8.67)min]和觉醒次数[(34.58±9.49)vs(13.46±4.03)]增多、N1期睡眠增加[(81.29±12.41)min vs(39.51±8.63)min],N2期、N3期睡眠减少[(94.23±16.53)min vs(162.84±18.93)min;(39.78±7.64)min vs(84.15±11.39)min],REM 睡眠减少[(47.52±7.64)min vs(73.56±9.43)min],上述组间差异均有统计学意义(P<0.05)。与PSG值比较,患者组主观评估睡眠潜伏期延长、睡眠时间减少、睡眠效率下降(P<0.05)。结论 首发精神分裂症患者有睡眠连续性和睡眠结构两方面异常,且对失眠有主观夸大特征。
首发精神分裂症 多导睡眠图
精神分裂症患者常合并睡眠障碍,失眠是导致患者就诊的主要原因之一。临床中往往可见患者的失眠感受与客观的睡眠状况不一致,存在主观夸大。多导睡眠图(Polysomnography,PSG)是一种能对睡眠定量的检查方法。既往研究发现,精神分裂症患者有睡眠潜伏期延长、睡眠时间减少和效率下降,以及I期睡眠增加和II、III、IV期睡眠减少,但慢波睡眠(III、IV 期睡眠)异常结果报道不太一致,其差异可能与抗精神药物治疗史和病程的影响有关[1]。故本研究选用急性起病、首次发作且未服药的精神分裂症患者为研究对象,探索精神分裂症多导睡眠图的特征。
1 对象与方法
1.1 研究对象 来自2010年6~12月汕头大学精神卫生中心门诊或住院精神分裂症患者。纳入标准:①符合中国精神障碍分类与诊断标准第三版(CCMD-3)精神分裂症诊断标准;②急性或亚急性起病,首次发病,总病程<3个月;③入组前未服用任何抗精神病药治疗;④年龄18~45岁。排除标准:睡眠呼吸紊乱指数>5和周期性腿动指数 >5(对照组同此标准)[2]。共入组22例患者,男性16例,女性6例,年龄19~39岁,平均 (26.72±4.16)岁,病程 1~3个月,平均(1.25±0.66)个月,平均体质量指数为(23.27±2.15)kg/m2。正常对照18名,均无精神疾病家族史,自身无神经精神疾病和精神活性物质滥用史。其中男性13名,女性5名,年龄21~38岁,平均(25.38±3.14)岁,体质量指数为(22.81±4.21)kg/m2。患者组与对照组比较,性别、年龄、体质量指数差异均无统计学意义(P>0.05)。所有被试者入组前均告知本实验无创伤性并由本人或法定监护人签署知情同意书。
1.2 方法
1.2.1 多导睡眠脑电图检查 使用丹麦Medtronic公司生产的PL-200多导睡眠仪系统记录监测。脑电图电极安装参照国际标准的10/20系统[3],电极电阻<5 kΩ,滤波0.53~35 Hz,灵敏度 50 uV/cm,电极组合为F4-M1和C4-M1导联。左眼(或右眼)外眦向下(或向上)各1 cm处记录眼动图(EOG)。下颌骨下缘、中间线两侧各2 cm处记录张力性肌电活动(EMG)。通过左腿胫骨前肌电活动监测肢体运动和周期性腿动。3导心电图监测心脏节律性变化。记录口鼻气流、胸腹式呼吸运动判断睡眠过程中的低通气、呼吸暂停等睡眠呼吸事件。所有被试者在专门的睡眠实验室按其正常作息时间接受PSG监测,检查当天禁止饮酒、喝茶和咖啡等精神活性物质。
1.2.2 睡眠脑电图判断标准和分析指标 根据2007年美国睡眠医学会(American Academy of Sleep Medicine,AASM)制定的最新睡眠分期判断标准,睡眠监测系统以每30 s一个时间单元(epoch)划分为3期:清醒期(W期)、非快动眼期(Non Rapid Eye Movement Sleep,nREM,包括N1、N2和N3期)和快动眼期(Rapid Eye Movement Sleep,REM)[3]。睡眠分析指标包括:①睡眠潜伏期(关灯到进入任何首个睡眠期的间隔时间);②总睡眠时间(Total Sleep Time,TST);③睡眠效率[(TST/总记录时间)×100%];④各睡眠期时间;⑤各睡眠期比例[(每一睡眠期总的睡眠时间/TST)×100%];⑥入睡后总觉醒时间[TST内的清醒时间减睡眠潜伏期];⑦微觉醒次数。睡眠分析由经过专门睡眠医学培训的医师作判断。
1.3 睡眠量表评定 PSG检测完毕后进行匹兹堡睡眠质量指数(Pittsburgh Sleep Quality Index,PIQS)量表评定。
1.4 统计方法 运用SPSS 11.5进行统计分析,数据以¯x±s表示。患者组和正常对照组各睡眠指标的比较采用t检验,患者组主-客观睡眠比较采用配对t检验。检验水准α=0.05,双侧检验。
2 结果
2.1 两组呼吸暂停低通气指数和周期性腿动指数比较 与对照组比较,患者组呼吸暂停指数(包括中枢性和阻塞性呼吸暂停指数)、低通气指数、周期性腿动指数差异均无统计学意义(t为1.25~1.39,P均大于0.05)。见表1。
2.2 两组睡眠连续性指标比较 与对照组比较,患者组睡眠连续性受损,具体表现为:睡眠潜伏期延长(t=2.19,P<0.05),总睡眠时间减少(t=2.44,P<0.05),睡眠效率下降(t=2.54,P<0.05),睡眠期觉醒时间和微觉醒次数明显增多(t=2.13,P<0.05;t=2.25,P<0.05)。两组间REM睡眠潜伏期差异无统计学意义(t=1.33,P>0.05)。见表2。
2.3 两组睡眠结构指标比较 与对照组比较,患者组睡眠结构损害,具体表现为:N1期睡眠时间延长(t=1.83,P<0.05),在总睡眠期内所占百分比增加(t=1.96,P<0.05);N2期、N3期睡眠时间减少(t=2.20,P<0.05;t=2.46,P<0.05),N2期、N3期在总睡眠期内所占百分比减少(t=2.31,P<0.05;t=2.39,P<0.05);REM睡眠绝对时间减少(t=2.37,P<0.05),但两组的REM睡眠比例的差异无统计学意义(t=1.14,P>0.05)。见表3。
2.4 两组主-客观睡眠比较 与对照组比较,患者组PSQI分值增高(t=3.72,P<0.05)。相对于客观睡眠,患者组主观睡眠潜伏期延长(t=2.38,P<0.05),总睡眠时间减少(t=2.66,P<0.05),睡眠效率降低(t=2.15,P<0.05)。对照组上述指标差异无统计学意义(P>0.05)。见表4。

表1 患者组与对照组呼吸暂停低通气指数和周期性腿动指数比较

表2 患者组与对照组睡眠连续性指标比较
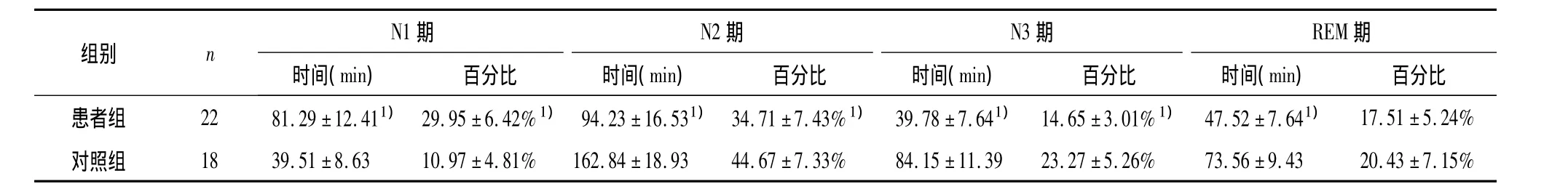
表3 患者组与对照组睡眠结构指标比较
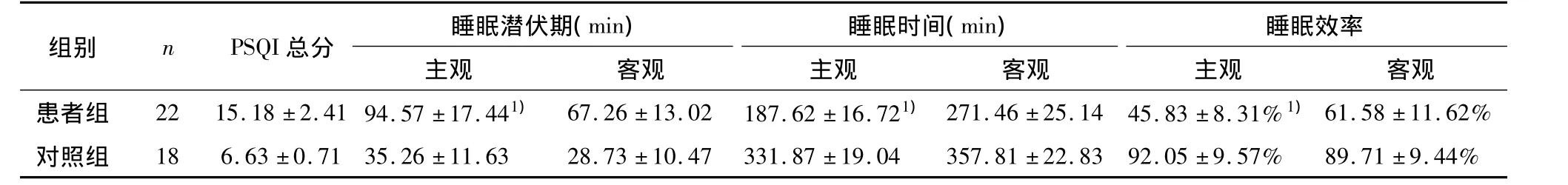
表4 患者组、对照组主-客观睡眠比较
3 讨论
精神分裂症患者各类睡眠障碍发生率高达30%~80%,长期睡眠不足可影响患者的认知功能[4],甚至导致自杀行为。因此,研究精神分裂症患者的睡眠障碍具有重要的临床意义。
本研究结果显示,患者组与对照组呼吸暂停低通气指数和周期性腿动指数均小于5,表明被试者均没有影响睡眠相关的原发性躯体疾病。与正常对照比较,精神分裂症患者有睡眠连续性和睡眠结构两方面异常。睡眠连续性异常表现为入睡潜伏期延长、总睡眠时间减少、睡眠效率下降、睡眠期觉醒时间和觉醒次数明显增多。睡眠结构异常表现为N1期睡眠时间和比例增加,N2期、N3期(慢波睡眠)睡眠时间减少、比例下降。结果与国内外多数报道相似,如张明岛等[5]通过正常对照研究显示,精神分裂症患者总睡眠时间减少,S2期睡眠和慢波睡眠减少,觉醒时间增多。同样,Sharpley等[6]的研究显示精神分裂症患者睡眠潜伏期延长,睡眠效率下降和慢波睡眠减少。
Maixner等[7]的研究提示睡眠连续性受损是反映精神分裂症患者疾病状态的可逆性指标,而慢波睡眠缺陷则是特征性睡眠脑电图改变,且是精神分裂症发生发展的重要病理生理基础,与前额叶皮质损害密切相关[8]。N2期睡眠减少与患者睡眠期的高警觉性有关[9]。但 Chouinard等[10]的研究未发现精神分裂症患者慢波睡眠与正常对照有明显差异。Keshavan等[11]的研究中精神分裂症患者睡眠潜伏期和睡眠效率与正常对照差异不明显。病程以及药物治疗史对患者多导睡眠图特征可能存在影响,有研究报道抗精神病药物停药6周后对睡眠的影响依然存在[12-13]。本研究选择首次发病,病程小于3个月,无精神药物服用史的精神分裂症患者为研究对象,结果可反映急性期精神分裂症患者多导睡眠图特征。与既往研究比较,本研究患者组和对照组REM睡眠时间相对均较少[14],可能与被试者对睡眠监测程序和睡眠环境改变适应不良有一定关系。
主-客观睡眠评估结果的比较显示,精神分裂症患者主-客观睡眠的睡眠潜伏期延长、睡眠时间减少和睡眠效率下降显著不一致,提示精神分裂症患者对睡眠问题存在主观夸大的特点。有报道分析主客观睡眠的差异与患者的焦虑特质及当时的焦虑状态水平有关[15]。
本研究参照美国睡眠医学会(AASM)制定的睡眠分期标准[3]。与传统R&K分期标准比较,尽管新标准取消了“三分钟”分期规则,取消了活动期,将III、IV期合并为N3期,从本研究结果看,两分期系统这些细微区别对睡眠结果判断并无大的影响。
[1] Cohrs S.Sleep disturbances in patientswith schizophrenia:impact and effect of antipsychotics[J].CNSDrugs,2008,22(11):939-962.
[2] American Sleep Disorders Association.The International Classification of Sleep Disorders-Revised:Diagnostic and Coding Manual[M].American Sleep Disorders Association,1997.52 -68.
[3] 张劲农,彭伟,Walker JM.睡眠及睡眠呼吸障碍学[M].北京,科学出版社,2009.26-39.
[4] Yang C,Winkelman JW.Clinical significance of sleep EEG abnormalities in chronic schizophrenia[J].Schizophr Res,2006;82(2-3):251-260.
[5] 张明岛,陈兴时,王红星,等.奥氮平对精神分裂症患者睡眠脑电活动的影响[J].诊断学理论与实践,2004,3(2):103-105.
[6] Sharpley AL,Vassallo CM,Cowen PJ.Olanzapine increases slow-wave sleep:evidence for blockade of central 5-HT2C receptors in vivo[J].Biol Psychiatry,2000,47(5):468 -470.
[7] Maixner S,Tandon R,Eiser A,et al.Effects of antipsychotic treatment on polysomngraphicmeasures in schizophrenia:a replication and extension[J].Am J Psychiatry,1998,155(11):1600 -1602.
[8] Sarkar S,Katshu MZ,Nizamie SH,etal.Slow wave sleep deficits as a traitmarker in patients with schizophrenia[J].Schizophr Res,2010,124(1 -3):127 -133.
[9] 刘知源,孙学礼,孙兆明,等.23例精神分裂症患者的多导睡眠图比较研究[J].上海精神医学,2001;13(1):1-4.
[10] Chouinard S,Poulin J,Stip E,et al.Sleep in untreated patients with schizophrenia:a meta-analysis[J].Schizophr Bull,2004,30(4):957-967.
[11] Keshavan MS,Reynolds CF,Miewald JM,et al.A longitudinal study of EEG sleep in schizophrenia[J].Psychiatry Res,1996,59(3):203-211.
[12] Neylan TC,Van Kammen DP,Kelley ME,et al.Sleep in schizophrenic patientson and off haloperidol therapy:Clinically stable vs relapsed patients[J].Arch Gen Psychiatry,1992,49:643 -649.
[13] Monti JM,Monti D.Sleep disturbance in schizophrenia[J].Int Rev Psychiatry,2005,17(4):247 -253.
[14] Poulin J,Daoust AM,Forest G,et al.Sleep architecture and its clinical correlates in first episode and neuroleptic-naive patients with schizophrenia[J].Schizophr Res,2003,62(1 -2):147 -153.
[15]潘集阳,马文彬,张继辉,等.慢性原发性失眠患者主客观睡眠质量差异及相关因素[J].中国神经精神疾病杂志,2007,33(2):69-72.
Polysomnographic study in first-episode schizophrenics.
WANG Junqing,LIN Yihuan,JIANG Liyun,WENG Bilan,XU Chongtao,ZHUO Yongning,ZHANG Jie,CHEN Quliang.The Mental Health Center of Shantou University,243 Daxue Road,Shantou 515063.China.Tel:0754 -82902708.
ObjectiveTo explore the feature of polysomnography(PSG)in acute first-episode schizophrenics.M ethods PSG and Pittsburgh Sleep Quality Index Scale(PSQIS)were used to evaluate subjective and objective sleep in twenty-two first-episode schizophrenics(patient group)and 18 normal controls(control group).Results Compared with control group,the patient group had significantly prolonged sleep latency,shortened total sleep time,decreased sleep efficiency,increased awake time in sleep continuity,and increased N1 stage,decreased N2,N3 and rapid eyemovementstage in sleep structure(Ps<0.05).Patients also had subjective sleep disturbances including prolonged sleep latency,shortened total sleep time and decreased sleep efficiency compared with those of objective sleep(P<0.05).Conclusions The firstepisode schizophrenics have both sleep continuity and sleep structure deficits,and tend to overrate the severity of their insomnia problem.
first-episode schizophrenics Polysomnography
R749.3
A
☆广东省医学科研基金资助项目(编号:A2010415)
* 汕头大学精神卫生中心(汕头 515063)
E-mail:stwangjunqing@21cn.com)
2010-11-23)
(责任编辑:曹莉萍)
·论 著·

