多巴丝肼联合己酮可可碱序贯治疗早期帕金森病的临床研究
王少颖 高洁 李宁 王莉迪 刘明 刘俐杰 王青青 李净兵 刘翠青

基金项目 2022年度河北省医学科学研究课题(No.20220799)
作者单位 河北省第八人民医院(石家庄 050000)
通讯作者 高洁,E-mail:603454337@163.com
引用信息 王少颖,高洁,李宁,等.多巴丝肼联合己酮可可碱序贯治疗早期帕金森病的临床研究[J].中西医结合心脑血管病杂志,2024,22(7):1310-1315.
摘要 目的:分析多巴丝肼联合己酮可可碱序贯治疗早期帕金森病(PD)的临床疗效及其对病人脑血流动力学、血管内皮功能和血清白细胞介素(IL)-17、高迁移率族蛋白1(HMGB1)、单核细胞趋化蛋白-1(MCP-1)水平的影响。方法:选取2020年3月—2022年3月我院收治的98例早期PD病人,按随机数字表法分为两组,各49例。对照组给予多巴丝肼片治疗,观察组在对照组基础上联合己酮可可碱序贯治疗。连续治疗14周后统计两组每日总“关”期时间、多巴丝肼用量及副反应情况,并评价两组运动功能状况。比较治疗前后两组颈总动脉血流动力学参数[平均流速(Vm)、阻力指数(RI)、搏动指数(PI)]、血清血管内皮功能指标[内皮素-1(ET-1)、前列环素(PGI2)、一氧化氮(NO)]以及IL-17、HMGB1和MCP-1水平。结果:治疗后,观察组每日总“关”期时间缩短幅度明显大于对照组(P<0.05),多巴丝肼用量的增加幅度明显小于对照组(P<0.05),统一帕金森病评定量表(UPDRS)中Ⅲ、Ⅳ部分评分的降低幅度均明显大于对照组(P<0.05)。治疗后,观察组Hoehn-Yahr分级较治疗前明显改善(P<0.05),观察组优于对照组(P<0.05)。与治疗前比较,治疗14周后观察组颈总动脉Vm明显加快(P<0.05),颈总动脉RI、PI和血清ET-1、IL-17、HMGB1、MCP-1水平均明显降低(P<0.05),血清PGI2和NO水平均明显上升(P<0.05);对照组治疗前后以上指标均无明显改变(P>0.05)。观察组不良反应发生率(20.4%)明显低于对照组(38.8%),差异有统计学意义(P<0.05)。结论:己酮可可碱序贯作为多巴丝肼的辅助用药方案,对早期PD病人具有确切的临床疗效,且安全可靠,并能进一步改善脑供血和血管内皮功能以及下调血清IL-17、HMGB1、MCP-1的表达水平。
关键词 帕金森病;己酮可可碱;多巴丝肼;脑血流动力学;血管内皮功能;炎症反应
doi:10.12102/j.issn.1672-1349.2024.07.028
帕金森病(PD)是具有患病率高、病残率高,以运动症状(震颤、姿势平衡障碍、肌强直等)和非运动症状(认知、精神、睡眠、嗅觉等障碍)为临床表现,以及病程呈慢性进展等特点的常见神经系统变性疾病。流行病学资料显示,PD发病率男性高于女性,我国≥65岁人群患病率为1.7%,且随着年龄增长而增高,预计到2030年患病例数将上升至500万例,约占全世界PD总人数的50%[1-2]。早期PD[即Hoehn-Yahr分级(H-Y分级)为1.0~2.5级]病情进展更为迅速,疾病一旦发生,运动及非运动症状将渐进性加重,因此该时期的有效治疗至关重要[3]。PD的治疗以达到有效改善症状、减少不良反应及提高生活质量和工作能力为目标,目前尚无统一治疗模式,临床治疗以多巴胺替代疗法为首选。作为左旋多巴与苄丝肼的复合制剂,多巴丝肼具有起效快、可补充脑内多巴胺递质、血脑屏障透过性大等优势,是早期PD最基本、最有效的对症治疗药物[4]。然而PD的发生发展并非单一因素引起,必须重视多因素作用及神经血管单元各部分的相互作用。因此,可考虑多靶点、多途径作用的药物联合使用,力求获得最佳治疗效果。己酮可可碱是磷酸二酯酶抑制剂,具有改善血液流变性、减少血管阻力、促进脑氧与葡萄糖代谢等作用,主要用于脑循环的改善[5]。本研究旨在观察多巴丝肼联合己酮可可碱序贯治疗早期PD的疗效及对脑血流动力学、血管内皮功能和血清白细胞介素(IL)-17、高迁移率族蛋白1(HMGB1)、单核细胞趋化蛋白-1(MCP-1)水平的影响。现报道如下。
1 资料与方法
1.1 一般资料
选取2020年3月—2022年3月我院收治的98例早期PD病人,其中,男57例,女41例;年龄50~80(64.7±8.2)岁;病程2~10(5.1±1.4)年;H-Y分级:1.0级14例,1.5级28例,2.0级22例,2.5级34例。按随机数字表法分为两组。观察组49例,男29例,女20例;年龄52~80(65.1±7.9)岁;病程2~10(5.3±1.5)年;H-Y分级:1.0级7例,1.5级15例,2.0级12例,2.5级15例。对照组49例,男28例,女21例;年龄50~79(64.2±8.4)岁;病程2~9(4.9±1.2)年;H-Y分级:1.0级7例,1.5级13例,2.0级10例,2.5级19例。两组基线资料比较差异无统计学意义(P>0.05),具有可比性。本研究经我院医学伦理委员会审批通过。
1.1.1 诊断标准
原发性PD诊断标准参照《国际运动障碍疾病协会帕金森病临床诊断新标准(2015)》中制定的标准执行[6]。
1.1.2 纳入标准
1)满足原发性PD诊断标准;2)病情处于早期[即H-Y分级(“关”期)为1.0~2.5级];3)年龄50~80岁;4)每日总“关”期时间<6 h;5)病程2~10年;6)病人自愿签订知情同意书;7)既往无其他脑部疾患史;8)多巴丝肼使用劑量≥375 mg/d。
1.1.3 排除标准
1)PD叠加综合征或继发性PD综合征;2)存在肝、肾、胃肠道、心血管系统或呼吸系统疾病;3)伴有酗酒或吸毒成瘾;4)合并己酮可可碱使用禁忌证;5)患有恶性肿瘤或精神疾病;6)无法配合完成统一帕金森病评定量表(UPDRS)调查;7)既往有脑部手术或外伤史。
1.2 治疗方法
对照组:予以多巴丝肼片[上海罗氏制药生产,规格:每片0.25 g(左旋多巴200 mg、苄丝肼50 mg),国药准字H10930198]口服治疗,具体是先按病人入组前用量继续用药,之后于入组后的第2周、第6周、第10周、第14周根据病人病情调整用量。在此基础上,观察组联合己酮可可碱序贯治疗,具体是先予以己酮可可碱注射液[石药集团欧意药业生产,规格:2 mL(0.1 g),国药准字H13023189]静脉输注治疗,每次将0.1 g己酮可可碱注射液加入250 mL 0.9%氯化钠注射液中混合均匀后给药,每日2次,连用2周;后改为己酮可可碱缓释片(石药集团欧意药业生产,规格:每片0.4 g,国药准字H10970265)口服治疗,每次0.4 g,每日2次,连用12周。连续治疗14周后评价两组疗效。
1.3 观察指标
1)统计两组治疗14周后每日总“关”期时间、多巴丝肼用量与基线值的差值。2)运动功能评估指标:采用H-Y分级和UPDRS中Ⅲ、Ⅳ部分评价受试者运动功能状况。其中H-Y分级共有8个等级,等级越高则病情越严重[7]。UPDRS中Ⅲ部分(运动功能检查)包含步态、腿部灵活性、手运动、强直等内容,评分为0~132分;UPDRS中Ⅳ部分(运动并发症)主要涉及异动症、临床波动、其他并发症等内容,评分为0~24分;UPDRS中Ⅲ、Ⅳ部分评分越高则运动功能越差[8]。治疗前和治疗14周后对每例病人各评估1次H-Y分级和UPDRS-Ⅲ、Ⅳ评分,并计算UPDRS-Ⅲ、Ⅳ评分与基线值的差值。3)治疗前和治疗14周后使用脑血管血液动力学监测仪(上海示才生物科技有限公司生产,型号:CVHD-3000)对受检者双侧颈总动脉血流动力学状态进行监测,记录参数:平均流速(Vm)、阻力指数(RI)和搏动指数(PI)。4)治疗前和治疗14周后抽取受试者静脉血6 mL,并制备血清标本(3 000 r/min离心15 min)。运用酶标仪(北京普朗医疗公司,型号9602G)并按酶联免疫吸附实验试剂盒(购自杭州联科生物)说明书要求检测血清内皮素-1(ET-1)、前列环素(PGI2)、IL-17、HMGB1和MCP-1水平;使用可见分光光度计(上海棱光技术公司,型号756S型)并按硝酸还原酶法试剂盒(均购自武汉明德生物)说明书要求测定血清一氧化氮(NO)水平。
1.4 不良反应
观察并记录两组不良反应(包括失眠、异动症、低血压、心律失常等)发生情况。
1.5 统计学处理
运用SPSS 23.0统计软件包处理数据。定性资料以例数、百分比(%)表示
,行χ2检验;等级资料行Wilcoxon秩和检验;符合正态分布的定量资料以均数±标准差(x±s)表示,采用t检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组每日总“关”期时间、多巴丝肼用量和UPDRS-Ⅲ、Ⅳ评分基线值比较
两组治疗前每日总“关”期时间、多巴丝肼用量和UPDRS-Ⅲ、Ⅳ评分比较,差异均无统计学意义(P>0.05)。详见表1。
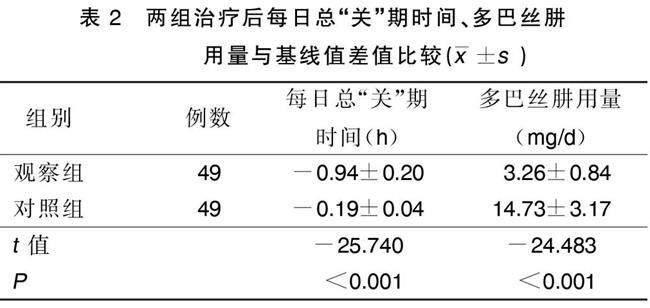
2.2 两组治疗后每日总“关”期时间、多巴丝肼用量与基线值差值比较
治疗14周后,观察组每日总“关”期时间缩短幅度明显大于对照组(P<0.05),多巴丝肼用量增加幅度明显小于对照组(P<0.05)。详见表2。
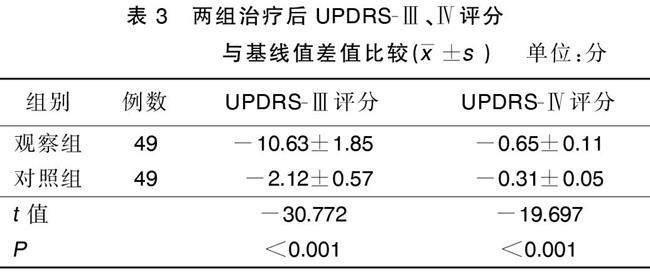
2.3 两组治疗后UPDRS-Ⅲ、Ⅳ评分与基线值差值比较
治疗14周后,观察组UPDRS-Ⅲ、Ⅳ评分降低幅度均明显大于对照组(P<0.05)。详见表3。
2.4 两组治疗前后H-Y分级比较
治疗14周后,观察组H-Y分级(“关”期)较治疗前明显改善(P<0.05);对照组治疗前后变化则不明显(P>0.05)。两组治疗后H-Y分级比较,差异有统计学意义(P<0.05)。详见表4。
2.5 两组脑血流动力学参数水平比较
与治疗前比较,治疗14周后观察组颈总动脉Vm明显加快(P<0.05),颈总动脉RI、PI均明显降低(P<0.05);对照组治疗前后颈总动脉Vm、RI、PI均无明显改变(P>0.05)。治疗14周后,观察组颈總动脉Vm较对照组明显加快;RI、PI较对照组明显降低,差异均有统计学意义(P<0.05)。详见表5。
2.6 两组治疗前后组血管内皮功能指标水平比较
与治疗前相比,治疗14周后观察组血清ET-1水平明显下降(P<0.05),血清PGI2和NO水平均明显上升(P<0.05);对照组治疗前后ET-1、PGI2和NO均无明显改变(P>0.05)。治疗后,观察组血清ET-1水平较对照组明显下降,血清PGI2、NO水平较对照组明显升高(P<0.05)。详见表6。
2.7 两组血清IL-17、HMGB1、MCP-1水平比较
观察组治疗14周后血清IL-17、HMGB1、MCP-1水平均较治疗前明显下降(P<0.05);对照组治疗前后IL-17、HMGB1、MCP-1水平均无明显变化(P>0.05)。治疗14周后,观察组血清IL-17、HMGB1、MCP-1水平均较对照组降低(P<0.05)。详见表7。
2.8 两组不良反应发生情况比较
观察组不良反应发生率明显低于对照组,差异有统计学意义(χ2=3.967,P=0.046),详见表8。研究对象均无其他严重不良事件发生。
3 讨 论
PD作为继肿瘤、心脑血管病之后中老年人的“第三大杀手”,已成为人口与健康领域中广泛关注的热点问题。该病以黑质多巴胺能神经元渐进性变性丢失为主要病理改变,其详细发病机制尚未清晰,年龄、环境、氧化应激、遗传、线粒体功能障碍、免疫炎症反应及α-突触核蛋白(α-Syn)调控异常等均可能参与了多巴胺能神经元的变性死亡过程[9]。多巴丝肼是临床常用的复方左旋多巴药物,其中左旋多巴作为多巴胺前体药,可替代不能透过血脑屏障的多巴胺进入中枢神经系统,并发生快速脱羧反应生成多巴胺;而作为外周脱羧酶抑制剂,苄丝肼则能对脑外组织中左旋多巴的脱羧反应加以抑制,以此减少相关不良反应。此外,近年来研究表明,神经血管单元(包括神经元、神经胶质细胞、微血管内皮细胞、细胞外基质等)各部分紧密相连共同维持血脑屏障渗透性、脑血流量及脑内稳態,而神经血管单元稳态失衡和功能障碍可能是PD发生和发展的重要原因[10]。因此,针对早期PD治疗采取单一细胞内途径或细胞类型的疗效有限,通过有效改善多巴胺能神经元内环境以阻碍其进行性变性很有可能成为药物治疗的新靶点,以及对抗左旋多巴药物副作用的新思路。己酮可可碱属于磷酸二酯酶抑制剂,具有提高血液流动性、修复脑血管内皮损伤、扩张血管、抗炎、增加组织带氧能力等多重药理作用,从而能有效改善脑血管微循环及神经血管单元功能障碍,促进早期PD病情减轻[11]。动物实验发现,己酮可可碱可能通过减轻氧化应激反应,对多巴胺能神经元起保护作用[12]。另外,为减少己酮可可碱的不良反应,此次研究中采用序贯治疗(即静脉应用己酮可可碱注射液2周与口服己酮可可碱缓释片12周)以增加用药安全性及巩固治疗效果。本研究结果显示,治疗14周后观察组每日总“关”期时间的缩短幅度明显大于对照组,多巴丝肼用量的增加幅度明显小于对照组,H-Y分级明显优于对照组,UPDRS-Ⅲ、Ⅳ评分的降低幅度明显大于对照组,提示联合己酮可可碱序贯治疗比单用多巴丝肼能有效缩短早期PD病人每日“关”期时间,减小多巴丝肼用量的增加幅度,改善运动功能,减缓病情进展。同时本研究发现,己酮可可碱序贯使用并未明显增加早期PD病人不良反应的发生风险,反而能大幅降低病人治疗相关副反应的发生率,究其原因可能与左旋多巴用量增加幅度下降有关。可见,己酮可可碱序贯联合多巴丝肼治疗早期PD是安全、有效且可靠的。
相关文献表明,大脑皮质区域血流灌注障碍、脑白质损害、黑质致密部微血管改变及铁沉积等因素可导致PD病人脑血流动力学异常,黑质处发生缺血、缺氧,从而引起一系列炎性改变、小胶质细胞激活、氧化应激反应、局部脑组织微循环障碍及血脑屏障破坏,影响局部脑组织能量输送和神经元代谢,促使多巴胺能神经元退化、坏死,加重PD病情的发展[13]。研究显示,PD病人脑血流动力学主要表现为Vm减慢,RI、PI增加,即病人脑血流速度下降,脑血管阻力增大、顺应性降低[14]。本研究显示,治疗14周后观察组颈总动脉Vm明显快于对照组,颈总动脉RI、PI均明显低于对照组,提示多巴丝肼联合己酮可可碱序贯治疗早期PD在改善病人脑血流动力学方面更具优势。药理研究表明,己酮可可碱能通过阻止微血管收缩、升高三磷酸腺苷量而增强红细胞变形能力、提高抗凝血酶Ⅱ水平、减少过氧化物释放、刺激纤维蛋白溶酶原活化因子释放、抑制血小板活化因子释放等途径,发挥抗凝、降低血液黏度、增加血液流动性、促纤溶及扩血管的作用,进而改善脑部血液循环,增加毛细血管和动脉血流量,降低血管阻力,提高顺应性[15]。故推测对脑血流动力学异常的纠正是备能够己酮可可碱在早期PD治疗中发挥良好效果的关键机制之一。
血管内皮功能障碍是导致PD发生、发展的重要环节,其中内皮介导的PGI2、NO合成障碍及ET-1与PGI2、NO的平衡失调,是血管内皮功能紊乱的重要原因[16]。由于PD病人存在脑血管内皮细胞损伤,导致依赖内皮细胞产生的ET-1增多,血管收缩增强;而PGI2和NO释放减少,致使扩血管及血管内皮功能保护作用减弱,从而引起血管病理性收缩与痉挛及局部脑组织血流灌注降低,加重脑组织缺氧,诱发炎症及氧化应激反应,影响血脑屏障对物质的吸收与转运,产生神经元毒性,促使多巴胺能神经元的损伤与凋亡。有文献显示,己酮可可碱能有效降低脑梗死病人血中ET-1水平,并提高其血中NO浓度,以保护血管内皮,进而起到神经保护作用[17]。本研究中,治疗14周后观察组血清ET-1水平明显低于对照组,而血清PGI2、NO水平均明显高于对照组,提示联合己酮可可碱序贯和多巴丝肼治疗早期PD能有效缓解病人血管内皮功能障碍。究其原因,与己酮可可碱具有纠正血管内皮功能紊乱、抗炎、改善脑血流动力学的作用密切相关。
免疫炎症反应已被证明是包括PD在内的多种神经退行性疾病的重要发病机制。IL-17是重要的促炎因子,在PD病人多巴胺能神经元缺失引起α-Syn大量释放并影响外周免疫系统后,其水平随着辅助性T细胞17(Th17)的增殖分化而上升,可通过增加其他炎性因子和趋化因子的表达,加重神经系统炎症,加剧多巴胺能神经元的损伤与丢失,从而导致恶性循环[18]。HMGB1为重要的核内非组蛋白,当脑组织细胞受损时由核内释放至胞外,通过激活Toll样受体4(TLR-4)/核转录因子-κB(NF-κB)信号通路引发炎症反应,其作为晚期炎症介质,在维持和放大炎性反应中发挥重要作用,参与了PD的神经性炎症发展过程[19]。MCP-1属于典型的趋化因子,在脑内多由神经元和神经胶质细胞产生,其与CC趋化因子受体-2(CCR-2)结合能调控单核细胞、小胶质细胞募集与活化,增强炎性细胞在中枢神经系统中的浸润能力,与PD炎症反应起始阶段关系密切[20]。Badawi等[21]研究显示,己酮可可碱可通过下调TLR-4、HMGB1等炎性介质表达,减少海马β淀粉样蛋白(Aβ)等毒性蛋白质的表达,从而逆转海马神经元的丢失,在脑部疾病中显示出神经保护潜力。本研究中,治疗14周后观察组血清IL-17、HMGB1和MCP-1水平下降程度均较对照组明显(P<0.05)。提示早期PD应用己酮可可碱序贯联合多巴丝肼治疗能更有效地减轻机体炎症反应。分析原因,与己酮可可碱的直接抗炎作用以及脑血液循环和血管内皮功能障碍的改善有关。
综上所述,己酮可可碱序贯作为多巴丝肼的辅助用药方案,对早期PD病人具有确切的临床疗效,且安全性较好,并能进一步纠正脑血流动力学异常和血管内皮功能障碍以及下调血清IL-17、HMGB1、MCP-1的表达水平。
参考文献:
[1] ZHANG Z X,ROMAN G C,HONG Z,et al.Parkinson′s disease in China:prevalence in Beijing,Xian,and Shanghai[J].Lancet,2005,365(9459):595-597.
[2] LI G,MA J F,CUI S S,et al.Parkinson′s disease in China:a forty-year growing track of bedside work[J].Translational Neurodegeneration,2019,8:22.
[3] 肖雪洋,胡琳珍.帕金森发病机制及其最新治疗策略[J].湖北大学学报(自然科学版),2021,43(5):514-521.
[4] BABA Y,FUTAMURA A,KINNO R,et al.The relationship between the distinct ratios of benserazide and carbidopa to levodopa and motor complications in Parkinson′s disease:a retrospective cohort study[J].Journal of the Neurological Sciences,2022,437:120263.
[5] 张小喜,成红学,邵春香.己酮可可碱辅助治疗急性脑梗死的效果[J].河南医学研究,2021,30(25):4753-4755.
[6] POSTUMA R B,BERG D,STERN M,et al.MDS clinical diagnostic criteria for Parkinson′s disease[J].Movement Disorders,2015,30(12):1591-1601.
[7] HOEHN M M,YAHR M D.Parkinsonism:onset,progression and mortality[J].Neurology,1967,17(5):427-442.
[8] GOETZ C G,TILLEY B C,SHAFTMAN S R,et al.Movement Disorder Society-sponsored revision of the Unified Parkinson′s Disease Rating Scale(MDS-UPDRS):scale presentation and clinimetric testing results[J].Movement Disorders,2008,23(15):2129-2170.
[9] 焦倩,姜宏.帕金森病病因与发病机制研究现状及其诊治意义[J].青岛大学学报(医学版),2021,57(2):159-162.
[10] IVANIDZE J,SKAFIDA M,PANDYA S,et al.Molecular imaging of striatal dopaminergic neuronal loss and the neurovascular unit in parkinson disease[J].Frontiers in Neuroscience,2020,14:528809.
[11] 王玉.己酮可可碱对衰老相关神经行为缺陷的改善作用及其机制[D].石家庄:河北医科大学,2021.
[12] WANG Y,KANG Y X,QI C X,et al.Pentoxifylline enhances antioxidative capability and promotes mitochondrial biogenesis for improving age-related behavioral deficits[J].Aging,2020,12(24):25487-25504.
[13] 劉昕,潘玉君.脑血流灌注影响因素与帕金森病相关性研究进展[J].临床神经病学杂志,2021,34(6):476-478.
[14] BRISSON R T,DE CSSIA LEITE FERNANDES R,FULGNCIO DE LIMA ARRUDA J,et al.Ultrasonographic changes in brain hemodynamics in patients with Parkinson′s disease and risk factors for cerebrovascular disease:a pilot study[J].Parkinson′s Disease,2021,2021:1713496.
[15] 张词侠,张桂林,李志勇,等.己酮可可碱的药理特性和治疗用途的研究
进展[J].中国临床药理学杂志,2008,24(1):74-77.
[16] 徐浩刚,陈正平,夏秋钰,等.多巴丝肼片联合银杏叶提取物对老年帕金森病病人黑质神经元细胞因子、血管活性物质及抗氧化物的影响[J].实用老年医学,2019,33(7):680-683.
[17] 刘雪松,李雪,张帅.己酮可可碱治疗动脉粥样硬化性脑梗死的疗效研究[J].实用中西医结合临床,2022,22(3):103-106.
[18] STORELLI E,CASSINA N,RASINI E,et al.Do Th17 lymphocytes and IL-17 contribute to Parkinson′s disease? A systematic review of available evidence[J].Frontiers in Neurology,2019,10:13.
[19] 陈建明,黄鹂丽,宋小娜,等.血清DEC1、HMGB1及AngⅡ水平与帕金森病认知功能障碍及预后的相关性研究[J].实验与检验医学,2020,38(3):537-539;602.
[20] 尤雪梅,种亚楠,狄海莉,等.帕金森患者血清MCP-1、CCR2水平与病情严重程度的关系[J].海南医学,2021,32(10):1238-1241.
[21] BADAWI G A,SHOKR M M,ZAKI H F,et al.Pentoxifylline prevents epileptic seizure via modulating HMGB1/RAGE/TLR4 signalling pathway and improves memory in pentylenetetrazol kindling rats[J].Clinical and Experimental Pharmacology & Physiology,2021,48(8):1111-1124.
(收稿日期:2022-07-27)
(本文编辑王丽)

