双源CT双动脉期增强扫描对肝动脉-门静脉瘘的评估价值及风险因素分析
许小兰 窦斌 杨斐 魏文鑫 朱晓宁 刘征
[摘要] 目的:探討双源CT双动脉期增强扫描模式对肝动脉-门静脉瘘(HAPVF)的评估价值及风险因素分析。方法:选取HAPVF和非HAPVF患者各60例,分别为HAPVF组和非HAPVF组,行双源CT双动脉期增强扫描,比较2组临床指标及CT征象差异。以DSA为金标准,对比动脉早期、动脉晚期和双动脉期对HAPVF的诊断敏感度、特异度,以及对HAPVF分型的诊断准确率。应用logistic回归分析探讨HAPVF的危险因素,采用ROC曲线评估危险因素预测HAPVF的价值。结果:双动脉期诊断HAPVF的敏感度、特异度、阳性预测值、阴性预测值及分型准确率均明显高于单独2期(均P<0.05)。2组肝癌大小、包膜类型、门静脉癌栓比较,差异均有统计学意义(均P<0.05)。logistic回归分析显示,肝癌大小、包膜类型、门静脉癌栓均是HAPVF的独立危险因素。ROC曲线表明,单因素预测HAPVF效果最好的是包膜类型,其次是门静脉癌栓,再次是肝癌大小。综合多因素联合预测分析显示,肝癌大小+包膜类型+门静脉癌栓预测效果最好。结论:双源CT双动脉期增强扫描模式对HAPVF的诊断敏感度、特异度较高,且在HAPVF分型中具有较好的诊断效果。HAPVF的临床及影像学征象具有一定特点,其中肝癌大小、包膜类型、门静脉癌栓均是HAPVF的独立危险因素,三者联合预测效果最好,能为临床及时诊治提供可靠依据。
[关键词] 体层摄影术,X线计算机;双动脉期增强扫描;肝动脉-门静脉瘘;评估价值;风险因素
Value of dual-source CT double arterial phases enhanced scan in the evaluation of hepatic artery-portal vein fistula and its risk factors analysis
[Abstract] Objective:To evaluate the dual-source CT double arterial phases enhanced scan for hepatic artery-portal vein fistulas (HAPVF) and its risk factors analysis. Methods:Sixty patients with HAPVF and sixty patients with non-HAPVF were selected. All patients underwent dual-source CT double arterial phases enhanced scan. The clinical indicators and imaging features were compared between the two groups. DSA findings were used as the gold standards,and the sensitivity and specificity of the early arterial phase,the late arterial phase and the double arterial phases were compared,and the accuracy for HAPVF classification was compared. Logistic regression analysis was applied to explore the risk factors of HAPVF,and ROC curve was used to evaluate the value of the risk factors prediciting HAPVF. Results:The sensitivity,specificity,positive predictive value,negative predictive value and the classification accuracy of the double arterial phases in diagnosis of HAPVF were significantly greater than those of the early and late arterial phases. The tumor size,envelope type and portal vein tumor thrombus were significantly different between the two groups (all P<0.05),and were all independent risk factors for HAPVF revealed by multivariate regression analysis. ROC curve analysis showed the best single-factor predictor was envelope type,then the portal vein tumor thrombus,and last the tumor size. Multifactor combined forecasting analysis revealed that the combined prediction of the three features was the best. Conclusions:Dual-source CT double arterial phases enhanced scan has the high sensitivity and specificity in the diagnosis of HAPVF,and it has a good diagnostic accuracy in HAPVF classification. Clinical indicators and CT findings of HAPVF include certain characteristics,and tumor size,envelope type and portal vein tumor thrombus are independent risk factors. The combined prediction of the three is the best,which provides a reliable and effective basis for timely clinical diagnosis and treatment.
[Key words] Tomography,X-ray computed;Dual-arterial contrast enhanced scanning;Hepatic artery-portal vein fistula;Diagnostic value;Risk factors
肝动静脉瘘是指肝动脉和肝静脉或门静脉之间形成的异常吻合的畸形血管团[1],可以是先天性的[2],也可由肝脏的各种疾病引起,主要包括肝硬化、肝癌、肝血管瘤、肝脓肿、肝转移瘤等[3-4]。肝动静脉瘘分为肝动脉-门静脉瘘(hepatic artery-portal vein fistula,HAPVF)、肝动脉-肝静脉瘘和混合型瘘[1]。与HAPVF相比,肝动脉-肝静脉瘘较少见,目前,全球仅报道8例[5]。肝动静脉瘘是中晚期肝癌常见并发症,发生率为12.1%~31.2%[6],肿瘤易通过瘘口引发转移及消化道出血、腹腔积液等,对治疗和预后有极大影响,并增加肝功能损伤、门静脉高压、异位栓塞等的发生风险,还可能导致脾大及加快恶性肿瘤的转移[6,7-8]。因此,早期诊断并有效治疗对肝动静脉瘘具有重要的临床意义。目前,肝动脉造影是诊断肝动静脉瘘的金标准,但费用高且为有创检查,不能作为筛查HAPVF的常规检查方法。随着CT技术的飞速发展,CT动态增强扫描、CTA、MSCT三维成像技术已成为研究肝内血流动力学变化的重要手段,且双源CT三维成像技术对肝动脉、门静脉、肝静脉系统行MPR、MIP,显示效果较好,特别是在显示细小血管方面与DSA接近。本研究通过分析双源CT双动脉期增强扫描模式对HAPVF的诊断价值,并对其风险因素进行评估,为临床及时、有效地诊治HAPVF提供可靠、有效依据。
1 资料与方法
1.1 一般资料
选取2018年1月至2021年3月经我院DSA检查确诊的HAPVF(HAPVF组)和非HAPVF(非HAPVF组)患者各60例。HAPVF组中,男47例,女13例;年龄43~84岁,中位年龄64岁;其中肝硬化23例,肝癌25例,肝血管瘤12例。非HAPVF组中,男46例,女14例;年龄50~68岁,中位年龄59岁;其中肝硬化18例,肝癌23例,肝血管瘤19例。2组性别、年龄等一般资料比较,差异均无统计学意义(均P>0.05)。
纳入标准:①未经临床治疗,其中肝癌患者未接受手术、介入及放化疗治疗;肝硬化患者未接受药物、手术治疗;肝血管瘤患者未接受介入、手术及药物治疗。②均行CT增强扫描。排除合并严重肝肾功能障碍、精神神经疾病患者。
1.2 仪器与方法
采用Siemens Somatom Definition Flash双源CT扫描仪。扫描参数:120 kV,150 mAs,层厚1 mm,矩阵512×512。增强扫描经静脉注射对比剂碘普罗胺(碘浓度300 mg/mL)90 mL,流率3.0 mL/s,注射后20~22 s行动脉早期扫描,在动脉早期基础上延迟14~15 s行動脉晚期扫描,再延迟13~16 s行门静脉期扫描,重建层厚0.5 mm,重建层距1 mm,并行MPR、MIP。
1.3 图像分析
由2位临床经验丰富的主治医师对CT图像进行分析。HAPVF诊断标准[9]:①肝动脉期门静脉主干或1级分支提早显影,而脾静脉和肠系膜上静脉尚未强化(中央型);②肝动脉期周围门静脉2级或2级以远分支提早显影,而近端门静脉主干及左右分支尚未强化(周围型)。
1.4 统计学分析
采用SPSS 23.0软件对数据进行分析。计量资料以[x]±s表示,组间比较行t检验;计数资料用例(%)表示,组间比较行[χ]2检验或Fisher精确概率检验。应用多因素logistic回归分析探讨HAPVF的危险因素,采用ROC曲线评估危险因素对HAPVF的预测价值。以P<0.05为差异有统计学意义。
2 结果
2.1 不同扫描期相检测结果对比
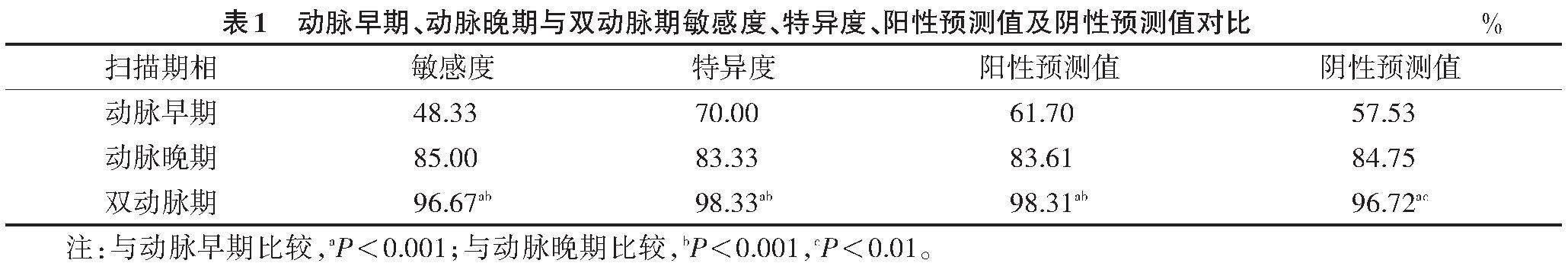
以DSA结果为金标准,双动脉期检出HAPVF的敏感度、特异度、阳性预测值及阴性预测值均明显高于动脉早期、动脉晚期,差异均有统计学意义(均P<0.05)(表1)。
2.2 不同扫描期相对HAPVF分型的诊断准确率
HAPVF组60例中,周围型34例,中央型26例。动脉早期、动脉晚期、双动脉期诊断周围型HAPVF准确率分别为62.07%、76.47%、94.83%,诊断中央型HAPVF准确率分别为68.97%、72.55%、93.10%。双动脉期对周围型、中央型HAPVF检测准确率均明显高于动脉早期、动脉晚期,差异均有统计学意义(均P<0.05)。
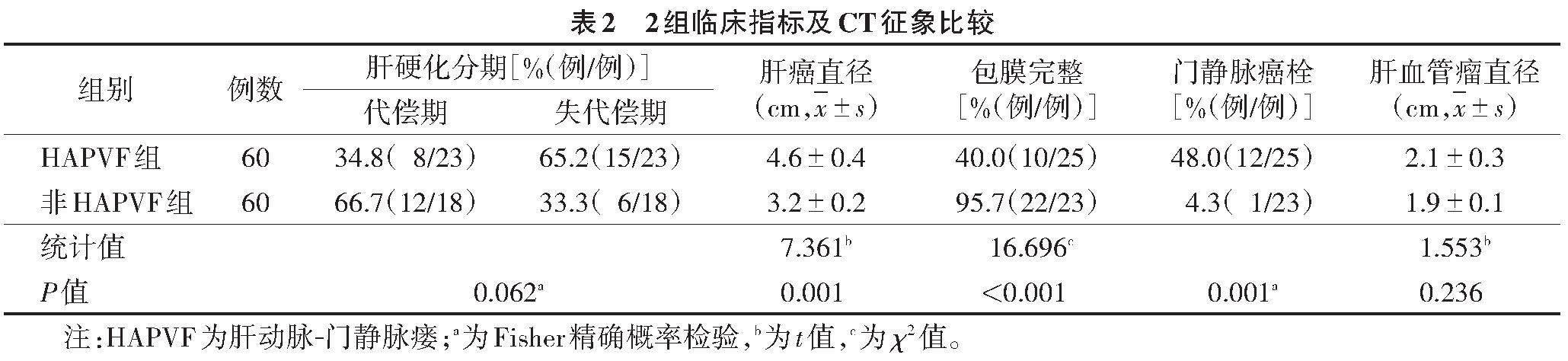
2.3 2组临床指标及CT征象比较(表2)
2组肝癌直径、包膜类型、门静脉癌栓差异均有统计学意义(均P<0.05);肝硬化分期、肝血管瘤直径差异均无统计学意义(均P>0.05)。
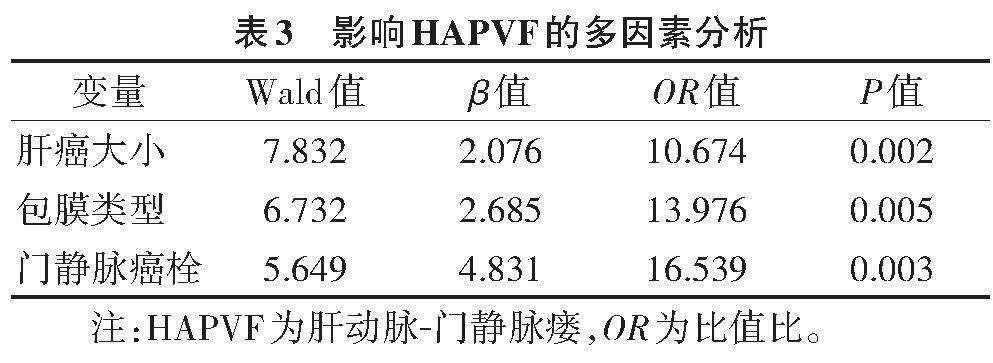
2.4 影响HAPVF的多因素logistic回归分析(表3)
肝癌大小、包膜类型、门静脉癌栓均是HAPVF的独立危险因素(均P<0.05)。
2.5 ROC曲线分析
单因素预测HAPVF效果最好的是包膜类型(AUC=0.778),其次是门静脉癌栓(AUC=0.741),再次是肝癌大小(AUC=0.738)(图1)。综合多因素联合预测分析显示,预测效果从高到低依次为:肝癌大小+包膜类型+门静脉癌栓(AUC=0.957)、肝癌大小+包膜类型(AUC=0.953)、包膜类型+门静脉癌栓(AUC=0.943)、肝癌大小+门静脉癌栓(AUC=0.780)(图2)。
3 讨论
肝动静脉瘘大多数由原发性肝癌引起,主要与肿瘤对门静脉主干、分支侵犯及肿瘤血管内皮生长因子分泌增加,导致肝动脉与门静脉间毛细血管网开放等有关[10]。肝动静脉瘘可增加肝功能损伤、门静脉高压、异位栓塞等的发生风险,还可能导致脾大及加快恶性肿瘤的转移,对肝癌治疗方法的选择和疗效有重要影响,是肝癌术后预后不良的因素之一[11]。目前,肝动脉造影是诊断肝动静脉瘘的金标准,但因其费用高、有创等特点,不能作为常规检查方法。以往,MSCT增强扫描通常采用动脉期、门静脉期、延迟期常规3期扫描,然而在动脉早期时,部分周围型肝动静脉瘘表现为异常强化的血管团,病变周围可出现一过性的局部异常高灌注,随着时间延长,病变区强化程度减弱,故在动脉晚期及门脉期表现为强化范围缩小,呈等或稍高密度影[12]。因此,常规CT 3期增强扫描方式易漏诊肝动静脉瘘。
既往关于HAPVF的CT诊断研究较少,梁祝红等[13]采用MSCT常规肝动脉期及门静脉期扫描诊断原發性肝癌合并HAPVF的敏感度为80.0%,中央型为100.0%,周围型为65.2%。本研究采用双动脉期增强扫描模式诊断HAPVF的敏感度、特异度明显高于动脉早期、动脉晚期,且对周围型、中央型的检测准确率也明显高于动脉早期、动脉晚期。本研究采用双动脉期增强扫描模式对总体及周围型HAPVF的诊断敏感度高于文献报道,中央型相近。刘文洪等[3]采用MSCT动脉增强扫描+CTA的检查方法诊断HAPVF,对周围型、中央型HAPVF的诊断准确率分别为95.00%、92.86%,与本研究相近。李万湖等[9]研究发现,MSCTA对中央型HAPVF检出准确率为100.0%,周围型为85.0%,总体准确率为93.8%,与本研究相近。双动脉期扫描方式与MSCTA相比,除能检出HAPVF外,还可显示肝脏内病变,评估HAPVF病因。
本研究应用双源CT双动脉期增强扫描模式对HAPVF的风险因素进行评估,以期为病情预测提供一定的参考价值。本研究中HAPVF组与非HAPVF组的肝癌大小、包膜类型和门静脉癌栓差异均有统计学意义,说明HAPVF患者多表现为肝癌直径大、包膜不完整及门静脉癌栓。另外,本研究发现肝癌大小、包膜类型及门静脉癌栓是HAPVF的独立危险因素,原因可能是:①肝癌瘤体越大,其对门静脉分支的压迫、侵犯力越大,从而形成瘘,或肝动脉与门静脉之间的吻合支开放形成瘘可能性越大;肝癌瘤体越大,其产生的血管生长因子越多,从而促进新生血管网生成,形成瘘的可能性也增加。②包膜越不完整,肝癌细胞对门静脉侵犯的可能性越大。③门静脉癌栓可能增加门静脉压,门静脉血流受阻时,较大的胆管周围血管丛或肝动脉的门静脉管壁分支均可异常开放,形成经管腔途径的瘘及直接的动静脉瘘。此外,ROC曲线显示,本研究中单因素预测HAPVF效果最好的是包膜类型,其次是门静脉癌栓,再次是肝癌大小。综合多因素联合预测分析,肝癌大小+包膜类型+门静脉癌栓预测效果最好。
综上所述,双源CT双动脉期增强扫描模式对HAPVF的检出及分型诊断具有良好效果,且能对其风险因素进行有效评估,具有重要的临床价值。
[参考文献]
[1] 李春霞,兰春慧. 肝动静脉瘘的研究进展[J]. 国际消化病杂志,2014,34(4):238-240.
[2] CAO B,TIAN K,ZHOU H,et al. Hepatic arterioportal fistulas:a retrospective analysis of 97 cases[J]. J Clin Transl Hepatol,2022,10(4):620-626.
[3] 刘文洪,罗光华,赵衡. 多层螺旋CT动态增强结合CTA对肝动静脉瘘的诊断效果分析[J]. 社区医学杂志,2017,15(7):49-50.
[4] 张学彬,吕维富,季学兵,等. 肝癌合并肝动静脉瘘的DSA表现及临床意义[J]. 医学影像学杂志,2001,11(3):160-163.
[5] DUTTA S,CHAPA U K,ANSARI M I,et al. Arterio-Hepatic venous fistula following liver biopsy:a rare case report and literature review[J]. Vasc Endovascular Surg,2021,55(2):177-182.
[6] 许飞,周纯武. 化疗栓塞治疗原发性肝癌合并肝动静脉瘘的临床研究[J]. 放射学实践,2017,32(5):529-532.
[7] 陈水兵,贺辉,金诗湘,等. 原发性肝癌合并肝动静脉瘘患者经导管动脉化疗栓塞后早期联合射频消融治疗的临床研究[J]. 中国现代医学杂志,2023,33(4):51-55.
[8] WANG Q,KONIARIS L G,MILGROM D P,et al. CT and MRI imaging and interpretation of hepatic arterioportal shunts[J]. Transl Gastroenterol Hepatol,2019,4:34.
[9] 李万湖,董帅,胡旭东,等. 多层螺旋CT血管造影对原发性肝癌动静脉瘘和肝外供血动脉评估价值[J]. 中华肿瘤防治杂志,2017,24(11):755-758.
[10] 蓝晓琳,倪霜玲,龙思琴. TACE联合栓塞治疗中晚期肝癌合并肝动脉-门静脉瘘[J]. 中华肿瘤防治杂志,2020,27(1):80-81.
[11] 郑爱民,刘本智,王潍博,等. 肝动脉栓塞治疗肝癌肝动脉-门静脉瘘所致的大量腹腔积液[J]. 医学影像学杂志,2007,17(1):49-51.
[12] TORABI M,HOSSEINZADEH K,FEDERLE M P. CT of non neoplastic hepatic vascular and perfusion disorders[J]. Radiographics,2008,28(7):1967-1982.
[13] 梁祝红,李成相,宗敏. 原发性肝癌合并肝动脉-门静脉瘘的多排螺旋CT成像探讨[J]. 实用肿瘤杂志,2011,26(3):259-261.

