内膜准备方案对PGT-A患者首次整倍体单囊胚移植妊娠结局及产科结局的影响
王宁宁 刘亚平 陈晓利 王世铭 苏迎春
郑州大学第一附属医院生殖医学中心(郑州 450052)
胚胎植入前遗传学检测(preimplantation genetic testing,PGT)主要包括PGT-A、胚胎植入前染色体结构重排检测和胚胎植入前单基因遗传病的检测[1]。PGT-A是对胚胎进行染色体非整倍体的筛查,主要用于高龄、反复种植失败、反复自然流产等患者改善妊娠结局。
近年来,冻融胚胎移植(frozen-thawed embryo transfer,FET)广泛应用于临床,常规的子宫内膜准备方案对妊娠结局的潜在影响是至关重要的。内膜准备方案大致可分为自然周期(natural cycle,NC)和激素替代周期(hormone replacement therapy,HRT)[2]。目前,许多研究比较了FET的子宫内膜准备方案对妊娠结局的影响,但结论仍存在争议。一项高质量的系统评价[3]表明,激素替代方案和自然周期方案具有相似的妊娠结局。然而,有研究[4-5]认为,自然周期方案的临床妊娠率和活产率高于激素替代方案。另有研究[6-7]提示与自然周期相比,激素替代周期显示出更好的临床妊娠率和活产率。就产科结局方面,结论同样存在争议。有文献[5,8]报道激素替代周期与自然周期有相似的产科结局。另有研究[9]表明激素替代周期方案胚胎移植后巨大儿的风险和剖宫产率显著高于自然周期。
本研究通过分析PGT-A助孕后整倍体单囊胚解冻移植周期不同内膜准备方案的结局,了解排除遗传因素影响后内膜准备方案对冻融胚胎移植周期妊娠结局及产科结局的影响,并首次在PGT-A患者中探究不同年龄组的最佳内膜准备方案。
1 资料与方法
1.1 研究对象回顾性分析2015年9月至2021年7月期间于郑州大学第一附属医院生殖医学中心行PGT-A助孕后首次整倍体单囊胚移植治疗的339个周期的临床资料。纳入标准:因女方高龄、反复种植失败、反复流产等行PGT-A助孕治疗周期;首次行整倍体单囊胚冻融周期。排除标准:子宫解剖结构异常、宫腔粘连、输卵管积水;夫妇一方或双方染色体异常或单基因病;赠卵/供精周期。本研究获河南省郑州大学第一附属医院机构伦理委员会批准(编号:2023-KY-0128),由于为回顾性研究,故免除了知情同意。
1.2 分组根据内膜准备方案分为自然周期组(NC组,n=80)和激素替代组(HRT组,n=259),既往阴道超声监测中被证实有排卵的患者或不愿服药的患者被分配到自然周期组。路途远、就诊不便或不排卵的患者被分配到HRT组。根据年龄分组,分为低龄组(<35岁,n=231)和高龄组(≥ 35岁,n=108)。
1.3 研究方法
1.3.1 囊胚活检、遗传学分析及保存PGT-A患者取卵日采用卵胞浆内单精子注射,受精后第5日或第6日,胚胎学家对可移植囊胚的滋养外胚层(trophoblastic ectoderm,TE)进行活检,再进行单细胞全基因组扩增,具体步骤已在我们先前的研究中描述[10],使用单核苷酸多态性(single mucleotide polymorphism,SNP)微阵列或高通量测序对扩增产物进行分析。活检后进行玻璃化冷冻并保存在液氮中。
1.3.2 子宫内膜准备方案按本中心常规进行[11-12]:(1)自然周期:从月经周期的第8~9天起,定期超声监测卵泡发育和子宫内膜情况,排卵日起肌肉注射黄体酮转化内膜,排卵后第6天进行囊胚移植。(2)激素替代周期:患者从月经来潮的第2~3天开始口服补佳乐(拜耳,德国)2 mg/qd。根据超声检测的子宫内膜厚度,适时调整用药剂量。12~14 d后,进行经阴道超声检查,并测定血清孕酮的浓度。若无优势卵泡,则注射黄体酮60 mg和口服地屈孕酮10 mg(该剂量2 d后改为20 mg),5 d后进行囊胚移植。
1.3.3 冻融囊胚移植胚胎培养和囊胚解冻均按本中心常规进行[13]。根据Gardner的评分标准对囊胚进行评分,胚胎评分≥ 3 BB为优质胚胎,移植过程在B超引导下进行。
1.4 观察指标(1)临床妊娠率:临床妊娠定义为移植后35 d行B超检查宫腔内可见孕囊;临床妊娠率=临床妊娠周期数/移植周期数× 100%。(2)活产率:活产定义为妊娠28周后生产活婴;活产率=活胎分娩周期数/移植周期数× 100%。(3)流产率:流产定义为妊娠28周前的妊娠丢失;流产率=流产周期数/临床妊娠周期数× 100%。(4)剖宫产率:剖宫产定义为经腹切开子宫取出胎儿的手术;剖宫产率=剖宫产周期数/活产周期数× 100%。(5)巨大儿发生率:巨大儿定义为出生体重≥ 4 000 g;巨大儿发生率=巨大儿周期数/活产周期数× 100%。(6)低体重儿率:低体重儿定义为出生体重<2 500 g;低体重儿率=低出生儿周期数/活产周期数× 100%。
1.5 统计学方法采用SPSS 25.0软件进行统计分析。计量资料为正态分布或偏正态分布用均数±标准差表示,采用t检验;偏态分布用中位数(P25,P75)表示,采用非参数检验(Wilcoxon检验);计数资料以率(%)表示,采用χ2检验。多因素logistic回归分析探究影响PGT-A整倍体单囊胚移植妊娠结局及产科结局的影响因素。P<0.05为差异有统计学意义。
2 结果
2.1 基本情况共纳入339个移植周期,其中自然周期组80个周期、激素替代组259个周期。两组间女方年龄、不孕年限、不孕类型、体质量指数(body mass index,BMI)、基础卵泡刺激素(basal follicle stimulating hormone,bFSH)、基础黄体生成素(basal luteinizing hormone,bLH)、反复流产史、反复种植失败史比较差异均无统计学意义(P>0.05)。见表1。
表1 两组患者基本资料的描述Tab.1 Basic data description between the two groups ±s,M(P25,P75)
项目周期数(个)女方年龄[n(%)]<35岁≥35岁不孕年限(年)BMI(kg/m2)bFSH(IU/L)bLH(IU/L)既往妊娠次数(次)既往流产次数(次)反复流产史[n(%)]有无反复种植失败史[n(%)]有无不孕类型[n(%)]原发不孕继发不孕NC组80 HRT组259 t/z/χ2值P值3.197 0.074 48(60.0)32(40.0)3.05 ± 2.72 23.06 ± 2.83 6.07 ± 1.80 3.82(2.37,6.21)2.39 ± 1.38 1.95 ± 1.14 183(70.7)76(29.3)2.64 ± 2.86 23.51 ± 2.97 6.04 ± 1.96 4.84(2.92,7.74)2.67 ± 1.56 2.15 ± 1.40 1.135 1.174 0.117 1.639 1.439 1.305 0.037 0.257 0.241 0.907 0.101 0.151 0.194 0.847 55(68.8)25(31.2)181(69.9)78(30.1)1.525 0.217 3(3.7)77(96.3)20(7.7)239(92.3)0.527 0.468 4(5.0)76(95.0)19(7.3)240(92.7)
2.2 内膜及胚胎移植情况激素替代组的优质囊胚率显著高于自然周期组(67.2%vs.50.0%,P<0.05);两组患者移植日子宫内膜厚度和囊胚发育天数差异均无统计学意义(P>0.05)。见表2。
表2 两组患者内膜及胚胎移植情况比较Tab.2 Comparison of endometrium and embryo transfer between the two groups ±s
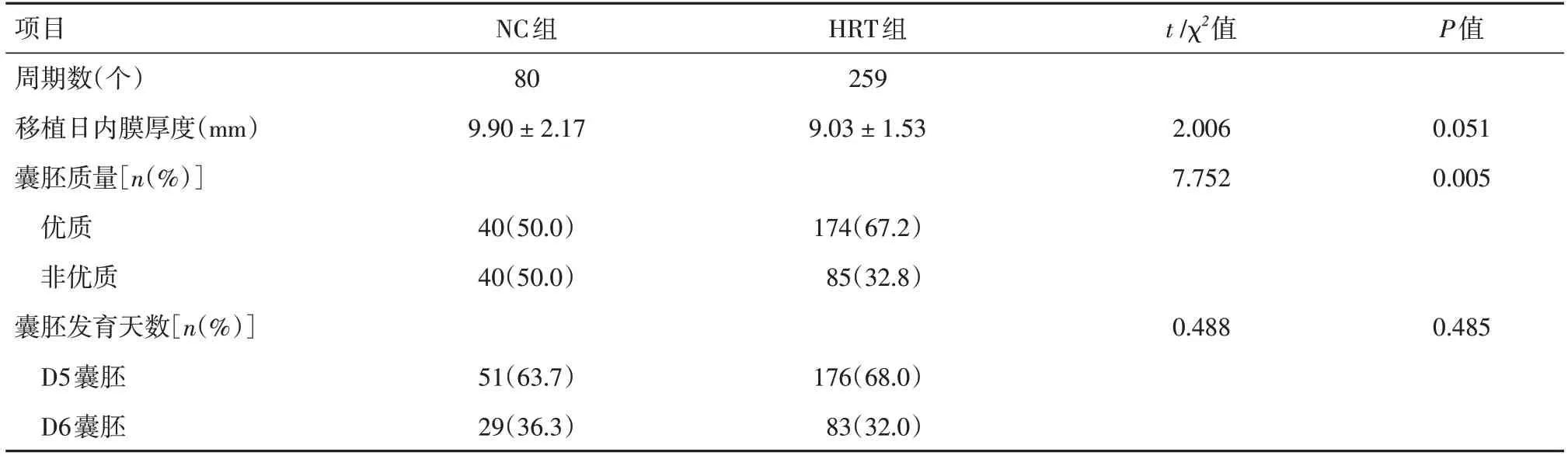
表2 两组患者内膜及胚胎移植情况比较Tab.2 Comparison of endometrium and embryo transfer between the two groups ±s
项目周期数(个)移植日内膜厚度(mm)囊胚质量[n(%)]优质非优质囊胚发育天数[n(%)]D5囊胚D6囊胚NC组80 9.90 ± 2.17 HRT组259 9.03 ± 1.53 t /χ2值P值2.006 7.752 0.051 0.005 40(50.0)40(50.0)174(67.2)85(32.8)0.488 0.485 51(63.7)29(36.3)176(68.0)83(32.0)
2.3 妊娠结局及产科结局与自然周期组相比,激素替代组的活产率显著降低(40.2%vs.53.8%,P=0.032),流产率显著升高(25.4%vs.8.3%,P=0.013),而两组临床妊娠率差异无统计学意义(54.8%vs.60.0%,P=0.442)。激素替代组的剖宫产率、巨大儿发生率均高于自然周期组(79.8%vs.72.1%,P=0.308;14.4%vs.7.0%,P=0.210),低体重儿率低于自然周期组(7.7%vs.11.6%,P=0.656),但差异均无统计学意义(P>0.05)。见表3。

表3 两组妊娠及产科结局的比较Tab.3 Comparison of pregnancy and obstetrical outcomes between the two groups
2.4 妊娠结局及产科结局的影响因素分析行logistic回归分析探究影响PGT-A患者整倍体单囊胚移植妊娠结局的影响因素,结果显示:女方年龄是影响流产率的独立因素(OR=0.172,95%CI:0.044~0.676,P=0.012);女方年龄和囊胚发育天数是影响活产率的因素(OR=4.972,95%CI:1.810~13.659,P=0.002;OR=2.845,95%CI:1.008~8.033,P=0.048);内膜准备方案不影响PGT-A患者的流产率和活产率。见表4。进一步探究影响PGT-A患者整倍体单囊胚移植产科结局的影响因素,结果显示:女方年龄、移植日内膜厚度、囊胚质量、囊胚发育天数和内膜准备方案均不是PGT-A患者剖宫产率和巨大儿发生率的影响因素。见表5。
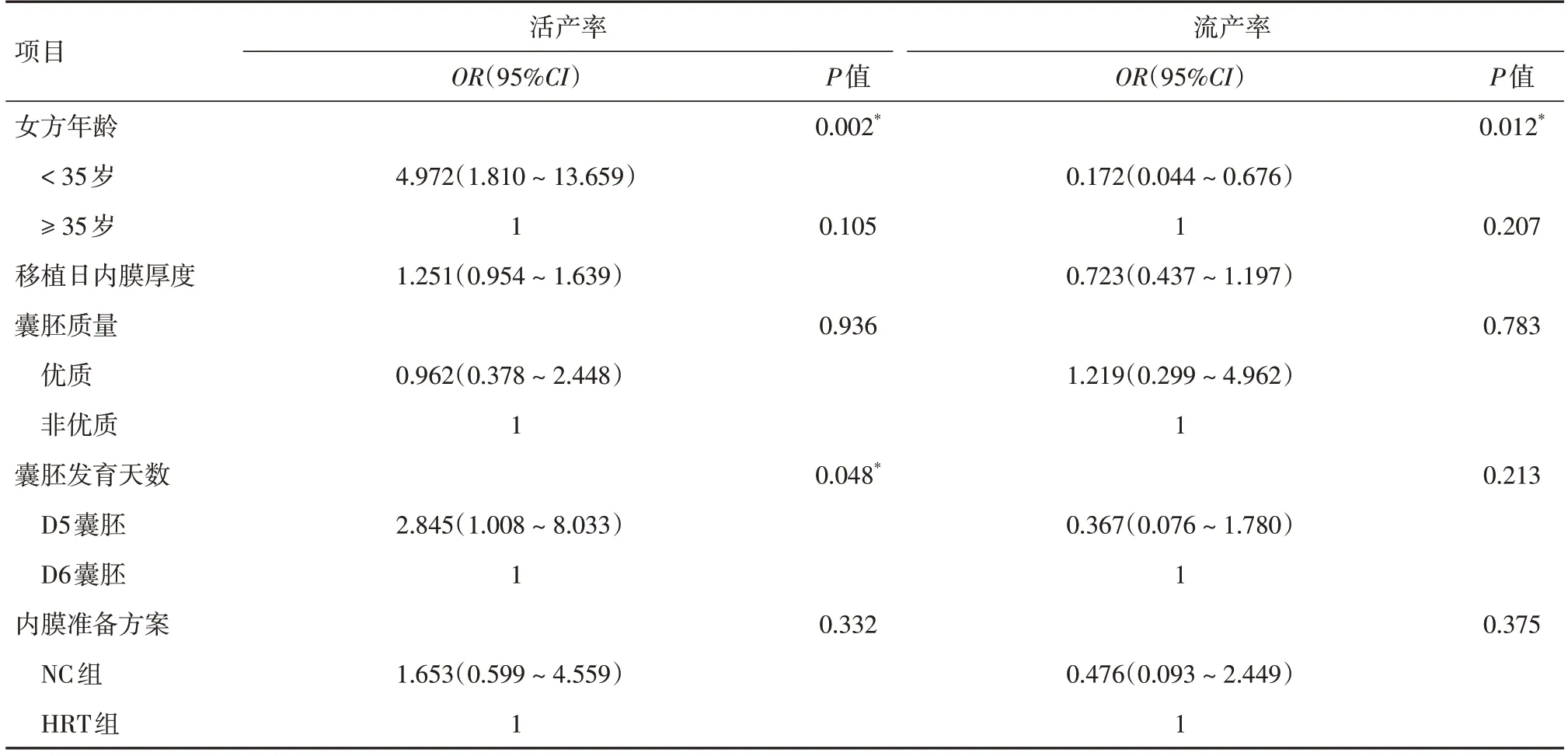
表4 影响妊娠结局的二元logistic回归分析Tab.4 Binary Logistic regression analysis affecting pregnancy outcomes
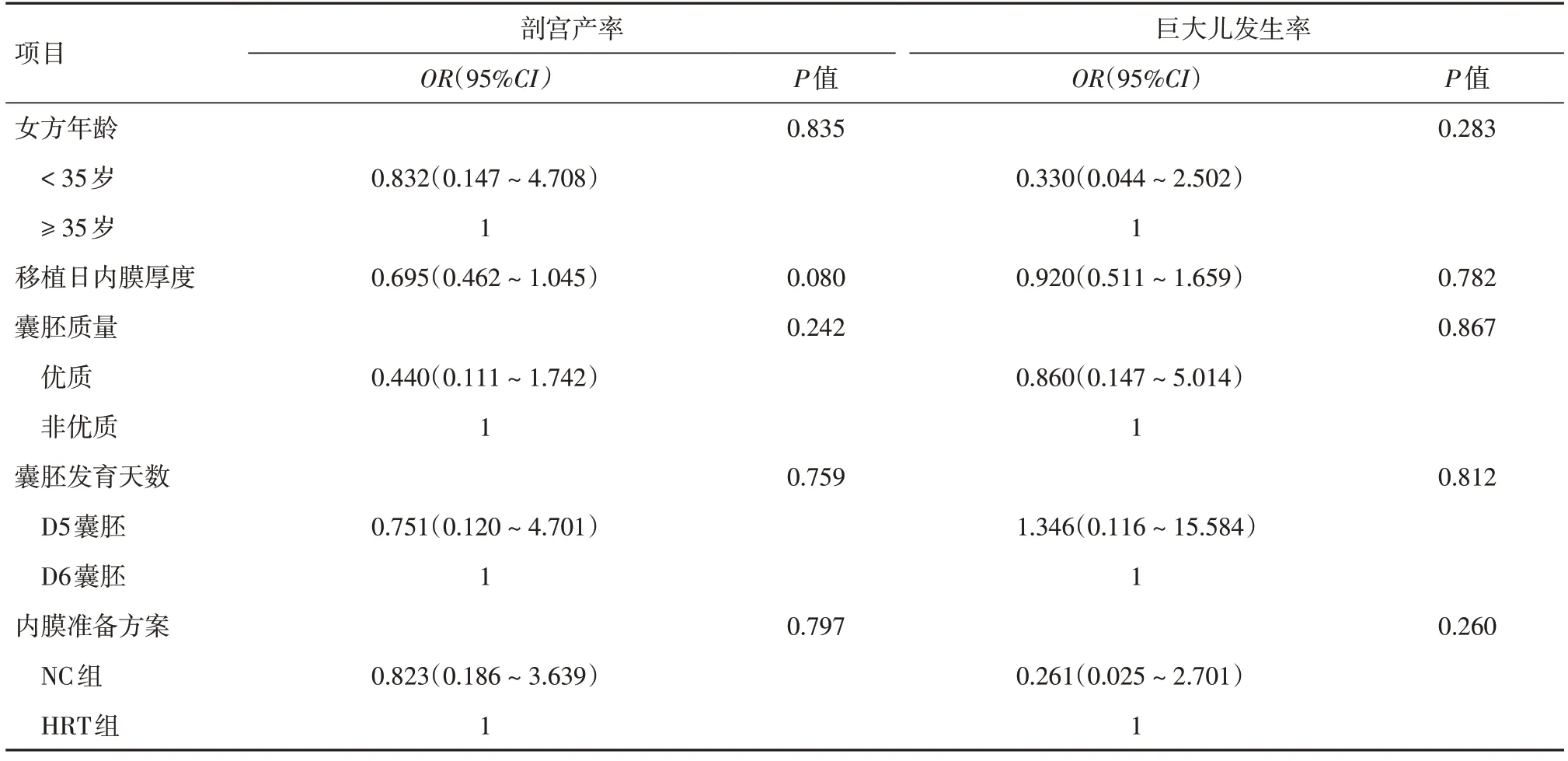
表5 影响产科结局的二元logistic回归分析Tab.5 Binary Logistic regression analysis affecting obstetrical outcomes
2.5 低龄组和高龄组中不同内膜方案的妊娠结局对年龄分层进行分析:低龄组中,其中自然周期组48个周期,激素替代周期组183个周期。结果显示:自然周期组和激素替代组的临床妊娠率、活产率和流产率差异均无统计学意义(P>0.05)。高龄组中,其中自然周期组32个周期,激素替代组76个周期。结果显示:自然周期组的活产率显著高于激素替代组(50.0%vs.28.9%,P=0.036),流产率显著低于激素替代组(10.5%vs.36.1%,P=0.043),两组间临床妊娠率差异无统计学意义。见表6。
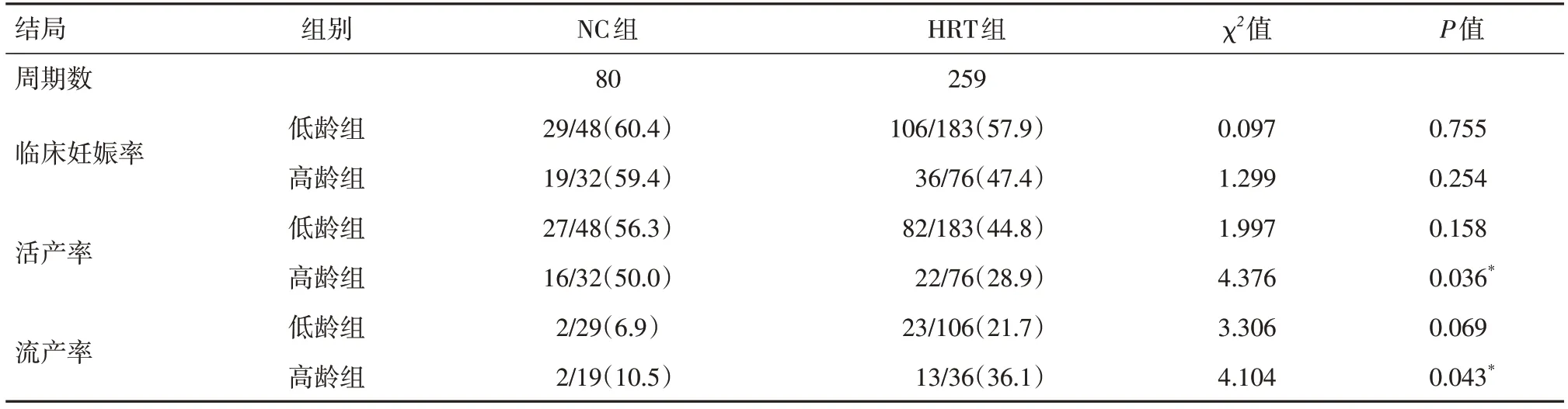
表6 不同年龄组内膜准备方案妊娠结局的比较Tab.6 Comparison of pregnancy outcomes of endometrial preparation programs in different age groups
3 讨论
随着玻璃化冷冻技术的进步,FET的应用在全球范围内急剧增加。研究[14]表明,与新鲜胚胎移植相比,FET不仅可以降低促排卵周期卵巢过度刺激综合征的风险以及相关产科并发症(如早产、低出生体重儿和围产儿死亡)的潜在发生率,还可用于女性生育力的保存[15]。PGT技术对于有严重遗传疾病风险但希望拥有健康家庭的夫妇来说是一种重要的选择。通过对植入子宫前的胚胎进行遗传学检测,排除了胚胎因素导致的植入失败并阻断了遗传性疾病传递给子代。PGT-A助孕技术筛选的整倍体胚胎可排除胚胎异常因素对妊娠结局的影响。对于高龄、反复流产、反复种植失败患者主要行PGT-A助孕。有研究[16-17]表明,高龄和反复种植失败患者囊胚移植的临床妊娠率明显高于卵裂期胚胎,因此越来越多的中心选择囊胚移植。
冻融胚胎移植能否成功妊娠受多种因素的影响,包括胚胎的整倍体性、子宫内膜容受性、以及内膜与胚胎发育的同步性等[18]。冻融胚胎移植患者如何准备子宫内膜,一直是临床医生探讨的热点问题。本研究通过PGT-A技术选择整倍体胚胎移植排除了胚胎因素导致妊娠结局失败的干扰,探究不同内膜准备方案对PGT-A整倍体单囊胚移植的妊娠结局和产科结局的影响。结果提示,两种方案对妊娠结局并无显著影响。自然周期组与激素替代周期组的活产率差异并无显著,与之前研究结果[19]一致。FU等[20]发现无论是否进行PGT-A,子宫内膜准备方案对活产率均无显著影响。本研究在进行多因素logistic回归分析后,结果提示激素替代方案的流产率虽高于自然周期方案,但差异并无统计学意义,子宫内膜准备方案不是流产的独立影响因素(OR=0.476,95%CI:0.093~2.449,P=0.375)。然而,在一项涉及570个FET周期的随机对照实验[21]中,研究人员发现激素替代方案的流产率高于自然周期方案(21%vs.12%,P<0.05)。另一项涉及非PCOS患者的6 840个FET周期的回顾性分析[22]显示,激素替代周期方案相对于自然周期方案有更高的流产率。与之前结论不一致可能原因是本研究人群是进行PGT-A助孕的患者淘汰了非整倍体的胚胎,和子宫内膜更同步。
采用自然周期方案的大部分患者可产生黄体,而激素替代周期方案一般不产生黄体。在胎盘形成之前,黄体是生殖激素和维持妊娠所需的其他物质的重要来源。黄体细胞不仅产生妊娠必需的雌孕激素,而且产生血管活性因子,如对胎盘形成有重要意义的松弛素,调节母体循环系统的变化[23]。若黄体缺失,活性因子缺乏则不良产科结局的风险可能增加。FU等[20]对3 400个FET周期进行了回顾性分析,研究选取月经周期规律的患者进行PGT助孕后玻璃化冷冻囊胚移植,调整相关混杂因素后,结果显示自然周期组和激素替代周期组的新生儿结局相似,而激素替代周期组的剖宫产率显著高于自然周期组。然而,本研究结果提示自然周期组和激素替代周期组的剖宫产率和新生儿结局均无显著差异。可能是本研究只选择PGT-A周期整倍体胚胎进行分析且周期数量有限,结果显示激素替代周期组的剖宫产率虽高于自然周期组,但差异并无统计学意义。
随着女方年龄的增长,其妊娠能力逐渐下降,流产率逐渐上升,采用PGT-A技术助孕可在一定程度上改善妊娠结局。本研究首次证明行PGT-A高龄患者排除非整倍体胚胎因素后,与激素替代周期方案相比,自然周期方案可获得更高的活产率和更低的流产率。可能原因是高龄孕妇是血栓形成事件的独立危险因素,而外源性激素又与血栓形成风险增加相关[24]。此外,雌激素通过不同的机制促进子宫胎盘循环:首先是促进子宫血管生成,其次是促进血管重塑,最后是控制血流动力学。在大多数哺乳动物妊娠中,雌二醇水平的逐渐升高与子宫-胎盘血流量的增加是一致的。这种子宫-胎盘血流量的增加是提供足够的氧气和营养所必需的,同时也是胎儿和胎盘生长发育以及正常妊娠结局所必需的。在孕妇中,血流不足与妊娠并发症有关,如早产、宫内生长迟缓,甚至先兆子痫。血流动力学的变化主要受血管阻力显著降低的影响,这主要是血管重塑和血管扩张增加的共同作用。雌激素可以在子宫-胎盘的血管形成过程中调节细胞滋养层细胞的分化和侵袭,以及以剂量依赖的方式促进绒毛膜外滋养层细胞的迁移。在这一过程中,由胎盘合成的雌二醇主要作用是调节侵袭性滋养层细胞的分泌活动以促进间质重塑和迁移,而雌二醇过早的升高可能导致滋养层细胞凋亡,并与子宫胎盘功能不全有关[25],因此使用激素替代周期方案的高龄女性的妊娠结局进一步恶化。
有研究[26]提出,玻璃化冷冻周期移植D6囊胚获得较低妊娠结局可能与较高的非整倍体率有关。本研究选择整倍体胚胎移植,消除了非整倍体胚胎因素导致不良妊娠结局的干扰,结果发现囊胚发育天数是活产的独立影响因素,内膜准备方案并不影响妊娠结局。与IRANI等[27]结论一致,与移植D6整倍体囊胚相比,D5整倍体囊胚产生更高的活产率。可能原因:首先,胚胎细胞的DNA会随着培养时间的延长发生损伤;其次,D5囊胚对子宫内膜可能具有更好的内膜容受性;此外,HASHIMOTO等[28]比较分析了D5囊胚和D6囊胚的着床率,发现D6囊胚会增加异常纺锤体的发生率,并降低玻璃化冷冻后胚胎移植的着床率。因此,囊胚发育天数在胚胎选择中仍然起着重要作用,即使在考虑整倍体囊胚时也是如此。
本研究局限性:为回顾性分析且样本量偏小,两组内膜准备方案的周期数相差较大,容易引起偏倚,后续需要大样本量和多中心高质量的前瞻性研究或随机对照试验来证实目前的研究结果。
综上所述,目前的结果表明,整体来看,PGTA患者冻融周期整倍体单囊胚移植时,子宫内膜准备方案并不影响妊娠结局及产科结局,但对于高龄患者,自然周期方案是最优选择。

