食品中一种新型伐地那非结构类似物的筛查与定量测定
刘雅婷,郭予昕,刘振强,刘建平,王 欢,刘 洋,戴洁芸,王美玲*
(1.中国检验认证集团湖南有限公司,湖南 长沙 410021;2.长沙海关技术中心,湖南 长沙 410004)
近年来,一些不法商家为了牟取暴利和逃脱监管,在食品中非法添加新型那非类、拉非类等磷酸二酯酶-5(PDE-5)抑制剂的结构类似物[1-12]。这些结构类似物通常由磷酸二酯酶-5 抑制剂的母核结构进行化学修饰、改变部分官能团而得到,由于未经国家药品监督管理部门批准,缺乏药理和毒性实验数据,服用后的不良反应难预料,严重危害群众身体健康[13-14]。为加强食品安全监管,打击食品违法犯罪,国家监管部门陆续颁布了保健食品或食品中非法添加西地那非等PDE-5抑制剂的多个补充检验方法[15-18],涉及100多种化合物。但现有检测方法仅针对指定的化合物检测列表进行靶向检测,无法对新型PDE-5抑制剂结构类似物进行鉴别和准确定量,易产生漏检和假阴性结果。市面上新型PDE-5抑制剂结构类似物不断出现,其结构未知且缺乏标准品,急需建立快速、准确的定性鉴定和定量分析方法,为食品安全监管提供有力的技术支持。
本研究采用液相色谱-四极杆飞行时间高分辨质谱对压片糖果中那非类物质进行筛查,发现一种新型的伐地那非结构类似物,推导出其裂解规律,通过红外光谱、核磁共振谱进行定性解析,最终确定该物质为丙氧基伐地那非,并采用高效液相色谱-串联质谱进行定量分析。为食品中非法添加的新型PDE-5抑制剂结构类似物的筛查、鉴定与定量分析提供了快速、准确、有效的方法。
1 实验部分
1.1 仪器与材料
LC-20ADXR 高效液相色谱仪(配PAD 检测器,日本岛津公司);LC-8A 型制备液相色谱仪(配UV检测器,日本岛津公司);AB Triple Quad 5500 三重四极杆串联质谱仪(美国SCIEX 公司);SCIEX X500R QTOF 超高压液相色谱/四极杆-飞行时间质谱仪(美国SCIEX 公司);Thermo Nicolet 380N 傅里叶变换红外光谱仪(美国Thermo 公司);核磁共振仪(德国Bruker 公司);XS105 电子天平(瑞士Mettler Toledo 公司);KQ-500DE 超声波清洗仪(昆山舒美公司);涡旋振荡器(其林贝尔仪器制造有限公司);H1750离心机(湖南湘仪公司)。
甲醇、乙腈为色谱纯(上海安谱科学仪器有限公司),其余试剂均为分析纯;实验用水为超纯水(美国Millipore超纯水仪制备);那非类快速检测试纸条(深圳市易瑞生物技术股份有限公司);伐地那非标准物质(纯度大于98%,上海安谱实验科技股份有限公司)。90种那非类药物混标(10 μg/mL,天津阿尔塔科技有限公司)。压片糖果、保健酒、蜂蜜酱等购自网络平台。样品制备:固体试样捣碎,混匀;液体试样,充分混匀。
1.2 标准溶液配制
精密称取伐地那非10 mg 于10 mL 容量瓶中,用甲醇溶解并稀释至10 mL,配制成质量浓度为1.0 mg/mL的标准储备液,于-18 ℃保存,有效期6个月。
1.3 样品前处理
精密称取1 g(精确至0.001 g)样品置于50 mL容量瓶中,加入适量甲醇超声提取15 min,放冷至室温,用甲醇定容,转移至50 mL 离心管中,5 000 r/min 离心5 min,上清液经0.22 μm 有机微孔滤膜过滤。取滤液,根据实际浓度用50%甲醇水溶液稀释至线性范围内,备用。
1.4 仪器条件
1.4.1 液相色谱条件色谱柱:安捷伦ZORBAX Eclipse XDB C18色谱柱(4.6 mm×250 mm,5 μm);流动相:A 为甲醇,B 为1%乙酸水溶液,采用二元等度洗脱(70% A、30% B);流速:1.0 mL/min;检测波长:230 nm;进样量:10 μL,柱温:30 ℃。PAD扫描,波长范围为200~400 nm。
1.4.2 液相色谱-串联质谱条件色谱条件:Agilent Poroshell 120 EC- C18(3.0 mm×50 mm,2.7 μm);柱温:35 ℃;进样量:2 μL;流动相:A 为0.1%甲酸水溶液,B 为乙腈;流速:0.2 mL/min。梯度洗脱:0.0~3.0 min,10% B;3.0~8.0 min,10%~50% B;8.0~9.0 min,50%~70% B;9.0~9.5 min,70%~90% B;9.5~11.4 min,90% B;11.4~11.5 min,90%~10% B;11.5~15 min,10% B。
质谱条件:电喷雾离子源(ESI),正离子;扫描方式:多反应监测(MRM);电喷雾电压(IS):5 000 V;气帘气(CUR):137.9 kPa;雾化气(GS1):379.2 kPa;辅助加热气(GS2):413.7 kPa;碰撞气(CAD):55.2 kPa;离子源温度(TEM):500 ℃;监测离子对:m/z503.2/151.2(定量离子对);m/z503.2/299.1(定性离子对)。
1.4.3 液相色谱-高分辨质谱条件色谱条件:Hypersil GOLD C18色谱柱(2.1 mm×100 mm,3 μm);柱温:40 ℃;进样量:5 μL;流速:0.2 mL/min;流动相:A 为0.1%甲酸水溶液,B 为甲醇;流速:0.2 mL/min。梯度洗脱:0.0~1.0 min,20% B;1.0~1.5 min,20%~95% B;1.5~5.5 min,95% B;5.5~6.0 min,95%~ 20% B;6.0~9.0 min,20% B。
质谱条件:ESI,正离子;扫描方式:TOF-MS/MS 模式;电喷雾电压:5 500 V;气帘气压力:241.3 kPa;雾化气压力:379.2 kPa;辅助气压力:379.2 kPa;离子源温度:500 ℃。全扫描一级质谱(MS),质量采集范围为100~1 000 Da;全扫描二级质谱(MS/MS),质量采集范围为50~600 Da。
2 结果与讨论
2.1 定性测定
2.1.1 那非类快检试剂盒测定按照快检试剂盒的操作步骤对压片糖果样品进行检测,结果呈阳性,表明样品中可能含有那非类物质。
2.1.2 液相色谱测定将压片糖果按“1.4.1”色谱条件进行定性分析,发现色谱图中8.54 min 处出现1 个色谱峰(见图1A),其保留时间与伐地那非标准物质相近。在200~400 nm 波长范围内,该色谱峰的光谱图与伐地那非标准物质的光谱图一致,在226 nm处均有最大吸收(见图1B)。因此推测该压片糖果中可能含有伐地那非结构类似物。
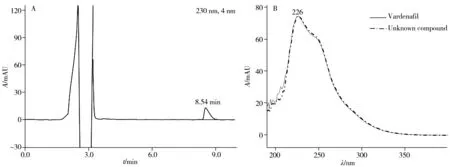
图1 压片糖果中未知化合物的色谱图(A),以及未知化合物与伐地那非标准物质的光谱图比较(B)Fig.1 Chromatogram of the unknown compound in a pressed candy(A),UV spectra of the unknown compound and vardenafil standard(B)
2.1.3 液相色谱-串联质谱测定将样品按照BJS 201805《食品中那非类物质的测定》[18]进行前处理后,采用液相色谱-串联质谱进行定性测定,结果未检出标准方法涵盖的90种那非类物质。但在MRM提取离子流色谱图中新出现1 个色谱峰,其保留时间与标准方法中伐地那非N-氧化物和丙氧苯基艾地那非均不同,但同时具有两者的特征监测离子对m/z505.2/151.1(伐地那非N-氧化物)和m/z503.2/283.2(丙氧苯基艾地那非),m/z503.2 与m/z505.2 相差2 amu,可能是同位素峰,从而推测该化合物可能为那非类结构类似物。
2.1.4 高分辨质谱筛查按照“1.4.3”条件进行定性筛查,在压片糖果样品总离子流色谱图的6.531 min 处出现1 个色谱峰(见图2A),其准分子离子峰为m/z503.234 9([M+H]+),推测该化合物的分子式为C24H34N6O4S,与伐地那非的准分子离子峰m/z489.219 9([M+H]+)相差14.015 0 amu,可能多1个CH2基团。二级质谱扫描中主要的特征碎片离子为m/z391.135 9、376.108 4、326.177 7、299.118 1、284.130 0、151.088 6(图2B)。其中m/z299.118 1、m/z284.130 0、m/z151.088 6均与伐地那非的特征碎片离子相同,而m/z391.135 9、m/z326.177 7 均比伐地那非的特征碎片离子m/z377.124 8、m/z312.161 0 大14 amu,说明该化合物具有伐地那非的母核结构,而取代基略有不同,可能多1 个CH2基团。结合伐地那非的结构和裂解规律[19-20],推测该化合物可能为伐地那非苯环上的乙氧基被丙氧基代替,其裂解途径如图3所示。
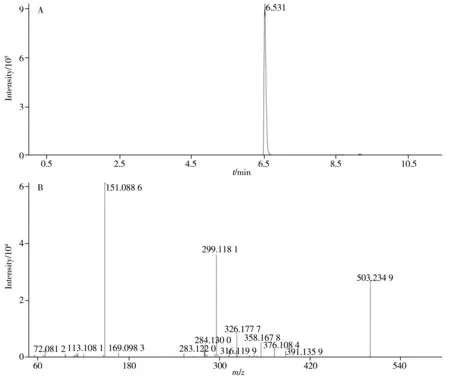
图2 样品中未知化合物的色谱图(A)和二级碎片离子质谱图(B)Fig.2 Chromatogram(A) and secondary fragment MS spectrum(B) of the unknown compound in a sample

图3 未知化合物的质谱裂解途径Fig.3 MS fragment pathway of unknown compound
2.1.5 分离纯化目标化合物称取约25 g 样品于500 mL 锥形瓶中,加入100 mL 甲醇,超声提取15 min,5 000 r/min 离心5 min,上层清液过滤。取滤液,重复提取2 次,滤液旋转蒸发浓缩至约10 mL,采用制备色谱纯化,色谱条件为甲醇-1%乙酸水溶液(70∶30);检测波长为230 nm,流速为10 mL/min。收集主色谱峰成分,减压蒸发除去溶剂后冷冻干燥,即得纯化目标化合物(约100 mg)。
称取纯化后的目标化合物20 mg 置于50 mL 容量瓶中,加甲醇超声溶解,稀释至刻度并混合均匀,即得测试溶液。将测试溶液按“1.4.1”条件测定,检测波长为230 nm,采用峰面积归一化法进行定量分析,得到纯度为98.0%。
2.1.6 红外光谱鉴定取“2.1.5”纯化样品进行红外光谱测定,光谱图显示含有仲氨基、苯环、甲基、亚甲基、羰基、咪唑环、碳氮双键、砜基、碳氮单键和碳氧单键等官能团的特征吸收峰。具体如下:①仲氨基的氮氢伸缩振动吸收峰(3 181、3 119 cm-1);②苯环的碳氢伸缩振动和面外弯曲振动吸收峰(3 076、824、772、737、729 cm-1);③甲基和亚甲基的碳氢伸缩振动和弯曲振动吸收峰(2 963、2 879、2 851、2 816、1 485、1 462、1 456、1 383 cm-1);④羰基的特征吸收峰(1 692 cm-1);⑤苯环和咪唑环的骨架伸缩振动吸收峰、碳氮双键伸缩振动吸收峰(1 622、1 597 cm-1);⑥砜基的特征吸收峰、碳氮单键和碳氧单键的伸缩振动吸收峰(1 350、1 325、1 306、1 275、1 171、1 146、1 117 cm-1)。因此,样品中的未知化合物与伐地那非具有相似的特征官能团。
2.1.7 核磁共振谱图及结构确证取“2.1.5”纯化样品,以DMSO-D6为溶剂,测试核磁共振氢谱(1H NMR)、碳-13 核磁共振谱(13C NMR)、无畸变极化转移谱(DEPT135)、同核位移相关谱(COSY)、异核单量子相关谱(HSQC)和异核多键相关谱(HMBC)(见图4)。1H NMR、COSY 谱数据和13C NMR、DEPT135、HSQC、HMBC 谱数据分别见表1 和表2。1H NMR 谱显示34 个质子信号;其中1 个活泼氢、4 个甲基、9 个亚甲基和1 个1,2,4-三取代苯环的质子信号。13C NMR 谱显示22 根碳谱线,哌嗪环结构对称,2 对碳信号两两重叠,与质谱分析所得分子式(C24H34N6O4S)一致,比较1H NMR 谱和1H NMR(+D2O)谱发现,活泼氢信号明显减弱至消失,归属为仲氨基的质子信号。通过1H NMR 谱、13C NMR 谱和DEPT135 谱,确定了4 个甲基、9 个亚甲基和1 个1,2,4-三取代苯环。结合HMBC 谱、HSQC 谱和COSY 谱可以确定相连的体系。综合质谱、红外光谱和核磁共振谱结果,确定该化合物为丙氧基伐地那非,由伐地那非苯环上的乙氧基被丙氧基代替而得到,其结构式见图5。

表1 未知化合物的核磁共振1H NMR与COSY谱数据Table 1 1H NMR and COSY data of the unknown compound
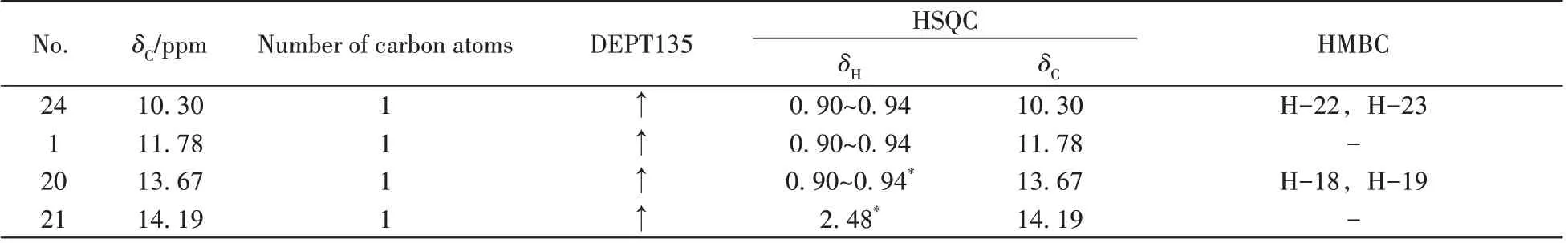
表2 未知化合物的核磁共振13C NMR、DEPT135、HSQC与HMBC谱数据Table 2 13C NMR,DEPT135,HSQC and HMBC data of the unknown compound

(续表2)
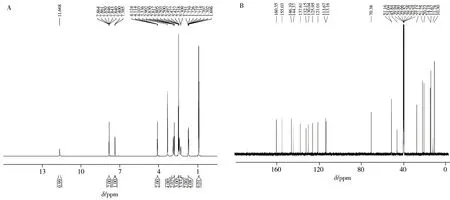
图4 未知化合物的1H NMR谱(A)与13C NMR谱(B)Fig.4 1H NMR(A) and 13C NMR(B) spectra of unknown compound
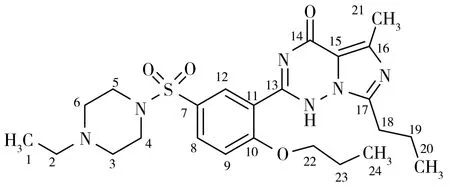
图5 丙氧基伐地那非的结构Fig.5 Structure of O-propylvardenafil
2.2 定量分析
2.2.1 标准溶液配制精密称取丙氧基伐地那非10 mg于10 mL 容量瓶中,用甲醇溶解并稀释至10 mL,配制成质量浓度为1.0 mg/mL 的标准储备液。准确吸取丙氧基伐地那非储备液适量,用50%甲醇水溶液稀释,摇匀,配制成质量浓度依次为1、2、4、6、8、10、20、40、60、80、100 ng/mL的系列标准工作液。
2.2.2 线性关系、检出限与定量下限取“2.2.1”标准工作液,按照“1.3”和“1.4.2”方法分别进行前处理和上机测定,采用外标法定量,以目标化合物的峰面积(y)对质量浓度(x)绘制标准曲线。目标化合物在1.0~100 ng/mL 范围内呈良好的线性关系,线性方程为y=12 606.33x-504.97,相关系数(r2)为0.999 2。以3 倍信噪比(S/N≥3)对应的空白样品添加质量浓度作为方法的检出限(LOD),以10倍信噪比(S/N≥10)对应的空白样品添加质量浓度作为方法的定量下限(LOQ),得到丙氧基伐地那非的检出限为0.02 mg/kg,定量下限为0.05 mg/kg。
2.2.3 基质效应采用提取后添加法评价基质效应(ME)的影响,将空白样品基质提取液用50%甲醇水溶液稀释不同倍数(10、20、50、100倍)后配制20 ng/mL 标准溶液进行测定。按下式计算基质效应:ME(%)=(Aae-As)/As×100%,式中Aae为样品基质溶液中化合物的峰面积平均值;As为标准溶液中化合物的峰面积平均值。ME 的绝对值随着基质效应的增强而变大,ME 为正值说明存在基质增强效应,负值则为基质抑制效应。当ME绝对值<20%时表示基质效应较弱,ME绝对值在20%~50%范围内时表示具有中等强度基质效应,ME绝对值大于50%时表示基质效应较强。
结果表明,保健酒和蜂蜜酱的ME 在±20%之间,基质效应较小。压片糖果有一定的基质效应,当采用50%甲醇水溶液将空白基质稀释50倍后,基质效应有所减弱。因此,阳性样品在前处理中增加稀释过程,以降低基质效应的影响。根据需要可采用空白基质提取液配制适当浓度的基质标准工作溶液进行定量。
2.2.4 回收率与相对标准偏差在压片糖果、保健酒和蜂蜜酱3种空白基质样品中,添加低、中、高3 个浓度水平的丙氧基伐地那非,分别制成0.05、0.1、0.5 mg/kg 的样品,每个浓度做6 次平行实验,考察方法的回收率和相对标准偏差(RSD)。表3 结果显示,不同加标水平下的平均回收率为76.5%~104%,RSD为1.6%~5.1%,满足分析要求。

表3 食品中丙氧基伐地那非的平均加标回收率及相对标准偏差(n=6)Table 3 Average recoveries and relative standard deviations of O-propylvardenafil in foods(n=6)
2.3 实际样品测定
采用本方法对网购的100 批次样品进行测定。结果表明,有5 批次糖果(含人参牡蛎压片糖果和人参糖)检出丙氧基伐地那非,含量为510~3.23×104mg/kg;3批次养生保健酒检出丙氧基伐地那非,含量为180~730 mg/kg。
3 结 论
本研究建立了一种快速、灵敏、准确的筛查和鉴定PDE-5抑制剂新型结构类似物的方法。通过高效液相色谱筛查、高分辨质谱初步推测、红外光谱和核磁共振进一步确证,发现并鉴定了一种新型的非法添加物丙氧基伐地那非。该化合物在国内未见报道,尚无相关检验标准,课题组目前已申请该化合物的CAS号登记,并进行标准物质研制,为打击食品违法犯罪提供了技术支撑。

