UPLC-Q-TOF-MS/MS 法分析栾樨叶的化学成分
肖观林,江洁怡,程青云,张靖年,汤瑞茵,李冬梅,李养学*
(1.广东省中医药工程技术研究院 广东省中医药研究开发重点实验室,广东 广州 510095;2.广州中医药大学附属中山中医院/中山市中医院,广东 中山 528401;3.广州中医药大学 第五临床医学院,广东 广州 510405)
阔苞菊Pluchea indica(L.) Less.又称冬青菊或栾樨,属菊科阔苞菊属植物,在亚洲、非洲、美洲的热带和亚热带地区分布,在我国主要分布在南部沿海一带,具有良好的开发前景[1]。其收录于《广西药用植物名录》《中药辞海》《广州植物志》和《岭南采药录》,作为广西民间常用药,主要有抗氧化、抗炎和神经药理学作用,常用于治疗小儿食积、瘿瘤痰核、风湿骨痛等症[2-3]。中药栾樨的药用部位是其茎叶,具有温中化食、软坚散结的功效,临床上多用于治疗淋巴结核、消肿解毒等病症,在抗结核活性、抗炎活性、体外抗癌等方面具有积极作用[4-7]。目前,关于栾樨叶化学成分的定性鉴别鲜有报道,国内也未见相关文献,不利于栾樨叶的全面质量控制和进一步深入研究。
超高效液相色谱-四极杆-飞行时间高分辨质谱(UPLC-Q-TOF-MS/MS)能同时对目标物的母离子和子离子进行数据采集并准确分析,具有高分辨率、高灵敏度等优点,在对照品不足的情况下可对成分进行结构预测分析,已成为当前中药复杂体系中化学成分定性分析的重要工具[8-11]。本研究采用UPLC-Q-TOF-MS/MS 技术对栾樨叶的化学成分进行定性分析,根据各色谱峰的一级和二级质谱信息、相关中药质谱数据库匹配及各成分的裂解规律进行解谱鉴别,为栾樨叶的化学成分解析、药效物质基础研究、质量变化规律探讨及开发利用提供了科学依据。
1 实验部分
1.1 仪 器
Milli-Q Advantage A10 纯水系统,ExionLC AC 型液相色谱仪(岛津公司),SCIEX X500R 飞行时间质谱仪(AB Sciex 公司),XS205 型1/10 万电子分析天平(Mettler-Toledo 公司),Sorvall Legend Micro 17R型离心机(Thermo Fisher Scientific 公司)。
1.2 试剂与药材
对照品:咖啡酸(批号110885-201703,质量分数≥98%)、异阿魏酸(批号111698-201904,质量分数≥98%)、绿原酸(批号110753-202018,质量分数为96.2%)、木犀草苷(批号111720-202111,质量分数为96.6%)、毛蕊花糖苷(批号111530-201914,质量分数为95.2%)购自中国食品药品检定研究院;蔓荆子黄素(批号M-037-180524)、隐绿原酸(批号Y-067-180425)、异绿原酸B(批号Y-069-180105)、新绿原酸(批号RFS-X01411804010)、异绿原酸A(批号Y-068-190329)购自成都瑞芬思生物科技公司;异绿原酸C(批号AF20121801)购自成都埃法生物技术有限公司。未标明纯度的对照品质量分数均大于98%。实验用水为屈臣氏蒸馏水,甲醇、乙腈、甲酸均为质谱纯(美国Fisher Chemical公司),其余试剂均为分析纯。植物原料于2021年10月采自广西省合浦县,由广东省第二中医院刘法锦研究员鉴定为阔苞菊Pluchea indica(L.) Less.。
1.3 实验方法
1.3.1 对照品溶液制备分别精密称取咖啡酸、异阿魏酸、绿原酸、木犀草苷、毛蕊花糖苷、蔓荆子黄素、隐绿原酸、异绿原酸B、新绿原酸、异绿原酸A、异绿原酸C 各对照品适量,置于10 mL量瓶中,用甲醇溶解稀释至刻度,制备成含各成分40~100 μg•mL-1的混合对照品溶液,经0.22 μm 微孔滤膜滤过备用,作为混合对照品溶液。
1.3.2 供试品溶液制备将真空干燥的栾樨叶粉碎过二号筛,称取约0.25 g粉末于50 mL具塞锥形瓶中,加入50%甲醇25 mL,25 ℃下超声(频率40 kHz,功率300 W)提取30 min,放冷,混匀,于13 000 r/min离心5 min。移取上层清液,过0.22 μm微孔滤膜,置于样品瓶中,即得。
1.3.3 色谱条件Waters UPLC BEH C18色谱柱(2.1 mm×100 mm,1.7 μm),流速:0.25 mL/min,柱温:40 ℃,进样量:1 μL。流动相为乙腈(A)-0.1%甲酸水溶液(B),洗脱梯度:0~3 min,5%~20% A;3~7 min,20%~43% A;7~14 min,43%~55% A;14~17 min,55%~98% A。
1.3.4 质谱条件采用电喷雾离子源(ESI),正、负离子模式扫描,MS扫描范围:m/z100~1 500,雾化气压(GS1):379.2 kPa,辅助气压(GS2):379.2 kPa,气帘气压(Cur):241.3 kPa,离子源温度:500 ℃。正离子模式:离子喷雾电压为5.5 kV,簇裂解电压为100 V,MS2碰撞能量为35 eV;负离子模式:离子喷雾电压为-4.5 kV,簇裂解电压为-80 V,MS2碰撞能量为35 eV。
2 结果与讨论
2.1 化学成分分析
在上述色谱、质谱条件下对栾樨叶进行正、负离子全扫描,获得基峰色谱图(BPC图)见图1。对色谱图中各色谱峰进行精确质量数识别,通过对照品、精确准分子离子峰、二级谱图等信息,结合文献数据、数据库及裂解规律等信息进行比对,从栾樨叶中共鉴别出52 个化学成分(见表1),包括2 个香豆素类(化合物12、17),15 个黄酮类(化合物20~21、23~30、34、41、44、46、48),16 个苯丙素类(化合物11、13~15、18~19、22、31~33、36~38、40、42~43),5 个生物碱类(化合物2、6~7、16、39),5个脂肪酸类(化合物45、47、49~50、52),3个有机酸类(化合物4~5、35),3个氨基酸类(化合物1、8~9),1 个酚酸类(化合物10)和2 个其他类化合物(化合物3、51)。其中23 个成分为栾樨叶中首次报道,11个化合物通过与对照品进行比对后得到明确识别。

表1 栾樨叶化学成分的UPLC-Q-TOF-MS/MS鉴定与分析Table 1 Qualitative analysis of chemical constituents in the leaves of Pluchea indica(L.) Less.by UPLC-Q-TOF-MS/MS
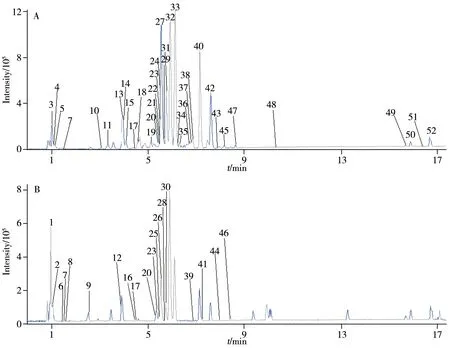
图1 栾樨叶在负(A)、正(B)离子模式下的基峰色谱图Fig.1 Base peak chromatograms of the leaves of Pluchea indica(L.) Less.in negative(A) and positive(B) ion modes
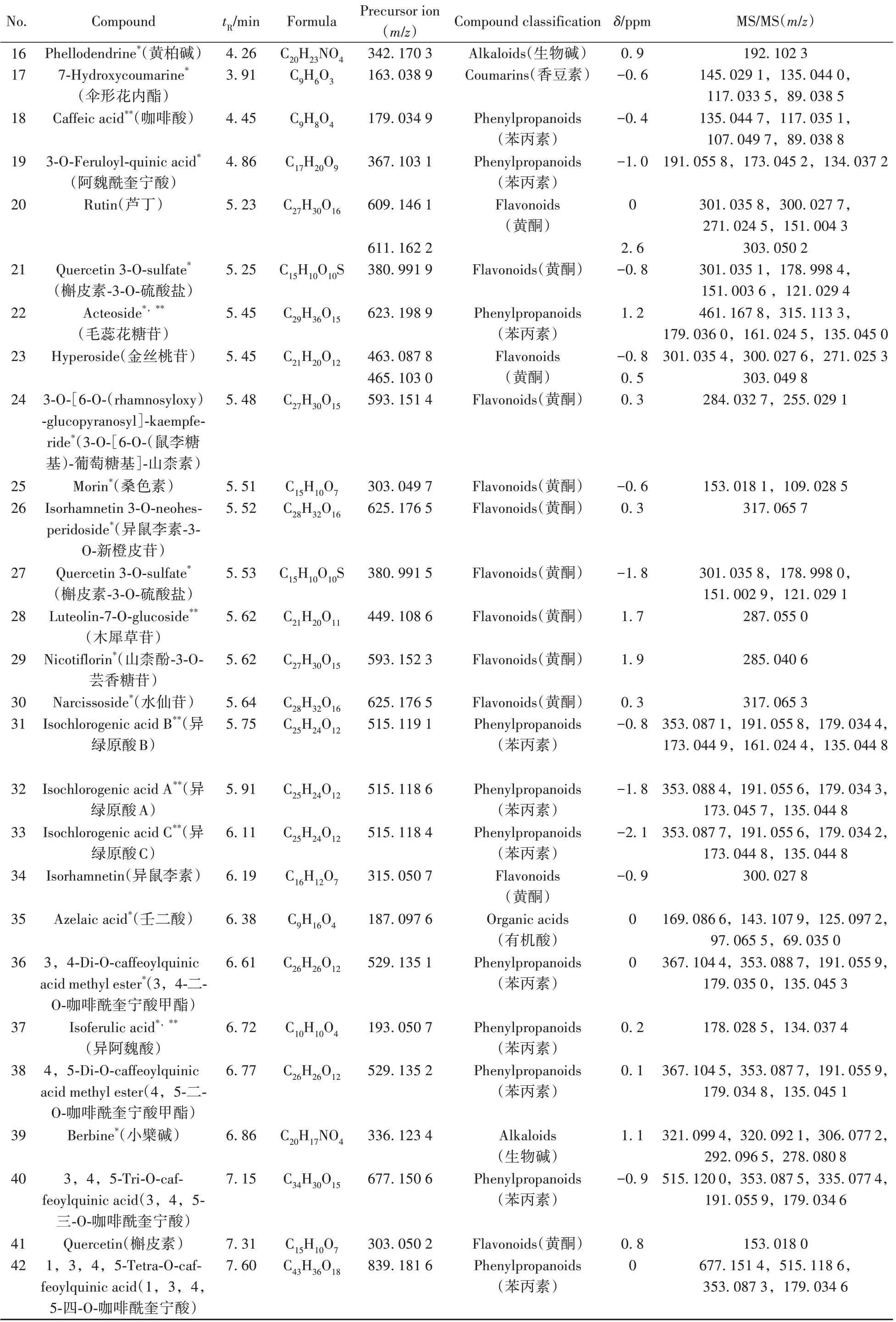
(续表1)
2.2 栾樨叶中各类化合物的质谱分析
2.2.1 香豆素类作为一大类植物次生代谢产物,香豆素类化合物多在正离子模式下响应好,在质谱裂解过程中常丢失一系列CO 的碎片离子峰。在正离子模式下,17 号峰的准分子离子峰为m/z163.038 9 [M+H]+,失去1分子H2O产生碎片离子m/z145.029 1 [M+H-H2O]+,然后失去1分子CO产生碎片离子m/z117.033 5 [M+H-H2O-CO]+;m/z163.038 9 [M+H]+还可失去1 分子CO 产生碎片离子m/z135.044 0 [M+H-CO]+,继而失去1分子CO和H2O产生m/z89.038 5 [M+H-2CO-H2O]+碎片离子。结合质谱裂解规律和文献[8]报道,推测其为伞形花内酯,可能的裂解途径见图2A。12号峰的准分子离子峰为m/z179.034 0 [M+H]+,其二级碎片离子有明显丢失H2O、CO 产生的离子碎片m/z151.038 5 [M+HCO]+、m/z133.029 0 [M+H-CO-H2O]+、m/z123.044 2 [M+H-2CO]+和m/z105.033 2 [M+ H-CO-H2OCO]+,通过对比质谱裂解规律以及文献[9]报道,推测其为秦皮乙素,可能的裂解途径见图2B。
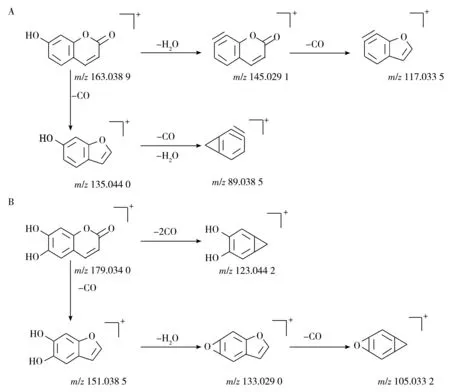
图2 伞形花内酯(A)和秦皮乙素(B)的质谱裂解途径Fig.2 Fragment pathways of 7-hydroxycoumarine(A) and esculetin(B)
2.2.2 黄酮及其苷类黄酮类化合物具有C6-C3-C6的基本骨架,其主要裂解方式是丢失中性离子,例如CO、CO2等以及RDA 裂解重排、糖苷键断裂、糖环裂解等。黄酮氧苷类化合物的裂解方式主要是糖苷键断裂,多见各种糖基如鼠李糖基(Rha)、葡萄糖基(Glc)和芸香糖基(Rutinose)等的丢失。在负离子模式下,20号峰的准分子离子峰为m/z609.146 1 [M-H]-,失去1分子葡萄糖基和1分子鼠李糖基,产生m/z301.035 8 [M-H-C6H10O4-C6H10O5]-和m/z300.027 7 [M-H-C6H10O4-C6H10O5-H]-,而其苷元再次RDA 裂解产生m/z151.004 3[M-H-C6H10O4-C6H10O5-C8H5O3]-和m/z271.024 5[M-H-C6H10O4-C6H10O5-CH2O]-,结合质谱裂解规律及文献[9]报道,推测其为芦丁,可能的裂解途径见图3A。负离子模式下,23号峰的准分子离子峰为m/z463.087 8 [M-H]-,二级特征碎片离子有m/z301.035 4 [M-H-C6H10O5]-、m/z300.027 6 [M-H-C6H10O5-H]-和m/z271.025 3 [M-H-C6H10O5-H-CO]-,通过分析其质谱裂解规律并结合文献[9]报道,推测其为金丝桃苷,可能的质谱裂解途径见图3B。
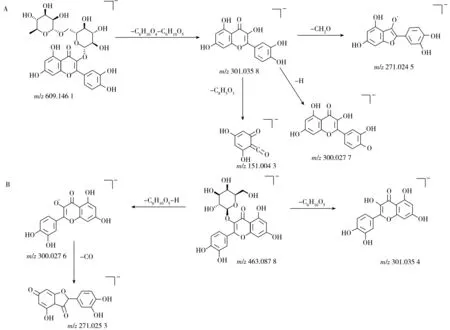
图3 芦丁(A)和金丝桃苷(B)的质谱裂解途径Fig.3 Fragment pathways of rutin(A) and hyperoside(B)
2.2.3 苯丙素类苯丙素类化合物主要以负离子[M-H]-的准分子离子峰形式存在,在高能碰撞下易发生18 Da(H2O)、45 Da(COOH)、44 Da(CO2)等中性分子丢失,从而产生相应的特征碎片离子峰。负离子模式下,18 号峰的准分子离子峰为m/z179.034 9 [M-H]-,二级碎片离子有明显丢失CO2、H2O、CO 产生的离子碎片m/z135.044 7 [M-H-CO2]-、m/z117.035 1 [M-H-CO2-H2O]-、m/z107.049 7 [MH-CO2-CO]-和m/z89.038 8 [M-H-CO2-CO-H2O]-,与对照品比对,可确证其为咖啡酸,可能的质谱裂解行为见图4A。13 号峰的准分子离子峰为m/z353.087 0 [M-H]-,二级质谱存在失去咖啡酰基的特征碎片离子m/z191.055 2 [M-H-C9H6O3]-,丢失奎宁酸的特征碎片离子m/z179.034 6 [M-H-C7H10O5]-,以及二级碎片m/z173.045 3 [M-H-C9H6O3-H2O]-、m/z161.024 5 [M-H-C7H12O6]-和m/z135.044 9 [MH-C7H12O6-CO2]-,与对照品比对,可确证其为绿原酸,可能的质谱裂解行为见图4B。32号峰的准分子离子峰为m/z515.118 6 [M-H]-,失去1 个分子的咖啡酰基特征碎片离子m/z353.088 4 [M-H-C9H6O3]-和单咖啡酰奎宁酸的特征碎片离子m/z191.055 6[M-H-2C9H6O3]-、m/z179.034 3 [M-H-C9H6O3-C7H10O5]-,以及二级碎片m/z173.045 7 [M-H-2C9H6O3-H2O]-和m/z135.044 8 [M-H-C9H6O3-C7H10O5-CO2]-,与对照品比对,可确证其为异绿原酸A,可能的质谱裂解行为见图4C。峰31、33 与32 具有相同的分子式且碎片离子相似,推断这3 个化合物应为同分异构体,经对照品比对,确证峰31 为异绿原酸B,峰32 为异绿原酸A,峰33 为异绿原酸C。峰36 的一级质谱信息显示,准分子离子峰为m/z529.135 1 [M-H]-,其二级特征碎片离子包括m/z367.104 4 [M-H-C9H6O3]-、m/z353.088 7 [M-HC9H6O3-CH2]-、m/z191.055 9 [M-H-C9H6O3-CH3-C9H6O3]-、m/z179.035 0 [M-H-C9H6O3-CH3-C7H10O5]-和m/z135.045 3 [M-H-C9H6O3-CH3-C7H10O5-CO2]-,结合裂解规律及文献报道[5],推断其为3,4-二-O-咖啡酰奎宁酸甲酯,可能的质谱裂解行为见图4D。36 号峰和38 号峰有相同的质谱裂解规律,结合文献[5]报道,推测其为4,5-二-O-咖啡酰奎宁酸甲酯。峰40的准分子离子峰为m/z677.150 6 [M-H]-,连续失去1 个分子的咖啡酰基生成碎片离子m/z515.120 0 [M-H-C9H6O3]-、m/z353.087 5 [M-H-2C9H6O3]-、m/z191.055 9 [M-H-3C9H6O3]-及m/z179.034 6 [M-H-2C9H6O3-C7H10O5]-,结合裂解规律及文献[5]报道,推断其为3,4,5-三-O-咖啡酰奎宁酸。峰42 的准分子离子峰为m/z839.181 6 [M-H]-,其二级质谱中同样出现连续失去咖啡酰基生成的碎片离子m/z677.151 4 [M-H-C9H6O3]-、m/z515.118 6[M-H-2C9H6O3]-、m/z353.087 3 [M-H-3C9H6O3]-和m/z179.034 6 [M-H-3C9H6O3-C7H10O5]-,结合裂解规律及文献[5]报道,推断其为1,3,4,5-四-O-咖啡酰奎宁酸。

图4 咖啡酸(A)、绿原酸(B)、异绿原酸A(C)、3,4-二O-咖啡酰奎宁酸甲酯(D)的质谱裂解途径Fig.4 Fragment pathways of caffeic acid(A),chlorogenic acid(B),isochlorogenic acid A(C) and 3,4-di-Ocaffeoylquinic acid methyl ester(D)
2.2.4 生物碱类本实验结合二级碎片特征及文献报道,从栾樨叶中共筛查出1个原小檗碱类生物碱及1个四氢原小檗碱类生物碱。同时,还筛查出鸟苷、腺苷与甜菜碱3个其他类生物碱。生物碱类化合物多以正离子形式存在。在正离子模式下,峰16 的准分子离子峰为m/z342.170 3 [M+H]+,其中m/z为192.102 3 的碎片离子来自于母核发生RDA 裂解或B 环发生裂解,进一步失去—CH3产生m/z为177.078 1的碎片离子,结合裂解规律及文献[11]报道,推断其为黄柏碱,可能的质谱裂解行为见图5A。峰39 的准分子离子峰为m/z336.123 4 [M+H]+,其产生特征碎片离子m/z321.099 4 [M+H-CH3]+、m/z320.092 1 [M+H-CH3-H]+和m/z306.077 2 [M+H-2CH3]+,在二级质谱中还可观察到由m/z320.092 1相继失去CO 和CH3产生的碎片离子m/z292.096 5 [M+H-CH4-CO]+与m/z278.080 8 [M+H-2CH3-CO]+,根据以上裂解方式,结合文献[9,11]报道,推断其为小檗碱,可能的质谱裂解行为见图5B。峰2 的准分子离子峰为m/z118.086 0 [M+H]+,二级碎片离子包括m/z59.072 7 [M+H-N(CH3)3]+和58.064 8 [M+H-CH3COOH]+,根据以上裂解方式,结合文献[9]报道,推断其为甜菜碱。
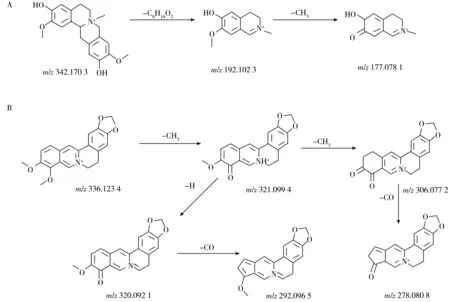
图5 黄柏碱(A)和小檗碱(B)的质谱裂解途径Fig.5 Fragment pathways of phellodendrine(A) and berbine(B)
2.2.5 脂肪酸类脂肪酸类化合物结构包含脂肪链和羧基或酯基基团,易发生α-裂解产生[M-HCO]-、[M-H-CO2]-、[M-H-H2O]-、[M-H-COOH]-、[M-H-CH]-和[M-H-CH2]-等类型的特征碎片离子。在负离子模式下,峰35 的准分子离子峰为m/z187.097 6 [M-H]-,二级质谱中可观察到准分子离子峰脱去1 分子H2O 得到碎片离子m/z169.086 6 [M-H-H2O]-,准分子离子峰脱去1 分子CO2得到碎片离子m/z143.107 9 [M-H-CO2]-,继续丢失1 分子H2O 得到碎片离子m/z125.097 2 [M-H-CO2-H2O]-,继续脱去C2H4得到碎片m/z97.065 5 [M-H-CO2-H2O-C2H4]-,连续再脱去C2H4得到碎片m/z69.035 0[M-H-CO2-H2O-2C2H4]-,结合裂解规律及文献[9]报道,推断其为壬二酸,可能的质谱裂解行为见图6。峰49 的准分子离子峰为m/z293.212 2 [M-H]-,二级质谱碎片离子包括m/z275.202 1 [M-H-H2O]-、m/z171.029 0 和m/z121.102 8,将这些特征离子与MassBank 数据库比对,推断峰49 为9(R)-羟基-10(E),12(Z),15(Z)-十八碳三烯酸。同理,根据相对分子质量、碎片离子与MassBank 数据库比对结果,推断峰45、47、50、52 分别为9(S),12(S),13(S)-三羟基十八碳-10-烯酸、9(S),12(S),13(S)-三羟基十八碳-10(E),16(Z)-二烯酸、13(S)-羟基-9(Z),11(E),15(Z)-十八碳三烯酸和9-羟基-10,12-十八碳二烯酸。
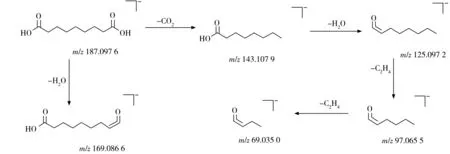
图6 壬二酸的质谱裂解途径Fig.6 Fragment pathways of azelaic acid
2.2.6 其他类除以上化合物外,本实验还从栾樨叶中鉴定出 2个核苷类化合物(腺苷和鸟苷)、3个氨基酸类化合物(精氨酸、亮氨酸和苯丙氨酸)及3种其他化合物(原儿茶酸、甘露醇和姜糖脂B)。
2.3 讨 论
栾樨叶的化学成分众多,类别主要包括黄酮类、苯丙素类、生物碱类、脂肪酸类和香豆素类化合物,其中不同类型、不同来源的活性成分可通过协同或互补作用,实现多成分、多通路、多靶点综合治疗。栾樨叶的主要化学成分为苯丙素类化合物,在本研究中苯丙素类主要包含咖啡酰奎宁酸类化合物,其多具有热不稳定性,易分解或异构化,临床上多用于抗菌、消炎、抗氧化、抗病毒、止咳、保肝等方面,而且对当前人们所关注的病症有极大潜力,如降血糖、降血脂、抗肿瘤等[5,12-14]。研究发现咖啡酰奎宁酸衍生物(峰32、38、40、42~43)为肠道麦芽糖酶抑制剂,奎宁酸部分的甲基酯化以及分子中咖啡基的数量有助于抑制活性[5]。同时,最新研究发现咖啡酰奎宁酸类化合物具有抑制甲型流感病毒神经氨酸酶的作用[15]。本研究利用UPLC-Q-TOF-MS/MS 技术对栾樨叶中化学成分进行分析,总结出不同化学成分的裂解规律,并构建了栾樨叶的化学成分数据库,为后续栾樨叶的开发利用、药效物质基础研究、质量控制及临床应用提供了依据。此外,栾樨叶中某些已知成分未在此次分析中检测到,可能与ESI的离子化效率有关,一些难区分的同分异构体的精确结构仅依靠QTOF进行指认存在一定局限,还需进一步结合核磁共振等波谱分析技术进行确证。
3 结 论
本研究利用超高效液相色谱-四极杆-飞行时间高分辨质谱技术分析栾樨叶中的化学成分,通过精确相对分子质量筛选分析,比较一级精确质荷比和二级碎片离子,并结合二级质谱裂解规律、化学对照品质谱信息、相关文献报道及Scifinder、MassBank 和ChemSpider 等数据库,从栾樨叶的50%甲醇提取物中分离和鉴定出52个化学成分,其中23个成分为首次在栾樨叶中发现,进一步丰富和完善了栾樨叶的化学成分库,为栾樨叶的质量控制及药效物质基础研究奠定了基础。

