胸腔镜肺段切除术和肺叶切除术对早期非小细胞肺癌患者肺功能及免疫功能的影响
张辉
(昌乐县人民医院胸外科,山东潍坊 261000)
非小细胞肺癌(NSCLC)早期症状不典型,一旦治疗不及时,癌细胞可向周围扩散或侵袭,引起多器官功能受累,增加患者死亡风险[1-2]。 目前,早期NSCLC治疗多以手术为主,可直接切除病灶,阻止其持续生长及转移, 以提高远期生存率。 胸腔镜手术在早期NSCLC 治疗中应用广泛,其切口小、出血少,借助胸腔镜视野亦可完成病灶的准确定位及切除,实现肿瘤的良好控制[3-4]。 肺段切除术与肺叶切除术均为常用胸腔镜术式,前者仅切除病变肺段,后者则切除病变所在的肺叶,两者均可清除病灶组织,改善患者预后[5-6]。但关于两种术式在早期NSCLC 中的具体应用效果及对肺功能的影响仍需深入明确。 基于此,本研究选取2020年1月—2022年12月我院收治的78 例早期NSCLC 患者为对象, 旨在分析胸腔镜肺段切除术和肺叶切除术在早期NSCLC 中的应用效果。报道如下。
1 资料与方法
1.1 一般资料
选取我院收治的78 例早期NSCLC 患者,按随机数字表法分为两组,各39 例。本研究经院医学伦理委员会批准。 对照组男24 例,女15 例;年龄43~68 岁,平均年龄(52.63±5.17)岁;肿瘤大小0.8~2.0 cm,平均肿瘤大小(1.22±0.23)cm; 肿瘤TNM 分期: Ⅰ期23例,Ⅱ期16 例;肿瘤位置:左肺22 例,右肺17 例。 观察组男23 例, 女16 例;年龄42~67 岁, 平均年龄(52.59±5.15)岁;肿瘤大小0.7~2.0 cm,平均肿瘤大小(1.19±0.21)cm;肿瘤TNM 分期:Ⅰ期22 例,Ⅱ期17例;肿瘤位置:左肺21 例,右肺18 例。 两组一般资料对比,差异无统计学意义(P>0.05),具有可比性。
1.2 入选标准
纳入标准:符合《中华医学会肺癌临床诊疗指南(2019 版)》中NSCLC 的诊断标准,经病理学检查确诊; 肿瘤TNM 分期Ⅰ~Ⅱ期; 均行胸腔镜手术治疗;心、肺器官功能正常;患者及家属知情同意。 排除标准:存在肝、肾器官功能衰竭;术前接受放、化疗;存在胸腔手术史;合并其他恶性肿瘤;伴有重症感染。
1.3 方法
两组均完善术前检查,行胸腔支气管插管静脉复合麻醉,取健侧卧位,术中健侧肺通气,并以四孔法开展腹腔镜手术,主操作孔位腋前线第四肋间作2.5 cm切口,副操作孔位腋后线第七肋间、第九肋间作1 cm切口,观察孔为腋前线第七肋间作1 cm 切口;观察组行胸腔镜肺段切除术治疗:术前借助影像学手段定位病灶,术中再观察胸腔内情况,准确定位病灶位置;游离解剖段门区,使靶段动脉暴露,沿叶间肺动脉将靶段肺动脉分支游离出病灶离断,之后自肺静脉向远端游离并处理段内静脉;开展患肺纯氧通气,使其充分膨胀,10~15 min 后,靶段肺组织持续处于膨胀状态,且呈鲜红色,其他肺组织萎缩并呈暗红色,做好段间平面标记;明确段平面后,电凝标记,并在中央处沿段间静脉分离,使其走形暴露清晰,之后切除靶段,周围肺组织用直线切割缝合器处理, 术中及时冰冻检查,若存在淋巴结转移、切缘阳性等,则需扩大切除,最后清扫纵膈淋巴结。 对照组行胸腔镜肺叶切除术治疗:充分萎陷患侧肺,若病灶处于外周,则行楔形切除;若病变接近肺门,则直接将肺叶切除,先游离使肺门显露,将肺静脉、肺动脉及肺叶支气管等游离出,解剖性分离并离断肺门结构, 同时开展第10、12 及部分11组的淋巴结清扫,完成肺叶切除后,顺支气管树开展第13、14 组淋巴结清除,并及时送检,之后清扫纵膈淋巴结。
1.4 观察指标
(1)手术情况:比较两组手术时间、术中出血量、术后引流量、术后引流时间的差异。 (2)肺功能:术前及术后1 个月,两组用肺功能检测仪测定用力肺活量(FVC)、第1 s 用力呼气容积(FEV1)及1 秒率(FEV1/FVC)变化。 (3)免疫功能:术前及术后7 d,两组均采集3 mL 静脉血, 离心后以流式细胞仪测定CD3+、CD4+、CD8+水平、CD4+/CD8+变化。(4)并发症:肺漏气、肺部感染、肺不张等。
1.5 统计方法
采用SPSS 22.0 统计学软件进行数据分析,计数资料以[n(%)]表示,用χ2检验;计量资料以(±s)表示,用t 检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组手术情况对比
观察组手术时间长于对照组,术中出血量、术后引流量少于对照组,术后引流时间短于对照组,组间差异有统计学意义(P<0.05)。 见表1。
表1 两组NSCLC 患者手术情况对比(±s)
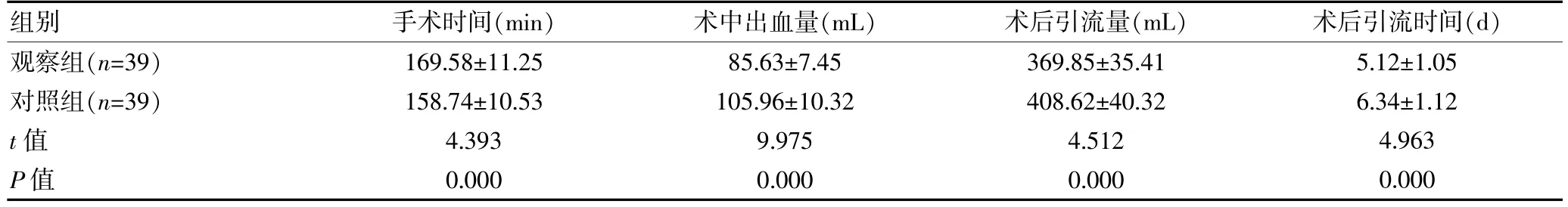
表1 两组NSCLC 患者手术情况对比(±s)
组别手术时间(min)术中出血量(mL)术后引流量(mL)术后引流时间(d)观察组(n=39)对照组(n=39)t 值P 值169.58±11.25 158.74±10.53 4.393 0.000 85.63±7.45 105.96±10.32 9.975 0.000 369.85±35.41 408.62±40.32 4.512 0.000 5.12±1.05 6.34±1.12 4.963 0.000
2.2 两组肺功能对比
术前,两组肺功能相比,差异无统计学意义(P>0.05);术后1 个月, 观察组FVC、FEV1、FEV1/FVC 均高于对照组,组间差异有统计学意义(P<0.05)。 见表2。
表2 两组NSCLC 患者肺功能对比(±s)
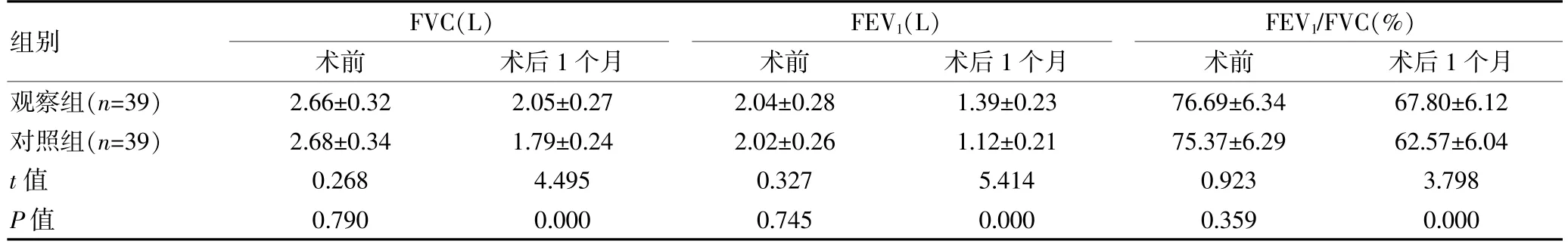
表2 两组NSCLC 患者肺功能对比(±s)
组别FVC(L)术前术后1 个月FEV1(L)术前术后1 个月FEV1/FVC(%)术前术后1 个月观察组(n=39)对照组(n=39)t 值P 值2.66±0.32 2.68±0.34 0.268 0.790 2.05±0.27 1.79±0.24 4.495 0.000 2.04±0.28 2.02±0.26 0.327 0.745 1.39±0.23 1.12±0.21 5.414 0.000 76.69±6.34 75.37±6.29 0.923 0.359 67.80±6.12 62.57±6.04 3.798 0.000
2.3 两组免疫功能对比
术前,两组免疫功能相比,差异无统计学意义(P>0.05);术后7 d,观察组CD3+、CD4+、CD4+/CD8+均高于对照组,CD8+低于对照组,组间差异有统计学意义(P<0.05)。 见表3。
表3 两组NSCLC 患者免疫功能对比(±s)
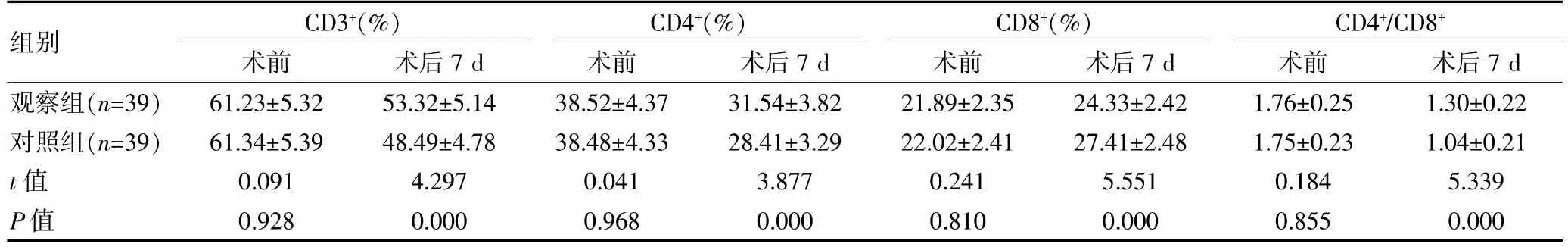
表3 两组NSCLC 患者免疫功能对比(±s)
组别CD3+(%)术前术后7 d CD4+(%)术前术后7 d CD8+(%)术前术后7 d CD4+/CD8+术前术后7 d观察组(n=39)对照组(n=39)t 值P 值61.23±5.32 61.34±5.39 0.091 0.928 53.32±5.14 48.49±4.78 4.297 0.000 38.52±4.37 38.48±4.33 0.041 0.968 31.54±3.82 28.41±3.29 3.877 0.000 21.89±2.35 22.02±2.41 0.241 0.810 24.33±2.42 27.41±2.48 5.551 0.000 1.76±0.25 1.75±0.23 0.184 0.855 1.30±0.22 1.04±0.21 5.339 0.000
2.4 两组并发症对比
对照组出现肺部感染2 例,肺漏气1 例,肺不张1 例,发生率为10.26%(4/39);观察组出现肺部感染1 例,发生率为2.56%(1/39)。 两组并发症相比,差异无统计学意义(χ2=0.855,P=0.355)。
3 讨论
NSCLC 病因复杂, 临床认为环境因素为其发生的始动因素,加之遗传、年龄、免疫等多种因素影响,致使体内致癌物无法被代谢酶及时溶解,从而产生基因突变。而基因突变又无法被DNA 系统及时修复,则可引起细胞周期紊乱,凋亡信号与增殖信号间的平衡被打破,进而出现细胞不可控的增殖现象,最终形成肿瘤组织[7-8]。 而恶性肿瘤不仅生长迅速,还具有较强的侵袭性、转移性,一旦肿瘤出现转移,则可引起受累器官功能障碍, 又进一步增加临床治疗难度。 早期NSCLC 的治疗多以手术为主, 既往多以开放式手术为主,但其创伤大、术后并发症多。而随着微创理念的普及,加之医学水平的提高,胸腔镜手术逐渐应用于临床,并具备创伤小、恢复快等特点,逐渐成为早期NSCLC 的首选术式。 但胸腔镜手术也存在多种术式,还需尽可能选择创伤更小、 术后恢复更快的手术方式,以满足临床及患者需求。
肺叶切除术为胸腔镜常用术式,其在胸腔镜视野下可准确定位病变位置,并明确病灶所处肺叶与周围组织关系,之后开展肺叶的切除,可直接清除体内肿瘤组织,避免其扩散或转移,以改善患者预后。但肺叶切除术的切除范围更为广泛,对机体创伤较大,术中出血量多,老年患者肺叶切除风险性高,且肺叶切除对肺功能影响较大,术后肺功能恢复缓慢。 本研究结果显示,观察组手术时间长于对照组,术中出血量、术后引流量均少于对照组, 术后引流时间短于对照组,术后观察组FVC、FEV1、CD3+、CD4+水平、FEV1/FVC与CD4+/CD8+均高于对照组,CD8+水平低于对照组,组间差异有统计学意义(P<0.05),两组并发症发生率比较,差异无统计学意义(P>0.05),这提示胸腔镜肺段切除术治疗早期NSCLC 效果更佳, 可减轻手术创伤,避免免疫过度抑制,加快肺功能恢复,安全可靠。分析原因为, 肺段切除术是一种更为精准的微创手术,相较于肺叶切除术,其仅切除病变所在的肺段,可保留该肺叶的其他正常肺组织,在清除肿瘤的同时进一步减少对肺组织结构的破坏,从而减轻手术创伤[9-10]。同时,随着医学水平的提高,术前可借助影像学手段精准定位病灶肺段,加之术中的观察确认,又可进一步提高靶段切除的准确性, 尽可能降低肺组织损伤,进而减少对正常肺生理功能的影响,利于术后肺功能的恢复。而肺段切除术在本研究中手术时间较肺叶切除术长,考虑可能与肺段切除术应切除范围小、肺组织破坏小有关, 上述的前提在于术中操作更为精确、细致,故相应延长手术时间。 但随着医学水平的提高及操作医师熟练度的增加, 肺段切除术所需时间也会随之减少。
综上所述, 胸腔镜肺段切除术治疗早期NSCLC效果优于肺叶切除术,可减轻机体创伤,减轻免疫抑制,加快肺功能恢复,安全可行。

