茯苓皮与白茯苓中三萜类成分的HPLC指纹图谱与化学模式识别研究
占慧慧,丁 婵,彭思源,刘 媛,孟俊华,肖作为,崔培梧*
1湖南中医药大学药学院;2国家中医药管理局中药药性与药效三级科研实验室;3湖南中医药大学菌物药研究室,长沙 410208
茯苓又名茯菟、茯灵、松腴等,系多孔菌科真菌茯苓Poriacocos(Schw.) Wolf的干燥菌核,味甘、淡,性平,归心、肺、脾、肾经,有利水渗湿、健脾宁心的功效[1]。茯苓收载于《中华人民共和国药典》(简称《中国药典》)2020年版一部,是中药四君八珍之一,有“十方九苓”之称[2]。茯苓的主要药效物质是茯苓多糖和茯苓三萜[3],现代药理学研究表明,茯苓三萜具有利尿[4]、抗肿瘤[5]、免疫调节[6]、抗炎[7]、抗衰老[8]、降血糖和调血脂[9]等作用,是当前用于表征茯苓质量和效应的重要指标[10-12]。目前市场流通的茯苓主要为栽培品种,不同的产地、加工方式、饮片规格等都可能影响茯苓药材和饮片的质量[11,13]。2020年版《中国药典》仅采用薄层色谱法鉴别控制茯苓和茯苓皮药材的质量,难以全面反映其质量的优劣。指纹图谱研究是现代中药领域内普遍被认可、应用较广泛的中药质量控制方法之一,具有整体性高、特征性强等优势,符合中药多成分综合作用的特点,有进一步鉴别、鉴定和分类的潜力[14,15]。化学模式识别可对指纹图谱的多维信息进行分析,准确反映药材的质量差异,从而达到整体描述和合理评价药材质量的目的[13]。本研拟究建立茯苓皮(源于茯苓菌核表皮)与白茯苓(源于茯苓菌核去皮后的部位)的HPLC指纹图谱,并结合模式识别手段分析各共有峰对指纹图谱的作用,找出其中的主要峰和特征峰,从整体上评价茯苓皮和白茯苓中各化学物质的差异,为茯苓药材的质量控制提供依据。
1 仪器与试药
1.1 仪器
Agilent 1200高效液相色谱仪(美国安捷伦科技公司);JS-40型超声波清洗仪(常州鸿泽实验科技有限公司)。
1.2 试药
对照品茯苓新酸B(批号140723,质量分数≥98%)、茯苓新酸A(批号140314,质量分数≥98%)、去氢茯苓酸(批号140903,质量分数≥98%)、松苓新酸(批号140902,质量分数≥98%)、茯苓酸(批号140212,质量分数≥98%)购自成都克洛玛生物科技有限公司;去氢土莫酸(批号AF21032,质量分数≥98%)购自成都埃法生物科技有限公司;乙腈为色谱纯,水为怡宝纯净水,其余试剂为分析纯。
茯苓药材样品来源见表1,经湖南中医药大学刘塔斯教授鉴定为多孔菌科真菌茯苓Poriacocos(Schw.) Wolf的不同药用部位,符合《中国药典》2020年版各项规定。

表1 样品信息
2 方法与结果
2.1 色谱条件
Agilent 5 TC-C18(2)(250 mm × 4.6 mm,5 μm)色谱柱;流动相为0.3%磷酸水溶液(A)-乙腈(B),梯度洗脱:0~18 min,50%→60%B;18~28 min,60%B;28~58 min,60%→92%B;58~68 min,92%B;检测波长为242 nm和203 nm;进样量10 μL;柱温25 ℃;体积流量1.0 mL/min。
2.2 溶液的制备
2.2.1 混合对照品溶液的制备
精密称取各茯苓三萜酸对照品适量,加甲醇溶解制成茯苓新酸B、去氢土莫酸、茯苓新酸A、去氢茯苓酸、茯苓酸、松苓新酸对照品质量浓度分别为0.020 7、0.071 4、0.006 4、0.038 6、0.037 1、0.017 1 mg/mL的混合对照品溶液。放于4 °C冰箱保存,备用。
2.2.2 供试品溶液的制备
取茯苓样品粉末2.0 g(过60目筛),精密称定,置100 mL干燥具塞锥形瓶中,加甲醇50 mL,密塞,称定质量,超声处理30 min,放冷,用甲醇补足减失质量,滤过,茯苓皮样品滤液经0.22 μm微孔滤膜过滤,取续滤液,即得;白茯苓样品滤液先旋转蒸干后定容至2.0 mL,再经0.22 μm微孔滤膜过滤,取续滤液,即得。
2.3 方法学考察
2.3.1 精密度实验
取云南茯苓皮样品(S8),按“2.2.2”项下方法制备供试品溶液,依据“2.1”项下的色谱条件,连续进样测定6次,以茯苓酸(10号峰)为参照峰,计算得各色谱峰的相对保留时间和相对峰面积的RSD值分别在0.04%~0.86%和0.22%~1.69%之间,表明仪器精密度良好。
2.3.2 稳定性实验
取云南茯苓皮样品(S8),按“2.2.2”项下方法制备供试品溶液,依据“2.1”项下的色谱条件,分别于0、2、4、6、8、12、24 h进样测定,测得各色谱峰的相对保留时间和相对峰面积并计算得RSD值分别在0.01%~0.27%和0.32%~1.19%之间,表明供试品溶液在24 h内稳定。
2.3.3 重复性实验
取云南茯苓皮样品(S8)6份,精密称定,按“2.2.2”项下方法制备供试品溶液,依据“2.1”项下的色谱条件进样测定,测得各色谱峰的相对保留时间和相对峰面积并计算得RSD值分别在0.02%~0.29%和0.81%~4.53%之间,表明方法重复性好。
2.3.4 溶剂峰和滞后峰的考察
取空白对照(甲醇)和云南茯苓皮样品(S8)溶液,检测时间延长至2 h,考察结果如图1所示,测试结果表明空白溶剂无干扰且未见滞后峰出现。
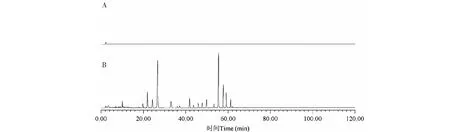
图1 溶剂峰(A)和滞后峰(B)的考察色谱图Fig.1 Investigation chromatograms of solvent peaks (A) and hysteresis peaks (B)
2.4 指纹图谱的建立
2.4.1 指纹图谱共有模式的建立
将14批不同产地不同药用部位茯苓样品的色谱图导入“中药色谱指纹图谱相似度评价系统(2012版)”软件分别生成茯苓样品的叠加图谱和对照指纹图谱。14批茯苓皮和白茯苓样品的叠加图谱和对照指纹图谱见图2,茯苓皮和白茯苓各自的对照指纹图谱及混合对照品HPLC色谱图见图3。由图2和3可知,茯苓皮与白茯苓样品共有的典型色谱峰有15个;经与混合对照品溶液色谱图比对,

图2 14批茯苓皮与白茯苓饮片的指纹图谱叠加图和对照指纹图谱Fig.2 Superimposed fingerprints and control fingerprint of 14 batches of Poriae Cutis and White Poria decoction pieces
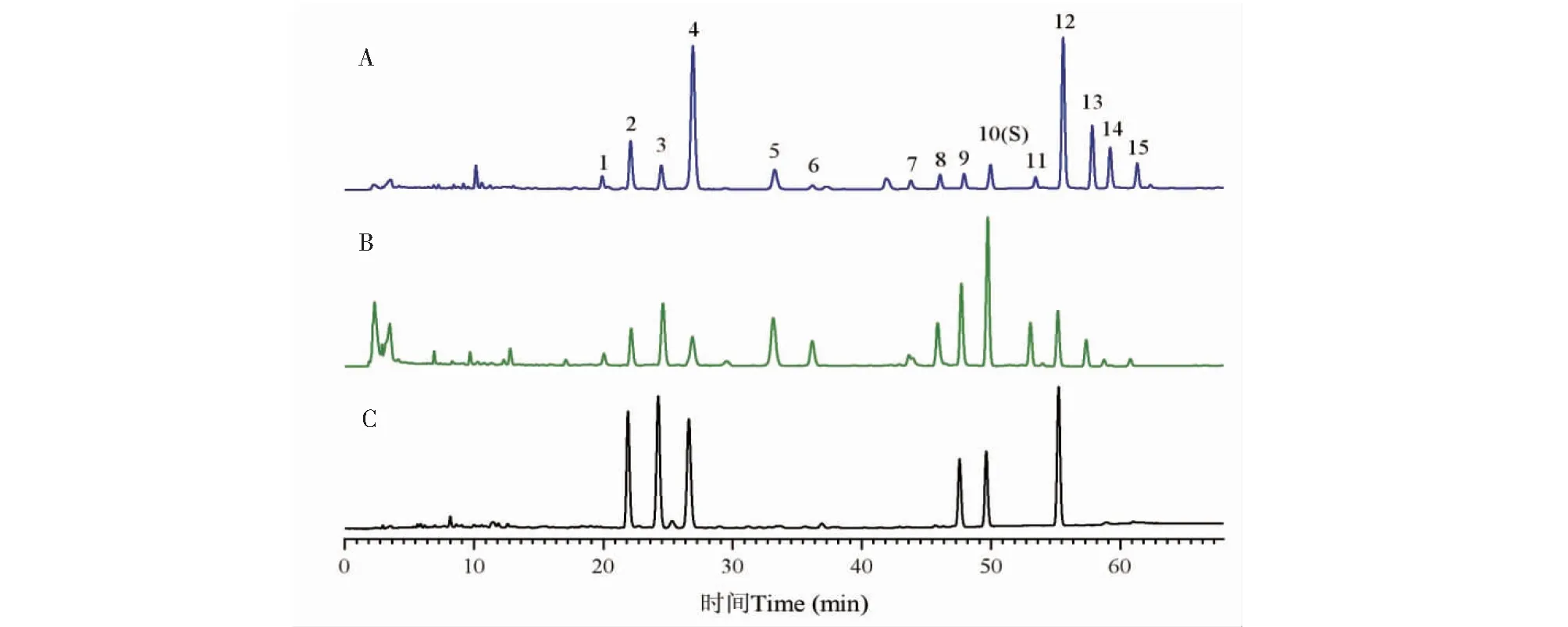
图3 不同产地茯苓皮(A)和白茯苓(B)饮片对照指纹图谱与混合对照品HPLC图(C)Fig.3 Control fingerprints of Poriae Cutis (A) and White Poria (B) decoction pieces from different regions and HPLC chromatogram of mixed standards (C)注:2:茯苓新酸B;3:去氢土莫酸;4:茯苓新酸A;9:去氢茯苓酸;10:茯苓酸;12:松苓新酸。Note:2:Poricoic acid B;3:Dehydrotumulosic acid;4:Poricoic acid A;9:Dehydropachymic acid;10:Pachymic acid;12:Dehydrotrametenolic acid.
指认了其中6个共有峰,分别为茯苓新酸B(2号峰)、去氢土莫酸(3号峰)、茯苓新酸A(4号峰)、去氢茯苓酸(9号峰)、茯苓酸(10号峰)、松苓新酸(12号峰);其中10号峰茯苓酸成分是茯苓中具有代表性的活性三萜酸类成分,性质稳定,峰面积所占比例较大,分离度好,因此确定其为参照峰(S)。
2.4.2 茯苓皮与白茯苓共有峰的相对保留时间与相对峰面积
以不同产地茯苓皮和白茯苓样品HPLC色谱图中的10号峰(茯苓酸)为参照峰(S),计算各个批次样品中其他共有峰与S峰的相对保留时间与相对峰面积,结果见表2和表3。由表2和表3可知,茯苓皮与白茯苓样品共有峰相对保留时间的波动较小(RSD值在0.02%~0.64%),而相对峰面积波动较大,表明茯苓皮与白茯苓HPLC指纹图谱中主要峰群的整体面貌基本一致,但同一批次样品各成分之间含有量及不同药用部位样品各成分含有量差别较大。
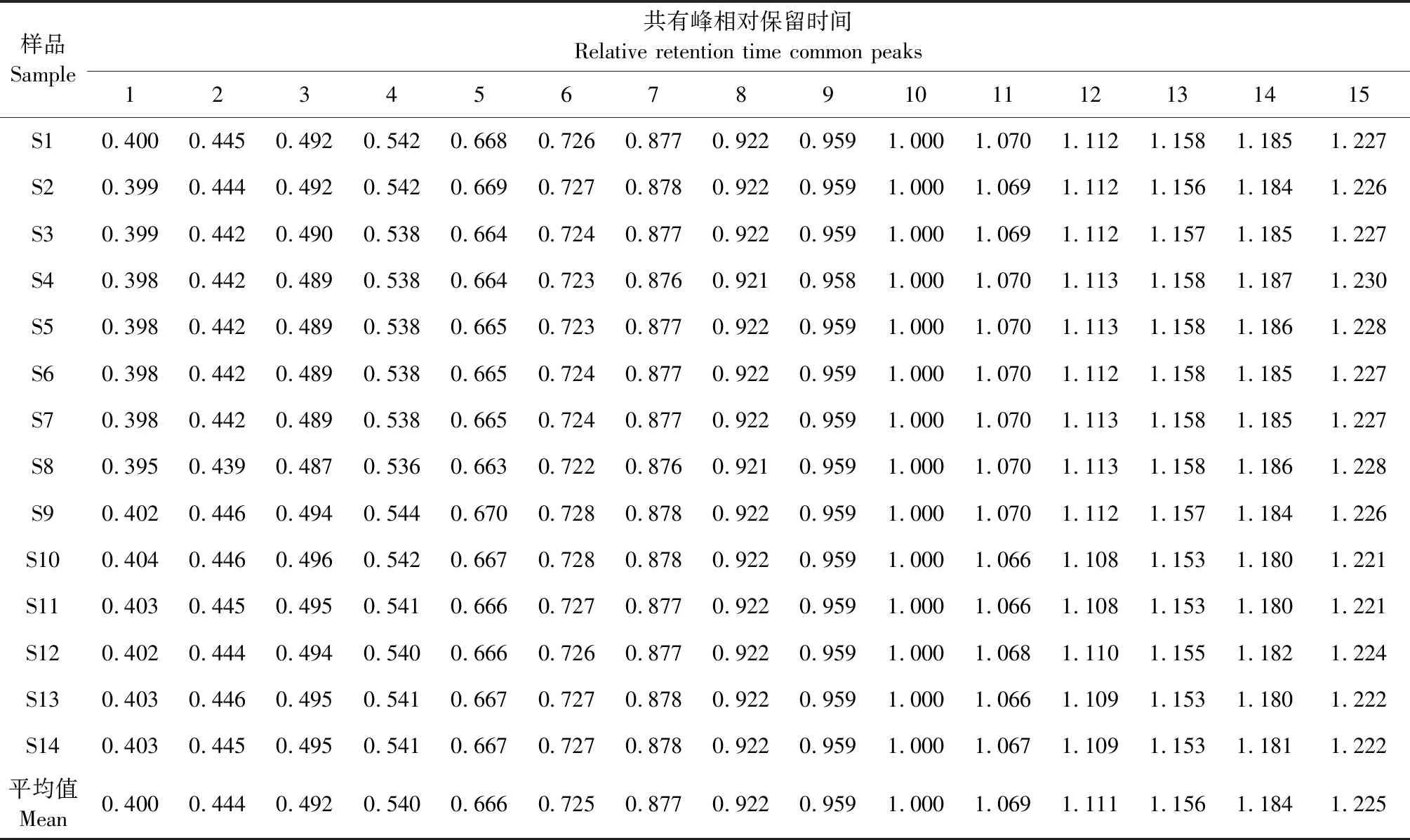
表2 14批茯苓皮与白茯苓饮片指纹图谱共有峰的相对保留时间
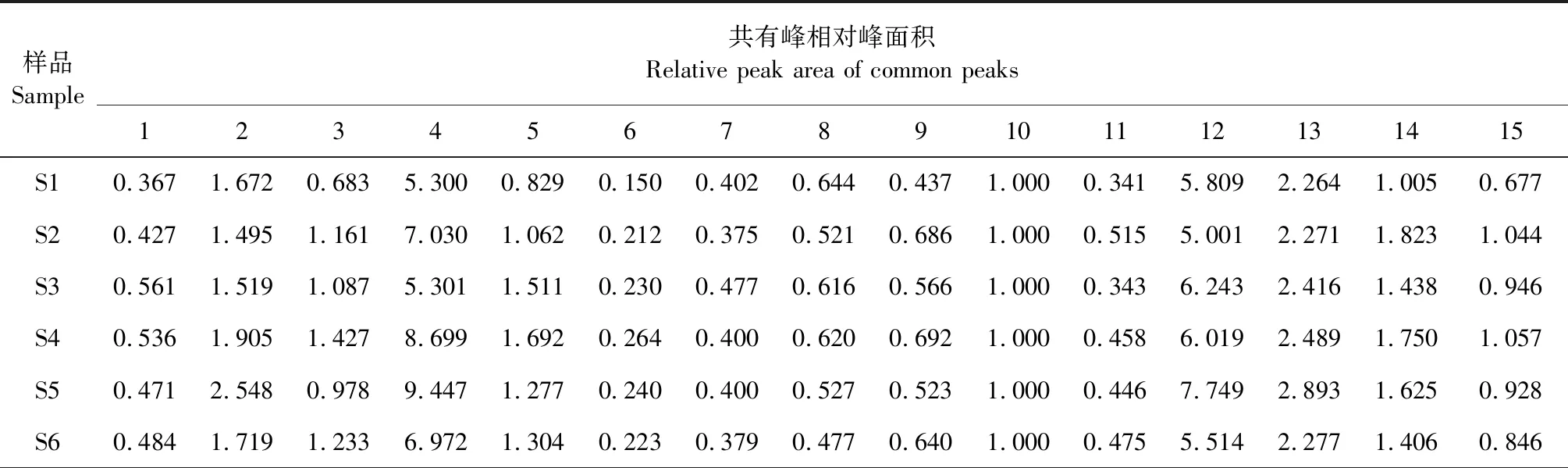
表3 14批茯苓皮与白茯苓饮片指纹图谱共有峰的相对峰面积
2.4.3 相似度分析
采用“中药色谱指纹图谱相似度评价系统(2012版)”软件计算14批茯苓样品HPLC指纹图谱的相似度(见表4),由结果可知,茯苓皮样品相似度在0.951~0.998,白茯苓样品相似度在0.894~0.993,表明不同产地同一药用部位茯苓样品相似度较好;茯苓皮与白茯苓之间相似度在0.389~0.765,说明不同药用部位的茯苓指纹图谱有明显区别。
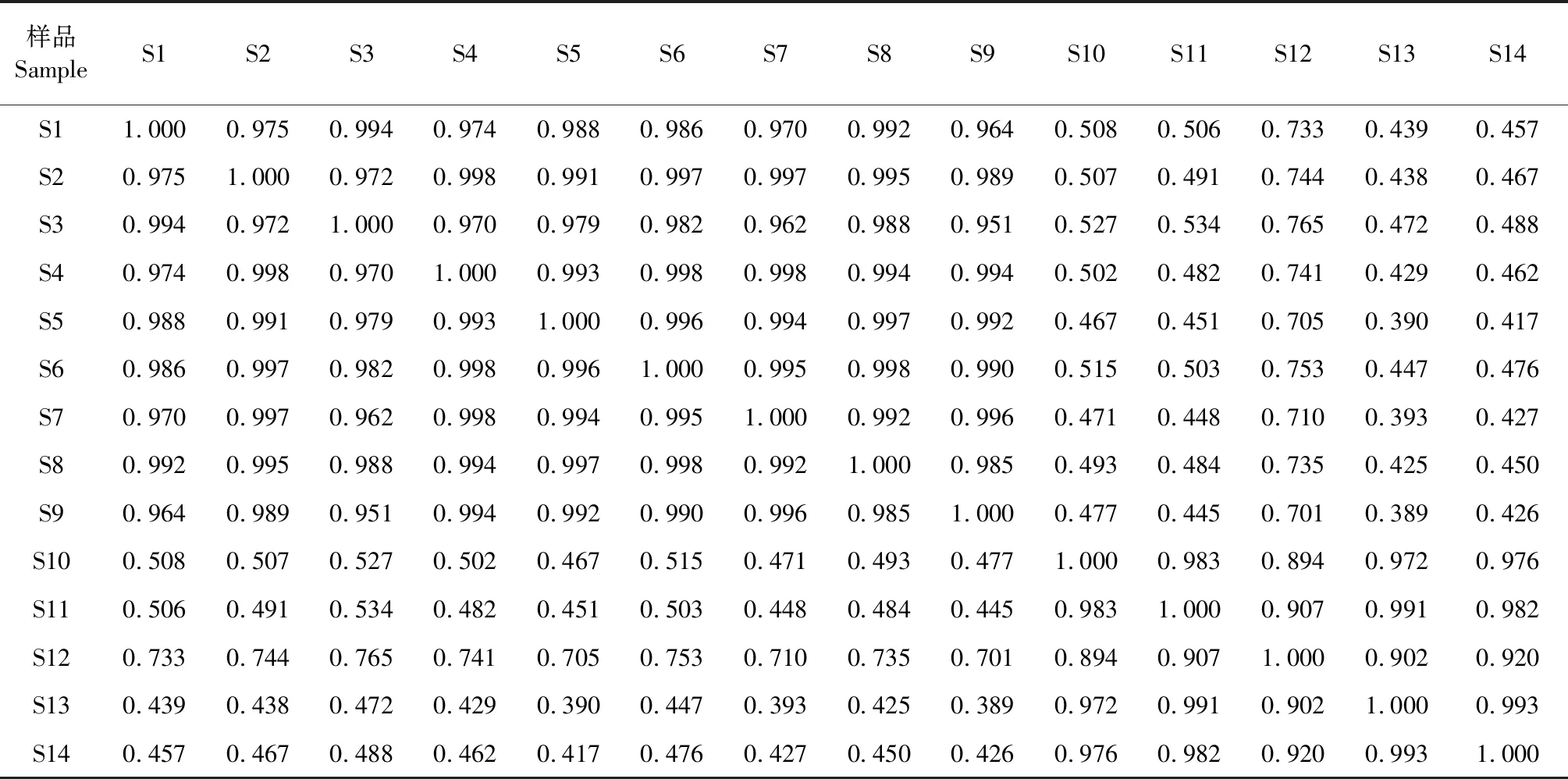
表4 14批茯苓皮与白茯苓饮片的相似度
2.5 各产地茯苓皮与白茯苓样品的聚类分析
聚类分析(CA)是一种按“物以类聚”原则通过将观察对象依据某些特征分类的多元统计分析手段,从而建立样本与样本之间的相似关系或亲疏关系,目前在中药方面的应用较广泛,如真伪鉴别、品种分类及质量评价等[16]。采用SPSS 26.0软件,以14批不同产地不同药用部位茯苓样品的15个共有峰峰面积为变量,用组间连接法、欧式距离为度量标准进行聚类,聚类结果见图4。由图4可知,14份茯苓样品被分成了2大类:第一大类为茯苓皮(S1~S9);第二大类为白茯苓(S10~S14),这与样品的性状鉴别结果吻合,表明不同药用部位间茯苓样品的差异较大,观察“2.4.2”项下各共有峰的相对峰面积均值可发现,茯苓皮中除峰6和峰9外其他共有色谱峰均高于白茯苓,提示各成分含量的高低可能是造成不同药用部位药材差异的主要原因。此外白茯苓样品按产地分为两类:I类样品为S10和S11,产自湖南;II类样品为S13和S14,产自云南。

图4 14批不同产地茯苓皮和白茯苓样品聚类分析树状图Fig.4 Cluster analysis of 14 batches of Poriae Cutis and White Poria samples from different regions
2.6 各产地茯苓皮与白茯苓样品的主成分分析
将不同产地茯苓皮与白茯苓样品各共有峰峰号对峰面积作折线图(见图5),从图可知在本实验条下茯苓样品峰面积数据拟合度较小,样本组间差异较大,故采用无监督的主成分分析(PCA)方法,使用的分析软件为SPSS 26.0和SIMCA 14.1。
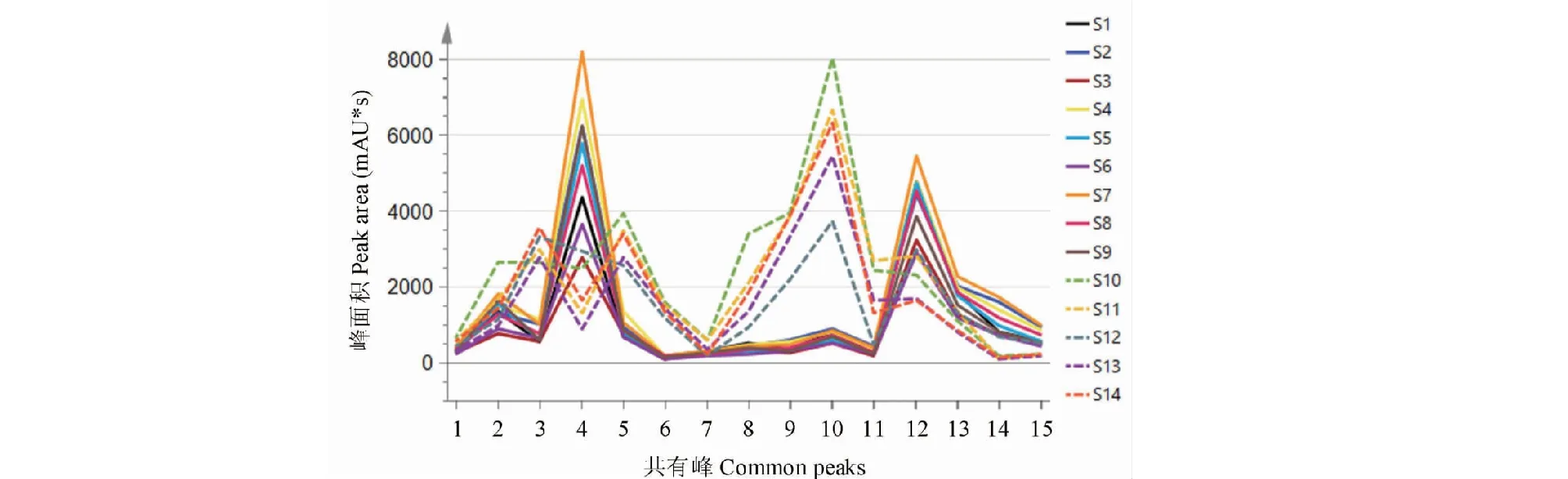
图5 14批不同产地茯苓皮和白茯苓样品峰面积折线图Fig.5 Peak area line chart of 14 batches of Poriae Cutis and White Poria samples from different regions
2.6.1 主成分结果
以标准化后的各共有峰峰面积为变量进行PCA分析。表5为主成分结果,前2个主成分解释了全部方差的90.387%,能够反映茯苓皮与白茯苓指纹图谱中共有峰的大部分信息,结合碎石图(见图6)可知,前2个主成分特征值相对较大,而其他主成分之间比较平缓,因此提取前两个主成分并标记为Y1和Y2。图7为14批茯苓样品的PCA散点得分图,结果表明,14批样品可分为2类,I类样品为S1-S9,II样品为S10-S14,该现象与CA分析结果基本一致。

图6 茯苓饮片样品PCA碎石图Fig.6 PCA scree plot of decoction pieces samples made from P.cocos sclerotium

图7 14批茯苓饮片样品的PCA散点得分图Fig.7 PCA score scatter plot of 14 batches of decoction pieces samples made from P.cocos sclerotium

表5 茯苓饮片样品的主成分结果
2.6.2 主成分表达式
根据标准化后的各个共有峰变量X1-15占主成分的权重(见表6),得到Y1、Y2的线性组合:Y1= 0.229X1+ 0.111X2+ 0.268X3-0.251X4+ 0.295X5+ 0.295X6+ 0.189X7+ 0.282X8+ 0.299X9+ 0.300X10+ 0.279X11-0.257X12-0.233X13-0.265X14-0.251X15,Y2= 0.331X1+ 0.504X2-0.091X3-0.304X4+ 0.094X5+ 0.015X6+ 0.360X7+ 0.191X8+ 0.041X9+ 0.077X10+ 0.157X11+ 0.290X12+ 0.360X13+ 0.231X14+ 0.265X15。

表6 茯苓饮片样品PCA的成分得分系数矩阵
由上式可知,在Y1中,3、5和6、8~11号峰(X3、X5,6、X8-11)的系数绝对值大于其他共有峰变量的系数绝对值,所以主成分Y1是7个共有峰的综合反应,观察“2.4.2”项下各共有峰的相对峰面积可发现,茯苓皮样品3、5和6、8~11号峰的相对峰面积均值与白茯苓3、5和6、8~11号峰的相对峰面积均值较接近,而其他共有峰的相对峰面积均值都相差很大,说明这7个共有峰及所代表的成分(包括已指认的共有峰代表成分:去氢土莫酸、去氢茯苓酸、茯苓酸)在评价茯苓皮和白茯苓质量优劣时是必不可少的。在Y2中,1和2、4、7、12~15号峰(X1,2、X4、X7、X12-15)的系数大于其他共有峰变量的系数,所以主成分Y2是由这8个共有峰来综合反应,根据各共有峰的相对峰面积可知,茯苓皮样品这8个共有峰的相对峰面积均值远大于白茯苓样品,提示这8个共有峰(包括已指认的共有峰,2号峰-茯苓新酸B、4号峰-茯苓新酸A、12号峰-松苓新酸)可以作为茯苓皮与白茯苓指纹图谱(见图2)中茯苓皮的特征鉴别分。
2.6.3 主成分得分和综合得分
表7是根据主成分表达式计算的各样本主成分得分和以各个主成分方差贡献率占两个主成分总方差贡献率的比率为权重计算的综合得分[17],主成分Y1得分比较高的是S10、S11、S13、S14,主成分Y2得分比较高的是S2、S4、S7、S10,综合得分比较高的是S10~S14,结合茯苓皮和白茯苓各自的对照指纹图谱(见图3A和图3B)或共有峰峰面积信息,可知在本研究的茯苓皮与白茯苓HPLC指纹图谱条件下,白茯苓样品(S10~S14)的3(去氢土莫酸)、5和6、8、9(去氢茯苓酸)、10(茯苓酸)、11号峰成分含量高于茯苓皮;而S2、S4、S7、S10样品的1和2、4、7、12~15号峰成分含量高于其他样品,其中S2、S4、S7都是茯苓皮样品,提示在本实验条件下测得的茯苓皮的1、2(茯苓新酸B)、4(茯苓新酸A)、7、12(松苓新酸)、13-15号峰成分含量普遍高于白茯苓;综合得分较高的都是白茯苓样品,说明白茯苓样品15个共有峰成分含量间差异普遍比茯苓皮小。此外,载荷图表明1、2(茯苓新酸B)、7号色谱峰对茯苓皮及白茯苓药材的整体质量起主要影响作用,如图8所示。

图8 14批茯苓饮片样品的主成分载荷图Fig.8 Loading scatter plot of PCA of 14 batches of decoction pieces samples made from P.cocos sclerotium

表7 主成分得分和综合得分
3 讨论与结论
本研究采用甲醇为提取溶剂、超声处理30 min的样品提取方法[18],考察了不同流动相(乙腈-水、乙腈-0.1%甲酸水、乙腈-0.1%磷酸水、乙腈-0.2%磷酸水、乙腈-0.3%磷酸水),不同色谱柱[Agilent 5 TC-C18(2)(250 mm × 4.6 mm,5 μm)、Welch Ultimate XB-C18(250 mm × 4.6 mm,5 μm)、Agilent Eclipse Plus C18(250 mm × 4.6 mm,5 μm)],不同体积流量(1.0、1.1、1.2 mL/min),不同色谱柱温度(22、25、28 ℃),不同采集波长(203、210、242 nm)对指纹图谱的影响,最终确定色谱条件为流动相为乙腈-0.3%磷酸水,Agilent 5 TC-C18(2)(250 mm × 4.6 mm,5 μm)色谱柱,体积流量为1.0 mL/min,色谱柱温度25 °C,变波长方式采集,此条件下基线平稳,色谱峰峰形较好,分离效果较佳。
在此基础上采用HPLC法建立了14批来自不同产地的茯苓皮与白茯苓指纹图谱,在茯苓皮与白茯苓指纹图谱的共有模式下共标定了15个共有峰,并通过化学对照品指认了其中6个化学成分:茯苓新酸B、去氢土莫酸、茯苓新酸A、去氢茯苓酸、茯苓酸、松苓新酸。通过14批不同产地茯苓皮和白茯苓样品聚类分析树状图和峰面积折线图结合相似度数据可知不同药用部位的茯苓样品组间差异较大,组内差异较小,白茯苓样品与产地的关联性较强。因此模式识别采用无监督的PCA方法,PCA结果将15个共有峰变量分成2个主成分Y1和Y2,Y1是包括去氢土莫酸、去氢茯苓酸、茯苓酸成分在内的7个共有色谱峰的综合反应,表明7个共有色谱峰在进行茯苓皮与白茯苓指纹图谱研究时必不可少;Y2是包括茯苓新酸B、茯苓新酸A、松苓新酸成分在内的8个色谱峰的综合反应,提示这8个色谱峰可作为在同时评价茯苓皮与白茯苓质量时茯苓皮的特征鉴别峰。对指纹图谱影响较大的共有峰变量参数为1、2(茯苓新酸B)、7号色谱峰。白茯苓这15个共有峰成分间含量差异比茯苓皮小。实际上白茯苓这15个共有峰成分含量都远低于茯苓皮,为了使茯苓皮与白茯苓指纹图谱的共有模式更完整和可测故而在制备白茯苓时加了一步浓缩步骤。
研究表明本文建立的方法简便、可靠、准确,可以为茯苓皮及白茯苓的质量评价、标准的制定及药材的合理利用提供参考依据。

