锰氧化膜包覆沸石的制备及其处理含锰水特性研究
金 星,傅金祥,张 黎,何 祥
(1.沈阳建筑大学市政与环境工程学院,沈阳 110170;2.南宁职业技术学院建筑工程学院,南宁 530000)
0 引 言
近年来,随着钢铁工业、电池材料等行业的迅速发展,金属锰的需求逐年增加[1-2]。锰矿的开采、冶炼促进了经济的快速发展,但是锰污染问题也逐渐显现[3-4]。若没有经过有效处理,含锰废水会通过土壤渗透、自然界水循环等方式对土壤、水资源等造成污染[5-6],长期饮用锰含量超标的水会对人体产生严重危害[7-9]。在净水厂采用的接触氧化法除锰工艺中,石英砂或锰砂滤料经过数月的成熟期,会在表面形成“锰质活性滤膜”[10-13]。通过滤膜的吸附和催化氧化作用,Mn2+被水中的溶解氧氧化为高价态的锰氧化物,并附着在滤料表面,新生成的锰氧化物可以进一步吸附和催化氧化Mn2+,产生“自催化氧化”过程。“锰质活性滤膜”的快速形成是接触氧化法除锰的关键步骤。
沸石的主要成分为硅铝氧化物[14],并包含少量钾、钠、镁、钙等金属离子,其具有复杂的立体网状结构和孔道空穴,以及较高的吸附性和离子交换能力[15-16]。与石英砂和锰砂相比,沸石吸附性更强、比表面积更大,成本与石英砂相近,远低于锰砂。白朗明等[17]采用改性沸石滤料耦合次氯酸钠预氧化来辅助滤柱启动,并将成熟期减少至14 d。Zanin等[18]采用沸石分子筛吸附溶液中重金属,可以有效去除水中85.1%的铁,25.0%的铜和4.0%(质量分数)的铬。以沸石逐步取代石英砂和锰砂作净水厂滤料具有广阔的应用前景。
本文以沸石作为基质材料,利用高锰酸钾和硫酸锰形成的锰氧化物在沸石表面沉积来制备锰氧化膜包覆沸石(manganese oxide membrane coated zeolite, MOMCZ),MOMCZ兼具沸石的吸附性和锰氧化物对Mn2+的“自催化氧化”特性,能提升除锰能力。采用SEM、EDS、XPS、XRD、BET、Zeta电位等方法表征MOMCZ的化学组成和结构特性,建立响应曲面模型,并对MOMCZ吸附Mn2+的影响因素进行综合分析,响应曲面模型的F检验统计量(F-distribution value,F-value)、显著性概率(probability value,P-value)、拟合度(R-squared,R2)、变异系数(coefficient of variation, CV)、信噪比(signal-noise ratio, SNR)等统计学参数用来检验模型数据的可行性[19-22],以期为接触氧化法除锰提供一种经济高效的滤料。
1 实 验
1.1 化学试剂与仪器
沸石取自辽宁省葫芦岛市,粒径为0.5~0.8 mm。制备MOMCZ的主要试剂包括高锰酸钾、一水合硫酸锰、氢氧化钠。Mn2+分析检测依据《生活饮用水标准检验方法》(GB/T 5750.6—2023)中的甲醛肟分光光度法,主要试剂包括甲醛溶液(质量分数为37%~40%)、乙二胺四乙酸二钠、盐酸羟胺、氨水(质量分数为25%~28%)、氢氧化钠、硫酸亚铁铵。化学试剂均为分析纯,购自国药集团化学试剂有限公司。试验用水为去离子水。
主要试验仪器:分光光度仪(上海光谱仪器, SP-752),恒温震荡培养箱(常州华怡仪器, HZQ-X100),pH仪(美国哈希仪器,HQ-40d),电子天平(上海舜宇恒平科学仪器,JA2003,精度0.001 g),扫描电子显微镜(捷克TESCAN MIRALMS),能谱分析仪(捷克TESCAN, Xplore 30型),X射线光电子能谱分析仪(Thermo Scientific K-Alpha),X射线衍射分析仪(日本理学,SmartLab-SE),比表面积分析仪(康塔, Autosorb-IQ-MP),纳米粒度及Zeta电位分析仪(Nano-ZS, ZEN3600)。
1.2 MOMCZ制备
沸石过20目(840 μm)筛,在105 ℃条件下烘干至恒重。在质量浓度为3.16 g/L的KMnO4溶液中投入10.0 g沸石,设置10 r/min转速搅拌,并逐滴加入 101.4 g/L MnSO4·H2O溶液和4 mol/L NaOH溶液,保持溶液pH值在7~8,至上清液恰好无色,形成锰氧化物沉淀,在105 ℃条件下烘干,制得11.89 g的MOMCZ,其中沸石与锰氧化物膜层质量比为10∶1.89。反应式如式(1)所示。
(1)
1.3 试验方法
MOMCZ吸附Mn2+的四个主要影响因素:负荷(水溶液中锰离子和MOMCZ的质量比,mMn2+/mMOMCZ, mg/g)、pH值、吸附温度(℃)、吸附时间(min),以Mn2+去除率为响应值,采用中心组合设计方法(central composite design, CCD)设计响应曲面模型,多项式回归分析对试验数据拟合,得到二次多项式模型,见式(2)。通过残差分析、方差分析、函数关系分析确定回归方程可行性,以及各影响因素对响应值的显著性,响应曲面因素水平及编码见表1。
(2)
式中:y为响应值或去除率,xi、xj为影响因素,i、j为系数序号,a为常数,bi为线性系数,bii为二次项系数,bij为交互项系数。
按照试验设计的影响因素x1,采用一水合硫酸锰配制模拟含锰废水和一定质量MOMCZ并置于500 mL有塞锥形瓶中。根据影响因素x2,采用氢氧化钠和硫酸调节溶液pH值。将锥形瓶置于恒温震荡培养箱中,根据影响因素x3和x4设定吸附温度和吸附时间。吸附结束后,取上清液通过0.45 μm滤膜,测定溶液中Mn2+质量浓度,锰去除率y计算公式如式(3)所示。
y=[(ρ0-ρe)/ρ0]×100%
(3)
式中:ρ0为Mn2+初始质量浓度,ρe为吸附结束时Mn2+质量浓度。
2 结果与讨论
2.1 表征分析
2.1.1 SEM及EDS分析
沸石和MOMCZ的SEM照片如图1所示。由图1(a)可知,沸石表面粗糙,表层疏松多孔,结构不规则,具有尖锐的菱角结构,菱角之间构成细微孔道和大量空穴,这种分子筛结构使沸石具有较大的比表面积。由图1(b)可知,MOMCZ表面结构发生了很大变化,变得立体复杂,保留了沸石的孔道和空穴,几乎无法观察到原有的菱角结构,锰氧化膜均匀包覆在沸石表面,呈多孔疏松的网状结构。在MOMCZ的制备过程中,KMnO4与MnSO4形成的锰氧化物沉淀呈絮状,包含大量结合水,絮状沉淀沉积在沸石表面,在烘干过程中,水分蒸发,原水分占有的点位出现空穴,在MOMCZ表面形成了网状结构,网状结构使MOMCZ具有了更大的比表面积和结合点位。
沸石和MOMCZ的EDS分析如图2所示。沸石主要组成元素为O、Si、Al、Ca、K、Mg和Na。除构成沸石的基本元素O、Si、Al外,Ca含量占比最高,但未检测到Mn元素。MOMCZ中检测到Mn原子数分数为1.95%。由于锰氧化膜的包覆,O、Si、Al、Ca、Mg原子数分数均有所下降。K和Na原子数分数由0.76%和0.35%分别上升至1.76%和1.85%,这两项元素原子数分数的上升是由于在制备MOMCZ过程中,采用的KMnO4和NaOH会使部分K+和Na+吸附在沸石和锰氧化膜表面。SEM和EDS的分析结果表明,锰氧化膜成功包覆沸石,改变了其表面形态和化学组成。

图2 沸石和MOMCZ的EDS分析
2.1.2 XPS及XRD表征
图3为沸石和MOMCZ的XPS谱和XRD谱。沸石和MOMCZ的XPS谱如图3(a)所示,其中在沸石Mn 2p轨道的XPS谱中,未发现明显峰形,强度很低,说明沸石中不含有锰元素。MOMCZ的Mn 2p轨道的XPS谱中出现两个明显峰形,且强度很高,说明在MOMCZ的制备过程中,锰氧化物成功负载在沸石表面。Mn具有六个稳定的氧化态(0、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅵ、Ⅶ),由于Mn(Ⅱ、Ⅲ、Ⅳ)的d轨道存在未配对电子,其XPS峰形呈现多重价态分裂[24]。Mn氧化态电子结合能及波峰半峰宽如表2所示。在MOMCZ的Mn 2p3/2的XPS谱中,在645.94 eV附近未出现明显的Mn(Ⅱ)特有的振激峰,说明MOMCZ中不含有Mn(Ⅱ);在638.60和645.50 eV处均未出现峰形,说明MOMCZ中不存在Mn(0、Ⅶ)。采用表2中Mn(Ⅲ、Ⅳ、Ⅵ)结合能和半峰宽对MOMCZ中Mn元素进行峰形拟合,结果发现,MOMCZ中Mn元素存在形式及摩尔分数分别为Mn(Ⅲ)51.28%,Mn(Ⅳ)48.72%,比例接近1∶1,且不含有Mn(Ⅵ)。
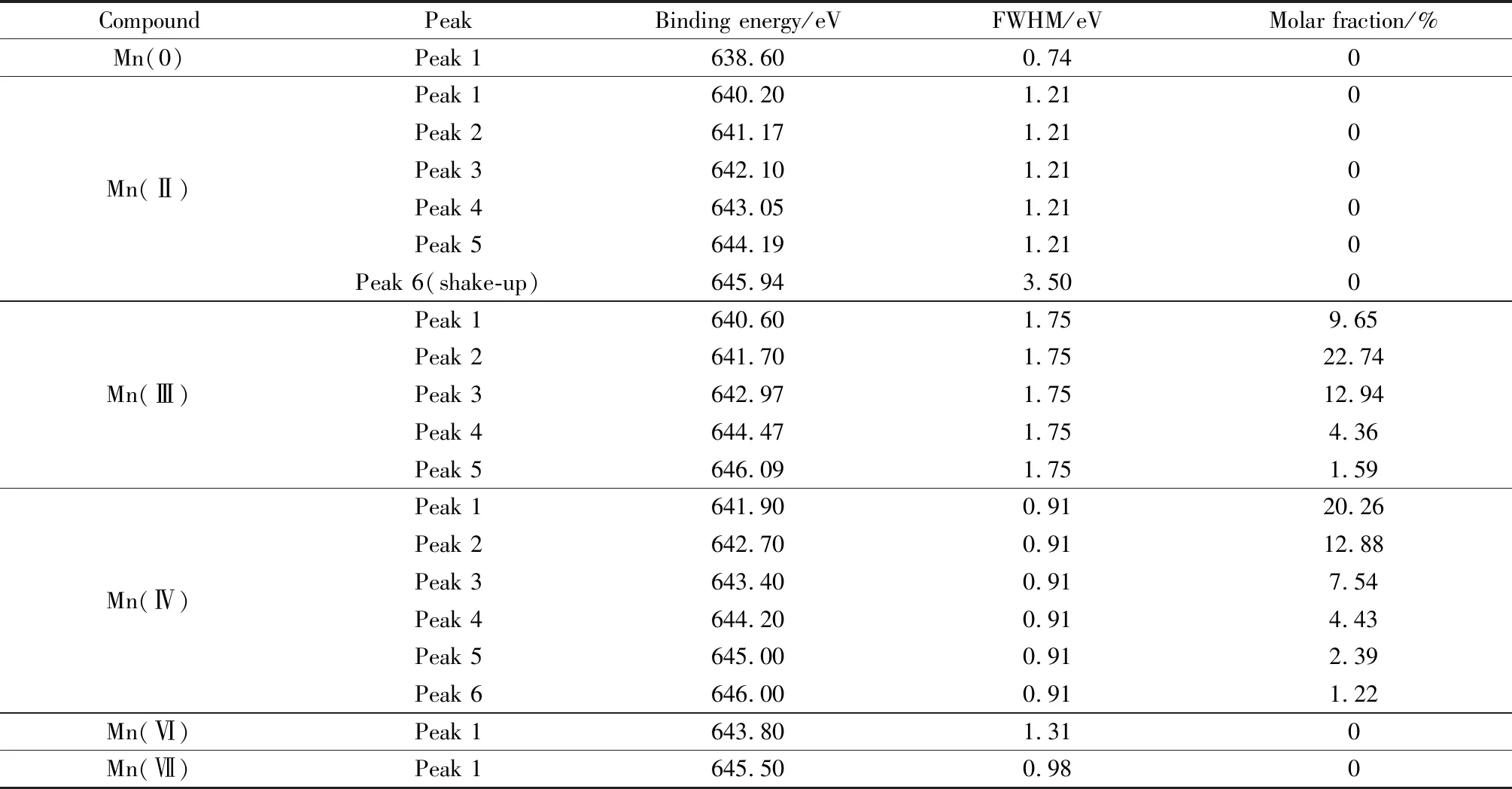
表2 MOMCZ表面Mn元素2p3/2轨道分峰拟合参数及含量
2.1.3 BET表征
沸石和MOMCZ的氮气吸附脱附曲线见图4(a)。MOMCZ的孔容达91.31 cm3/g,远大于沸石37.71 cm3/g。当相对压力较小时,沸石的氮气吸附量提升不明显,属于单层吸附;随着相对压力提高,多层吸附逐步形成,拐点出现在接近饱和蒸汽压(p/p0=1,p为氮气压力,p0为饱和蒸汽压)附近。MOMCZ的吸附量在低相对压力区提升明显,说明在小孔径范围内MOMCZ具有更多的空穴;随着相对压力提升,MOMCZ的曲线与沸石趋于相同,说明氮气向MOMCZ内部扩散,在大孔径范围内MOMCZ内层沸石起到吸附作用。沸石和MOMCZ的比表面积和孔径分布曲线见图4(b)(dV为体积的偏微分),沸石比表面积为10.24 m2/g,MOMCZ比表面积为38.76 m2/g,锰氧化膜的包覆显著提升了材料的比表面积。沸石和MOMCZ的孔径集中分布在3~40 nm,属介孔范围。在3~10 nm,MOMCZ的介孔数量显著多于沸石,介孔数量的增加使锰氧化物沸石具有更大的比表面积,吸附点位更多,有利于提高吸附容量。
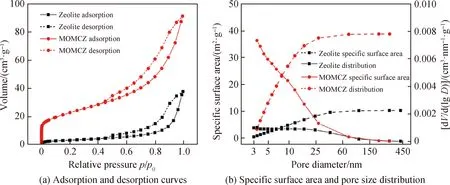
图4 沸石和MOMCZ的氮气吸附脱附曲线、比表面积及孔径分布
2.1.4 Zeta电位表征
沸石和MOMCZ的Zeta电位曲线见图5。pH值的改变会影响材料表面的水解平衡和带电特性。当pH值为1~9时,沸石的Zeta电位测定值在3.55~-12.07 mV,MOMCZ的Zeta电位测定值在2.55~-16.53 mV。沸石和MOMCZ的Zeta电位值都随着pH值的升高而降低。其中沸石的等电点在pH=3.20附近,MOMCZ的等电点在pH=2.36附近。结合XRD表征分析结果,MOMCZ表面的锰氧化膜的主要成分为钠锰氧化物水合物,等电点在pH=2.0左右[25],在锰氧化物的包覆作用下,MOMCZ的等电点发生了整体负移。当pH值小于等电点时,材料表面呈正电性,对阴离子具有吸附性,当pH值大于等电点时,材料表面呈负电性,对阳离子具有吸附性。MOMCZ的等电点pH值低于沸石,使MOMCZ在吸附阳离子时具有比沸石更宽的pH值范围。在相同pH值时,MOMCZ的表面Zeta电位值均小于沸石,说明MOMCZ对阳离子具有更强的吸附能力。
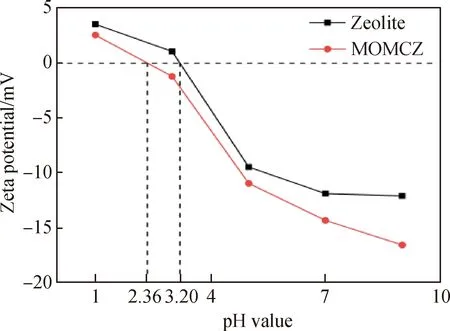
图5 沸石和MOMCZ的Zeta电位曲线
2.2 响应面法研究MOMCZ处理含锰水特性
2.2.1 回归方程分析
根据响应面模型中心组合方法设计得到的30组试验,每组试验进行3次平行试验,去除率取3次试验结果均值,得到试验结果见表3。多项式回归分析对试验数据拟合,得到去除率y与4项影响因素关系回归方程,具体如式(4)所示。
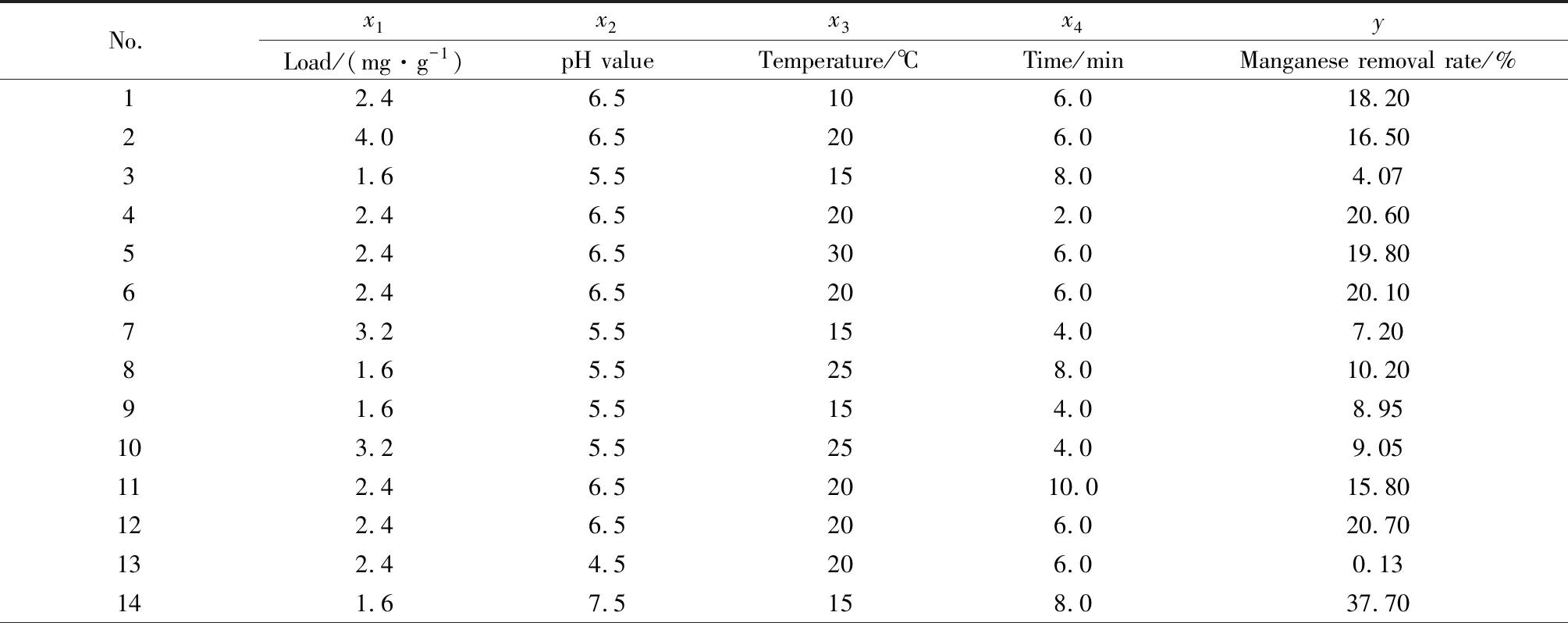
表3 试验设计方案及结果
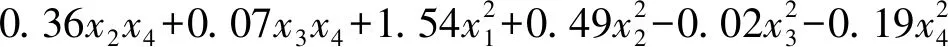
(4)
2.2.2 响应面模型方差分析
对MOMCZ吸附Mn2+响应面模型进行统计学方差分析,结果见表4。试验模型的F-value代表拟合方程的显著性,一般认为F-value越大拟合结果越好。MOMCZ吸附Mn2+拟合结果中F-value为180.7,可见该模型的拟合效果良好。试验模型的P-value代表模型的精确程度,P-value小于0.05说明拟合效果显著,P-value小于0.01说明拟合效果极显著。MOMCZ吸附Mn2+模型中P-value小于0.000 1,说明响应模型对试验数据的模拟效果达到了极显著水平。失拟项(lack of fit)的P-value为0.443 4(>0.05),说明失拟项不显著,同样说明该模型对试验数据的拟合效果良好。回归模型的相关系数R2=0.994 1,说明99.41%的试验数据可以用此方程来解释。通过统计学方程的分析,用此模型可以有效地分析负荷、pH值、吸附温度、吸附时间在MOMCZ吸附Mn2+过程中的影响,并预测吸附Mn2+最佳条件。每项影响因素在模型中有对应的F-value和P-value,F-value越大代表该因素对MOMCZ吸附Mn2+影响越大,负荷、pH值、吸附温度、吸附时间的F-value分别为254.69、2 105.75、15.97、19.31,说明四项影响因素对去除率y的影响程度关系是:pH值>负荷>吸附时间>吸附温度。试验模型的CV和SNR代表试验的真实合理性,CV越小模型越合理,当CV小于10%时模型具有较高的合理性;SNR越大代表试验真实可信,当SNR大于4时,试验真实可信。MOMCZ吸附Mn2+试验中CV=6.29%,SNR=52.99,说明本次试验模型可行性与精确程度较高,数据真实可靠。
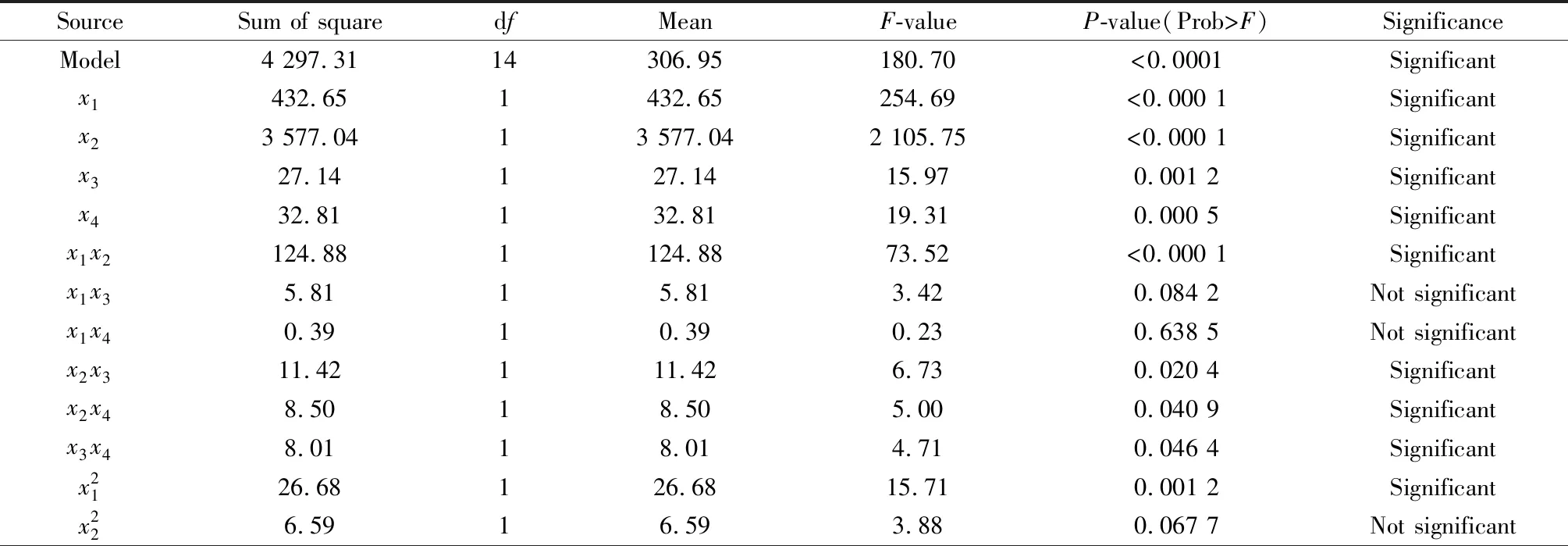
表4 方差分析结果
2.2.3 响应面模型残差分析
对试验数据进行残差分析,结果如图6所示。Mn2+实际去除率与模型预测去除率关系如图6(a)所示,可见预测值与实际值点贴近拟合曲线,说明拟合效果较好。采用该模型能够较为准确地预测MOMCZ对Mn2+的吸附效果。图6(b)和(c)的残差均围绕零点随机分布,说明试验数据的随机误差满足方差齐性,残差值分布介于±3.00之间,说明拟合效果好,不存在异常点,试验可信性强。图6(d)为内学生化残差与正态分布关系图,内学生化残差代表标准偏差与实际值的决定值大小,内学生化残差呈线性分布,只有少数点偏离直线,说明模型可行性较高,拟合程度较好。
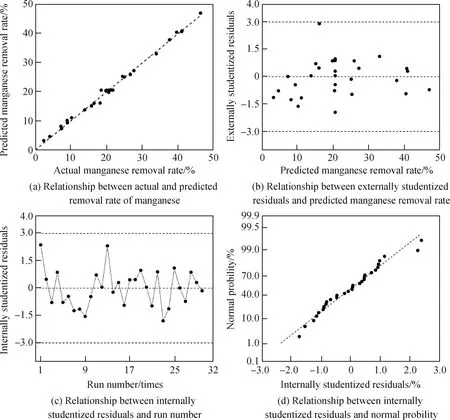
图6 响应面模型残差分析
2.2.4 响应面影响因素交互关系分析
图7为负荷、pH值、吸附时间、吸附温度四项因素两两之间的关系对Mn2+去除率效果的影响。图7(a)为负荷与pH值的交互作用图,在MOMCZ吸附Mn2+过程中,负荷越低去除率越高,pH值越高,去除率越高。在试验设计范围内,当负荷为0.8 mg/g、pH=8.5时,锰去除率达到最高值。图7(b)为负荷与吸附温度的交互作用图,当吸附温度为10~30 ℃时,锰去除率随着温度升高而升高,但升高趋势不明显。图7(c)为负荷与吸附时间的交互作用图,随着负荷降低,锰去除率单调增加;随着吸附时间增加,锰去除率呈先增加后减少的趋势,当吸附时间为0~6 min,锰去除率逐渐增加,6~10 min时锰去除率出现小幅度下降。这可能是由于吸附时间增加,部分已经吸附在MOMCZ表面的锰离子在布朗运动作用下出现少量脱附现象。图7(d)、(e)分别为pH值与吸附温度、pH值与吸附时间交互作用图,在这三项因素中,pH值起主导作用,吸附温度和吸附时间对锰去除率的影响较小。图7(f)为吸附时间和吸附温度交互作用图,二者交互作用较为明显,锰去除率随着时间增加或温度增加都呈先增加后下降的趋势。在吸附温度为20 ℃和吸附时间为6 min左右时,锰去除率出现了最大值。分析原因可能是因为当温度较低时,分子热运动较低,锰离子需要更多的时间吸附在MOMCZ表面,锰去除率随着温度、时间增加而升高;当温度超过20 ℃时,分子布朗运动增加,已经吸附在MOMCZ表面的锰离子少量脱附,随着时间和温度进一步提高,更多的锰离子从MOMCZ表面脱附,锰去除率呈下降趋势。
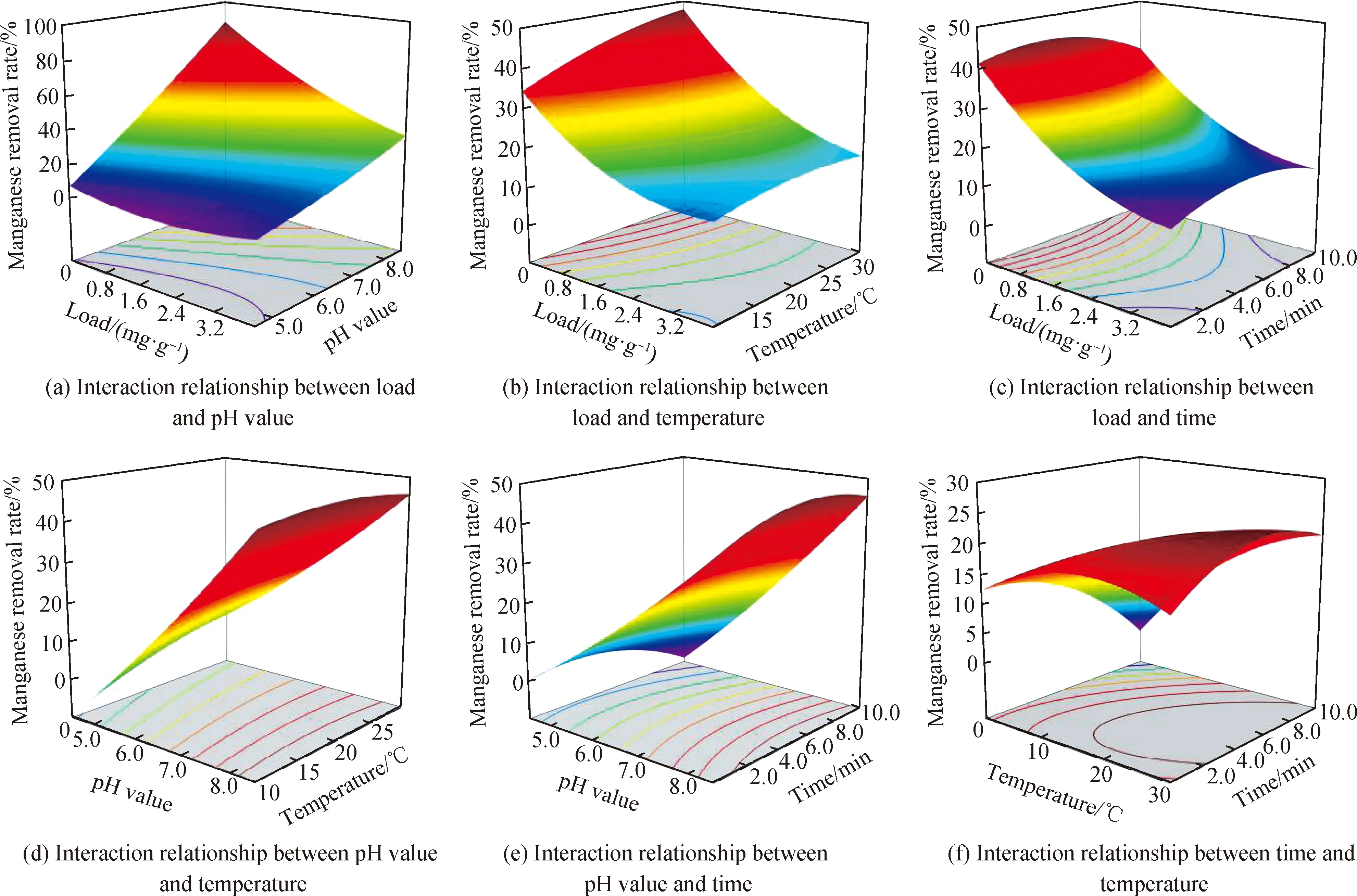
图7 响应面模型因素交互作用关系
2.2.5 响应面模型优化和验证
在影响因素负荷为0.8~4.0 mg/g、pH值为4.5~8.5、吸附温度为10~30 ℃、吸附时间为2~10 min的条件下,根据响应面的回归方程式(2),求解锰离子去除率的最大值,得到MOMCZ吸附锰离子的优化条件:负荷为0.8 mg/g,pH值为8.5,吸附温度为23.40 ℃,吸附时间为6.58 min,此时锰去除率达到最大值70.82%。
为了对MOMCZ吸附锰离子响应面模型进行验证,随机选取四组影响因素条件和最佳影响因素条件,分别进行吸附锰离子试验和模型预测,得到试验数据与预测值之间的关系,模拟验证结果见表5。四组试验数据的实际试验数据与预测值之间的相对误差在0.36%~2.39%,试验数据与预测值相对误差均保持在2.5%以内,说明模型可通过试验验证,模型准确率高,预测准确。
3 结 论
1)KMnO4和MnSO4生成的锰氧化膜包覆在沸石表面,制备了MOMCZ,MOMCZ结合了沸石的吸附性能和锰氧化物的催化氧化性。锰氧化膜改变了沸石的表面结构和化学组成,呈现出复杂立体的网状结构。
2)在MOMCZ表面的锰氧化膜中,Mn元素存在形式及摩尔分数分别为Mn(Ⅲ)51.28%,Mn(Ⅳ)48.72%,形成的化合物为Na0.55Mn2O4(H2O)1.5。MOMCZ比表面积为38.76 m2/g,孔径集中分布在3~40 nm,等电点pH=2.36。
3)在MOMCZ吸附锰离子响应曲面模型中,对锰去除率的影响关系顺序为pH值>负荷>吸附时间>吸附温度,经过模型优化,在负荷为0.8 mg/g、pH值为8.5、吸附温度为23.40 ℃、吸附时间为6.58 min时,锰去除率达到最大值70.82%。负荷与吸附温度和吸附时间交互作用不显著,其他因素间的交互作用明显。试验的实际数据和模型的模拟值间的相对误差均小于2.5%,模型准确率高。

