基于铜渣制备γ-Fe2 O3 及其光催化-降解性能研究
蒋 周,李 鹏,闫炳基,国宏伟
(苏州大学 沙钢钢铁学院,江苏 苏州 215137)
0 引言
世界上有超过80%的铜是通过火法冶炼从硫化铜精矿中提取出来的[1],但采用火法生产精炼铜不可避免会产生大量的炉渣,每生产出1 t 精炼铜将伴随着2~3 t 的铜渣[2-3]。据统计,2021 年我国精炼铜产量达到了1 049 万t,铜渣产量超过2 000 万t。铜渣[4-5]通常易碎难磨,密度高,矿相组成复杂,其主要成分为铁橄榄石(Fe2SiO4)、磁性氧化铁(Fe3O4),且含有少量As、Co、Cu、Pb 和Zn[6]。国内铜渣主要应用于制备水泥、建筑材料和提取有价金属。铜渣属于低钙高硅熟料,可以直接作为铁原料加入到水泥中,加入超细铜渣的混合水泥可有效降低水泥的累积水化热[7];铜渣作为细骨料加入量40%时[8],混凝土仍具有良好的力学性能,但其中的重金属限制了铜渣在水泥行业的大规模应用。铜渣具有良好的力学性能、稳定性与耐腐蚀性,可广泛应用于道路修筑、耐火材料等,以铜渣为原料生产的地质聚合物具有良好的隔热性能[9],但对于其中的金属元素利用率低下。由于铜渣含有大量的铁资源(31.3%~40.5%),因此长期以来铁的综合利用是铜渣处理的研究热点。目前,主要的处理方式有磨矿磁选、湿法浸出和改性焙烧,但由于铁橄榄石具有较高的热力学稳定性,铁硅分离过程较困难,不可避免需要消耗大量的能量,工艺产物附加值较低。因此寻求一条简单高效的铜渣资源化途径具有重要意义。
铁氧体是一种具有重要应用价值的功能材料,主要包括氧化铁(Fe3O4、α-Fe2O3和γ-Fe2O3)以及其他尖晶石(MeFe2O4,Me 代表Mg、Co、Zn、Ni 等)。其中,磁赤铁矿(γ-Fe2O3)是一种具有阳离子空位的亚稳磁性材料,在污水处理、生物医学和催化领域具有广泛的应用。Rezvan 等[10]利用铜渣负载CoFe2O4制备出一种对苯酚具有降解效果的催化剂,但仅利用了铜渣良好的机械性能和热稳定性,没有充分利用其中的铁元素。Liu 等[11]使用氧化铁和氢氧化钠合成铁酸钠然后经过水解和热处理获得了具有9.03 emu/g 饱和磁化强度和322.8 Oe 矫顽力的γ-Fe2O3。郑航等[12]利用化学共沉淀法制备出Fe3O4纳米颗粒并通过加热氧化得到粒径10 nm 的红棕色γ-Fe2O3。尹晓红等[13]利用共沉淀法结合溶胶-凝胶法制得磁载光催化剂TiO2/Al2O3/γ-Fe2O3,经过1.5 h 光降解后进行染料污水净化试验,染料去除率可达90%,并且可通过外加磁场使得催化剂和液相分离。Sun 等[14]合成出非堆积γ-Fe2O3/C@TiO2双层中空纳米颗粒,减少了催化剂的禁带宽度,并且由于·OH、·O2-空穴的协同处理,苯酚被快速降解。
本文以铜渣为原料,通过碱熔-水解-煅烧获得具有较高纯度的γ-Fe2O3,并对其成分、结构进行表征,还进行了试验,研究其在不同亚甲基蓝染料浓度和不同双氧水用量情况下的光催化-降解性能,本研究为铜渣的资源化利用提供一种新途径。
1 试验部分
1.1 原料
试验所使用的铜渣产自国内某铜厂,经过处理后的铜渣粒度均小于74 μm,将其放于真空干燥箱中90 ℃下干燥12 h,然后取出并密封保存。大量研究表明[15-16],铜渣中的全铁含量一般在40%左右,主要化学成分见表1,结合XRD 分析(图1),可以判断该铜渣主要矿相为Fe2SiO4和Fe3O4,同时还有少量Al2O3、CaO、ZnO 等金属氧化物。

图1 铜渣原料的XRD 结果Fig.1 XRD results of copper slag raw materials

表1 铜渣的主要化学组成(质量分数)Table 1 Main chemical components of copper slag(mass fraction) %
1.2 γ-Fe2O3 的制备及其光降解性能研究
试验流程及参数如图2 所示。为保证水解时γ-FeOOH 的生成,需加入过量的氢氧化钠。首先将等质量的铜渣和氢氧化钠(国药,AR)研磨混匀后,置于反应炉内在空气气氛中(500 ℃、800 ℃)进行碱熔焙烧1 h。随后待炉温降至300 ℃,迅速取出样品放于干燥罐中自然冷却。接着,将焙烧样品浸于80 ℃去离子水中搅拌1 h,随后将浆液离心分离得到固体沉淀,放入烘箱中干燥。最后,将样品放于马弗炉中在500 ℃煅烧3 h 获得γ-Fe2O3。

图2 基于铜渣制备γ-Fe2O3 光催化-降解材料及其性能测试Fig.2 Preparation based on copper slag γ-Fe2O3 photocatalytic-degradation material and performance tests
利用合成的γ-Fe2O3开展亚甲基蓝光催化-降解性能试验,并对其动力学进行研究。首先,配置3 组不同浓度12 mg/L、15 mg/L、20 mg/L 的亚甲基蓝溶液,利用紫外可见分光光度计测量溶液吸光度并建立浓度与吸光度的关系基线。然后,向光催化反应器中加入200 mL 一定浓度的亚甲基蓝溶液,并置于黑暗环境中以避免亚甲基蓝自行光解。接着,称取30 mg γ-Fe2O3加入到光催化反应器中,以300 r/min 转速下进行搅拌,待120 min 后吸附达到平衡。随后打开氙灯光源在30 ℃温度下进行光降解。在吸附与光降解过程中每隔30 min 取样,在离心机中以3 000 r/min 离心3 min 后取上层溶液放入石英比色皿,通过紫外可见分光光度计测量其浓度变化,并根据式(1)计算去除率。
式中:C0为溶液初始浓度,mg/L;Ct为t 时刻的溶液浓度,mg/L。
1.3 表征手段
使用X 射线衍射(XRD,UltimaI IV,日本科学株式会社)测定原料矿相,工作条件为Cu-Ka 辐射、40 kV 工作电压、40 mA 工作电流,在10°~90°范围内以20°/min 扫描速度进行测量。通过扫描电子显微镜(SEM,SU5000,日本日立公司Oxford EDS XMAX 20,牛津)观察反应产物的形貌,并通过能谱仪(EDS)分析材料微区的元素种类和含量。通过X射线荧光光谱分析(XRF,XRF-1800,日本岛津)获得样品的化学成分和含量,元素测定范围:4Be-92U,管电流140 mA,最大扫描速度300°/min。利用紫外可见漫反射光谱(UV-3600I PLUS,日本岛津)对样品进行光谱分析。使用美国Quantachrome Nova 4000e 进行比表面积和孔径分布测试。使用美国Lake Shore 公司7404 型对样品进行磁滞回线(VSM)表征,测试灵敏度可达到5 ×10-7emu,测试条件为±2 T。使用北京普析TU-1810 紫外可见分光光度计测定亚甲基蓝的吸光度来表征浓度变化。
2 结果与讨论
2.1 γ-Fe2O3 的合成
由图3(a)可知,当焙烧温度为550 ℃时,焙烧产物主要为α-NaFeO2、Na4SiO4和少量的Na2SiO3,而焙烧温度为800 ℃时,焙烧产物中α-NaFeO2转变为β-NaFeO2。化学反应见式(2)~(4),在富氧条件下铜渣中含铁矿相(Fe2SiO4、Fe3O4)加速氧化,同时NaOH 分解为Na2O,促进铁橄榄石氧化,并结合生成NaFeO2,而过量的Na2O 会和SiO2反应生成硅酸钠。

图3 样品XRD 分析Fig.3 XRD analysis of samples
图3(b)为制得的γ-Fe2O3样品XRD 结果,从图中可以发现经500 ℃煅烧后样品在30.31°、35.26°、43.36°、57.35°和62.90°附近存在较强的衍射峰,分别与γ-Fe2O3(#39-1346)的晶面(2 2 0)、(3 1 1)、(4 0 0)、(5 1 1)和(4 4 0)相对应。铜渣经550 ℃碱熔后主要产物为α-NaFeO2,α-NaFeO2是一种典型的层状AMO2材料,Na+和Fe3+在氧化物离子层之间交替堆叠形成特殊的菱形结构[17],而在随后的水解过程中极易与水中质子发生交换反应,形成中间产物纤铁矿(γ-FeOOH)[18](式(5)~(6)),进一步在500 ℃煅烧3 h 后,获得带有弱磁性的γ-Fe2O3(式(7))。
合成样品的XRF 结果见表2,主要成分为Fe2O3,且纯度达86%。样品中少量的氧化物如SiO2、ZnO、Al2O3和CaO 等均来源于铜渣中杂质。其中CaO 难以与NaOH 发生反应,留在样品中。SiO2、Al2O3与NaOH 反应可生成Na2SiO3、Na4SiO4、NaAlSiO4(由于生成量较低并未在图3(a)中发现),Na2SiO3、Na4SiO4可在随后的水浸中去除,而NaAl-SiO4由于在水中溶解度较低留在样品中。ZnO 在铜渣中存在形式主要为Zn2SiO4,碱熔后可生成Na2ZnSiO4、Na2Zn(OH)4和Na2ZnO2(式(10)~(13)),其中Na2ZnO2易溶于水,而Na2ZnSiO4溶解较慢会部分残留于样品中[19]。若需进一步提高材料纯度,后续可通过酸浸、磁选等工艺进行深度除杂。

表2 γ-Fe2O3 样品化学成分分析(质量百分数)Table 2 Chemical composition analysis of γ-Fe2O3 sample(mass fraction) %
图4 为所合成γ-Fe2O3的微观形貌,可以发现样品颗粒大小不一(小粒径几百个纳米,大粒径2~3 μm),呈现出规则的形状。

图4 γ-Fe2O3 样品微观形貌Fig.4 Micromorphology of γ-Fe2O3 sample
2.2 γ-Fe2O3 材料性质表征
γ-Fe2O3光催化剂的紫外可见漫反射光谱如图5 所示。可以看出,γ-Fe2O3光催化剂在200~600 nm 范围内均表现出很强的吸光性。其禁带宽度通过Tauc 方程可以得出,见式(14)。

图5 γ-Fe2O3 紫外可见漫反射光谱和tauc 法求禁带宽度Fig.5 UV-visible diffuse reflectance spectra of γ-Fe2O3 and tauc method for calculating band gap
式中:α 为吸光指数;hυ 是光子能量,eV;n 为半导体跃迁类型;B 为带边参数常数;Eg为禁带宽度。
吸光指数α 与吸光度A 成正比,用A 代替α 作图,普朗克常量h 取6.63 ×10-34J·s,γ-Fe2O3属于直接间隙半导体,n 取0.5。最终得出γ-Fe2O3光催化剂禁带宽度大约为2.2 eV,与文献报道相一致[20],表明其在可见光范围内具有良好的光催化活性。
针对合成的γ-Fe2O3进行了N2等温吸脱附测试,曲线如图6(a)所示,该反应属于Langmmuir IV型,在0.4~0.9 的相对压力范围内出现了明显的滞后环,表明样品存在介孔结构。由BET 测试得出样品比表面积为9.354 m2/g。图6(b)可知孔径分布范围较宽,最可几孔径为2.9 nm,平均孔径为14.88 nm,孔容为0.034 8 cm3/g。
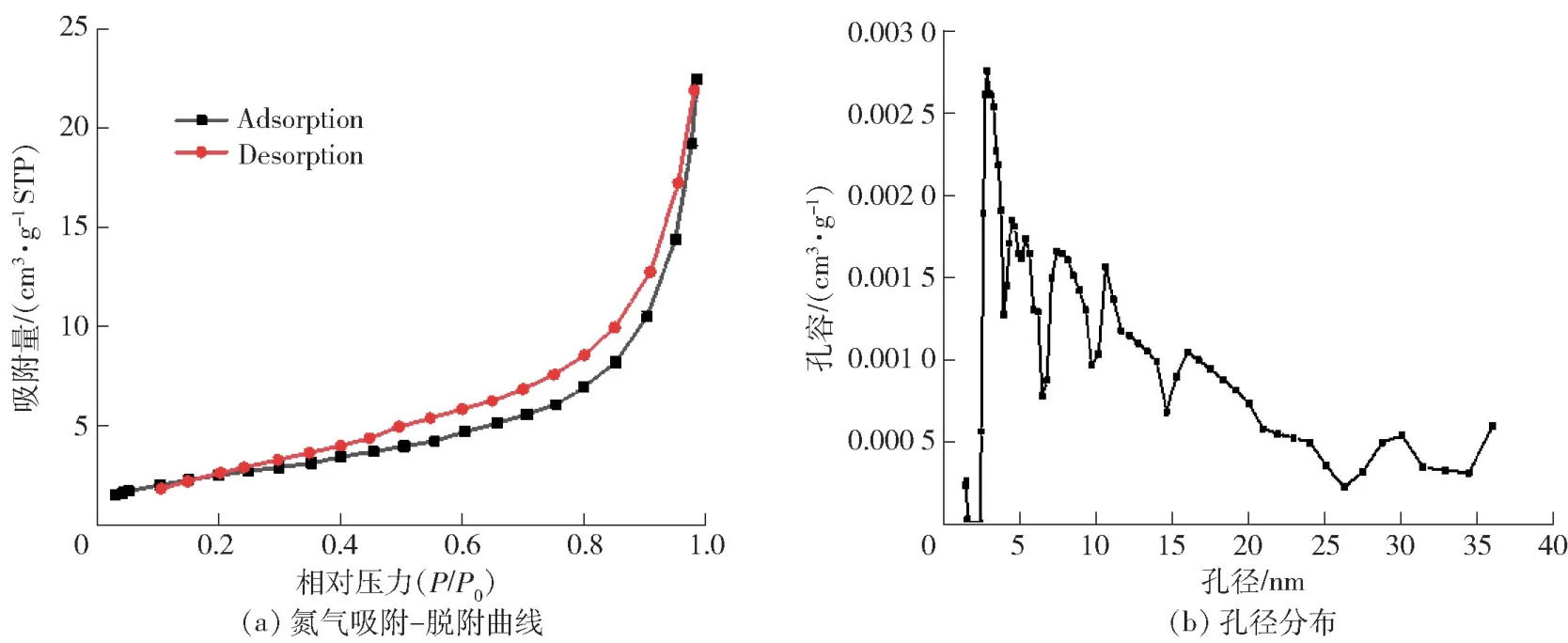
图6 γ-Fe2O3 材料氮气吸附-脱附曲线和孔径分布图Fig.6 Nitrogen adsorption desorption curve of γ-Fe2O3 materials and pore size distribution diagram
对样品进行磁滞回线分析,结果如图7(a)所示。饱和磁化强度值代表测试样品的磁性能大小,发现γ-Fe2O3样品饱和磁化强度为19.13 emu/g,这与文献报道[11]的9.03 emu/g 差别较大,这是由于样品中含有少量的ZnO 等掺杂导致饱和磁化强度增加。矫顽力可以从放大图中读取,大约为27.15 Oe,矫顽力接近于0,表明在室温下呈现超顺磁性。图7(b)为去离子水中γ-Fe2O3粉末样品在受外加磁场作用下的状态。γ-Fe2O3样品为赤红色粉末,通过外加磁铁样品在去离子水中被磁铁吸附,具有较良好的磁性,便于回收循环使用。

图7 γ-Fe2O3 材料的磁滞回线及其在水中被磁铁吸引Fig.7 Hysteresis loop of γ-Fe2O3 materials and attraction by magnet in water
2.3 亚甲基蓝光降解行为
首先,研究不同体积占比双氧水加入量(0、0.1%、0.2%和0.3%)下γ-Fe2O3对亚甲基蓝的光降解行为的影响。从图8(a)可以发现,在120 min内γ-Fe2O3对亚甲基蓝呈现出较弱的吸附行为,所以合理地认为亚甲基蓝的去除主要是来自于光降解。未加入双氧水时,经过4 h 的光降解,亚甲基蓝浓度降低了80%,良好的光降解能力与γ-Fe2O3的带隙能有关;当双氧水加入量为0.3%,4 h 内亚甲基蓝的降解率可达到95%,即使加入少量双氧水也可将降解时间大大缩短至3 h 内,这是由于双氧水可以与γ-Fe2O3发生协同作用[21-22]。一方面光照产生的光生电子(e-)促进了Fe3+向Fe2+的转变,而光生空穴(h+)和H2O 反应生成·OH;另一方面Fe2+与H2O2发生氧化还原反应生成·OH,从而使得亚甲基蓝被·OH 氧化为CO2和H2O。然后,研究不同亚甲基蓝浓度(20 mg/L、15 mg/L 和12 mg/L)对γ-Fe2O3光降解行为的影响。图8(b)为不同亚甲基蓝浓度下染料去除率随时间的变化曲线,在达到吸附平衡后进行光降解测试,发现随着染料浓度的降低,亚甲基蓝降解速率增加,且反应4 h 后降解率不再提高,降解达到阈值,这是由于反应器中亚甲基蓝染料较少,能够在较短的时间内聚集到γ-Fe2O3表面进行降解,表明γ-Fe2O3光催化剂在较低的亚甲基蓝浓度下有着良好的光降解性能。
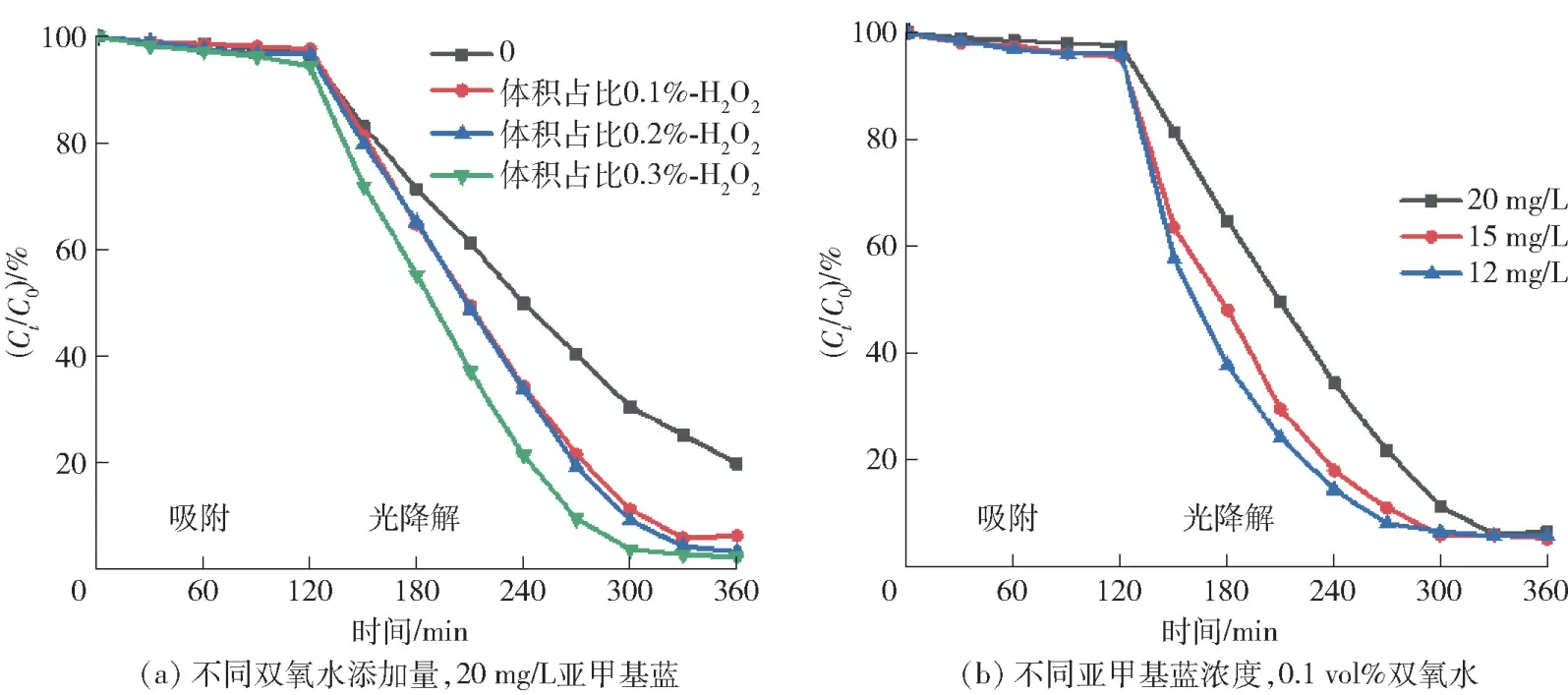
图8 不同条件下γ-Fe2O3 对亚甲基蓝溶液降解的影响Fig.8 Effect of γ-Fe2O3 under different conditions on the degradation of MB
γ-Fe2O3材料在光降解染料过程中的稳定性也是一个非常重要的指标,因此开展了光降解循环测试,结果见图9。向200 mL 浓度为20 mg/L 的亚甲基蓝溶液中加入30 mg γ-Fe2O3和0.1 vol%双氧水进行试验,经过五次光催化-降解循环后,亚甲基蓝的光降解率没有出现明显的下降,这是由于光照作用下产生e-,促进了Fe2+的生成,而H2O2又与Fe2+反应生成Fe3+和·OH,完成了γ-Fe2O3的稳定循环。结果表明利用铜渣制备出的γ-Fe2O3材料具有稳定的光催化活性,结合其具有超顺磁性,便于从液相中回收,重复使用。
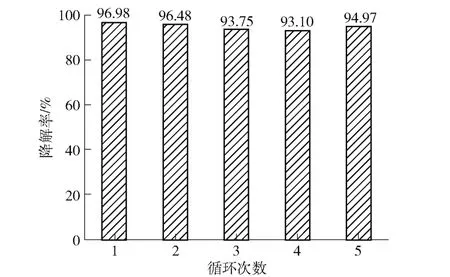
图9 铜渣基γ-Fe2O3 材料对亚甲基蓝的循环降解性能Fig.9 Cyclic degradation of MB by γ-Fe2O3 material based on copper slag
2.4 光降解动力学分析
为了探究亚甲基蓝浓度对γ-Fe2O3材料光催化-降解性能的影响,对其动力学进行研究,并将结果用拟一阶动力学方程(式(15))和拟二阶动力学方程(式(16))进行拟合,拟合结果见图10 和表3。并用式(17)计算出对应的半衰期t1/2。
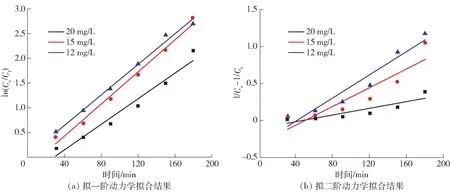
图10 γ-Fe2O3 分别在不同浓度亚甲基蓝溶液中光降解动力学拟合结果Fig.10 The kinetics fitting results of γ-Fe2O3 photodegradation in different concentrations MB

表3 γ-Fe2O3 光催化-降解亚甲基蓝溶液的拟一阶和拟二阶动力学拟合数据Table 3 Pseudo first and pseudo second order kinetics fitting data of γ-Fe2O3 photocatalytic-degradation of MB
式中:Ce为材料达到吸附平衡时溶液中的亚甲基蓝的平衡浓度,mg/L;K 为反应速率常数;t 为降解时间,min。
由表3 可知,相比拟二阶动力学模型(0.80
3 总结
本文以铜渣为原料,通过碱熔-水解-煅烧获得具有较高纯度的γ-Fe2O3,并进行表征,研究其在不同亚甲基蓝染料浓度和不同双氧水用量情况下的光催化-降解性能,得出以下结论。
1)将等质量铜渣和氢氧化钠在550 ℃下焙烧1 h,经过水浸烘干后再将其置于马弗炉中500 ℃下煅烧3 h 可获得γ-Fe2O3。
2)表征结果表明:铜渣经550 ℃碱熔后主要产物为α-NaFeO2,800 ℃下焙烧产物中α-NaFeO2转变为β-NaFeO2;制备的γ-Fe2O3品位大于86%;合成γ-Fe2O3颗粒大小不一,呈现出规则的形状;γ-Fe2O3样品比表面积为9.354 m2/g,孔径分布范围较宽,孔容为0.034 8 cm3/g;γ-Fe2O3在200~600 nm 范围内均表现出很强的吸光性,在可见光范围内具有良好的光催化活性;γ-Fe2O3为赤红色粉末,具超顺磁性,便于回收循环使用。
3)光催化-降解试验结果表明,加入双氧水在一定程度上能够促进γ-Fe2O3的光降解反应,3 h 内亚甲基蓝的降解率达到95%;循环光降解试验表明γ-Fe2O3具有稳定的光催化-降解活性,经5 次循环后,降解率仍能达到94.97%。
4)动力学结果表明γ-Fe2O3光催化-降解亚甲基蓝的过程符合拟一阶动力学模型。

