钠-葡萄糖协同转运蛋白2抑制剂治疗晚期心力衰竭1例
刘凡凡,张越强,杨文静,王晓艳,陈还珍
作者单位:1山西医科大学第一临床医学院,山西 太原 030000;2山西医科大学第一医院心血管内科,山西 太原030000
心力衰竭是多种原因导致心脏泵功能下降的临床综合征,发病率及病死率都非常高,其5年生存率与某些肿瘤相近。我国2003 年流行病学调查示35~74 岁人群慢性心力衰竭患病率为0.9%,2010 年中国心血管病报告表明全国心血管病2.3 亿人,其中心力衰竭病人达420 万人[1-2],最新推算我国心力衰竭现患人数约890 万[3]。随着人口老龄化加重,我国心力衰竭病情将更加严峻[4]。我国心力衰竭指南[5]指出,晚期心力衰竭是指器质性心脏病不断进展,虽经积极的内科治疗心力衰竭症状仍持续存在。据统计,晚期心力衰竭1 年死亡率约为25%~75%[6],其治疗至今仍然是一大难题。现报告1例晚期心力衰竭病人,多种利尿剂应用效果差,病人在拒绝肾脏替代治疗后给予口服卡格列净改善病人短期心力衰竭症状。
1 资料与方法
1.1 一般资料本病例来自山西医科大学第一医院,男,67 岁,间断胸憋、气短2 年余,加重伴双下肢水肿5 d 于2019 年10 月23 日入院。现病史:病人2年前无明显诱因出现双下肢水肿,夜间不能平卧,当地医院考虑“心力衰竭、肾衰竭”,给予对症支持治疗,症状好转后出院;1 年前胸憋、气短症状加重,伴双下肢可凹性水肿,就诊于我院急诊,给予对症支持治疗,症状较前好转出院,院外规律服用心力衰竭规范治疗药物,控制入量,监测体质量,气短症状仍间断出现;半月前再次出现双下肢可凹性水肿,自行增减利尿药物,效果欠佳;5 d 前胸憋、气短加重,夜间端坐呼吸,双下肢水肿加重,为求进一步诊治住院治疗。病人及其近亲属知情同意,本研究符合《世界医学协会赫尔辛基宣言》相关要求。
既往史:病人既往吸烟50 年余,戒烟18 月余。诊断原发性高血压史10 年余,最高达180∕100 mmHg,血压控制尚可;诊断2 型糖尿病史16 年;诊断糖尿病肾病,糖尿病肾病Ⅲ期2 年余。其院外用药见表1。
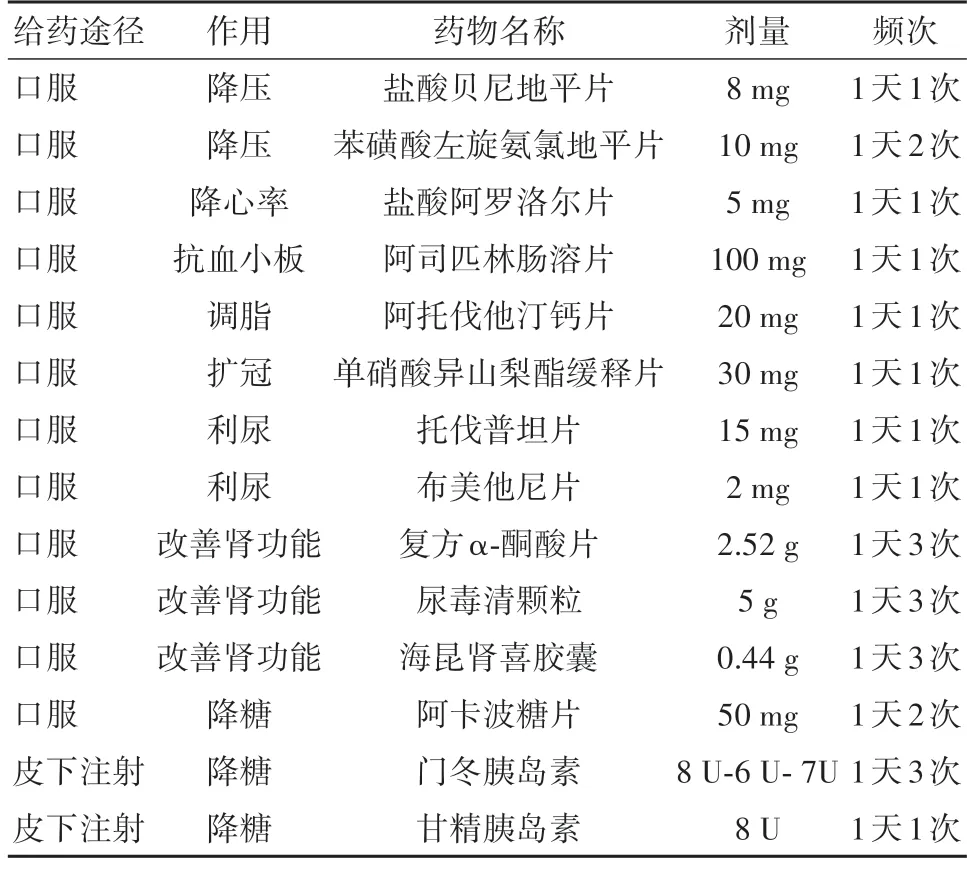
表1 晚期心力衰竭1例院外用药清单
入院查体:体温36.5 ℃,脉搏37 次∕分,呼吸18次∕分,身高172 cm,体质量74 kg,血压158∕72 mmHg(1 mmHg=0.133 kPa),意识清楚,精神差,半卧位,双肺呼吸音粗,双肺可闻及大量湿性啰音,心音正常,心率73 次∕分,律齐,肺动脉瓣第二心音亢进,未闻及心包摩擦音,腹部膨隆,全腹无压痛、反跳痛,肝肋下4 cm,脾肋下未触及,未触及腹部包块,移动性浊音(-),双下肢重度可凹性水肿。
入院首次相关化验:N 末端-B 型钠尿肽前体(NT-proBNP)6 564.13 ng∕L(参考值0~125 ng∕L);肌酸激酶同工酶1.24 μg∕L(参考值0~3.7 μg∕L);总胆固醇2.11 mmol∕L(参考值3.25~5.18 mmol∕L),三酰甘油0.50 mmol∕L(参考值0.2~1.7 mmol∕L),高密度脂蛋白胆固醇0.58 mmol∕L(参考值≥1.04 mmol∕L),低密度脂蛋白胆固1.48 mmol∕L(参考值0~3.12 mmol∕L);同型半胱氨酸26.10 μmol∕L(参考值6~15 μmol∕L);空腹血糖6.74 mmol∕L(参考值3.9~6.0 mmol∕L),糖化血红蛋白4.73%(参考值4.8%~5.9%);尿素22.18 mmol∕L(参考值2.8~7.6 mmol∕L),肌酐233.0 μmol∕L(参考值64~104 μmol∕L),尿酸291 μmol∕L(参考值210~440 μmol∕L),肾小球滤过率(eGFR)=24.51 mL·min-1·(1.73 m²)-1(MDRD 公式),α1 微球蛋白90 mg∕L(参考值10~31 mg∕L),β2微球蛋白16.32 mg∕L(参考值0.6~2.4 mg∕L),钾离子4.78 mmol∕L(参考值3.5~5.5 mmol∕L),钠离子144 mmol∕L(参考值137~147 mmol∕L),氯离子106.0 mmol∕L(参考值99~110 mmol∕L);红细胞3.36×1012∕L(参考值4.3~5.8×1012∕L),血红蛋白100.0 g∕L(参考值130~175 g∕L),红细胞比容31.70%(参考值40%~50%)。
入院超声心动图检查示左房前后径53 mm,右房大小57 mm×43 mm,左室舒末内径58 mm,右室前后径25 mm,肺动脉压71~76 mmHg,左室射血分数51%,提示心脏扩大,肺动脉重度高压。2019 年11月19 日静息心肌血流灌注显像估测左室射血分数(LVEF)为38%。入院诊断:①全心力衰竭竭D 期原因待查:缺血性心肌病?高血压心脏病?糖尿病性心脏病?纽约心脏协会(NYHA)心功能分级Ⅳ级;②高血压3级,很高危心脏扩大;③2型糖尿病;④慢性肾功能不全。
1.2 治疗予降压、降糖、扩张血管、保护肾功能、抗血小板聚集、调脂稳斑、降低心室率、平喘等心力衰竭规范化治疗,针对病人全身容量负荷重,给予利尿治疗,具体利尿方案及日出入量见图1 和图2,同时监测病人NT-proBNP(见图3)和eGFR。
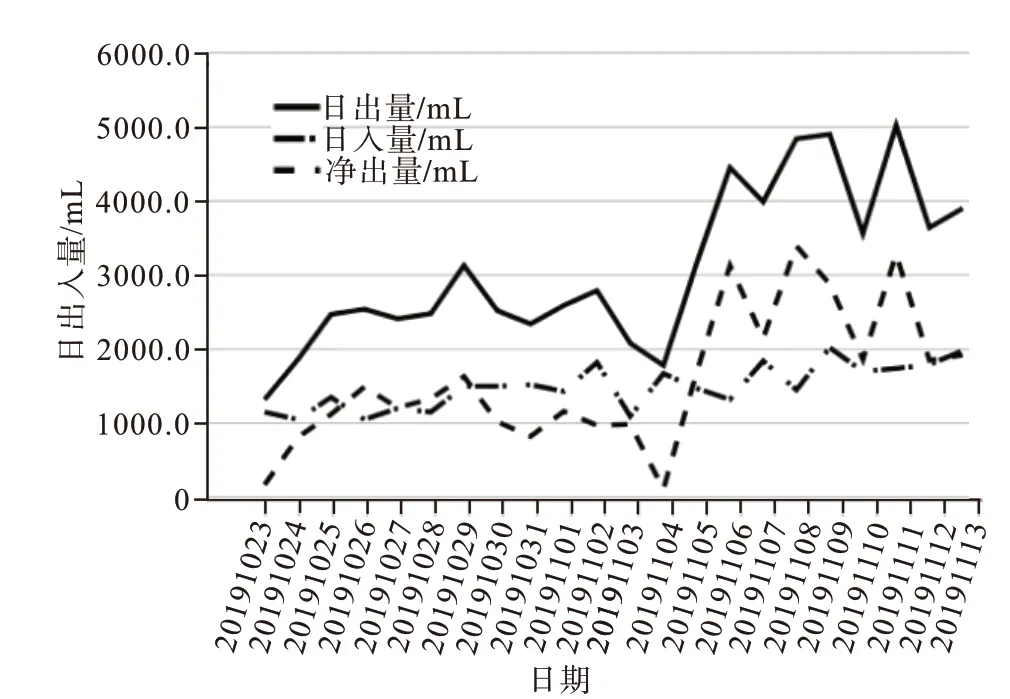
图1 晚期心力衰竭1例住院期间日出入量
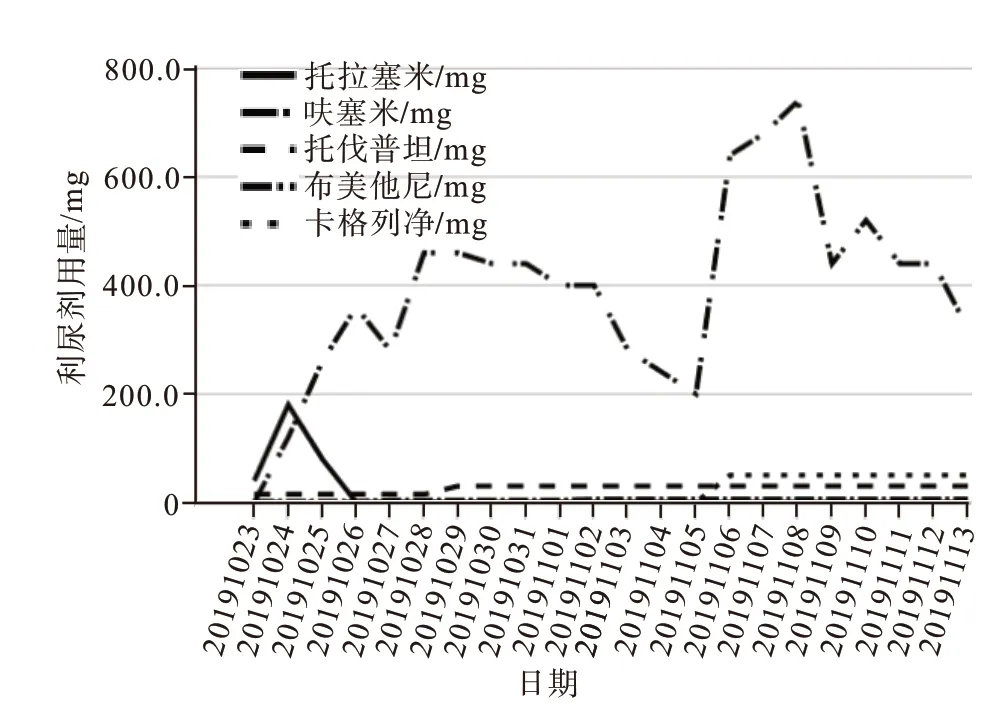
图2 晚期心力衰竭1例住院期间利尿药物及剂量
根据图1、2 可知,病人日净出量并未与利尿剂单日用量呈明显的正相关关系,长期大量袢利尿剂使用使得病人肾功能下降,对利尿剂敏感性下降,产生利尿剂抵抗。2019年11月6日给予病人口服卡格列净50 mg∕d,同时监测病人血糖水平,根据血糖水平调整胰岛素等降糖药物用量。加用卡格列净后,病人每日尿量较未用卡格列净前呈现增加趋势,由于用药前后并没有每日监测NT-proBNP和eGFR,图3 中显示,卡格列净与以上两者的相关关系不甚明显,似与NT-proBNP 降低和肾小球滤过率升高相关。

图3 晚期心力衰竭1例住院期间N末端-B型钠尿肽前体变化趋势
2 结果
病人于2019 年11 月25 日(口服卡格列净50 mg∕d,20 d)监测体质量较入院时下降2 kg,喘憋症状、双下肢可凹性水肿均较前明显缓解,肝下界未触及;可自由活动。遂于该日出院。出院诊断:①心脏扩大NYHA心功能Ⅳ级;②冠状动脉性心脏病,不稳定型心绞痛;③高血压3 级,很高危;④2 型糖尿病,糖尿病肾病Ⅳ期。嘱出院后继服卡格列净50 mg∕d。门诊随访。随访时间及相关指标见表2。
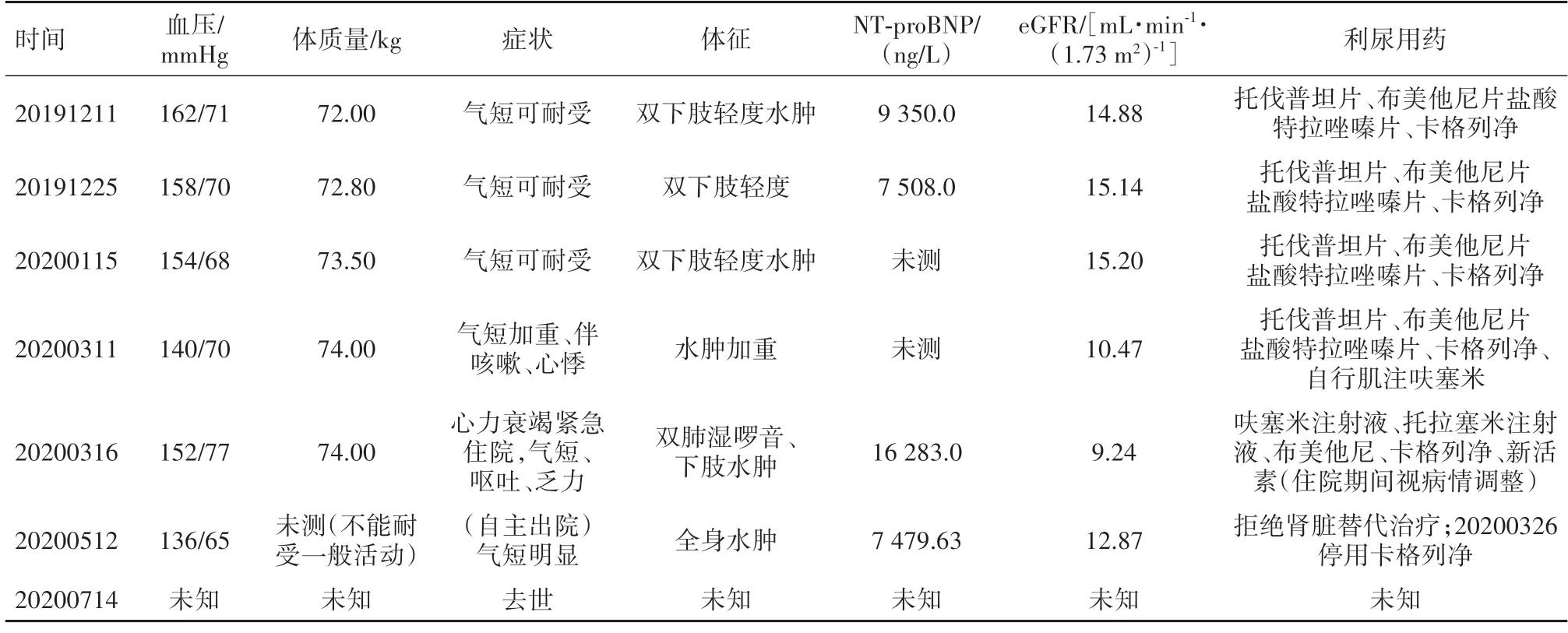
表2 晚期心力衰竭1例出院后随访及随访内容
3 讨论
依据病人症状、体征及实验室检查,该病例病人心力衰竭晚期诊断明确,同时合并有冠心病、高血压、糖尿病、肾病多种疾病。在该病人诊治过程中,病人容量负荷大,多种利尿剂联合治疗效果差,鉴于病人坚决拒绝肾脏替代治疗,给予病人口服卡格列净,病人尿量显示短期内增加,症状在短期内有所缓解。由此病例引发SGLT2 抑制剂对晚期心力衰竭治疗的思考。
晚期心力衰竭的管理策略包括药物治疗、肾脏替代、机械循环支持、心脏移植、症状控制和临终关怀[7-10]。2021 年ESC 指出,在长期机械循环支持植入或心脏移植可行之前,晚期心力衰竭病人可能需要药物治疗和短期机械循环支持植入[9]。胡盛寿[11]指出,约有30%晚期心力衰竭病人是双心室衰竭,而人工心脏为这类病人治疗带来新的曙光。目前限于经济状况与技术支持等原因,药物治疗在晚期心力衰竭中至关重要。自CVOT 研究结果公布,心力衰竭治疗从原来的金三角升级为现在的新四联,SGLT2 抑制剂成为心力衰竭治疗的基石,发挥越来越大的作用,各国也将SGLT2 抑制剂加入心力衰竭治疗指南中[9,12-13]。
肾功能不全和袢利尿剂抵抗通常是晚期心力衰竭病人的临床特征。那么对于拒绝肾脏替代治疗的晚期心力衰竭病人,如何有效利尿来改善症状?关于SGLT2 抑制剂的研究似为这类病人带来新希望。
EMPA-REG OUTCOME、CANVAS Program、DECLARE-TIMI58、SCORED、VERTIS CV 研究结果显示,SGLT2 抑制剂对心血管获益;DAPA-HF、EMPEROR-Reduced、EMPEROR-Preserved、SOLOISTWHF 研究结果显示,SGLT2 抑制剂可以改善心力衰竭病人的心血管结局[14-16]。SGLT2 抑制剂具有降糖、降压、利尿、减重、改善心肌代谢等多重作用[17-18],但是其减少心力衰竭心血管风险的具体机制尚不明确。有研究显示[19],卡格列净通过SGLT1∕AMPK∕Rac1 信号通路直接抑制了心肌还原型烟酰胺嘌呤二核苷酸磷酸(nicotinamide adenine dinucleotide phosphate oxidase,NADPH)氧化酶的活性,从而在心肌中产生抗炎和抗凋亡作用起到心脏保护作用。本病例中,卡格列净表现出对晚期心力衰竭病人良好的短期利尿作用。笔者此前研究显示,SGLT2 抑制剂的利尿作用机制可能为:减少水的重吸收来间接降低钠离子重吸收的渗透性利尿、降低皮肤组织钠浓度而改善水钠潴留、抑制心力衰竭病人肾小管近段的钠氢交换、降低交感神经系统和肾素-血管紧张素-醛固酮系统的活性、下调水通道蛋白2 影响水的重吸收、通过抑制瘦素对钠离子的吸收发挥作用[20]。但是对于SGLT2 抑制剂对晚期心力衰竭病人心肌重构、NT-ProBNP 下降等方面的作用机制有待进一步研究。
卡格列净药物说明书指出eGFR 低于45 mL·min-1·(1.73 m²)-1时慎用该药物[21]。对于卡格列净应用于降低心血管风险,治疗开始前评估肾功能,若eGFR≥60 mL·min-1·(1.73 m²)-1,建议初始剂量口服100 mg,每日1 次;对于eGFR<60 mL·min-1·(1.73 m²)-1的病人,需咨询肾脏科调整剂量,但是若已经启动治疗则可以继续口服100 mg,每天1次,以降低终末期肾病、血清肌酐倍增、心血管死亡和心力衰竭住院的风险[22]。EMPA-REG OUTCOME 和CANVAS Program 试验结果暗示,SGLT2抑制剂可以降低慢性肾脏病(CKD)中肾脏疾病进展的风险。DAPACKD 试验纳入了eGFR 在25~75 mL·min-1·(1.73 m²)-1的肾病病人,结果表明,达格列净使得2~4 期CKD 恶化比率较安慰剂平均减少39%[23]。肾小球内高压被认为是各种病因导致CKD 共有的最终途径,蛋白尿和∕或eGFR 较低的人群中,SGLT2抑制剂可能通过抑制肾小球内压起到保护肾脏的作用[24]。正在进行中的EMPA-KIDNEY 试验纳入20 mL·min-1·(1.73 m²)-1≤eGFR<45 mL·min-1·(1.73 m²)-1或45 mL·min-1·(1.73 m²)-1≤eGFR<90 mL·min-1·(1.73 m²)-1且尿白蛋白与肌酐比值≥200 mg∕g 的CKD 病人,欲证明无论eGFR 是否降低,SGLT2 抑制剂均可以降低广泛的慢性肾病病人的心肾风险[24-25],其结果值得期待。真实世界中,一项关于心力衰竭合并2型糖尿病病人应用卡格列净的研究中CKD≥3期占25.6%,结果显示,使用卡格列净的病人在用药后6个月和12 个月时显著降低利尿剂使用,且在心血管-肾脏风险方面受益[26]。2021 ESC 心力衰竭指南指出,开始SGLT2 抑制剂治疗后eGFR 的小幅下降是可以预期的,eGFR 的初始下降被认为是肾小球内压降低的指标,与安慰剂组相比,在长期治疗中,eGFR 的下降明显缓慢并且是可逆的,不应过早停药[9,24,27-28]。该病人eGFR=24.51 mL·min-1·(1.73 m²)-1,使用卡格列净后短期内未见明显肾功能损害症状,可能与病人高容量负荷状态相关,关于其对晚期心力衰竭的远期治疗效果有待更多的临床数据及研究。
——卡格列净的研究进展

