GLP-1受体激动剂对2型糖尿病患者心血管结局影响的Meta分析
杨琴,马玉东,周冰
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型随机对照试验(RCT),文种限英文和中文,无论是否采用了盲法和分配隐藏。
1.1.2 研究对象接受GLP-1受体激动剂药物治疗的2型糖尿病患者。
1.1.3 干预措施试验组使用“艾塞那肽”、“利拉鲁肽”、“利西司那肽”、“塞马鲁肽”、“杜拉鲁肽”或“阿比鲁肽”降糖治疗;对照组采用安慰剂治疗。用药途径为口服,用药剂量、时间及疗程不限。
1.1.4 结局指标主要结局指标:①经典MACE的三种心血管疾病;②心血管药物死亡率;③致命/非致命性心肌梗死;④致命/非致命性卒中。次要结局指标:①全因死亡率;②因心力衰竭住院的风险;③因不稳定型心绞痛住院的风险。④视网膜病变;⑤肾脏疾病新发或加重的风险。
1.1.5 排除标准①有其他系统严重基础疾病(心、肝、肾以及未控制的高血压)的患者 ②GLP-1联合其他药物,包括中医中药等辅助治疗的干预研究;③未设立对照组、未随机分组的研究;④动物实验、综述、个案报道、述评和系统评价;⑤无法获取全文者;符合上述任意一条排除标准的文献不纳入本研究。
混凝土自身对局部现浇强度的影响体现为混凝土自身的强度以及混凝土的收缩徐变[10].现浇混凝土宜选用与预制墩柱相同强度的混凝土,以使二者有良好的相容性.现浇混凝土在初期一般与预制节段之间会有很好的黏结性能,但是随着现浇混凝土收缩,会导致接触界面上的应变逐渐增大,致使黏结发生破坏,所以对于现浇混凝土宜选用收缩小的材料,以保证局部现浇段在后期有良好的黏结性能.
1.2 文献检索策略
1.2.1 检索范围计算机检索:中国生物医学文献数据库(CBM)(1978~2021-6-30)、中国学术期刊全文数据库/中国知网(CNKI)(1979~2021-6-30)、万方数据库(1998~2021-6-30)、PubMed(1996~2021-6-30)、Web of Science(1990~2021-6-30)、EMbase(1994~2021-6-30)及Cochrane Library(从建库至2021-6-30),包括学位论文、会议论文以及注意检索未发表的文献,必要时采用手工检索,保证文献检索的全面性。
1.2.2 检索策略中文数据库:胰高血糖素样肽-1受体激动剂、艾塞那肽、利拉鲁肽、利西塞那肽、塞马鲁肽、杜拉鲁肽、阿比鲁肽、安慰剂、心血管药物死亡率、心肌梗死及卒中。外文数据库:Glucagon-like peptide-1 receptor agonists、Cardiovascular mortality、Myocardial infarction、Stroke、Heart failure、Lixisenatide、Exenatide、Liraglutide、Semaglutide、Albiglutide、Dulaglutide、Placebo及Randomized Clinical Trial。
以上述主题词组成检索式,进行文献检索,以PubMed 为例,检索策略如下:


1.3 文献筛选、质量评价及资料提取
1.3.1 文献筛选与资料提取由两名评价员独立对文献进行筛选,并按照纳入与排除标准提取文献资料,主要包括研究的基本信息、方法学信息、干预的过程及方法(是否有经费支持、降糖药使用的疗程、剂量和时间)、经典的MACE和次要结局指标的发生情况、不良事件的报道(包括严重低血糖、胃肠道反应、急性胰腺炎、胰腺癌、甲状腺髓样癌和肾脏疾病等)。遇到无法提取的或模糊不明的信息,与原文作者取得联系以获取明确信息。
1.3.2 纳入研究的方法学质量评价根据Cochrane系统评价Handbook 5.1.0[5]中RCT试验的评价标准,对纳入的文献方法学质量进行独立的偏倚风险评估。
1.4 统计学分析采用RevMan 5.3软件进行Meta分析[6]。计数资料采用计数资料采用相对危险度(Relative risk,RR)及95%CI为疗效分析统计量。纳入研究结果间的异质性采用χ2检验和I2进行定量分析,当I2≤50%,提示具有同质性,采用固定效应模型;若I2>50%,提示存在高度异质性,采用随机效应模型进行分析,并进行亚组分析或敏感性分析。采用漏斗图评估潜在的发表偏倚。
2 结果
2.1 文献筛选结果初检出925篇文献,经过对文献的题目、摘要及全文进行阅读,层层筛选最终纳入7个RCT研究[7-13],共纳入56 004例受试者,文献筛选结果及流程见图1。

图1 文献筛选结果及流程图
2.2 纳入研究的基本特征7篇(包括56 004名参与者)RCT研究符合条件被纳入Meta分析,纳入研究的基本特征见表1,偏倚风险评价结果见表2。

表1 纳入研究的基本特征

表2 纳入研究的偏倚风险评价结果
2.3 纳入研究的方法学质量评价①随机方法:4个研究采用计算机生成随机序列,均为低风险,3个研究随机方法未描述不清楚;②分配方案隐藏:2个研究清楚的说明了分配隐藏的方法,其余研究未报道;③盲法:7项研究均采用双盲(受试者与研究者),为低风险;④不完全结果数据:2个研究无失访研究对象,其余研究均报道有一定数量的患者未如期完成所有的治疗干预而中途退出试验;⑤选择性报告:7项研究均报道了主要结局指标和次要结局指标,所有研究均报道了不良事件的发生情况,为低风险;⑥亚组分析:3项研究进行了亚组分析,其余研究未报道;⑦其他偏倚:1项研究报告了无医药公司的经济支持,其余6项研究均未报道。
2.4 Meta分析结果
2.4.1 经典MACE的三种心血管疾病风险纳入的7篇文献均观察了MACE,结果显示27 977例接受GLP-1受体激动剂治疗的患者中2948例发生MACE,28 027例单用安慰剂治疗的患者中3304例发生MACE。异质性检验,I2=45%,P=0.09,固定效应模型显示,GLP-1受体激动剂组MACE的发生风险显著低于安慰剂组,差异有统计学意义(RR=0.89,95%CI:0.85~0.94,P<0.00001),(表3,图2)。
2.4.2 心血管死亡率纳入的7篇文献均观察了心血管死亡率,结果显示27 977例接受GLP-1受体激动剂治疗的患者中1213例发生心血管死亡,28 027例单用安慰剂治疗的患者中1371例发生心血管死亡。异质性检验,I2=9%,P=0.0002,固定效应模型显示,GLP-1受体激动剂组心血管死亡率显著低于安慰剂组,差异有统计学意义(RR=0.89,95%CI:0.82~0.96,P=0.002),(表3,图3)。

图3 GLP-1受体激动剂与安慰剂两组心血管死亡率比较的森林图
2.4.3 致命或非致命性心肌梗死纳入的7篇文献均观察了致命或非致命性心肌梗死,结果显示27 977例接受GLP-1受体激动剂治疗的患者中1540例发生致命或非致命性心肌梗死,28 027例单用安慰剂治疗的患者中1662例发生致命或非致命性心肌梗死。异质性检验,I2=41%,P=0.12,固定效应模型显示,GLP-1受体激动剂组致命或非致命性心肌梗死的发生率显著低于安慰剂组,差异有统计学意义(RR=0.93,95%CI:0.87~0.99,P=0.03),(表3,图4)。
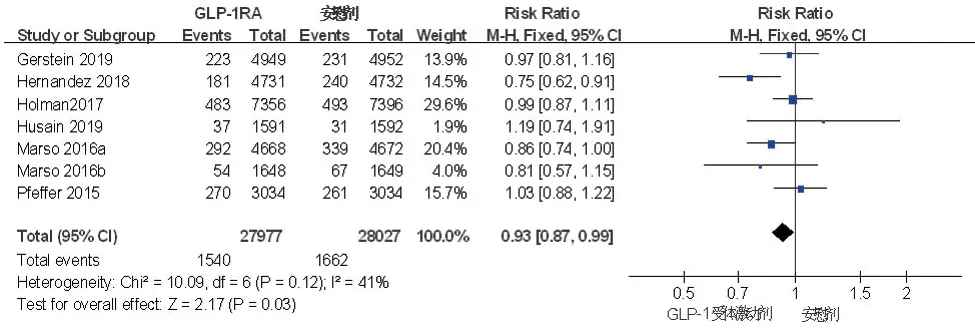
图4 GLP-1受体激动剂与安慰剂两组致命/非致命性心肌梗死比较的森林图
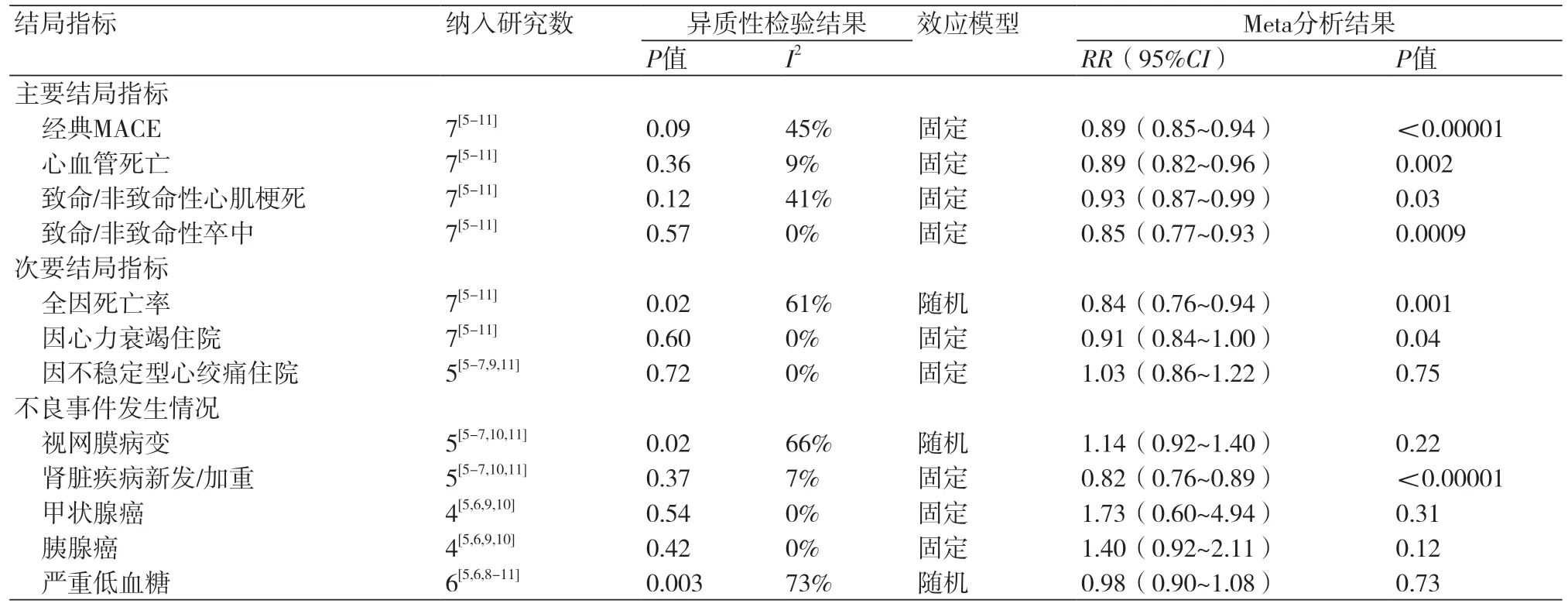
表3 Meta分析结果表
2.4.4 致命或非致命性卒中纳入的7篇文献均观察了致命或非致命性卒中,结果显示27 977例接受GLP-1受体激动剂治疗的患者中721例发生致命或非致命性卒中,28 027例单用安慰剂治疗的患者中852例发生致命或非致命性卒中。异质性检验,I2=0%,P=0.57,固定效应模型显示,GLP-1受体激动剂组致命或非致命性卒中的发生率显著低于安慰剂组,差异有统计学意义(RR=0.85,95%CI:0.77~0.93,P=0.0009),(表3,图5)。
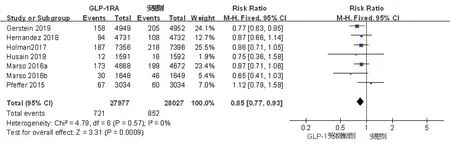
图5 GLP-1受体激动剂与安慰剂两组致命/非致命性卒中比较的森林图
2.4.5 全因死亡率纳入的7篇文献均观察了全因死亡率,结果显示27 977例接受GLP-1受体激动剂治疗的患者中1916例死亡,28 027例单用安慰剂治疗的患者中2246例死亡。异质性检验,I2=61%,P=0.02,随机效应模型显示,GLP-1受体激动剂组全因死亡率显著低于安慰剂组,差异有统计学意义(RR=0.84,95%CI:0.76~0.94,P=0.001),(表3,图6)。
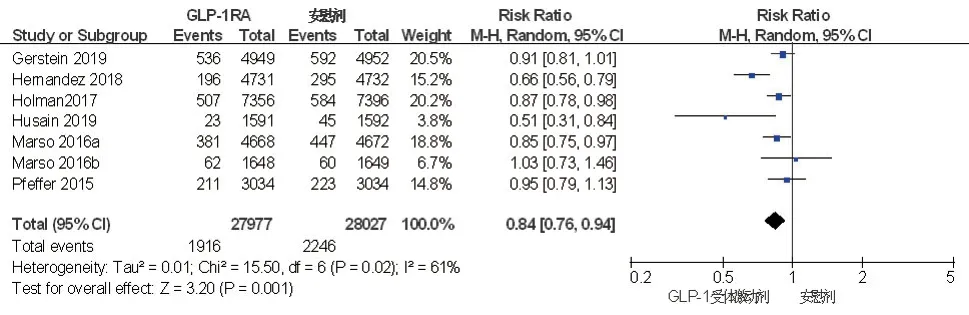
图6 GLP-1受体激动剂与安慰剂两组全因死亡率比较的森林图
2.4.6 因心力衰竭住院的风险纳入的7篇文献均观察了心力衰竭住院风险,结果显示27 977例接受GLP-1受体激动剂治疗的患者中931例因心力衰竭住院,28 027例单用安慰剂治疗的患者中1021例因心力衰竭住院。异质性检验,I2=0%,P=0.60,固定效应模型显示,GLP-1受体激动剂组因心力衰竭住院的风险显著低于安慰剂组,差异有统计学意义(RR=0.91,95%CI:0.84~1.00,P=0.04),(表3,图7)。

图7 GLP-1受体激动剂与安慰剂两组因心力衰竭住院风险比较的森林图
2.4.7 因不稳定型心绞痛住院的风险纳入的7篇文献中有5篇[7-9,11,13]观察了不稳定型心绞痛住院的风险,结果显示15 890例接受GLP-1受体激动剂治疗的患者中252例不稳定型心绞痛住院,15 899例单用安慰剂治疗的患者中有245例因不稳定型心绞痛住院。异质性检验,I2=0%,P=0.72,固定效应模型显示两组因不稳定型心绞痛住院的风险相似,差异无统计学意义(RR=1.03,95%CI:0.86~1.22,P=0.75),(表3,图8)。

图8 GLP-1受体激动剂与安慰剂两组因不稳定型心绞痛住院风险比较的森林图
2.4.8 不良事件的种类及发生率纳入的7篇文献中有5篇[7-9,12,13]观察了视网膜病变和肾脏疾病新发或加重的风险,结果显示17 573例接受GLP-1受体激动剂治疗的患者中有643例发生视网膜病变、1288例发生肾病或肾功能恶化;17 580例单用安慰剂治疗的患者中617例发生视网膜病变、1533例发生肾病或肾功能恶化。随机效应模型显示两组视网膜病变的发生风险相似,差异无统计学意义(异质性检验,I2=66%,P=0.02;RR=1.14,95%CI:0.92~1.40,P=0.22)。固定效应模型显示,GLP-1受体激动剂肾脏疾病新发或加重的风险显著低于安慰剂组,差异有统计学意义(异质性检验,I2=7%,P=0.37;RR=0.82,95%CI:0.76~0.89,P<0.00001)。4篇文献[7,8,11,12]分析结果显示,17 382例接受GLP-1受体激动剂治疗的患者中有9例发生甲状腺癌、53例发生胰腺癌,17 390例单用安慰剂治疗的患者中3例发生甲状腺癌、38例发生胰腺癌。固定效应模型显示两组甲状腺癌(异质性检验,I2=0%,P=0.54;RR=1.73,95%CI:0.60~4.94,P=0.31)和胰腺癌(异质性检验,I2=0%,P=0.42;RR=1.40,95%CI:0.92~2.11,P=0.12)的发生风险相似,差异无统计学意义。6篇文献[7,8,10-13]分析结果显示,26 329例接受GLP-1受体激动剂治疗的患者中有848例发生严重低血糖,26 378例单用安慰剂治疗的患者中有864例发生严重低血糖。异质性检验,I2=73%,P=0.003,随机效应模型显示两组严重低血糖的发生风险相似,差异无统计学意义(RR=0.98,95%CI:0.90~1.08,P=0.73),(表3)。
2.5 发表偏倚基于经典MACE的三种心血管疾病发生风险的漏斗图,对称性均较好(图9),提示其存在发表偏倚的可能性较小;其他结局指标(包括心血管死亡率、致命/非致命性心肌梗死、致命/非致命性卒中、全因死亡率、因心力衰竭或不稳定性心绞痛住院的风险)的漏斗图均较对称,提示存在发表偏倚的可能性小。由于纳入的研究数量较少,因此发表偏倚的评价意义有限。
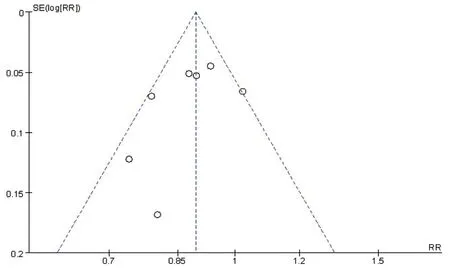
图9 GLP-1受体激动剂与安慰剂两组经典MACE的三种心血管结局比较的漏斗图
3 讨论
GLP-1是一种内源性肠促胰岛素分泌剂,在稳定血糖中起着重要作用,GLP-1受体存在于许多器官,包括胰腺、大脑、心脏、肾脏和胃肠道[14,15],多项研究表明其在降低心血管疾病的发生率方面具有优势性[16],GLP-1对糖尿病患者体内的GLP-1受体激动剂多靶点发挥效应,有效避免或干预了多种诱发心血管疾病的危险因素。与既往研究相比[17,18],本研究纳入的研究对象和MACE终点事件均增加30%左右,其中研究对象增加13 084例,MACE终点事件增加1394例,且患者治疗时间更长。本研究纳入的人群不仅包括已确诊心血管疾病的患者,还包括具有心血管疾病危险因素的一级预防患者。研究的干预措施中增加了GLP-1受体激动剂的同源药物杜拉鲁肽,且比以往的研究干预的时间更长,除此之外,还纳入了一种新的口服制剂塞马鲁肽。总体而言,纳入的7篇文献中6篇研究了经典的MACE风险,GLP-1受体激动剂的使用可使MACE的发生率减少12%(相对风险),而卒中和心肌梗死的风险(包括致命或非致命性)相对减少15%和7%,在最近的一篇荟萃分析中[19],作者观察了SGLT2抑制剂的心血管结局,随访3.3年的时间,发现MACE的发生率相对降低11%,阿比鲁肽,杜拉鲁肽,利拉鲁肽和塞马鲁肽与天然的GLP-1在结构上更相似,而艾塞那肽和利西塞那肽从结构上看,基于烯酸-4[20,21],因此利拉鲁肽、塞马鲁肽和阿比鲁肽相比艾塞那肽能更有效的激活GLP-1受体。另外,药代动力学的差异也导致药物之间不同的生物学效应,这与药物的半衰期有关。一些GLP-1受体激动剂的药物半衰期较短,如利西塞那肽为2~3 h,利拉鲁肽为12 h;另外一些药物的半衰期较长,如杜拉鲁肽为120 h,皮下给药的塞马鲁肽为170 h;还有缓释配方的艾塞那肽[20],这些决定了药物每日或每周的使用剂量,例如口服制剂的塞马鲁肽需要每日给药。虽然药物的持续作用时间似乎并不影响疗效,但研究认为药物之间具有不同的分子结构也可能影响药效学特性,基于烯酸-4的药物对MACE的发生可能存在潜在影响。
参加研究的人群不同是这些临床研究结果存在差异的可能原因[23]。与之前的GLP-1受体激动剂试验相比,Holman等[10]的试验中主要MACE终点事件明显减少,可能与该研究很大一部分患者无心血管疾病有关,而Gerstein等[7]的试验中纳入了心血管疾病患者,MACE终点事件几乎是Holman等[10]试验的2倍。但由于MACE结局事件人数较少,故这项研究的统计效能受到了一定的限制。虽然MACE终点事件在一级和二级预防的患者中未发现异质性,但无法确定GLP-1受体激动剂的使用能否使一级预防患者MACE的风险与二级预防患者一样降低,因为无心血管疾病的人群本身发生MACE的风险就相对较低,即使可以,一级预防人群的绝对风险降低幅度也较小,且治疗的成本效益不大,因此目前对于指南建议GLP-1受体激动剂仅用于心血管疾病患者的证据不足[24]。随访时间是另一个导致研究结果间差异的潜在因素。在两项最早的大型GLP-1受体激动剂心血管结局试验中,Pfeffer[11]试验的随访时间(中位数2.1年)比Marson[8]试验更短(中位数为3.8年),但是随访的持续时间并未改变药物干预对MACE主要终点事件的影响。基于年龄的亚组分析也得出了一致性的结果,年龄越大MACE发生风险越高,而对高龄患者的益处可能也相对更大。
本研究首次显示GLP-1受体激动剂可降低因心力衰竭住院的风险,尽管相对风险降低很小(RR=0.91,95%CI:0.84~1.00,P=0.04),虽然既往研究提示SGLT2抑制剂对心力衰竭住院风险的降低可达31%,但对于不能耐受SGLT2抑制剂或存在禁忌症的心力衰竭或肾功能损害的患者,GLP-1受体激动剂可作为一种替代选择[19]。GLP-1受体激动剂可减少心力衰竭的风险目前尚不清楚,可能是因为荟萃分析中发现GLP-1受体激动剂可减少心肌梗死的风险,而心肌梗死是心力衰竭常见的前兆,但这一假设还需进一步研究调查(如需明确个体心血管事件发生的时间顺序)。总体来说,GLP-1受体激动剂具有明显的心脏保护作用,尤其体现在个体心血管事件预防试验中,GLP-1受体激动剂主要有抗动脉粥样硬化的效果。实验研究表明,GLP-1受体激动剂通过抑制细胞内钙超载和高糖诱导的凋亡来减少心肌梗死面积和再灌注损伤[25,26]。而SGLT2抑制剂对心血管疾病结局的影响更快,对心力衰竭的影响更为显著,这两种抗糖尿病药物的协同作用可更好地降低心血管疾病风险。研究显示利用GLP-1类药物造成肾病事件减少,提示其在减少糖尿病相关肾病方面的有利作用[27,28],本荟萃分析结果也提示GLP-1受体激动剂可显著降低新发肾病或肾功能衰竭的风险(RR=0.82,95%CI:0.76~0.89,P<0.00001)。同样,GLP-1受体激动剂并不增加急性胰腺炎和胰腺癌的发生风险,也不增加严重低血糖和甲状腺癌的风险。GLP-1受体激动剂也未增加视网膜病变的风险,由于终点事件数量有限,荟萃分析的结果与纳入的文献研究并不一致,今后仍需更加全面分析降糖药物对眼部的影响。
4 结论
对于2型糖尿病患者而言,GLP-1受体激动剂的使用可减少MACE三种心血管事件的发生,降低致命或非致命性心肌梗塞、卒中、全因死亡率和因心力衰竭住院的风险。GLP-1受体激动剂同时减少2型糖尿病患者肾功能恶化的风险,且并不增加视网膜病变、严重低血糖、胰腺炎等胃肠道不良反应和甲状腺癌的风险。GLP-1受体激动剂可达到较好的利弊平衡,应针对患者需求进行个体化药物选择。

