心脏磁共振组织追踪技术在急性心肌梗死后心肌应变评估中的应用
孙小伶,王 丹,朱 雪,王佳丽,戚云杰(通信作者)
(徐州医科大学附属医院影像科 江苏 徐州 221000)
急性心肌梗死(acute myocardial infarction,AMI)是临床常见病及多发病之一,指冠状动脉血管阻塞或狭窄等,导致心肌缺氧、缺血等一系列病理改变。心肌发生缺血坏死后,在室壁应力作用下可逐渐拉伸并变薄,继而导致了左心室重构[1]。心肌应变是临床用于定量评估心肌运动情况的指标,不仅可评定心肌功能,还可准确反映心肌形变程度[2-4]。心脏磁共振(cardiac magnetic resonance imaging,CMR)具有无辐射性、无创伤性及安全性高等特点,已成为心肌功能评估金标准,多采用组织追踪技术(tissue tracing,TT)对心肌应变情况进行分析[5]。本研究旨在探讨AMI后心肌应变评估中CMRTT的应用价值,现报道如下。
1 资料与方法
1.1 一般资料
选取2019年8月—2021年3月徐州医科大学附属医院收治的97例AMI患者为AMI组,选取同期CMR检查结果正常的97名健康体检者作为对照组。纳入标准:①AMI患者均符合《急性心肌梗死诊断和治疗指南》中AMI诊断标准;②研究对象年龄>18岁;③患者发病后1个月内接受CMR检查;④患者及健康体检者资料完整。排除标准:①合并严重心脏疾病如重度心力衰竭、心脏瓣膜病及心肌病者;②中途退出者;③合并精神系统疾病者。AMI组男52例,女45例;年龄最小31岁,最大75岁,平均(51.18±2.31)岁。健康体检者中,男49例,女48例;年龄最小33岁,最大73岁,平均(51.29±2.27)岁。两组患者的一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究符合《赫尔辛基宣言》要求。
1.2 方法
入组者均行CMR检查。①设备选用飞利浦Ingenia 3.0T磁共振,线圈选用48通道腹部线圈,联合呼吸心电门控。先行真稳态进动快速成像序列(true fast imaging with stead-state precession,SSFP)扫描,取矢状位、冠状位及轴位行定位扫描,于轴位、冠状位图像中对心脏长轴进行平行定位,对类两腔图像进行扫描,对类四腔图像进行定位;以类两腔、类四腔图像为依据,对左心室短轴图像进行准确定位,后对两腔、四腔及左室流入流出道层面图像进行扫描;左室短轴扫描范围需覆盖左心室,由心尖部直至基底部,共8~10层。扫描参数设定:TE、TR分别调节为1.7 ms、3.8 ms,FOV设定为36 cm×36 cm,重建矩阵设置为256×256,翻转角设置为55°,层厚设定为8 mm。②后行反转恢复快速梯度回波序列扫描,对比剂选用扎喷酸葡胺注射液(北京北陆药业股份有限公司;国药准字H20013088;12 mL:5.63 g),将剂量为0.2 mL/kg对比剂经肘静脉注射,控制高压注射器流率为4.0 mL/s,扫描短轴、四腔、两腔及左室流入流出道层面图像,覆盖左心室完成左室短轴扫描,由心尖部直至基底部,共8~10层;设定扫描参数:以心肌信号最低层面为依据确定T1,设定TE为3.2 ms,TR设置为6.8 ms,FOV设置为36 cm×36 cm,重建矩阵设置为256×256,设置翻转角为25°,层厚设置为8 mm。
1.3 观察指标
对比两组心功能参数,左心室心肌应变参数,分析AMI左室各节段心肌应变变化情况,并分析梗死节段预测中AMI左室心肌阶段应变参数的作用。①将扫描所得图像上传至工作站,运用3D-short工具于四腔长轴对左心室范围进行划定,于短轴层面舒张及收缩末期描绘心外膜及心内膜轮廓,经软件计算得出左心室收缩末期容积(left ventricular end systolic volume,LVESV)、左心室舒张末期容积(left ventricular end diastolic volume,LVEDV)、每搏输出量(stroke output,SV)、心输出量(cardiac output,CO)及左室射血分数(left ventricular ejection fraction,LVEF)。②应用TissueTracking工具于舒张末期对心外膜及心内膜轮廓进行勾画,采用软件追踪功能以心动周期内心肌变化为依据对心肌运动改变进行追踪,得出2D短轴环向应变(2D SA Ecc)、2D短轴径向应变(2D SA Err)、2D长轴径向应变(2D LA Err)、2D长轴纵向应变(2D LA Ell)、3D整体环向应变(3D Ecc)、3D整体径向应变(3D Err)及3D整体纵向应变(3D Ell),将心室壁分为心尖段、基底段及中间段,心肌节段共16个。③以LGE阳性结果为依据对梗死节段进行判断,应用TissueChar工具于短轴各层面对心外膜及心内膜轮廓进行勾画,并对比各节段图像,分为远隔节段、梗死节段及相邻节段3个亚组。
1.4 统计学方法
使用SPSS 19.0统计软件进行数据处理。符合正态分布的计量资料采用(± s)表示,行t检验;计数资料用频数(n)和百分率(%)表示,组间比较采用χ2检验;采用受试者工作特征(receiver operating characteristic,ROC)曲线、ROC曲线下面积(area under curve,AUC)、灵敏度、特异度比较两种工具的预测价值,P<0.05为差异有统计学意义。
2 结果
2.1 两组心功能参数对比
AMI组LVEF、SV及CO水平均显著低于对照组;AMI组LVEDV、LVESV水平高于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组心功能参数比较( ± s,%)
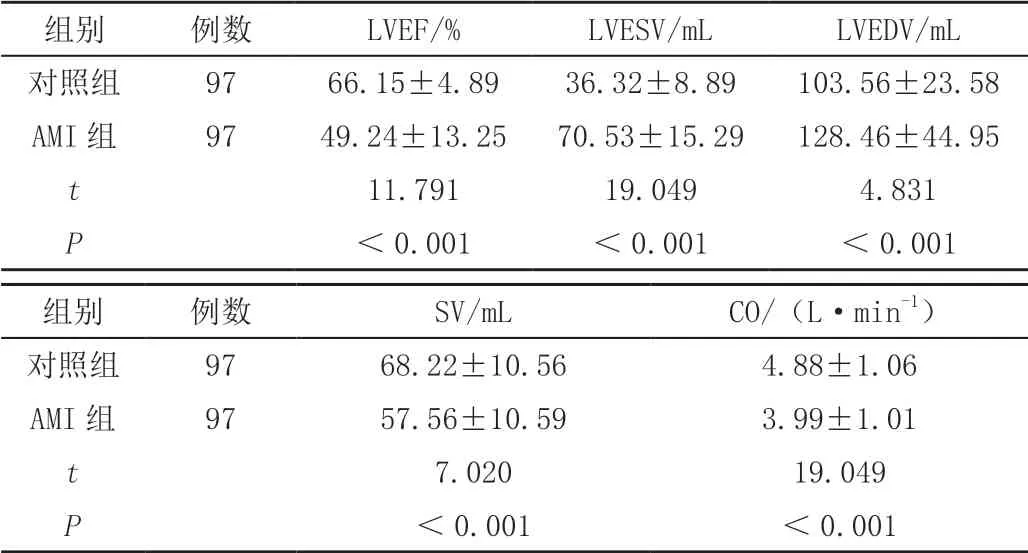
表1 两组心功能参数比较( ± s,%)
注:AMI,急性心肌梗死;LVEF,左室射血分数;LVEDV,左心室舒张末期容积;LVESV,及左心室收缩末期容积;SV,每搏输出量;CO,心输出量。
2.2 两组左心室心肌应变参数对比
AMI组2D与3D各方向的整体心肌应变值均低于对照组,差异均有统计学意义(P<0.05),见表2。
表2 两组左心室心肌应变参数比较( ± s,%)
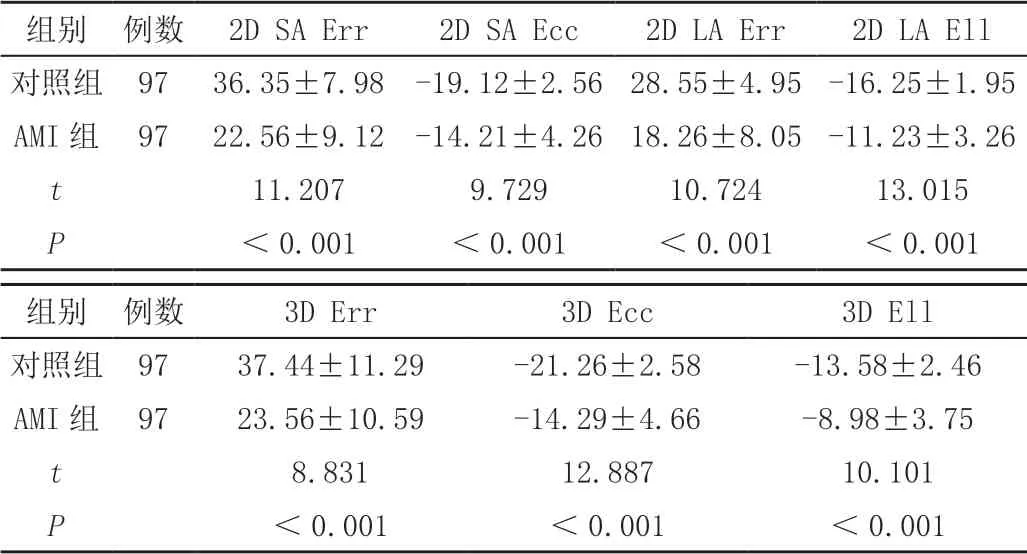
表2 两组左心室心肌应变参数比较( ± s,%)
注:AMI,急性心肌梗死;2D SA Ecc,2D短轴环向应变;2D SA Err,2D短轴径向应变;2D LA Err,2D长轴径向应变;2D LA Ell,2D长轴纵向应变;3D Ecc,3D整体环向应变;3D Err,3D整体径向应变;3D Ell,3D整体纵向应变。
2.3 AMI左室各节段心肌应变变化情况分析
相邻节段、梗死节段在2D、3D各方向的节段心肌应变值均低于正常节段,差异有统计学意义(P<0.05),见表3。
表3 AMI左室各节段心肌应变变化情况( ± s,%)
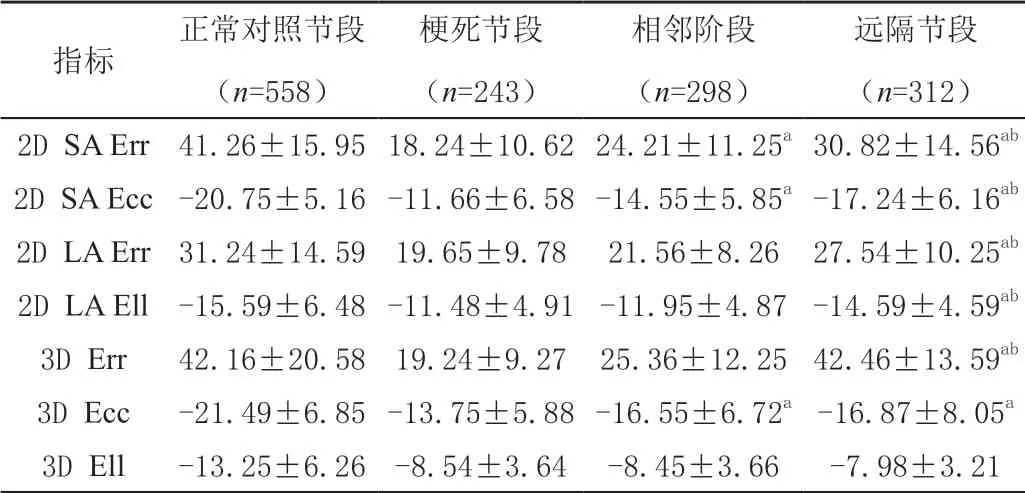
表3 AMI左室各节段心肌应变变化情况( ± s,%)
注:与梗死节段比较,aP<0.05;与相邻节段比较,bP<0.05。
指标正常对照节段(n=558)相邻阶段(n=298)梗死节段(n=243)远隔节段(n=312)2D SA Err41.26±15.9518.24±10.6224.21±11.25a30.82±14.56ab 2D SA Ecc-20.75±5.16-11.66±6.58-14.55±5.85a-17.24±6.16ab 2D LA Err31.24±14.59 19.65±9.78 21.56±8.26 27.54±10.25ab 2D LA Ell-15.59±6.48-11.48±4.91-11.95±4.87-14.59±4.59ab 3D Err 42.16±20.58 19.24±9.27 25.36±12.2542.46±13.59ab 3D Ecc -21.49±6.85-13.75±5.88-16.55±6.72a-16.87±8.05a 3D Ell -13.25±6.26 -8.54±3.64 -8.45±3.66 -7.98±3.21
2.4 AMI左室心肌应变参数对梗死节段的预测作用分析
预测梗死节段时,3D Ecc敏感性最高,2D SA Ecc特异性最高,见表4。
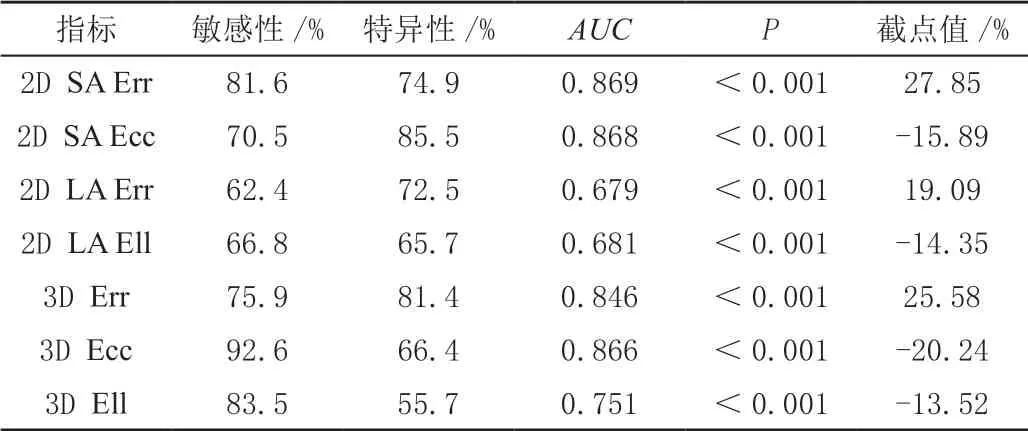
表4 AMI左室心肌应变参数对梗死节段的预测价值
3 讨论
心肌应变指肌纤维在一个心动周期中所发生的运动形变,已有研究发现,心肌应变指数用于心肌功能评估相较于LVEF更为敏感,可准确反映心脏收缩期功能[6]。CMR可通过无创检查完成对心脏结构、功能等检查与评价,不仅是临床检测梗死瘢痕心肌的金标准,也是心肌功能评估的金标准[7]。CMR-TT具有可重复操作、成像时间短等优势,可对心脏运动、形变等情况进行定量评估,现已被广泛应用于多种心脏疾病的诊断及评估中[8-10]。
人体心肌纤维分布较为复杂,不仅包括心外膜心肌、心内膜心肌,还包括心肌中层纤维,正常心室运动需以上各方向心肌纤维紧密合作。心肌应变是对心肌形变实现定量测量的一种重要方法,可评估心肌段长度变化情况,负值提示心肌增厚缩短,而正值提示心肌变薄延长[11]。心肌收缩运动可从3个方向计算应变值,即径向、纵向及环向。已有大量研究证实,心肌应变参数用于心脏功能早期评估相较于LVEF更为敏感。应用CMR-TT技术评估AMI后心肌应变,仅需通过常规序列扫描成像及后处理,即可得出准确评估数据,该种技术对功能恢复评估、梗死范围判断等均不亚于LGE,且无需造影剂、特殊序列,具有可重复操作、成像时间短等优势,患者接受度更高[12-14]。此外,国外研究证实Ecc可用于左心室重构预测,且与左心室功能具有直接相关性。本研究结果显示,采用CMR-TT技术对97例AMI患者开展检查,结果显示,与对照组比较,AMI组左室射血分数(LVEF)、每搏输出量(SV)、心输出量(CO)均更低,左心室舒张末期容积(LVEDV)及左心室收缩末期容积(LVESV)水平均更高(P<0.05);与对照组比较,AMI组2D与3D各方向的整体心肌应变值均更低(P<0.05);预测梗死节段时,3D环向应变(3D Ecc)敏感性最高,2D短轴环向应变(2D SA Ecc)特异性最高。提示应用CMR-TT技术对心肌梗死早期进行检查,并结合心肌应变评估,可快速鉴别胸痛原因,准确判断梗死范围[15]。
综上所述,CMR-TT技术用于AMI后心肌应变评估,能够准确反映心肌受损程度,有利于识别心室重构,为临床诊治提供指导。

