氧化镧掺杂的双孔镍基催化剂甲烷干重整反应性能研究
吴兴亮,王毅婕,吕凌辉,张 静,范 辉,曾春阳,马清祥,赵天生
(1.宁夏大学 化学化工学院 省部共建煤炭高效利用与绿色化工国家重点实验室,宁夏 银川 750021;2.中国石油和化学工业联合会,北京 100723)
近年来温室效应导致全球气候变暖,环境问题日趋加剧,如何减少温室气体成为当前亟待解决的问题。甲烷干重整反应(DRM)可同时转化甲烷和二氧化碳两种温室气体,且转化产物为氢碳比接近于1的合成气,可作为制备二甲醚等碳氢化合物的原料[1]。这对缓解温室效应以及能源危机问题有巨大潜力,因此,DRM研究受到了广泛关注。目前,DRM的关键在于催化剂的开发,其中常用催化剂有Pt、Ru和Pd等贵金属催化剂[2-4],Ni、Co和Fe等非贵金属催化剂[5-7]以及Ni3C等碳化物催化剂[8-10]。镍基催化剂因其廉价易得、初始催化活性与贵金属催化剂相当并具有良好工业化应用前景而成为当前的研究热点[11]。
然而,镍基催化剂存在高温下易烧结、易因积炭而失活等问题,导致催化剂催化效果不佳。积炭反应主要包括甲烷裂解反应(反应式(1))与一氧化碳歧化反应(反应式(2)):

研究显示[12],积炭通常在两种情况下产生:(1)金属团簇尺寸大于临界尺寸;(2)载体呈酸性。因此,如果希望从根本上解决DRM反应的积炭问题,主要可从催化剂的设计和制备入手。对于催化剂的设计,研究人员一般从“堵”与“疏”两方面展开研究。“堵”即通过各种方式减少积炭的产生,如改变催化剂结构、制备小尺寸镍金属颗粒以及使用碱性助剂等[13-15];“疏”即通过引入适当反应转化催化剂表面生成的积炭[16-17]。
近年来,具有介孔结构的镍基催化剂因具有优异的比表面积和孔容、较好的金属颗粒分散性、良好的催化性能而被大量研究。同时,介孔结构的“限制效应”可抑制镍金属颗粒长大,从而提高催化剂的抗积炭能力。常用作介孔载体的物质有Al2O3[18-20]、SiO2[21-22]等,其中Al2O3因具有良好的热稳定性而被广泛应用。研究[23]表明,通过简单的一锅法制备的有序介孔Al2O3可在900 °C下保持稳定,且其孔径可调、比表面积较大。然而对于Ni-Al2O3催化体系,虽然其初始活性高,但催化剂表面存在的大量路易斯酸性位点容易形成积炭,影响催化剂稳定性。在具有中-大双孔结构的催化剂中,介孔可为催化剂提供大的比表面积及孔容,大孔有助于反应物及产物分子的扩散并增强催化剂的容碳能力[24-27],因此这类催化剂受到了研究者的广泛关注。本课题组在前期的工作中,采用一步法制备了中-大双孔Ni-Al2O3催化剂[28-29],催化剂表现出优异的抗积炭性能。
据报道,在催化剂中掺杂La2O3可增加其碱性[30]。YU等[31]指出,La2O3的引入不仅增加了催化剂的碱性和表面活性位点数目,还通过形成碳酸氧镧中间物种(La2O2CO3)消除了积炭,具体反应如下:(1)La2O3+CO2→La2O2CO3;(2)La2O2CO3+C→La2O3+2CO。VERYKIOS[32]以La2O3为载体负载镍基催化剂进行研究,通过同位素标记分子瞬态发现La2O3和La2O2CO3在反应条件下通过形成动态氧池参与消碳过程。徐军科等[13]制备了La2O3改性的Ni/Al2O3催化剂,研究表明,La2O3的加入可通过减小金属镍颗粒的尺寸抑制积炭成核,并产生更多活性Cα物种,使催化剂具备更好的活性和稳定性。综上所述,La2O3助剂的引入有以下作用:(1)中和部分酸性位点;(2)缩小催化剂中活性金属的粒径;(3)消除积炭提高催化剂的稳定性[33-34]。
为进一步优化镍基双孔催化剂的催化性能,本文针对碱性助剂La2O3的特点,通过一步法将其引入到双孔镍基催化剂中,结合La2O3与双孔结构的协同效应,考察La2O3掺杂及其含量对双孔镍基催化剂的活性、稳定性、结构以及抗积炭性能等的影响。
1 实验部分
1.1 实验试剂
六水合硝酸镍(Ni(NO3)2·6H2O)、无水乙醇(C2H5OH)购自天津市大茂化学试剂厂;浓硝酸(HNO3,质量分数为65%~68%)购自烟台市双双化工有限公司;六水合硝酸镧(La(NO3)3·6H2O)、异丙醇铝(C9H21AlO3)购自阿拉丁试剂有限公司;聚苯乙烯微球((C8H8)n)购自上海辉质生物科技有限公司;三嵌段共聚物P123(EO20PO70EO20)购自Sigma-Aldrich公司。
1.2 双孔镍基催化剂制备
双孔镍基催化剂通过一步法制备,具体步骤如下:称取1.0000 g P123、2.0424 g C9H21AlO3、0.2196 g Ni(NO3)2·6H2O和一定量的La(NO3)3·6H2O(n(La):n(Al) 分别为0%、1%、3%、5%和7%,以此表示La2O3含量)溶于20 mL无水乙醇中,搅拌一定时间后加入1.6 mL浓硝酸,将混合溶液继续搅拌5 h,随后加入适量的聚苯乙烯微球,继续搅拌使其均匀分布到溶液中。搅拌结束,将上述溶液置于60 °C烘箱干燥72 h后,移入马弗炉中于700 °C焙烧4 h。制得的双孔镍基催化剂记为M100-OM-8%Ni/Lax-Al(x=0、1、3、5和7)(M100表示模板为100 nm的大孔,OM表示有序介孔,镍的质量分数为8%)。
1.3 催化剂表征
催化剂物相结构由Bruker公司的D8 Advance X射线衍射仪测试分析。Cu靶Kα射线为辐射源,管电压、管电流分别为40 kV、40 mA。广角XRD扫描范围为3°~85°,扫描速率8 (°)/min,步长0.02°;小角XRD扫描范围为0.3°~5.0°,步 长0.01°。催化剂晶粒尺寸采用谢乐公式进行计算,具体为:D=Kλ/(βcosθ)(D为晶粒垂直于晶面方向的平均厚度,nm;K为Scherrer常数,0.89;λ为X射线波长,nm;β为衍射峰半高宽,rad;θ为衍射角,°)。
催化剂孔结构参数在北京精微高博JW-BK122F型分析仪上通过N2物理吸/脱附曲线分析得到。样品预处理在N2气氛、200 °C下进行,预处理结束后,液氮温度保持-197 °C测试吸/脱附曲线。比表面积及孔径分布分别由BET方法及BJH方法计算得到。
TG测试在法国Setaram公司的综合热分析仪(SETSYS16)上进行。在N2气氛100 °C下恒温处理0.5 h以清除杂质气体和催化剂表面水分,随后切换至空气气氛将样品以10 °C/min的升温速率从100 °C加热至800 °C,记录曲线。
TPH测试在美国Micromeritics公司全自动程序升温化学吸附仪(AutoChem II 2920)上进行。测试条件为,称取40 mg反应后样品装管,以10 °C/min的升温速率从室温升至150 °C;通入He吹扫1 h除去杂质,气体流速为30 mL/min;随后切换至10%H2/Ar,以30 mL/min的流速吹扫直至基线稳定;将温度升至900 °C,记录曲线。
Raman在法国Horiba公司的高分辨率显微拉曼光谱仪(DXR)上进行,首先将拉曼光谱仪预热30 min,在硅晶片校准后,将研磨后的样品在波长532 nm下进行测试。
H2-TPR采用美国Micromeritics公司的全自动程序升温化学吸附仪(AutoChem II 2920)进行测试。测试条件如下:样品(焙烧后)用量为50 mg,以与TPH相同的升温速率将样品从室温升到350 °C,用He以30 mL/min的流速吹扫1 h;待温度降至50 °C,将气体切换至10%H2/Ar,以30 mL/min的流速吹扫至基线稳定,将温度升至900 °C,记录氢气的消耗量曲线。
样品表面元素化合价态及结合能采用美国Thermo Fisher Scientific公司的X射线光电子能谱仪(Thermo ESCALAB 250XI)进行测量。样品用量为10 mg,采用Al Kα为X光源,在真空环境下进行测试。
通过透射电镜对样品的形貌进行表征,采用美国FEI公司的TECNAI G2 F20型透射电镜以200 kV的加速电压进行测试。
1.4 催化剂性能测试
双孔镍基催化剂活性测试在固定床反应器上进行,选用内径为6 mm的石英管作为反应器。将0.1 g催化剂与0.3 g石英砂混合均匀后装入石英反应管的中间段,催化剂两端分别装填适量的石英棉。石英管中部放置热电偶用于监测催化剂的反应温度。首先将Ar通入反应器进行气密性检验,随后以5 °C/min的升温速率将温度升至还原温度700 °C,此时通入还原气(5%H2/95%N2)以40 mL/min的流速还原2 h,最后通入反应气(n(CH4):n(CO2):n(Ar) =45:45:10)。反应条件为:反应温度700 °C,反应时间为80 h,接触时间W/F(W为催化剂质量,g;F为反应气流速,mol/h)为1 g/(mol/h)。
反应产生的尾气经过冷凝除水后进入GC-9560色谱进行在线分析,根据反应物及产物的峰面积进行转化率等的计算。CH4、CO2转化率(XCO2、XCH4)和n(H2)/n(CO)由式(3)~式(5)计算得到。
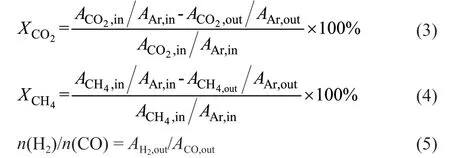
式中,Ai为i组分的色谱峰面积,μV·s;Ain为进气色谱峰面积,μV·s;Aout为出气色谱峰面积,μV·s。
2 结果与讨论
2.1 催化剂的性能
图1和表1为不同La2O3掺杂量的双孔镍基催化剂对DRM的催化活性及稳定性评价数据。80 h活性评价内,未掺杂La2O3催化剂的稳定性较差,甲烷转化率由75.4%降为52.3%,二氧化碳转化率由83.8%降为67.0%。与未掺杂La2O3催化剂相比,掺杂La2O3的催化剂稳定性显著增强。综合来看,催化剂M100-OM-8%Ni/La3-Al的活性及稳定性最好,80 h后反应物转化率与初始转化率相差不超过1%,n(H2)/n(CO)基本不变;而当n(La):n(Al) >5%时催化剂的稳定性较前者有所下降,催化剂M100-OM-8%Ni/La7-Al的CH4转化率由78.8%降为73.2%,CO2转化率由82.7%降为81.8%。表明适量La2O3的引入可提升催化剂的稳定性,使之在较长反应时间内保持较高催化活性。过量La2O3的加入可能导致了强碱性位点的产生,吸附了更多的CO2使金属镍颗粒被氧化,进而降低催化剂的活性[35]。因此经过长时间反应后n(La):n(Al) >5%时的催化剂活性较催化剂M100-OM-8%Ni/La3-Al有所降低。
图1及表1还显示所有样品的CO2转化率均高于CH4转化率,且n(H2)/n(CO)均小于1,主要是由于逆水煤气变换反应(RWGS,CO2+H2=CO+H2O)消耗了部分CO2和H2,同时产生了较多CO[36]。

图1 双孔镍基催化剂的稳定性Fig.1 Stability of Ni-based catalysts with bimodal porous structure
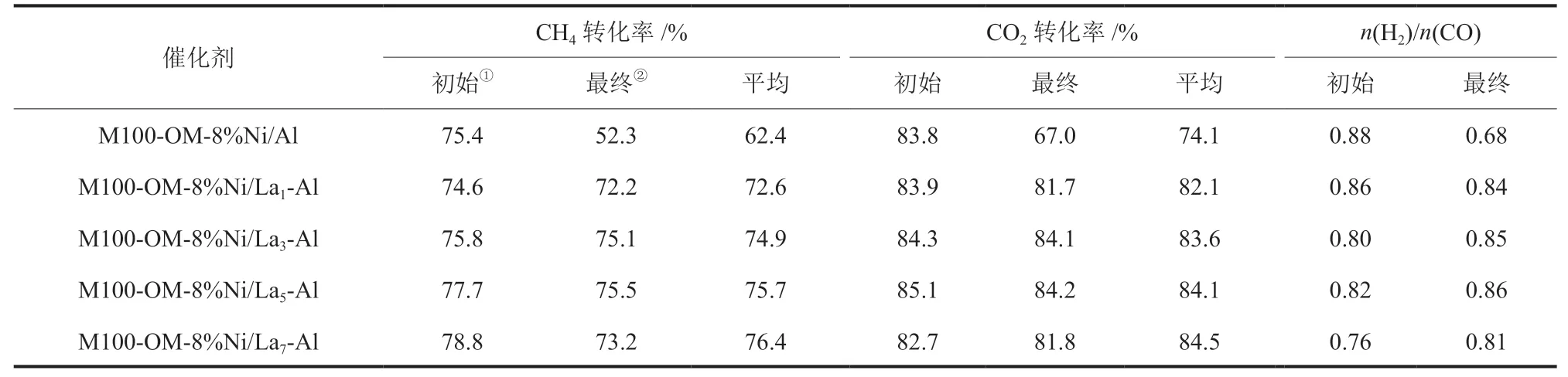
表1 双孔镍基催化剂的DRM催化活性Table 1 Catalytic activity of Ni-based catalysts with bimodal porous structure in DRM reaction
2.2 催化剂的表征
2.2.1 BET分析
为探究不同含量La2O3掺杂双孔镍基催化剂的结构及比表面积对催化活性的影响,对催化剂进行了N2物理吸/脱附表征。图2(a)显示,当n(La):n(Al) ≤ 3% 时,催化剂均呈现IV型吸附等温线且具有H1型回滞环,说明存在圆柱型介孔结构。当n(La):n(Al) > 3%时,催化剂仍为IV型吸附等温线但回滞环呈H3型,表明合成的掺La2O3双孔镍基催化剂呈狭缝形孔或其金属颗粒呈板状,说明催化剂的孔道结构因La2O3含量的增多产生了变化[37]。所有样品在p/p0>0.9时,等温线呈上升趋势,此为大孔的毛细凝聚现象所致,说明样品均具有大孔结构[38-39]。通过孔径分布图(图2(b))可清晰地观察到所有催化剂均具有大孔和介孔结构,其中大孔孔径约70 nm,介孔结构在10 nm左右。当n(La):n(Al) >3%时,催化剂介孔及大孔的衍射峰强度大幅度减弱,说明La2O3含量过高时催化剂的孔结构有所坍塌。因此推断La2O3过量时催化剂稳定性有所降低与过量La2O3破坏了催化剂的孔道结构有关。

图2 双孔镍基催化剂的N2物理吸/脱附曲线(a)及孔径分布(b)Fig.2 N2adsorption/desorption isotherms (a) and pore size distributions (b) of Ni-based catalysts with bimodal porous structure
表2为系列La2O3掺杂双孔镍基催化剂的结构特性参数,可以看出当n(La):n(Al) >3%时,随着La2O3含量增加,催化剂的比表面积及孔体积降低,这可能与La2O3的比表面积低、热稳定性差有关[40]。因此,比表面积与孔体积的减小导致活性组分不能良好分散是造成催化剂催化活性下降的原因之一。

表2 双孔镍基催化剂的结构特性参数Table 2 Structural characteristic parameters of Ni-based catalysts with bimodal porous structure
2.2.2 XRD分析
为进一步探究催化剂晶相结构与性能之间的关系,通过X射线衍射分析对催化剂进行表征(图3)。结果显示,La2O3改性双孔镍基催化剂的广角XRD谱图(图略)中所有催化剂均无衍射峰存在,说明一步法制备的催化剂镍物种、镧物种在催化剂中高度分散。小角XRD谱图显示,样品在2θ为0.7°~0.9°出现衍射峰,此为γ-Al2O3的(100)晶面,表明催化剂成功制得二维六方p6mm有序介孔结构[41]。其中催化剂M100-OM-8%Ni/La3-Al的衍射峰强度最明显,说明该催化剂的孔结构最有序。但当La2O3含量继续增多时,衍射峰的强度开始降低,当n(La):n(Al) ≥5%时,衍射峰极不明显,说明过量的La2O3会破坏样品的有序介孔结构,这与N2物理吸/脱附曲线分析得到的结果一致。图3(b)为还原后的XRD谱图,所有催化剂均出现了Ni、Al2O3的衍射峰,且均未检测到La2O3的衍射峰,说明La2O3高度分散到催化剂骨架结构中。与未掺杂La2O3催化剂相比,掺杂La2O3催化剂的衍射峰强度明显减弱,说明引入La2O3对催化剂的物相结构有影响。
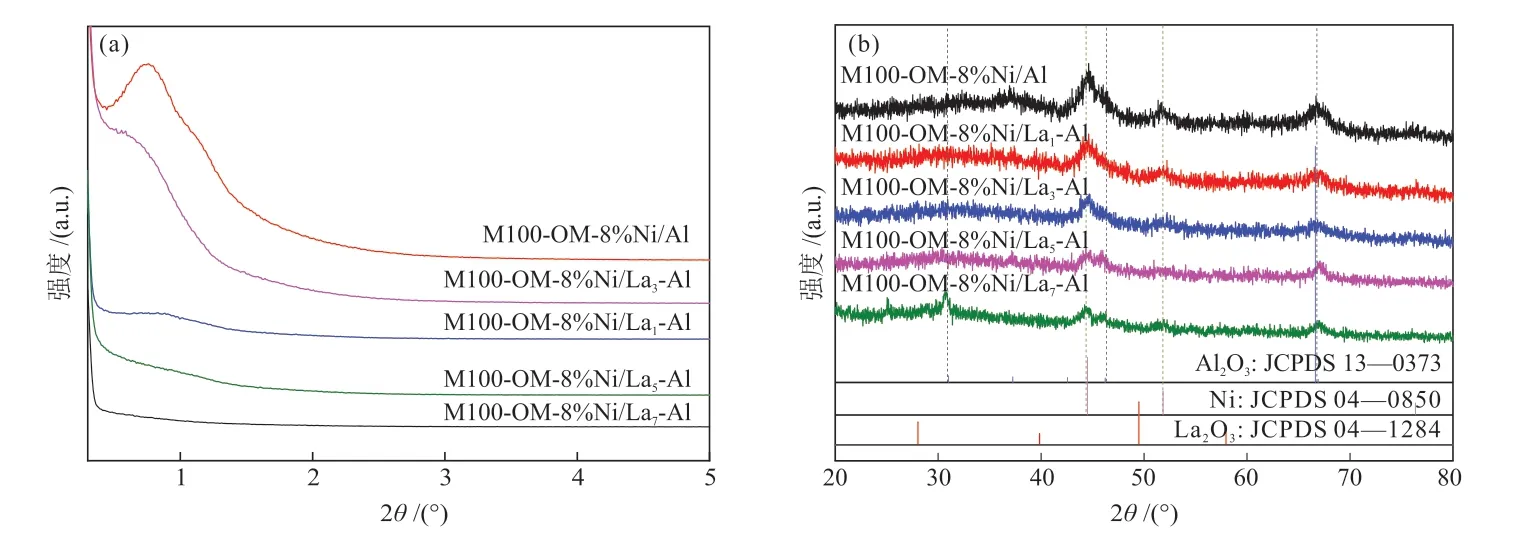
图3 双孔镍基小角XRD谱图(a)及其还原后的XRD谱图(b)Fig.3 Small-angle XRD patterns of Ni-based catalysts with bimodal porous structure (a) and XRD patterns of these after reduction (b)
2.2.3 TEM分析
通过透射电镜分析了双孔镍基催化剂的形貌。由图4可知,当La2O3含量较低时,催化剂具有高度有序的圆柱型孔。随着La2O3含量的增加,催化剂的孔道结构产生明显变化,有序度降低,说明La2O3含量增多,中孔孔道结构遭到严重破坏。这与N2物理吸/脱附曲线、小角XRD表征结果一致,说明加入过量La2O3会破坏催化剂孔道结构的完整性,导致催化剂在长时间反应后催化活性下降。

图4 双孔镍基催化剂的TEM照片Fig.4 TEM images of Ni-based catalysts with bimodal porous structure
2.2.4 H2-TPR分析
对双孔镍基催化剂进行了H2-TPR表征,由图5可知,与未掺杂La2O3催化剂相比,掺杂La2O3催化剂的还原温度随着La2O3含量增加而降低,这表明La2O3的掺杂增强了催化剂的还原性[42]。当n(La):n(Al) ≥3%时,在400~500 °C出现了一个微弱的还原峰,这归属于少量纯氧化镍的还原,600~700 °C 的还原峰表明金属与载体间存在较强的相互作用[43];当n(La):n(Al) ≥5%时,催化剂在800 °C左右出现了还原峰,可能为La-Ni六铝酸盐的还原特征峰[44]。这说明,加入La2O3可增强催化剂还原性,同时金属与载体间有较强的相互作用。

图5 双孔镍基催化剂的H2-TPR谱图Fig.5 H2-TPR spectra of Ni-based catalysts with bimodal porous structure
2.2.5 XPS分析
通过XPS对掺杂La2O3的双孔镍基催化剂进行表面化学组成及变化情况分析。图6显示,所有催化剂的Ni 2p特征峰出现在相似位置,且由表3可以看出各掺杂La2O3催化剂元素的结合能相差不大,说明掺杂La2O3后对样品的电子环境没有影响。另外根据XPS谱图的特征峰位置,结合能在853 eV左右为NiO特征峰[42],说明当n(La):n(Al) ≥3%时催化剂表面存在NiO。Ni 2p3/2的特征峰在855 eV左右出现且在862 eV左右伴随卫星震激峰,同时在 873 eV附近出现Ni 2p1/2的特征峰,这说明所有催化剂均存在与载体有强相互作用的Ni2+物质[45-46]。大量研究[47-48]也表明,在Ni/Al2O3催化体系中,氧化镍物种极易与载体产生强相互作用。

图6 双孔镍基催化剂的XPS谱图Fig.6 XPS spectra of Ni-based catalysts with bimodal porous structure
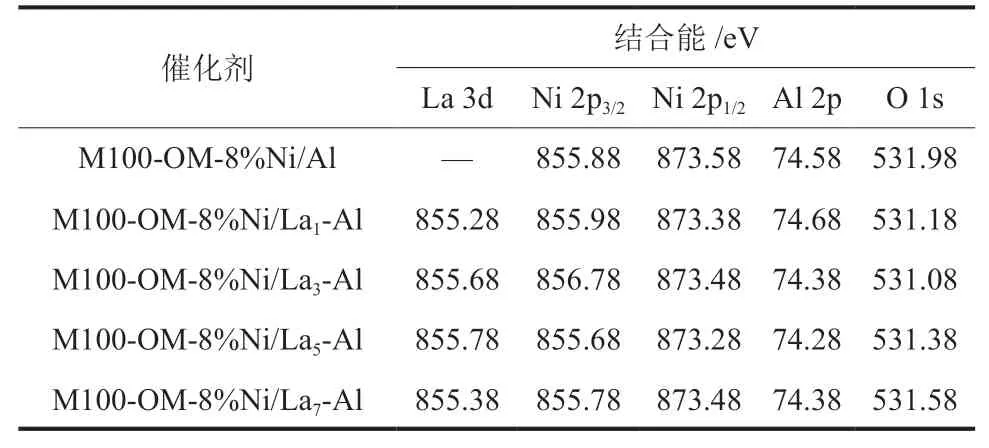
表3 双孔镍基催化剂的表面元素结合能Table 3 Binding energy of surface elements of Ni-based catalysts with bimodal porous structure
2.3 催化剂积炭分析
2.3.1 广角XRD分析
通过广角XRD谱图探究反应后双孔镍基催化剂的物相变化,图7中2θ为44.5°、51.8°和76.4°均为金属镍的衍射峰,2θ为37.3°、46.3°和67.0°均为Al2O3的衍射峰,与反应前催化剂相比无明显变化。但所有样品在反应后均未出现石墨碳的峰,这可能是因为催化剂积炭多为无定型碳或积炭量较少未达到仪器最低检测限。
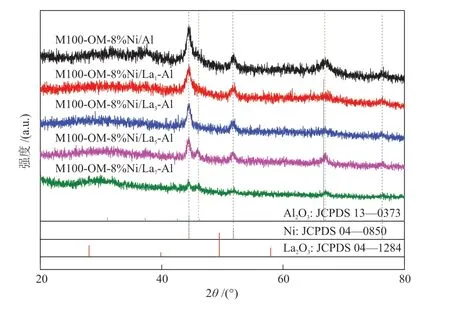
图7 反应后双孔镍基催化剂的广角XRD谱图Fig.7 Wide-angle XRD patterns of Ni-based catalysts with bimodal porous structure after reaction
2.3.2 TEM分析
为进一步探究双孔镍基催化剂积炭情况,通过透射电子显微镜对反应后催化剂表面进行了观察。由图8可知,未掺杂La2O3的催化剂表面有碳纳米管存在。掺杂La2O3后,当n(La):n(Al) <3%时,未观察到碳纳米管的存在;随着La2O3含量的增加,碳纳米管逐渐增多,当n(La):n(Al) =7%时,催化剂表面出现了大量碳纳米管,表明过量La2O3的加入导致催化剂产生更多积炭,催化剂孔道被堵塞,催化剂活性下降。

图8 反应后双孔镍基催化剂的TEM照片Fig.8 TEM images of Ni-based catalysts with bimodal porous structure after after reaction
2.3.3 热重分析
为得到反应后双孔镍基催化剂的积炭量,对催化剂进行了热重分析。结果显示,所有样品均在300 °C之前出现明显的失重,此为无定型碳的氧化;在300~500 °C之间,样品呈轻微的增重趋势,此为金属镍的氧化[49];温度在500 °C以上,样品表现出的失重为石墨碳的氧化[50];在温度高于600 °C后,M100-OM-8%Ni/La5-Al和M100-OM-8%Ni/La7-Al催化剂的质量呈上升趋势,可能为催化剂中La2O3与气氛中的二氧化碳作用生成了La2O2CO3[32],从而增加了样品质量。由图9可知,催化剂M100-OM-8%Ni/La1-Al和M100-OM-8%Ni/La3-Al在温度低于300 °C及高于500 °C时出现的失重均低于样品M100-OM-8%Ni/Al。通过计算可知,催化剂M100-OM-8%Ni/Al、M100-OM-8%Ni/La1-Al和M100-OM-8%Ni/La3-Al的失重总量分别为4.44%、2.61%和3.11%,说明掺杂适量La2O3后催化剂的抗积炭性能增强,而过量La2O3的添加易造成金属镍的氧化,导致催化剂催化活性下降。
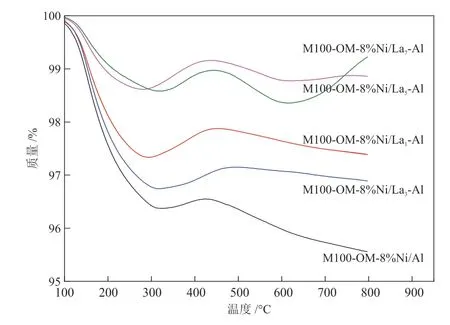
图9 反应后双孔镍基催化剂的TG曲线Fig.9 TG curves of Ni-based catalysts with bimodal porous structure after after reaction
2.3.4 TPH分析
为测定样品的积炭类型,对反应后所有样品进行了TPH表征。由图10可知,催化剂M100-OM-8%Ni/Al在200~300 °C、400~500 °C和 高 于500 °C3个 温度段均出现耗氢峰,分别对应无定型碳、层状碳及石墨碳的氢化[51]。不同含量的La2O3掺杂后对催化剂的积炭类型有很大影响。当n(La):n(Al) ≤3%时,耗氢峰主要集中在200~300 °C,在温度高于300 °C时未出现明显的耗氢峰,说明反应后催化剂的积炭类型主要为无定型碳;当n(La):n(Al) >3%时,催化剂在温度高于300 °C时出现了耗氢峰,其中催化剂M100-OM-8%Ni/La5-Al在500~700 °C之间出现了明显的耗氢峰,此峰归属于石墨碳的氢化;催化剂M100-OM-8%Ni/La7-Al在高于800 °C时出现了耗氢峰,说明存在大量石墨碳,这与TEM表征结果一致。总之,掺杂适量La2O3可有效抑制积炭,而掺杂过量时,催化剂会产生更多较难被还原或氧化消除的石墨碳。
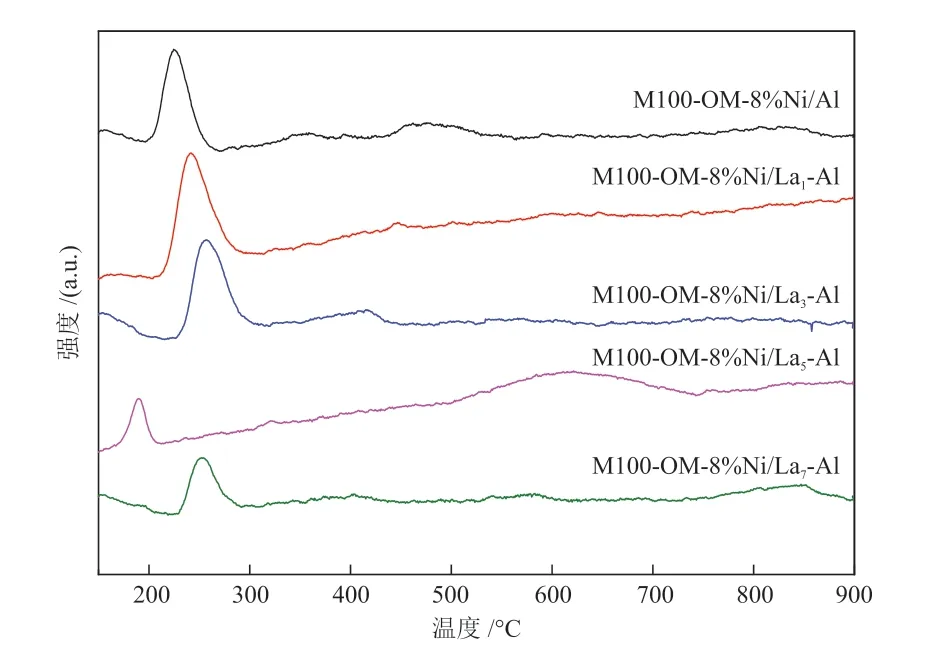
图10 反应后双孔镍基催化剂的TPH谱图Fig.10 TPH spectra of Ni-based catalysts with bimodal porous structure after after reaction
2.3.5 Raman分析
由图11可知,所有催化剂在波数为1300 cm-1、1580 cm-1附近均出现衍射峰。

图11 反应后双孔镍基催化剂的Raman谱图Fig.11 Raman spectra of the Ni-based catalysts with bimodal porous structure after after reaction
通过比较峰强度可知,M100-OM-8%Ni/Al、M100-OM-8%Ni/La1-Al、M100-OM-8%Ni/La3-Al、M100-OM-8%Ni/La5-Al和M100-OM-8%Ni/La7-Al的R值分别为1.09、0.91、1.15、1.07和1.33,可知当n(La):n(Al) ≤5%时,M100-OM-8%Ni/La3-Al的R值最大,该催化剂的积炭无序程度最大。可观察到当M100-OM-8%Ni/La1-Al、M100-OM-8%Ni/La3-Al的衍射峰强度最低,说明这两种催化剂的积炭量较少。而催化剂M100-OM-8%Ni/La7-Al的R值为1.33,说明积炭的无序度较高,但该样品的D峰与G峰峰强度最强,说明该样品的积炭量最多。与TPH表征结果一致,Raman分析结果也表明适当La2O3的掺杂导致生成的积炭更加无序、更易在反应过程中被消除,因此有更好的催化活性及稳定性。
3 结论
以La2O3为助剂,采用一步法制备了一系列不同n(La):n(Al)(0%、1%、3%、5%、7%)La2O3掺 杂的双孔镍基催化剂,对催化剂催化性能、构效关系以及积炭情况进行了研究,得到如下主要结论。
(1)催化剂80 h活性评价中,当n(La):n(Al) <5%时,催化剂的稳定性明显增强,其中催化剂M100-OM-8%Ni/La3-Al的活性及稳定性最好;而过量La2O3的掺杂会导致催化剂的稳定性下降。
(2)具有良好双孔孔道结构的催化剂与碱性助剂La2O3的协同作用,使催化剂表现出优异的催化活性与稳定性。当n(La):n(Al) ≤3%时,催化剂的孔道结构保持良好;当n(La):n(Al) >3%时,催化剂的孔结构被严重破坏,比表面积和孔容急剧降低。
(3)当n(La):n(Al) ≤3%时,La2O3掺杂的双孔镍基催化剂的积炭明显减少,且积炭无序程度大,多为无定形碳;而当n(La):n(Al) >3%时,La2O3掺杂的催化剂积炭增多且难以消除。

