恩替卡韦联合阿德福韦酯与泰诺福韦酯单药在急性加重期肝炎患者中的应用分析
王冰(江西省鹰潭市人民医院,江西 鹰潭 335000)
乙型肝炎是一种具有挑战性的疾病,通过抑制病毒复制或消除病毒可以防止肝损伤、纤维化和癌症的进展[1-3]。阿德福韦酯(ADV)等长期抗病毒治疗选择的耐药HBV突变体降低了临床治疗的疗效[4]。与其他核苷类似物相比,阿德福韦酯(ADV)同样有效,且耐药率相对较低,无交叉耐药。第二代核苷类似物,如恩替卡韦(ETV)和泰诺福韦酯(TDF),具有很高的遗传屏障,具有很强的抗HBV效应,并且仍然保持很低的耐药率[5]。在目前的实践指南中,TDF和ETV被推荐用于肝炎的一线治疗,尤其是对病毒突变有耐药性的患者。ETV加ADV联合疗法和TDF单一疗法与新型抗病毒药物的联合使用是防止因病毒复杂性而产生多重耐药性的两种潜在选择。ETV+ADV联合疗法和TDF单一疗法都能有效抑制慢性乙型肝炎病毒[6]。本研究旨在分析ETV联合ADV与TDF单药在急性加重期肝炎患者中的应用价值。
1 资料与方法
1.1 临床资料 本研究包括2015年1月-2016年12月在我院就诊的100例肝炎患者,其血清HBV DNA水平(≥1.0×103国际单位/毫升)。这些患者血清呈乙型肝炎e抗原阳性(HBeAg),丙氨酸氨基转移酶(ALT)水平比正常水平高2倍(UNL)。患有甲、丙肝炎病毒或艾滋病病毒混合感染的患者都被排除在本研究之外。同样,肝细胞癌或糖尿病患者也被排除在外。此外,肝硬化患者不包括在内,这些患者是根据病史、检查、肝硬化的放射学体征确诊的。所有参与本研究的患者都已知情同意本研究内容,并了解常规程序。
1.2 研究设计 患者被随机分配到单一治疗组(48名患者)或联合治疗组(52名患者)。比较两组之间的基线数据,以确保可比性。所有患者在接受抗病毒治疗前都获得了详细的研究信息并对研究知情同意。联合治疗组的患者接受ETV和ADV治疗(分别为每天0.5mg和10mg),而单一治疗组接受TDF治疗(每天300mg)。
1.3 观察和跟踪 分别在治疗开始时和第12、24、36、48、60、72、84和96周之后的周末对各组进行随访,以测试生化功能、HBV血清标记物、HBV DNA负荷,并进行肝脏超声检查。使用实时荧光聚合酶链反应检测HBV DNA水平。本研究使用的DNA检测下限为1000IU/mL。HBV DNA>1000国际单位/毫升被认为显示HBV阳性。
1.4 统计分析 采用SPSS16.0(芝加哥,SPSS Inc.)软件用于数据分析。测量值以平均标准偏差的形式表示,并使用t检验进行比较。比例以百分比(%)表示,比率比较采用卡方检验。
2 结果
2.1 基线特征 表1显示了治疗开始时临床和实验室特征的基线。100名患者被纳入ETV+ADV联合治疗组(n=52)或TDF单一治疗组(n=48)。在联合治疗组中,41名患者为男性(41/52),平均年龄为(51.33±11.36)岁(范围:22-54岁)。TDF单一疗法组36名患者为男性(36/48),平均年龄为(54.27±10.55)岁(范围:21-55岁)。HBV DNA分别是(8.17±1.63)、(8.07±1.67)。两组之间的基线特征没有显著差异。
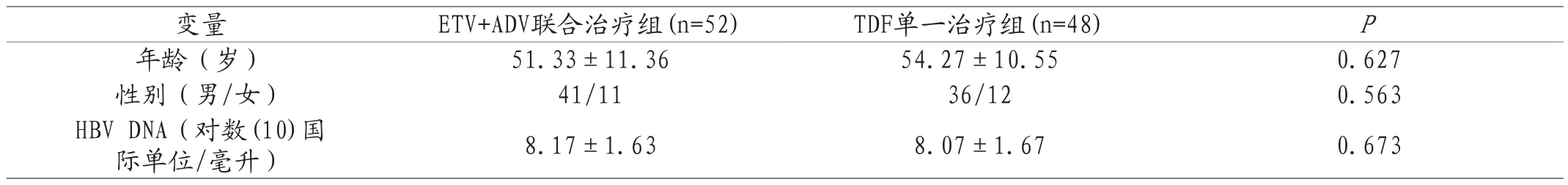
表1 患者的基线特征
2.2 病毒学效应 在基线和第12、24、36、48、72和96周检测ETV+ADV联合治疗组和TDF单一治疗组的血清HBV DNA水平。在ETV+ADV组联合治疗组的52名患者中,分别有40名和48名患者在第48周和第96周达到检测不到的HBV DNA水平(HBV DNA<1000国际单位/毫升)。相应的病毒学应答分别为76.9%和92.3%。在TDF单一治疗组的48名患者中,分别有39名和46名患者在第48周和第96周达到了检测不到的HBV DNA水平。其相应的病毒学应答分别为81.3%和95.8%。两组之间未发现统计学显著差异(第48周和第96周的P值分别为0.631和0.679)(见表2)。
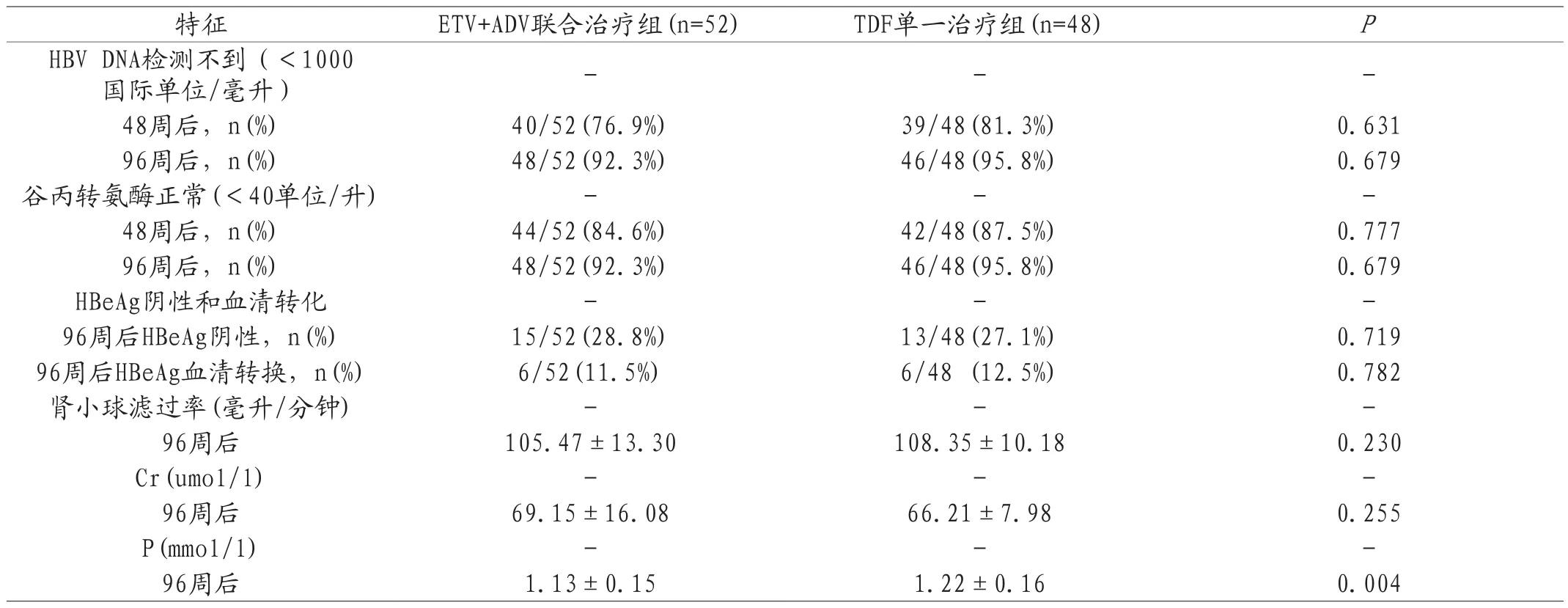
表2 全部患者的病毒学和生化反应及不良事件
2.3 生化反应 在52名接受ETV联合ADV综合治疗的患者中,44名和48名患者分别在第48周和第96周达到谷丙转氨酶正常化(谷丙转氨酶<40国际单位/升)。相应的生化反应率分别为84.6%和92.3%。在接受TDF单一治疗的48名患者中,分别有42名和46名患者在第48周和第96周达到谷丙转氨酶正常。单一治疗组的相应生化反应率分别为87.5%和95.8%(见表2)。这些差异没有统计学意义(第48周和第96周P值分别为0.777和0.679)(见表2)。
2.4 血清学反应 在基线时HBeAg阳性的100名患者中,ETV+ADV联合治疗组有15例[15/52(28.8%)],TDF单一治疗组有13例[13/48(27.1%)]在第96周时抗原呈阴性。ETV+ADV联合治疗组和TDF单一治疗组的HBeAg血清转换率分别为11.5%(6/52)和12.5%(6/48)。HBeAg阴性和血清转化之间没有统计学差异(第96周P值分别为0.719和0.782)(见表2)。
2.5 病毒学突破与耐药性 本文检测了5例患者(ETV+ADV联合治疗组4例;TDF单一治疗组1例),96周后未达到检测不到的HBV DNA水平。没有检测到额外的抗性替代。
2.6 不良事件 在这项研究中,共有100名患者在应用纳入和排除标准后被纳入。所有患者均完成治疗和随访。到第96周,ETV+ADV联合治疗组的不良事件包括:2名患者的肾小球滤过率低于90ml/min(分别为67.25ml/min和77.61ml/min);1例患者肌酐水平为142μmol/L,高于UNL值;血清磷酸盐为0.65mmol/L,低于正常下限。这2名患者没有身体症状或其他明显的主诉。治疗96周后,ETV+ADV联合治疗组和TDF单一治疗组之间的血清磷水平[(1.13±0.15)mmol/L VS(1.22±0.16)mmol/L,P=0.004]存在统计学显著差异(见表2)。
3 讨论
以前已经就抗病毒治疗对肝炎患者的益处达成共识,预防HBV抗病毒药物对核苷酸类似物的耐药性,并在出现耐药性时进行适当的管理,已成为慢性乙型肝炎管理的主要重点[7-9]。本研究表明,两种不同的治疗策略,ETV+ADV联合治疗和TDF单药治疗,是治疗中国慢性乙型肝炎HBeAg阳性的ADV耐药患者的有效方法。在这两种策略中,大多数患者表现出有效的病毒抑制,并且没有出现额外的可检测的HBV抗性突变。在完成96周的治疗后,分别在ETV+ADV联合治疗组和TDF单一治疗组中,4名患者和2名患者的HBV DNA水平未达到不可检测的水平(<1000国际单位/毫升)。相应的病毒学应答分别为92.3%和95.8%,两组之间没有统计学显著差异。在ETV+ADV联合治疗组中,尽管4名患者未达到HBV DNA的检测水平,但2名患者仍显示谷丙转氨酶正常。在TDF单一疗法组中,2名未达到检测不到的HBV DNA水平的患者中的1名也显示谷丙转氨酶水平正常。治疗96周后,分别有4名和1名患者在ETV+ADV联合治疗组和TDF单一治疗组中未出现谷丙转氨酶正常化(谷丙转氨酶<40国际单位/升)。然而,在4名未达到谷丙转氨酶正常化的患者中,有2名患者的HBV DNA水平检测不到。2例血脂轻度升高的患者也经B超诊断为脂肪肝。脂肪肝可能是2名患者未达到谷丙转氨酶正常化的一个促成因素。在这项研究中,尽管大多数患者获得并维持了病毒学应答,但在ETV+ADV联合治疗组和TDF单一治疗组中,96周时HBeAg血清转换率分别为11.5%和12.5%。在第96周,总的HBeAg血清转换率仅为12%,这与以前治疗初治慢性乙型肝炎患者的报告形成鲜明对比[10]。这一发现表明宿主免疫因素在实现血清学反应中的影响,并表明在耐药HBV变异体患者中进一步治疗是不可避免的[11-13]。
综上所述,本文结果表明ETV+ADV联合治疗和TDF单一治疗对中国ADV耐药HBV突变型慢性乙型肝炎患者都是有效的治疗方法。此外,病毒学突破率很低,没有出现额外的耐药突变。然而,直到第96周,HBeAg血清转换率非常低,这表明有必要对这些患者进行持续治疗以维持病毒抑制。此外,长期ETV+ADV联合治疗可导致肾功能损害和次磷酸盐。在目前的研究中,观察时间太短,需要通过长期观察进行进一步研究,以获得可靠的数据。笔者建议定期监测血清磷酸盐和血清肌酐水平,并评估ADV治疗患者的肾小球滤过率。如果诊断为肾小球滤过率降低或低磷血症,应减少ADV剂量或用替代抗病毒剂替代。

