基于网络药理学和分子对接探讨理气枳壳改善非酒精性脂肪性肝病作用机制
郑 慧 王思为 蓝 天 楼丽君 张 峰
非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD)是指除过量饮酒和其他明确肝损害因素导致的肝内脂肪过度沉积,与2 型糖尿病、肥胖、代谢综合征、心血管疾病等多种代谢异常疾病密切相关[1]。中医认为,NAFLD 主要以肝郁脾虚证和湿热蕴结证为主,属于“肝着”“积聚”“肥气”等范畴[2],治疗原则上主要以疏肝、健脾、理气、化痰、活血为主[3]。枳壳,归肝、胃、脾经,具有理气宽中、行滞消胀的功效,经常被用于中医临床治疗脂肪性肝病[4]。本课题组前期对枳壳替代药材—衢枳壳防治代谢性疾病进行了研究,证实衢枳壳提取物具有稳定血糖[5]、抑制肥胖[6]、抗肝纤维化[7]、抗氧化[8]、抗炎[9]等作用,且能够显著抑制高脂饮食诱导的肥胖小鼠肝脏脂质积累[6],提示衢枳壳可能具有改善NAFLD 的作用,但作用机制尚需进一步研究。本研究基于网络药理学方法,预测枳壳改善NAFLD 的潜在靶点和作用机制,为后续实验研究提供依据。
1 材料与方法
1.1 枳壳相关靶点筛选 通过中医药系统药理学数据库(TCMSP)检索枳壳活性成分及其靶点,根据口服生物利用度(oral bioavailability,OB)≥30%且类药性(drug-likeness,DL)≥0.18 的属性值对活性成分进行初步筛选,并根据课题组前期对枳壳成分的分析以及既往文献研究证实枳壳存在的主要成分,将有关化合物纳入研究中,获得候选化合物。再通过TCMSP 数据库查找到有效成分的靶点,通过Uniprot蛋白质数据库(https://www.uniprot.org)将收集到的蛋白质靶点信息校正为标准基因名称。若TCMSP 数据库无法查找到有效成分的靶点,则以Probability>0为条件通过Swiss Target Prediction 数据库对该成分进行靶点预测,将两者汇总后删除重复值得到该药物靶标。
1.2 NAFLD 相关靶点筛选 以“non-alcoholic fatty liver disease”为关键词,在GeneCards 数据库(https://www.genecards.org)、DisGenet 数据库、OMIM 数据库(http://www.omim.org)、TTD数据库(http://bidd.nus.edu.sg/group/cjttd)等疾病基因数据库检索与筛选NAFLD 的潜在靶点。在Genecards 数据库中,Score值越高则代表该靶点与疾病联系密切,若靶点过多则设定Score 大于中位数的目标靶点为非酒精性脂肪肝的潜在靶点;在DisGenet 数据库中,根据该数据库推荐标准,以综合评分分值≥0.3 为条件,筛选相关靶点,最后将所有疾病数据库得到的靶点汇总后排除重复值,从而得到NAFLD 靶点。
1.3 枳壳-有效成分-靶点网络构建与关键成分筛选 将枳壳有效成分及靶点通过CytoScape3.7.2 构建有效成分-靶点网络,通过其内置的Network Analyzer 分析其网络拓扑学参数。根据degree 值大小来筛选关键成分,degree 值越大,说明该成分越重要,越有可能是枳壳治疗NAFLD 的主要活性成分。
1.4 枳壳有效成分-NAFLD 靶点PPI 网络构建与核心网络筛选 为了明确枳壳治疗NAFLD 的潜在靶标间的相互作用,利用STRING 11.0 数据库(https://string-db.org),构建蛋白互作(PPI)网络模型。将生物种类设定为“Homo sapiens”,最小互相作用阈值设定为“highest confidence”(>0.4),其余设置均为默认设置,得到PPI 网络,然后将获取的PPI 网络图通过CytoScape 3.7.2 软件中内置的Network Analyzer 提取枳壳治疗非酒精性脂肪肝核心网络。
1.5 枳壳有效成分-NAFLD 靶点功能与通路的富集分析 运用Metascape 平台(http://metascape.org/gp/index.html)对靶点进行通路富集分析。将枳壳治疗NAFLD 的潜在靶点录入Metascape 平台进行GO 和KEGG 分析。
1.6 活性成分-靶点分子对接验证 通过PPI 核心网络筛选获得核心靶点,根据Degree 值选取排名前6 的靶点,然后选取对应的活性成分,利用分子对接软件AutoDock Vina1.5.6 验证预测的枳壳活性成分和关键靶点的可信度。首先通过PubChem 数据库下载活性成分的2D 结构,使用Chem3D 软件将2D 结构转换为3D 结构,然后从PDB 数据库中下载核心靶点的晶体结构,运用Pymlol 软件删除晶体结构中的水分和配体,用蛋白受体与活性配体成分进行AutoDock Vina1.5.6 对接,最后,比较结合自由能。
2 结果与分析
2.1 枳壳活性成分靶点获取 通过TCMSP 数据库查找到衢枳壳17 个活性成分,再根据OB 和DL 参数筛选后获得5 种化合物,然后根据课题组前期对枳壳成分的研究以及相关文献的进一步检索,其中naringin、hesperidin、L-Limonen、neohesperidin 的OB或DL 较小,但在枳壳中含量丰富,依然列入候选化合物,最终纳入9 个活性成分进行研究,见表1。通过TCMSP 数据库查找到8 个有效成分的靶点,共计96个,其中MOL013383 成分靶点未在TCMSP 中找到,以Probability>0 为条件在Swiss Target Prediction 平台对该成分进行靶点预测,补充获得26 个靶点。汇总两个数据库的成分靶点,排除重复值后得到衢枳壳有效成分119 个靶点。
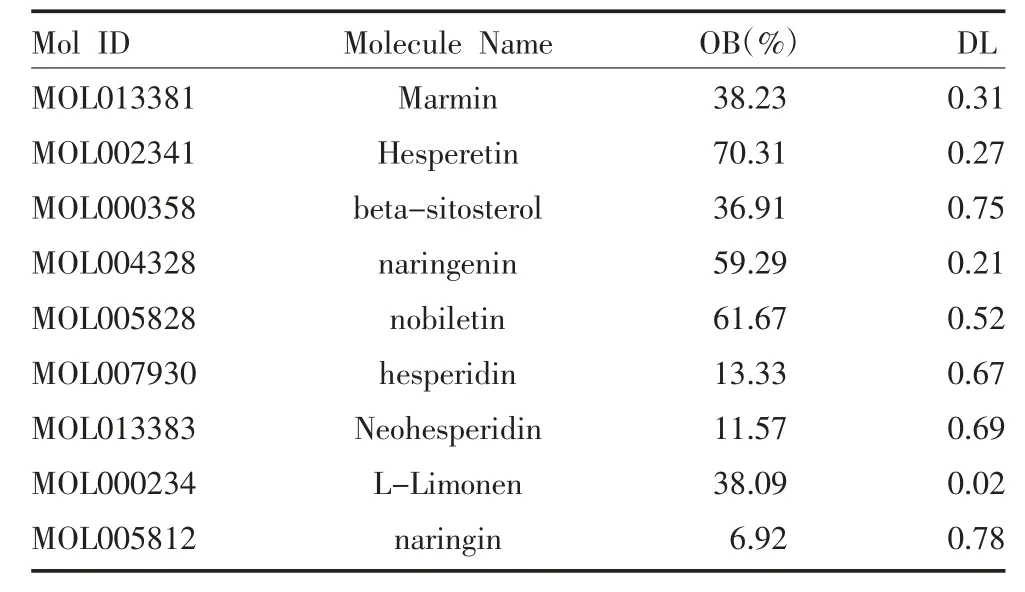
表1 枳壳中经筛选得到的候选化合物
2.2 NAFLD 相关靶点的获取 从Genecards 数据库、OMIM 数据库、DisGenet 数据库、TTD 数据库中分别获得NAFLD 靶点为1612 个、512 个、1059 个、4个。在Genecards 数据库中,根据经验设定Score 大于中位数目标靶点为NAFLD 潜在靶点。通过Genecards 查询到NAFLD 靶点Score 最大值为100.16,最小值为0.33,中位数为4.93,故设定Score>4.93 的条件,最终纳入807 个潜在靶点;通过Dis-Genet 数据库检索到1059 个疾病相关基因,根据数据库推荐标准,综合评分分值≥0.3 的70 个靶点认为与NAFLD 较为密切。合并以上所有数据库经筛选后的相关靶点,并排除重复值,最终得到1311 个NAFLD 相关靶点。应用Venny 取交集,得到枳壳有效成分-NAFLD 共同靶点56 个。
2.3 枳壳药物-有效成分-潜在靶点网络构建 运用Cytoscape3.7.2 软件将枳壳9 种有效成分及119个潜在靶点导入,得到枳壳有效成分-潜在靶点可视网络图(见图1),其中红色代表枳壳药物,深紫色代表其活性成分,蓝代表潜在靶点,共得到128 个节点、161 条边。Degree 值大小通过节点大小反应,节点越大,该成分越重要,所以β-sitosterol、naringenin、nobiletin、neohesperidin 有可能是枳壳干预NAFLD较为重要的活性成分。
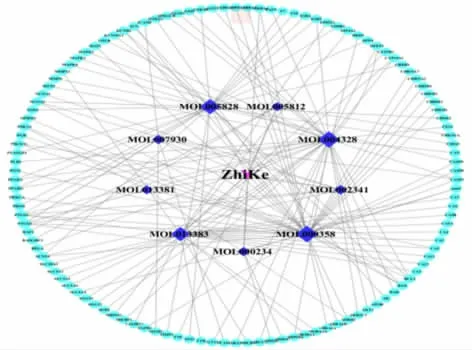
图1 枳壳-活性成分-靶点网络图
2.4 枳壳有效成分-NAFLD 靶点PPI 核心网络构建将候选基因提交至STRING 11.0 平台,得到枳壳-NAFLD 靶点PPI,再将该PPI 网络信息导入Cytoscape3.7.2 软件,利用Network Analyzer 插件筛选得到该蛋白相互作用核心网络(见图2)。图2 中含有26 个节点和223 条边。根据节点大小和颜色深浅反映度值大小,Degree 值越大,颜色越亮,表示该靶点越重要,与药物和疾病的相关性越强。线条的粗细也反映了两个靶点之前的重要性,线条越粗,说明该连接越重要。排名较前的为AKT1、TNF、TP53、CAT、JUN、MAPK8 等靶点。选取degree 值排名前10 基因靶点,见表2。
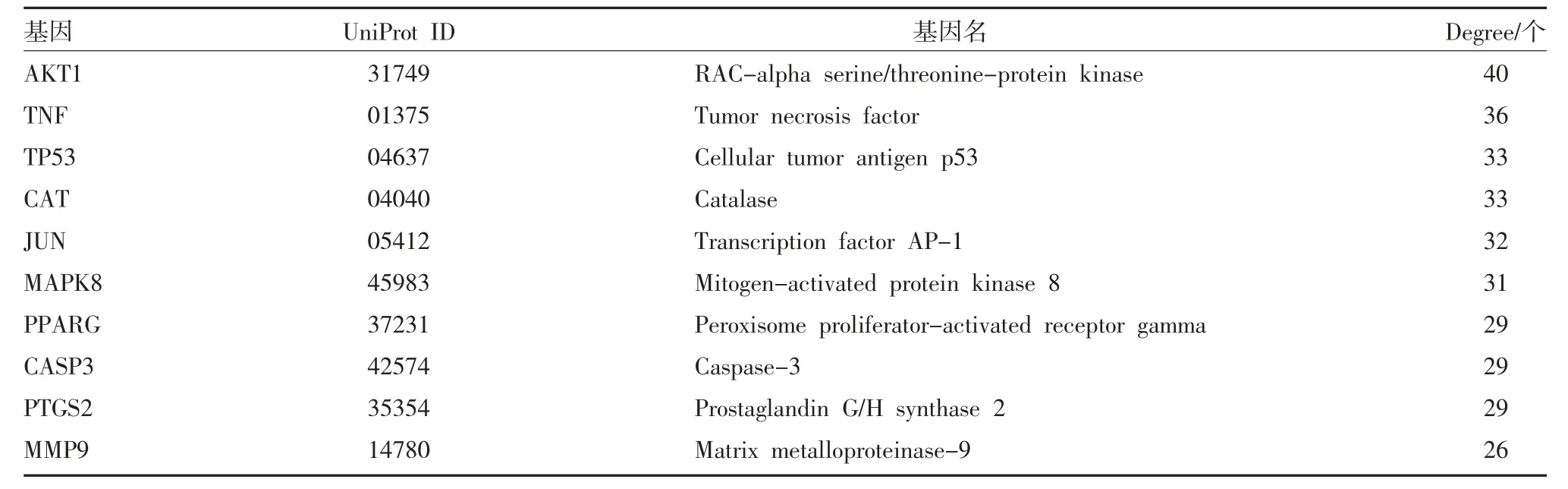
表2 枳壳干预非酒精性脂肪性肝病核心靶点拓扑性质
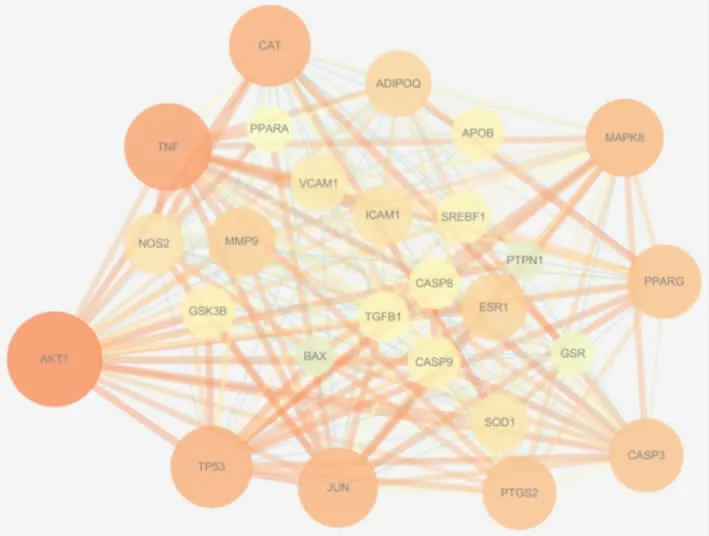
图2 枳壳干预非酒精性脂肪性肝病核心PPI 网络
2.5 枳壳主要成分-靶点-疾病气泡图 本研究使用Metascape 平台对56 个关键靶点进行GO 富集分析和KEGG 分析,包括生物过程(BP)、细胞组成(CC)和分子功能(MF)3 个分支,共显示1368 个结果富集,其中BP 为1224 个,CC 为71 个,MF 为73 个,KEGG 富集255 条通路。根据-log10(pvalue)排序,选择前20 个通过http://www.bioinformatics.com.cn 平台绘制气泡图(见图3)。图中P 值的颜色越红,表示显著性越强,关系越紧密,气泡节点大小代表富集在上面的基因数量,气泡越大,表示相关的基因越多,反之越小。
从图3 可知,枳壳干预NAFLD 的靶点在生物过程中,主要涉及对有害物质的反应(response to toxic substance)、患者体内营养水平的调节(response to nutrient levels)、对细胞外刺激所产生的反应(response to extracellular stimulus)以及凋亡信号通路(apoptotic signaling pathway)等;从细胞组分结果可以看出,枳壳干预NAFLD 过程中主要通过细胞中脂筏(membrane raft)、膜微区(membrane microdomain)、膜区(membrane region)等细胞膜部位进行;从分子功能结果看,主要与蛋白酶结合(protease binding)、蛋白质均二聚活性(protein homodimerization activity)和氧化还原酶活性(oxidoreductase activity)关系较为密切。在KEGG 通路富集结果中,结果显示与癌症途径(pathways in cancer)、NAFLD、糖尿病并发症中的AGE-RAGE 信号通路(AGE-RAGE signaling pathway in diabetic complications)、TNF 信号通路(TNF signaling pathway)等枳壳干预NAFLD的作用机制紧密相关。
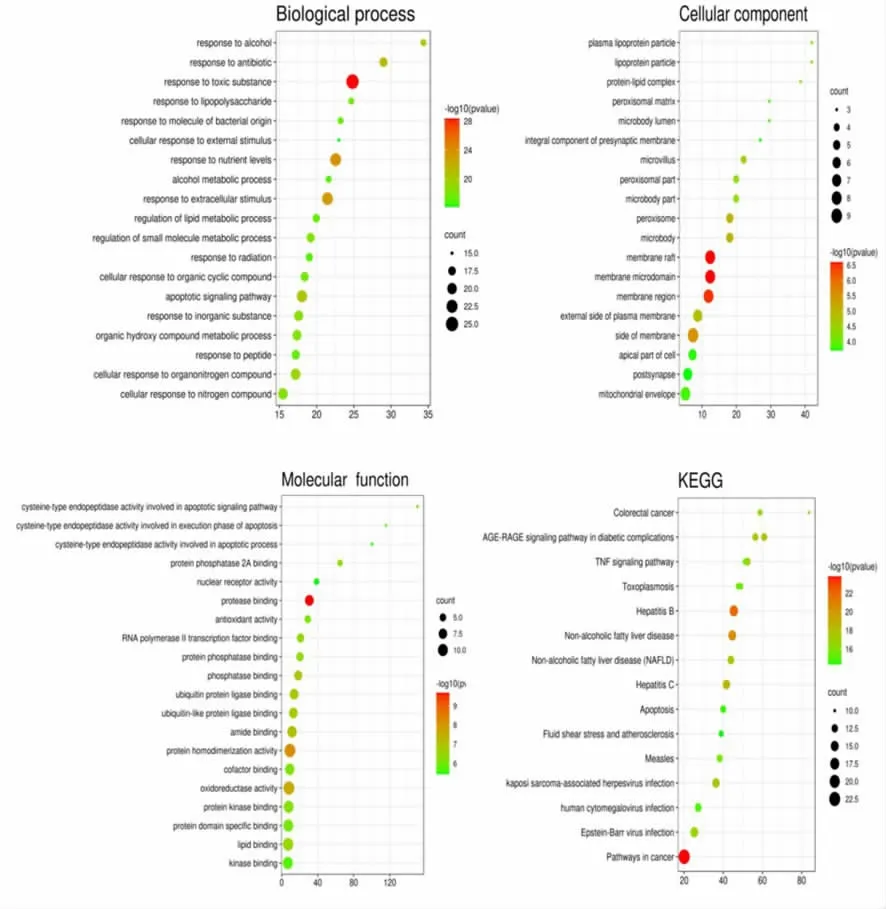
图3 枳壳干预非酒精性脂肪肝关键靶点GO、KEGG 气泡图
2.6 分子对接验证 根据PPI 核心网络分析选取排名前6的靶点蛋白AKT1、TNF、TP53、CAT、JUN、MAPK8,与对应的活性成分进行分子对接,分子对接自由能越小,则表示构象越稳定,两者结合程度越高。一般认为,当对接结合能≤-5.0kcal/mol 时,配体与受体有较好的结合活性,因此,本研究中的关键靶点与相应的活性成分之间具有较好的结合活性,见表3。

表3 配体与受体对接结合自由能
3 讨论
基于枳壳-活性成分-靶点网络图,我们发现枳壳干预NAFLD 关键成分主要为β-sitosterol(β-谷甾醇)、naringenin(柚皮素)、nobiletin(川陈皮素)、Neohesperidin(新橙皮苷)。研究指出,β-谷甾醇可调节高脂饮食诱导的2 型糖尿病大鼠中IRS-1/AKT 介导的胰岛素信号分子,可减弱胰岛素抵抗(IR),减轻高脂饮食引起的脂肪组织有害变化[10]。柚皮素能抑制肝细胞Nrf2 蛋白及其下游抗氧化酶表达,抑制肝脂质过度积累的作用[11]。川陈皮素与柚皮素类似,也具有抗氧化[12]、抑制肝细胞脂质沉积和细胞凋亡的作用[13]。我们前期研究发现,新橙皮苷能抑制肝脏氧化应激反应和炎症反应,有望开发成为肝保护剂[14]。基于关键靶基因分析中,AKT1、TNF、TP53、CAT、JUN等靶点有可能在枳壳治疗NAFLD 中起到重要作用。通过上述分析,提示枳壳具有多成分、多靶点干预NAFLD 的特点。
富集分析结果显示,枳壳治疗疾病的部位可能发生在细胞膜,主要从对外界有害物质刺激所产生的反应、患者体内营养水平以及氧化还原过程等方面进行干预。NAFLD 在多种细胞外刺激下,磷酸化JNK 等信号通路,引起脂质调节异常,导致IR 发生,促进NAFLD 的发展[15]。不同的饮食模式或营养成分可以通过促进肝脏TG 积累和抑制抗氧化活性直接促进NAFLD 发生,也可以通过影响胰岛素敏感性和餐后TG 代谢间接促进NAFLD 发生[16]。我们前期研究表明,衢枳壳提取物能够改善高脂饮食引起的小鼠肝脏脂质积累,可作为治疗NAFLD 的膳食补充剂[6]。KEGG 通路富集分析中NAFLD、AGE-RAGE 信号通路、TNF 信号通路等富集显著性较高,这些通路能减轻肝脏脂肪变性,减少炎症反应发生。NAFLD与脂毒性、IR 等紧密相关,IR 会加重疾病的进展。有研究发现,AGEs 水平升高和AGE-RAGE 轴激活会引起氧化应激和肝脏炎症,与NAFLD 发病机制相关[17]。TNF-α 是促进IR 及NAFLD 发生发展的细胞因子,在NASH 患者肝脏组织表达水平增加,TNF-α 还可通过多途径参与脂质过氧化和氧化应激,诱发肝脏炎症反应[18]。相反,通过抑制TNFR1 可使MAP 激酶MKK7 基因及其下调基因JNK 的激活减轻,从而改善IR,延缓NAFLD 的发生[19]。
通过分子对接验证得到核心靶点蛋白与活性成分结合较强,表明靶点与成分之间较好的结合力是枳壳发挥作用的基础。其中CAT 与naringenin 结合活性最强。CAT 作为抗氧化因子,可以限制脂肪酸的氧化反应,保护机体免受脂质过氧化物的伤害。唐晓飞等[20]研究证明,柚皮素可能通过促进SOD 和CAT生成,抑制肝细胞氧化应激损伤,从而改善NAFLD。
综上所述,本研究我们在前期证实枳壳具有改善NAFLD 的实验基础上,通过网络药理学与分子对接验证法,收集枳壳治疗NAFLD 潜在靶点,预测可能的作用机制,其中主要涉及IR、氧化应激和炎症反应等机制,为后续实验研究提供理论指导。

