3M MDS沙门氏菌分子检测试剂盒的评价
林 杰,徐 珊,郑 晶,柯 璐,陈 彬,张温玲,曾维杨
(福州海关技术中心//福建省检验检疫技术研究重点实验室,福建 福州 350003)
沙门氏菌是一群形态、培养、生化反应和抗原构造相类似的革兰氏阴性杆菌,迄今已发现的沙门氏菌有2 000多个种(或型),我国发现200多种菌型。沙门氏菌是食品中常见的主要肠道杆菌,能够引起急性胃肠炎、伤寒、食源性动物败血症[1-3]。沙门氏菌感染人的途径大多直接或间接地与动物性食品有关,沙门氏菌很容易在自然环境及动物体内存活和增殖,因此准确快速地检测食品中的沙门氏菌,对于保护人畜健康有着十分重要的意义[4-5]。由于商品化试剂盒方法具有简便快速、灵敏度高、特异性强的特点,可以节约大量培养基配制和操作时间,因此近年来得到广泛应用,相关产品也有不少[6-10]。3M MDS分子检测试剂盒采用环介导等温扩增技术来快速扩增,结合使用生物发光特性来检测扩增,实时报告阳性结果,阴性结果将在60 min内得到。该方法具有高特异性和高敏感性的特点,并且检测快速、易于操作。为了更加科学规范的使用试剂盒,根据SN/T 3256—2012《食品微生物检验方法确认技术规范》[11]和SN/T 2775—2011《商品化食品检测试剂盒评价方法》[12]的要求,对3M MDS分子检测试剂盒进行评价试验,评估其在食品中沙门氏菌检测的准确性和适用性。
1 材料与方法
1.1 材料与试剂
菌株:肠炎沙门氏菌,ATCC13076;大肠埃希氏菌,ATCC25922,均购自上海汉尼生物技术有限公司。
试剂:缓冲蛋白胨水,3M MDS沙门氏菌分子检测试剂盒,亚硒酸盐胱氨酸(SC)增菌液,沙门氏菌显色板,营养琼脂平板。
1.2 仪器与设备
KD-TBC-300M电子天平,福建科迪技术有限公司;Stomacher3500拍击式均质器,英国SEWARD;恒温培养箱,德国BINDER;3M分子检测仪器,美国3M公司;VITEKⅡ微生物鉴定仪,法国梅里埃公司。
1.3 方法
1.3.1标准菌株及菌悬液的制备
将标准菌株肠炎沙门氏菌(ATCC13076)复活后,接种于营养琼脂,36℃培养 18 h 备用。
1.3.2两种方法对比灵敏度、特异性和准确度
根据SN/T 3256—2012《食品微生物检验方法确认技术规范》和SN/T 2775—2011《商品化食品检测试剂盒评价方法》的要求,选择5类15种样品进行试验。每种食品基体需要有3个样品(标准的测试组分为25 g),其中一个未污染、一个样品的污染水平为1~9 CFU/25 g、一个样品的污染水平为10~99 CFU/25 g。对于低和高的污染水平,分别进行16次平行测试;未接种的样品进行5平行测试。添加菌为肠炎沙门氏菌(ATCC13076)。每种样品同时按照3M MDS分子检测试剂盒方法和GB 4789.4—2016《食品安全国家标准 食品微生物学检验 沙门氏菌测定》[13]进行检测。结果见表1。灵敏度、特异性和准确度统计分析见表2。
1.3.3试剂盒耐变性
耐变性是指对同一样品用一个分析方法,在各种正常检测条件下进行分析,保证该分析方法的可行性。耐变性评价由以下步骤组成:确定可能影响检测结果的因素、对每一种因素稍作改变、采用合适的方法进行耐变性检验。确定需要评价的变量3个:裂解时间(13 min,17 min)和裂解体积(18 μl,22 μl),反应体积(18 μl,22 μl),每个变量取两个不同的水平。采用纯培养的1株目标菌(肠炎沙门氏菌,ATCC13076)与1株非目标菌(大肠埃希氏菌,ATCC25922)进行耐变性实验。目标菌的浓度在1~9 CFU/25 g的水平,非目标菌浓度在10~99 CFU/25 g的水平。目标菌和非目标菌均采用检测方法所要求的培养基,采用试剂盒方法进行分析。结果见表3。
1.3.4试剂盒批间变异
为了验证试剂盒的稳定性,取3个不同批号试剂盒进行批间变异实验,采用纯培养的1株目标菌(肠炎沙门氏菌,ATCC13076)与1株非目标菌(大肠埃希氏菌,ATCC25922)进行实验。目标菌的浓度在1~9 CFU/25 g的水平,非目标菌浓度在10~99 CFU/25 g的水平。结果见表4。
1.3.5试剂盒包容性和排他性
包容性是指确定某一检测方法从众多菌中检测到目标菌的能力。排他性是指某一检测方法对可能引起交叉反应的相关非目标菌株的抗干扰能力。包容性:选择100株沙门氏菌的纯化菌株,用3M测试方法进行测试。排他性:选择30株非沙门氏菌的纯化菌株,用3M测试方法进行测试。
1.3.6实验室间协同试验
选择牛奶样品,添加肠炎沙门氏菌(ATCC13076),制备未接种(L0)、低(L1)、高(L2)三个接种水平样品,每一水平8个平行样品。同时用3M测试方法和参考方法进行测试,7家实验室进行协同实验。检测结果见表5,数据分析见表6。
2 结果和分析
2.1 灵敏度、特异性和准确度
15个食品类型的试验结果见表1。
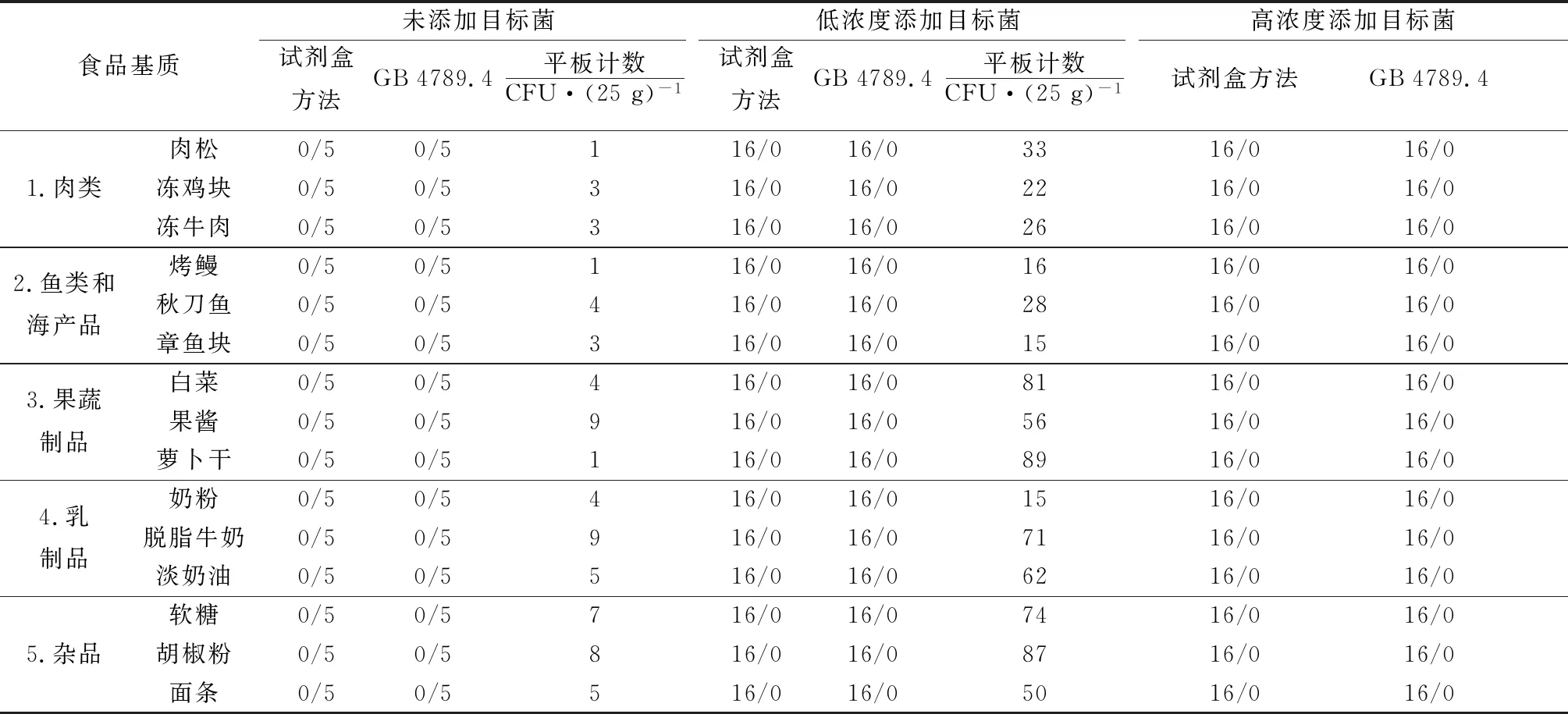
表1 15个食品类型的试验结果(+/-)
试验结果统计分析见表2。
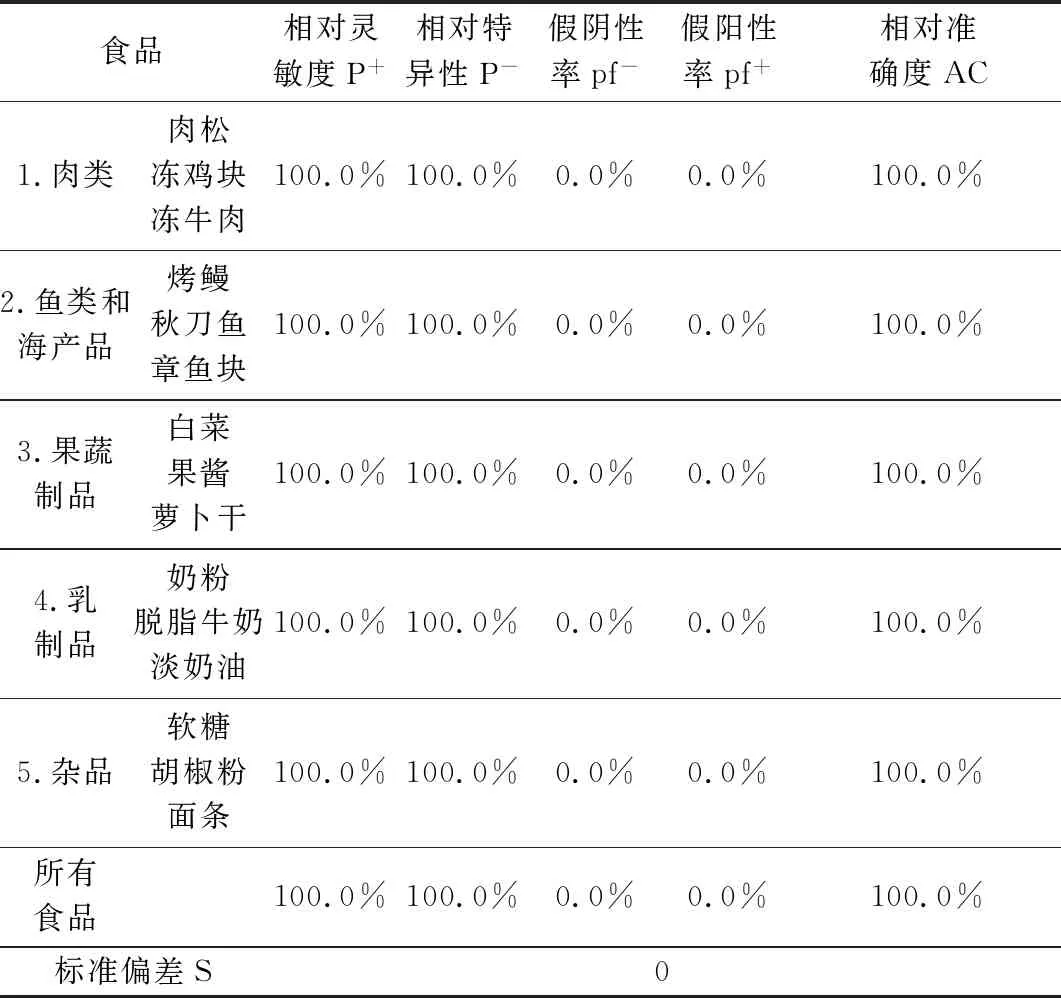
表2 试验结果统计分析
式中,FP为假阳性的测试数;N为未接种样品L0的总测试数。
式中,TP为阳性的测试数;N为低浓度(L1)和高浓度(L2)样品的总测试数。
式中,PA为两种方法相同的阳性测试数;NA为两种方法相同的阴性测试数;N为所有样品的总测试数。
该试剂盒用作检测沙门氏菌时,在5个食品种类,15个食品类型的样品的检测结果表明,该试剂盒相对灵敏度高、假阴性率低,相对特异性好假阳性率低,相对准确度高。两种方法标准偏差S为0,说明两种方法在统计学上无显著性差异。
2.2 试剂盒耐变性
耐变性实验结果见表3。

表3 耐变性实验结果(+/-)
目标菌在3变量10平行检测均检出,非目标菌在3变量10平行检测均未检出。检测结果表明,其它变量无显著性差异。
2.3 试剂盒批间变异
批间差异实验结果见表4。

表4 批间差异实验结果(+/-)
目标菌肠炎沙门氏菌在3批次10平行检测均检出,非目标菌大肠埃希氏菌在3批次10平行检测均未检出。检测结果表明,该试剂盒的批间变异无显著性差异。
2.4 试剂盒包容性和排他性
选择经确认的100株沙门氏菌标准菌株以及实验室自行分离的沙门氏菌菌株,用3M试剂盒检测,结果均为阳性,表明该试剂盒在包容性上表现良好。
选择经确认的30株非沙门氏菌的标准菌株,用3M试剂盒进行测试,结果均为阴性,表明该试剂盒在排他性上表现良好。
2.5 试剂盒协同试验
协同实验结果及结果统计分析见表5、表6。

表5 协同实验结果(+/-)
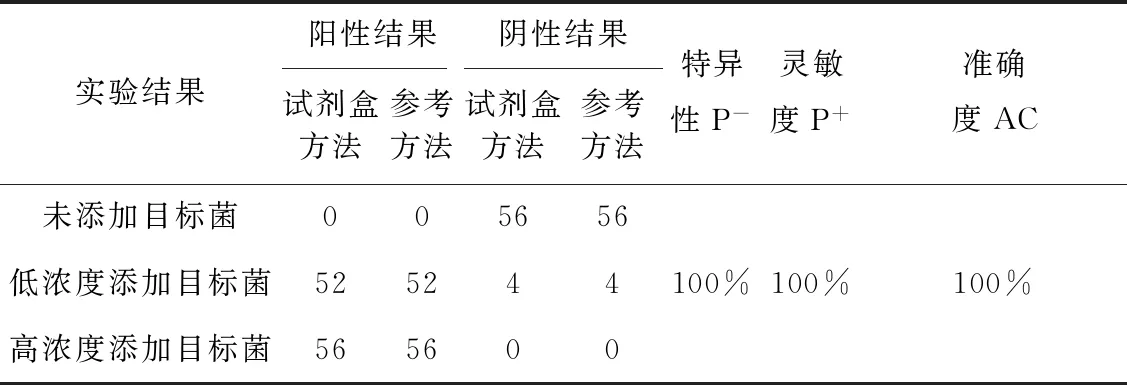
表6 协同实验结果统计分析
7家实验室对三个接种水平样品的测试结果分析表明,试剂盒方法和参考方法检测结果无差异,试剂盒方法稳定可靠。
3 结论
通过5大类15种食品两种检测方法的比对试验,灵敏度、特异性和准确度试验结果,以及7家实验室协同试验结果分析均说明3M MDS沙门氏菌分子检测试剂盒和国家标准GB 4789.4—2016在食品检测上无显著性差异。耐变性结果表明试剂盒在检测的裂解时间和裂解体积及反应体积范围内对检测结果没有影响;批间变异结果表明不同批号试剂盒的检测结果无显著差异,说明试剂盒稳定性良好。包容性和排他性试验均未出现假阴性和假阳性结果。综上所述,3M MDS沙门氏菌分子检测试剂盒检测结果准确,产品性能稳定,特异性强,相对GB 4789.4—2016检测时间可缩短48 h,能满足食品中沙门氏菌的检测要求。

