抗癫痫药物对婴幼儿骨代谢的影响
陈丽婷,曾甲斌,柯钟灵,林 希,陈素清,吴 斌
据世界卫生组织报道,全球大约有6 500万癫痫患者,我国癫痫患病率约为0.715%[1]。各个年龄段的人群均可罹患癫痫,但以婴幼儿及儿童的患病率最高。虽然目前癫痫有许多可供选择的治疗方法,包括迷走神经刺激(vagal nerve stimulation,VNS)、外科手术和生酮饮食等,但采用抗癫痫药物治疗始终是首选。研究发现,50%以上服用抗癫痫药物治疗的患者存在骨代谢异常[2],提示抗癫痫药物与骨质疏松、骨折等密切相关[3]。儿童期及青春期是骨骼发育、骨骼骨矿化的高峰期,其骨骼的生长发育对其将来成年后的身高、运动及生活等极为重要,因此,抗癫痫药物对此时期骨代谢的影响备受关注,近年的研究也多集中于此时期的患儿[4-5],只有极少数研究关注了婴幼儿[6]。然而,骨骼发育是一个连续的过程,婴幼儿期的骨代谢异常也可能造成严重后果,如出现佝偻病、骨骼发育畸形等。本研究拟通过对癫痫婴幼儿骨代谢生化指标的评估,探讨抗癫痫药物对婴幼儿骨代谢的影响,为临床诊疗提供参考。
1 对象与方法
1.1 对象 收集2015年9月-2019年9月就诊于笔者医院的癫痫患儿32例作为研究组,男童14例,女童18例,年龄(20.44 ±11.26)个月(3~36个月),病程1周~33个月。癫痫诊断参照国际抗癫痫联盟2010癫痫和癫痫综合征的分类诊断标准[7]。癫痫发作类型:部分性发作21例,全面性发作11例。视频脑电图检查:正常脑电图2例,1例 Rolandic区大量放电,其余为少量尖波、尖慢波;影像学检查:头颅MRI示结构性改变2例,其中结节性硬化1例,大脑皮层发育不良1例。患儿均服用奥卡西平、丙戊酸钠等抗癫痫药物治疗。
另收集同期初诊尚未开始治疗的癫痫患儿22例作为对照组,男童11例,女童11例,年龄(18.09±10.12)个月(3~36个月),病程1~7 d。两组患儿还需符合下列标准:(1)从出生后10 d~2岁均规则服用维生素D 400 IU/d;(2)研究组使用抗癫痫药物治疗>1周,对照组病程<1周;(3)排除其他影响骨代谢的内分泌系统疾病(如佝偻病、骨发育不全、甲状腺疾病以及严重的肝肾疾患等);(4)正常饮食和活动。本研究经笔者医院伦理委员会批准,患儿监护人均知情同意。
1.2 方法
1.2.1 药物治疗 抗癫痫药物如下:奥卡西平口服混悬液(曲莱,瑞士诺华制药有限公司);丙戊酸钠口服溶液[德巴金,赛诺菲(杭州)制药有限公司];左乙拉西坦口服溶液[开浦兰,优时比(珠海)制药有限公司];托吡酯片(妥泰,西安杨森制药有限公司)。研究组进一步分层:根据用药时间的长短分为≤1 a组及>1 a组;根据用药的种类分为单药治疗组(只使用上述药物中的1种)及多药治疗组(使用≥2种上述药物,联用≥1个月)。药物剂量根据说明书使用,用药时间1周~33个月,中位数为4个月。单药治疗组进一步进行亚组分析,根据所服用药物分为丙戊酸钠组和奥卡西平组,而左乙拉西坦及托吡酯单药治疗患儿例数少,未再进行亚组分析。
1.2.2 采集血清样本 患儿于清晨采集空腹静脉血3 mL,室温静置后于3 000 r/min下离心10 min,留取血清样本,置于-20 ℃冰箱中保存备用。
1.2.3 骨代谢生化指标 总1型胶原氨基端延长肽(total N-terminal propeptide of type 1 procollagen,TP1NP)、β胶原降解产物(β-collagen specific sequences,β-CTX)、25羟基维生素D(25-hydroxy-vitamin D,25-OHD)、N端骨钙素(N-terminal midfragment of osteocalcin,NMID)的检测采用电化学发光法进行。
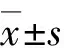
2 结 果
2.1 骨代谢指标比较 两组患儿血清中的TP1NP、β-CTX和25-OHD水平比较,差别均无统计学意义(P>0.05),但研究组的NMID水平较对照组高,差别有统计学意义(P=0.01,表1)。
2.2 抗癫痫药物不同疗程对骨代谢的影响 ≤1 a组(25例)与>1 a组(7例)的β-CTX、25-OHD和NMID水平差别均无统计学意义(P>0.05),两组间的TP1NP水平差别有统计学意义(P=0.03,表1)。
2.3 单药治疗组与多药治疗组骨代谢指标比较 单药治疗组23例,男童8例,女童15例,年龄(20.04±11.49)个月,用药时间中位数4个月;多药治疗组9例,男童6例,女童3例,年龄(21.44±11.25)个月,用药时间中位数6个月。两组在性别、年龄、用药时间上差别无统计学意义(P>0.05);两组的TP1NP、β-CTX、25-OHD、NMID水平差别均无统计学意义(P>0.05,表1)。
2.4 丙戊酸钠组与奥卡西平组骨代谢指标比较 丙戊酸钠组13例,男童4例,女童9例,年龄(22±10.99)个月,用药时间中位数4个月;奥卡西平组7例,男童2例,女童5例,年龄(15.86 ±11.94)个月,用药时间中位数8个月。两组在性别、年龄、用药时间上无明显差异;两组的TP1NP、25-OHD、NMID水平比较,差别无统计学意义(P>0.05),但丙戊酸钠组的β-CTX较奥卡西平组高(P<0.05,表1)。

表1 不同分组组间骨代谢指标比较
3 讨 论
癫痫是小儿神经系统的常见疾病之一,首选抗癫痫药物治疗。但抗癫痫药物已被证实与儿童和青少年的骨密度降低有关[8],而儿童生长发育相关的身高、体质量、营养和认知状况与骨代谢密切相关[9]。抗癫痫药物的使用是癫痫儿童维生素D缺乏和骨骼健康受损的重要危险因素之一,建议对服用抗癫痫药物治疗的儿童进行骨代谢监测并补充维生素D[10]。维生素D缺乏也会影响婴幼儿的骨发育或导致一些非骨代谢相关的疾病,如肌无力等[11-12]。
骨骼的形成是一个动态吸收和分解的过程,骨代谢相关指标中,TP1NP水平作为一个可靠的成骨标志物,反映了胶原合成的速度;NMID是骨钙素中的稳定成分,主要负责维持正常的骨矿化速度;TP1NP及NMID是骨形成标志物;β-CTX是Ⅰ型胶原降解的特异性标志物,是骨吸收标志物[13];25-OHD是反应血中维生素D水平的敏感指标。这些骨转化标志物均可用来监测骨形成和吸收的速度,是反应骨代谢的敏感指标[14]。
本研究发现,研究组的骨代谢指标TP1NP、β-CTX和25-OHD与对照组比较无明显差异,但NMID水平较对照组明显升高,提示其骨合成活跃,与文献报道一致[15-17]。Papassava等[16]的研究发现,使用丙戊酸钠、奥卡西平、拉莫三嗪等抗癫痫药物治疗的患者,NMID水平升高。鞠俊[15]的研究亦发现,拉莫三嗪单药治疗组与未治疗组比较,NMID水平明显升高,认为癫痫疾病本身可引起骨胶原类骨质骨架的代谢障碍,进而影响骨的矿化作用,故癫痫控制后,NMID水平升高。上述研究提示,抗癫痫药物及癫痫疾病本身均可能影响患儿的NMID水平,进而影响骨代谢。
药物的疗程不同对骨代谢的影响可能不同。本研究显示,使用抗癫痫药物>1 a的婴幼儿,其TP1NP水平降低,骨合成能力下降,提示抗癫痫药物使用时间越长,对婴幼儿骨代谢的影响越明显。这与上述的抗癫痫药物对儿童骨代谢影响的结果一致[18]。癫痫是慢性疾病,需长期使用癫痫药物治疗,故对长期用药的婴幼儿需注意监测和评估骨代谢指标。
除药物疗程外,药物种类的多寡对骨代谢的影响亦可能存在差异。既往研究发现,多药治疗的患儿骨密度降低的风险较单药治疗的患儿明显升高[19-20]。Saket等[21]的研究发现,多药治疗的患者25-OHD水平明显下降。本研究显示,单药或多药治疗对婴幼儿骨代谢的影响并没有差异,可能与多药治疗组的病例数较少有关。
另外,不同药物对骨代谢的影响也不同。丙戊酸钠是传统的抗癫痫药物,可能通过直接激活孕烷X受体途径增加了CYP24A和CYP3A4的基础和维生素D诱导的表达,导致维生素D分解代谢,从而降低其活性,对骨代谢产生影响[16]。多数研究认为,丙戊酸钠会影响骨代谢,导致骨密度降低,甚至骨折等[6,22]。奥卡西平是新型的抗癫痫药物,对骨代谢是否有影响仍存在争议。部分研究认为,奥卡西平能够降低血液中的25-OHD及钙离子,影响骨吸收[2,23];另一些研究认为,奥卡西平对骨代谢没有影响[5,15]。本研究发现,与奥卡西平组比较,丙戊酸钠组的β-CTX水平较高,提示丙戊酸钠组较奥卡西平组骨吸收更为活跃,说明丙戊酸钠对骨代谢影响更为明显。
本研究纳入的对象主要为婴幼儿,受到年龄限制,且多数患儿的病程及服用药物时间均较短,无法深入评估病程及药物疗程对骨代谢的影响,但以抗癫痫治疗1 a为界,已发现其骨合成能力受影响。为了严格控制补充维生素D对骨代谢的影响,仅纳入完全按婴幼儿保健要求补充维生素D的患儿,病例来源受限,病例数较少,有待将来大样本的病例对照研究进一步明确。

