肝胆胰患者术后术区感染风险因素的分析
邢 岩,姜 傲,高莹莹,鄂长勇
(吉林大学中日联谊医院 肝胆胰外科,吉林 长春130033)
肝胆外科具有手术时间长、手术创伤大等特点,这些特点造成术后较容易发生感染。术区感染(SSI)增加了住院时间、资源利用率和再入院率,造成相当大的经济负担[1]。肝切除术后胆汁渗漏和胰腺切除术后胰腺瘘是肝胆胰腺手术患者器官及腹腔间隙术区感染的常见原因[2-3]。重要的危险因素包括超重状态、造口、伤口种类≥Ⅲ级、美国麻醉医师协会(ASA)生理状况≥3及手术时间延长。由于肝胆胰腺手术过程复杂,不同的危险因素和临床结果与切口型术区感染和器官-腹腔间隙型术区感染相关[3]。本研究旨在探讨肝胆胰腺手术后切口型或器官-腹腔间隙术区感染的发生率,分析肝胆胰腺手术中不同类型术区感染的危险因素。
1 材料与方法
1.1 研究对象
2017年1月至2019年12月在吉林大学中日联谊医院肝胆胰腺外科进行诊治的患者,获医院伦理委员会批准。入选标准:行胰十二指肠切除术(胰十二指肠切除术、胰腺远端/中段切除术),肝切除合并胆道切除,肝切除不伴胆道切除或开腹胆囊切除术。排除标准:腹腔镜胆囊切除术。术前1 h内静脉滴注头孢替唑钠,术后持续48 h。术前行胆道外引流的患者,根据胆汁标本中分离出的细菌选择预防性抗生素。延长手术每3 h给药一次(头孢替唑钠)。其他抗生素根据半衰期确定再给药间隔。所有患者术后随访至少30天。
1.2 术区感染诊断标准
切口型SSI的诊断标准是术后30天内发生的涉及皮肤、皮下组织的感染,或切口处深层软组织(如筋膜和肌肉层),且至少有以下一种:①有或没有实验室检查证实,但切口处有脓性引流;②从无菌获得的液体培养物或从切口处提取的组织中分离出细菌;③至少有以下一种感染症状:疼痛或压痛、局部肿胀、发红、发热或发烧(≥38℃);④自发性的伤口开放;⑤脓肿在直接检查、再手术、组织病理学或放射学检查中发现的涉及筋膜或肌肉层的脓肿或其他感染迹象。
器官及腹腔间隙术区感染的诊断标准是术后30天内发生的涉及腹腔的感染,且至少有以下之一:①脓液从一个瘘管通过伤口进入器官-腹腔间隙;②从器官-腹腔间隙中无菌获得的液体或组织培养物中分离出来的微生物;③在直接检查、再次手术、组织病理学或放射学检查中发现的涉及器官-腹腔间隙的脓肿或其他感染证据。
1.3 危险因素与术区感染相关性的变量
病人相关的变量:年龄≥65岁,性别,体质量指数<18.5 kg/m2或≥25.0 kg/m2,ASA生理状态≥3,合并症(糖尿病、高血压、肾脏疾病包括血液透析、肝病、心脏病),吸烟,肿瘤复发,远处转移,白蛋白≤3.5 g/dL,血糖≥200 mg/dL,总胆红素≥2.0 mg/dL,INR≥1.15,6个月内用药(免疫抑制剂、干扰素、生物剂、类固醇、抗癌化疗)。术前和术后护理或治疗相关变量:射频消融、经导管动脉化疗栓塞、手术、抗生素使用(持续30天)、胆道引流、血糖水平≥200 mg/dL(2天内)和血液产品使用(1周内)。术中或者其他术中相关因素变量:手术过程,腹腔镜手术,手术时间延长(≥60 min),切口种类≥Ⅲ级,术中出血(≥150 mL),低体温,输血等。
1.4 统计方法
通过χ2检验估计各变量的风险率和95%置信区间,并通过交叉表格检查潜在的混杂因素,这些单变量分析选择的变量(P<0.1)随后进入Logistics回归模型,以估计相关性的大小(比值比)和95%置信区间。所有分析均选用 SPSS 20.0 软件进行分析,其中计数资料用例数(%)表示,显著性水平设置为P<0.05。
2 结果
2.1 研究对象基本资料
共分析了627例患者(男性392例;女性235例)。平均年龄(63.5±14.7)岁。ASA生理状态≥3的患者占总患者的40.8% [1,n=21(3.3%);2,n=350(55.8%);3,n=254(40.5%);4,n=2(0.3%)]。原发性疾病以肝肿瘤为主353例,其次为胆管癌118例、胰腺癌116例、良性胆管疾病27例、良性胰腺疾病9例和良性肝脏疾病4例。363例患者行肝切除而不切除胆道,55例患者行肝切除并胆道切除,136例患者行胰十二指肠切除,40例患者行远端/中段胰腺切除术,33例患者行开腹胆囊切除。
2.2 术区感染发生率相关统计
627例肝胆胰腺手术患者中术区感染111例[切口型术区感染的发生率为2.2%,14例;器官-腹腔间隙型术区感染的发生率为12.6%,79例;其中两者皆有型(混合型)为2.9%,18例],发生率为17.7%。器官-腹腔间隙SSI的发生率明显高于切口SSI [12.6%(79/627) vs.2.2%(14/627);P<0.001]。肝切除联合胆道切除的SSI发生率为38.2%,胰切除的SSI发生率为29.0%。与肝切除不切除胆道术相比, SSI的发生率明显更高(P<0.001),术后住院时间30.9±23.7天。SSI患者的住院时间明显长于无SSI患者(分别为56.6±33.2天和25.3±16.4天,P<0.001),见表1。
2.3 病原菌感染情况及构成比
111例术区感染患者共获得引流液标本135份,共检出184株细菌,主要培养出的微生物为屎肠球菌59株,其次是金黄色葡萄球菌23株,克雷伯氏菌18株,铜绿假单胞菌17株,肠杆菌10例株,见表2。
2.4 相关变量与术区感染的分析
表3显示了单变量分析中与SSI相关的变量。表4显示了多因素分析中与总SSI、切口型SSI、器官-腹腔间隙型SSI及两者皆都类型相关的独立危险因素。手术相关因素中,独立危险因素为远端/中段胰脏切除术、胰十二指肠切除、肝切除联合胆道切除术、手术时间延长、术中出血。在术前护理-治疗相关因素中,胆道引流是SSI的唯一危险因素。在切口型和器官-腹腔间隙型SSI之间确定了不同的危险因素(不包括延长手术时间)。在多因素分析中,肝切除加胆道切除、胰十二指肠切除和远端/中段胰腺切除术是器官/空间型SSI的独立危险因素。此外,术前胆道引流和术中大量出血也与器官-腹腔间隙型 SSI相关。虽然ASA身体状态≥3与切口SSI相关,但这与器官-腹腔间隙型SSI无关。无胆道切除的肝切除术可降低切口SSI的风险。

表2 从术区感染中分离出来的微生物及构成比
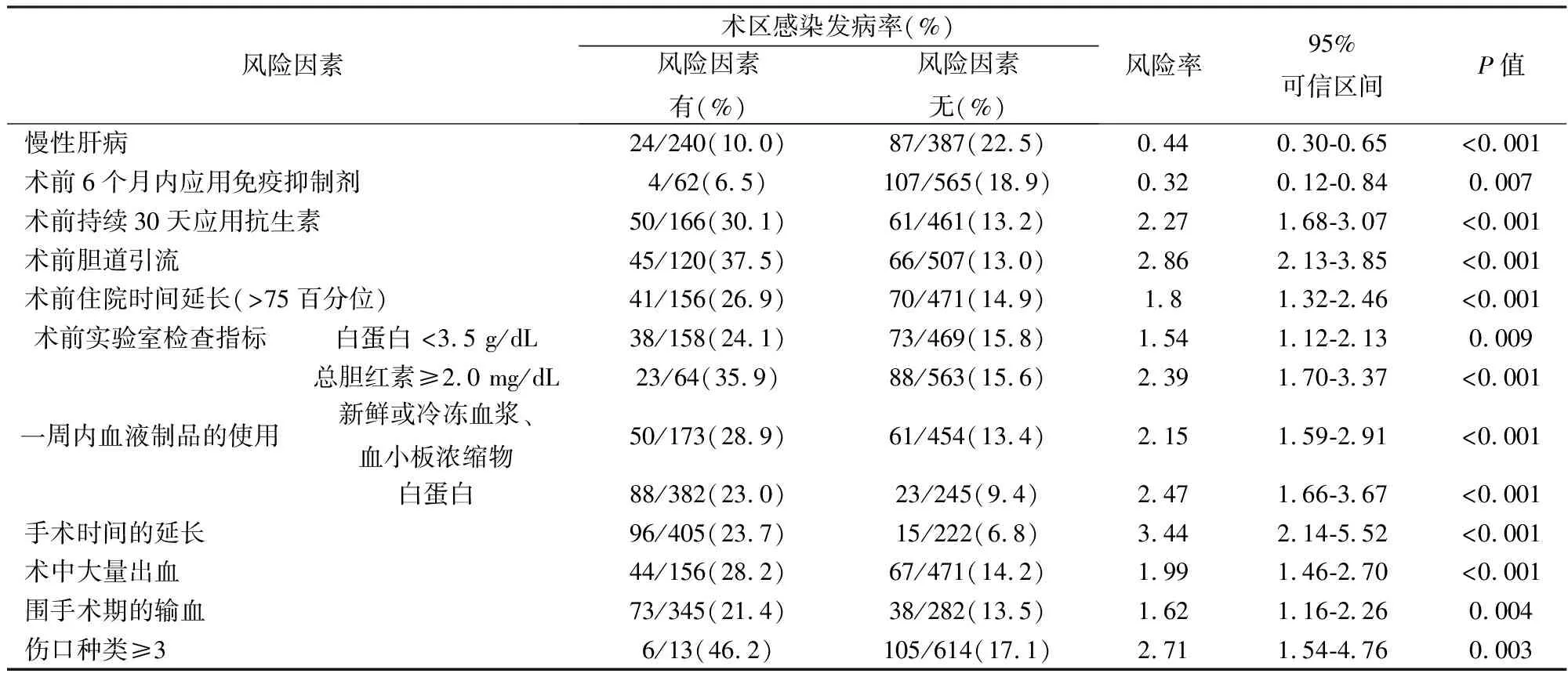
表3 与术区感染相关变量的单因素分析
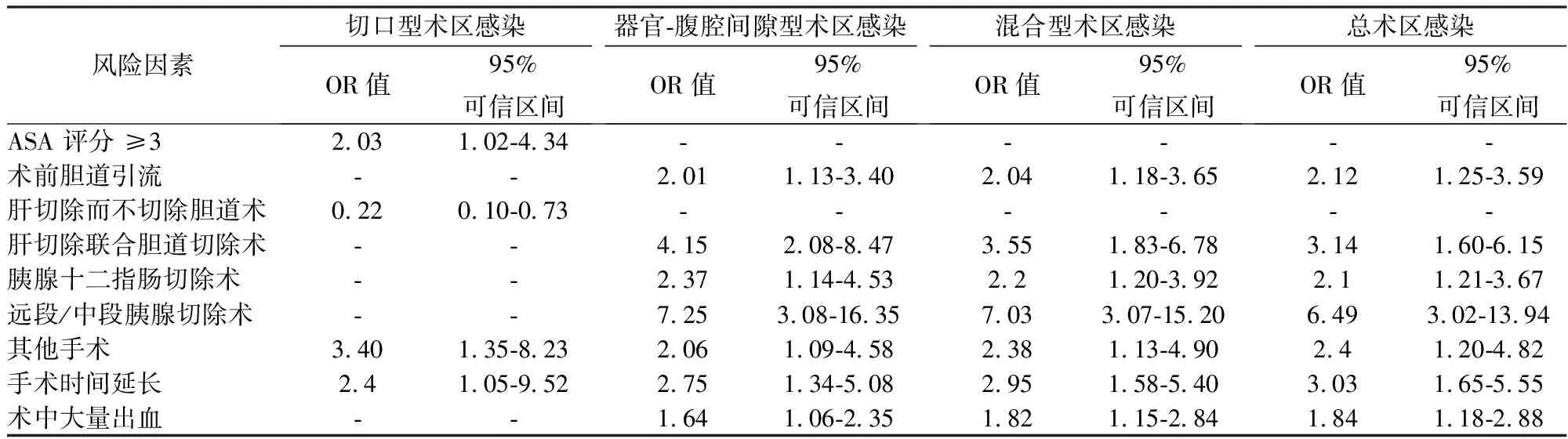
表4 多因素分析中与SSI相关的独立因素
3 讨论
本研究中肝胆胰腺手术中SSI的发生率为17.7%,其中肝切除联合胆道切除(38.2%)、胰十二指肠切除(28.7%)和远段/中段胰腺切除术(30.0%)发生率较高。在这些手术中,SSI的发生率明显高于不切除胆道的肝切除术。胰腺切除术和肝切除术合并胆道切除术可能的共同因素是淋巴结清扫、大量失血和手术时间延长,此类手术也是技术上最复杂的手术之一,包括重建胃肠道及胆道的精细吻合,这些变量中的每一个都可能有助于感染的发展。K.Okano等[4]报道称,胰十二指肠切除术患者的切口SSI、感染胰瘘和腹内脓肿的发生率分别为13.0%、21.4%和14.1%,而远段胰腺切除术患者的发生率分别为5.0%、24.6%和12.4%。Nakahira等[5]报道称,肝切除术(12.8%)与伴有胆道重建的肝切除术(41.9%)、PD(39.3%)和部分或远端胰腺切除术(31.8%)相比,SSI的发生率显著降低。在本研究中,器官-腹腔间隙型SSI占肝胆胰区手术患者SSI的71.2%。胰腺手术后SSI发生的因素包括手术时间、主胰管直径、胰瘘、术后出血[2,6]等与手术相关的因素。由于在接受肝胆胰区大型手术的患者中,器官-腹腔间隙SSI的发生率相当高。ASA身体状态评分≥3分、延长手术时间均与切口SSI相关,肝切除不切除胆道手术可降低风险。此外,术前胆道引流、肝切除联合胆道切除、胰十二指肠切除术、远端/中段胰腺切除术被确定为器官-腹腔间隙SSI的危险因素。Sadamori 等[3]报道二次肝切除术和胆漏是肝细胞癌肝切除术后脏器-腹腔间隙型SSI的独立危险因素。
在本研究中,术前胆道引流与SSI相关,近端梗阻的患者如果需要进行大手术,通常需要胆道引流[7]。外部或内部胆道引流导管的存在和高直接胆红素浓度被发现是肝胆外科[8]的特定危险因素。胆汁培养阳性患者的伤口感染率较高,从SSI分离的微生物与大多数患者围手术期胆汁培养中分离的[9]相同。这一观察结果支持根据术前胆汁培养结果使用特定的抗生素预防。在本研究中,SSI的主要微生物是屎肠球菌,其次为金黄色葡萄球菌、克雷伯氏菌、铜绿假单胞菌和肠杆菌。Sugiura 等[2]报道,在SSI最常见的微生物是肠球菌,其次是肠杆菌和克雷伯氏菌。术前胆道引流导致无支架患者的胆道微生物从大肠杆菌转向屎肠球菌污染增加[10]。
综上所述,肝胆胰区手术后主要的SSI类型是器官-腹腔间隙SSI,手术相关因素和术前胆道引流为SSI的独立危险因素。为了防止SSI,对于接受肝胆胰腺手术的患者,术前应仔细评估,加强护理,积极干预控制术前、术中危险因素,提高医疗服务质量。

