西妥昔单抗联合DF化疗方案在中晚期食管癌患者中的治疗效果
曹珊珊,苏永立,王春江,吴 雪,王 勇
食管癌是消化系统较为常见的一种恶性肿瘤,多发于40岁以上人群,早期多无明显症状,当患者出现进行性吞咽困难、纳差、腹部不适等症状时多已处于中晚期,单纯手术切除效果常不理想[1]。因此临床上常在术后通过化疗来提高手术效果,延长患者的生存期。DF化疗方案是目前公认的中晚期食管癌标准化疗方案,但客观缓解率较低,且毒副反应明显。西妥昔单抗作为一种人型单克隆抗体,可作用于表皮生长因子受体来促进肿瘤细胞凋亡[2]。本研究以我院收治的80例中晚期食管癌患者为研究对象,探讨西妥昔单抗联合DF化疗方案的治疗效果,现报道如下。
1 资料与方法
1.1 一般资料选择我院2019年1月至2021年3月住院治疗的80例中晚期食管癌患者,用随机数字表法分为两组,观察组和对照组各40例,入组标准:所有患者经病理活检确诊为食管癌,临床分期为Ⅱb~Ⅳ期,预计生存期6个月以上,且排除合并多器官功能障碍、凝血机制异常、既往接受过放化疗治疗、精神认知障碍、沟通障碍、免疫系统疾病、治疗依从性差及临床资料不全者。患者自愿签署知情同意书,本研究经我院伦理委员会批准。观察组中男23例,女17例,年龄42~74(58.78±4.32)岁;病变位置:上段16例,中段10例,下段14例;TNM分期:Ⅱb期11例,Ⅲ期13例,Ⅳ期16例。对照组中男22例,女18例,年龄42~74(58.01±2.63)岁;病变位置:上段14例,中段12例,下段14例;TNM分期:Ⅱb期9例,Ⅲ期14例,Ⅳ期17例。患者的基本资料无组间显著性差异(P>0.05)。
1.2 方法对照组患者行常规DF化疗,第一至第三天给予25 mg·m-2顺铂(云南生物谷药业)静脉滴注2 h;第一至第五天给予750 mg·m-25-氟尿嘧啶(上海旭东海普药业有限公司,国药准字H31020593)连续静脉泵入,21 d为一个周期。观察组患者在对照组的基础上联合西妥昔单抗(德国默克里昂制药公司,注册证号S20050095)治疗,第1周给予500 mg·m-2静脉滴注2 h,之后每周维持剂量为250 mg·m-2。每次用药前给予10 mg地塞米松静脉注射,同时给予托烷司琼、阿托品等进行辅助治疗,两组均连续治疗4个周期。每个疗程治疗前均行肝肾功能、心电图、血尿常规、肿瘤标志物等检查,比较两组患者的客观缓解率及毒副反应发生率,并于治疗前后取患者空腹静脉血5 mL,以3 000 r·min-1离心分离出上清液,采用Cobas601电化学发光免疫分析仪,利用化学发光法检测两组患者血清癌胚抗原(carcinoembryonic antigen,CEA)与鳞状细胞癌抗原(squamous cell carcinoma,SCC)水平[3]。
1.3 疗效评价标准[4]根据WHO指定的实体瘤疗效评估标准进行评价。完全缓解(complete response,CR):已知病灶消失且持续4周以上;部分缓解(partial response,PR):已知病灶缩小过半且保持4周以上;病情稳定(stable disease,SD):已知病灶缩小25%~50%,未出现新病灶;病情进展(progressive disease,PD):已知病灶增加25%以上,且发现新病灶;总缓解(overall response rate,ORR)=CR+PR。
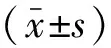
2 结果
2.1 客观缓解率观察组患者客观缓解率(72.50%)显著高于对照组(55.00%),组间比较差异有统计学意义(P<0.05)。见表1。
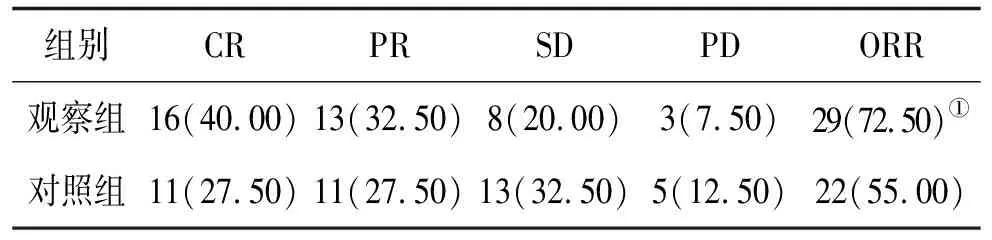
表1 客观缓解率(n=40) 例(%)
2.2 标志物水平变化两组患者的CEA与SCC水平,在治疗前无统计学差异(P>0.05),治疗后观察组患者的CEA和SCC均明显低于对照组(P<0.05)。见表2。
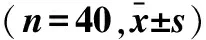
表2 肿瘤标志物水平变化 分
2.3 毒副反应发生率观察组患者胃肠道反应、骨髓抑制、肝肾损伤、皮疹等毒副反应的发生率均低于对照组。两组间毒副反应的总发生率(12.50% VS 37.50%)有统计学差异(P<0.05)。见表3。

表3 毒副反应发生率(n=40) 例(%)
3 讨论
近年来,随着国民生活节奏及饮食结构的变化,我国食管癌的发病率逐年增长。据统计,我国每年新增食管癌患者约25万例,且处于中晚期的患者高达70%以上[5]。食管癌治疗的首选方法为根治性手术治疗,但由于其早期无特殊临床症状,且我国医疗配置城乡差距大,疾病的筛查率较低,人们体检意识淡薄,多数病例在发现时已经错过了手术时机,从而使同步放化疗成为治疗的重要手段[6]。但目前同步放化疗模式的治疗效果仍不能令人满意,如何增加患者抗肿瘤效果,降低毒副作用,提高预后和生存率仍是需要探索解决的主要问题。DF化疗方案是中晚期食管癌治疗的主要手段,其中顺铂为多种实体瘤化疗一线用药,5-氟尿嘧啶可抑制DNA的合成,联合使用可有效抑制肿瘤细胞增殖及转移,提高患者的预后质量[7]。近年来,国内外研发出了许多新型的分子靶向药物。这些药物以肿瘤细胞特有的分子变化为目标,可精准抑制或杀死癌细胞,与传统细胞毒性药物相比毒副作用低,疗效显著[8]。西妥昔单抗可特异性作用于表皮生长因子受体,在治疗转移性结直肠癌、非小细胞肺癌和头颈部肿瘤方面疗效显著[9],但在食管癌治疗中临床疗效如何,结论不一[6],因此临床疗效观察就显得尤为重要。表皮生长因子(epidermal growth factor receptor,EGFR)是治疗食管癌的重要靶点,能激发多条下游信号传导通路,促使正常细胞增殖、转移、恶变或者凋亡[10]。西妥昔单抗是一种单克隆抗体药物,可与肿瘤细胞表面EGFR受体特异性结合并竞争性阻断EGFR和TGF-α等配体,抑制酪氨酸激酶活性,另外还可抑制TK活性来阻断细胞内信号转导途径,抑制肿瘤细胞分裂,促进癌细胞凋亡,与DF方案联合应用可协同性地提高杀灭肿瘤细胞,使病灶较快得到控制,增进患者的治疗信心,从而缓解毒副作用[11]。本研究结果显示,观察组患者近期缓解率显著高于对照组,治疗前两组患者的CEA与SCC水平无显著性差异(P>0.05),治疗后观察组的CEA与SCC水平及毒副反应发生率均显著低于对照组(P<0.05),进一步证明西妥昔单抗联合DF化疗对食管癌患者具有良好的临床效果。
综上所述,西妥昔单抗联合DF化疗方案可有效提高近期疗效,降低肿瘤标志物水平,且毒副反应轻微,对中晚期食管癌患者病情控制具有积极意义。

